UTILIDAD DE LA ESPIROMETRIA MAS DLCO PARA EL













- Slides: 14

“UTILIDAD DE LA ESPIROMETRIA MAS DLCO PARA EL DIAGNÓSTICO OPORTUNO DE NEUMOCONIOSIS” DR. JORGE ARMANDO LOPEZ ARMAS RIMT

INTRODUCCIÓN El término neumoconiosis fue introducido por Zenker en 1867 y deriva del griego pneuma: ‘aire’ y kovni (o kónis): ‘polvo’. La primera vez que se diferenció el polvo de origen inorgánico del orgánico como agente etiológico de neumopatías de etiología laboral fue en las descripciones de Charles Thackrah en 1831. Sin embargo, ya en 1494 se hablaba de los efectos perjudiciales del polvo inhalado por los mineros. Desde la antigüedad se sabe que respirar el polvo de las minas es perjudicial para la salud. Agrícola (De Re Metálica, 1494) ya hablaba de los efectos perniciosos del polvo inhalado en los mineros. Desde entonces ha ido creciendo el conocimiento sobre los diferentes aspectos del depósito de polvo en los pulmones asociado a una respuesta patológica, que es lo que hoy denominamos neumoconiosis. El sílice, debido a su poder patógeno y a su abundancia en la corteza terrestre, es el principal protagonista en la mayoría de las neumoconiosis, mas no el único. De ahí que con frecuencia el término silicosis se utilice para denominar cualquier neumoconiosis. No obstante, hay tipos de polvo capaces de producir neumoconiosis independientemente de la sílice, como el carbón, o conjuntamente con la misma. Hoy es bien conocido que la relación entre la exposición al polvo inorgánico y los efectos sobre la salud que produce dependen de la dosis acumulada, es decir, de la concentración del polvo en el aire y de la duración de la exposición y también del tiempo de residencia de este polvo en los pulmones. Así mismo se sabe que existe un período de latencia entre el inicio de la exposición y el comienzo de las manifestaciones clínicas que puede ser más o menos largo dependiendo del tipo de neumoconiosis. Así pues, las neumoconiosis son evitables si se puede reducir sustancialmente la cantidad de polvo en el medioambiente de trabajo y la cantidad de polvo que penetra en los pulmones. Los conocimientos actuales sobre la patogenia de la enfermedad y los avances tecnológicos que permiten poner en práctica medidas de control pueden prevenir la progresión de la enfermedad, sobre todo las formas agudas o aceleradas que están asociadas a una mayor exposición a polvo. Por lo tanto, es fundamental la evaluación continua de las condiciones de trabajo y la evaluación periódica de la salud, incluyendo la vigilancia de la misma después de haber cesado la exposición. Teniendo en cuenta estas premisas, el número de neumoconiosis debería ir en disminución. Sin embargo, aunque ha diminuído el número de personas ocupadas en actividades tradicionalmente relacionadas con las neumoconiosis (minería del carbón, fundiciones, etc. ), no es menos cierto que otras actividades extractivas y oficios en los que se trabaja con minerales pueden seguir provocando nuevos casos en el futuro.

DEL TEMA GENERAL AL OBJETO ESPECÍFICO DE INVESTIGACIÓN La neumoconiosis constituye una causa importante de incapacidad permanente. No existen datos actuales de prevalencia global en el país y la información registrada por lugar de trabajo varía de acuerdo a las condiciones ambientales locales. En los últimos 40 años la situación ha mejorado notoriamente ya que existe un mayor control del ambiente laboral. Etiología Se produce por inhalación de polvo de bióxido de sílice (entre otros minerales), que es el principal constituyente de la corteza terrestre (tierra, arena, rocas, cuarzo, etc. ). Su acción sobre el organismo depende de las siguientes variables: 1. - Tamaño de las partículas en suspensión. Las más activas son aquellas que tienen entre 1 y 5 micrones de diámetro. Las mayores se atrapan en las vías aéreas superiores y las menores pasan a la sangre o se vuelven a espirar. 2. - Concentración de partículas en el aire ambiente. Este factor es directamente proporcional a la generación de partículas en las labores e inversamente proporcional a la ventilación del lugar de trabajo. 3. - Tiempo de exposición. El tiempo como factor de riesgo de enfermedad depende de los factores anteriores y de la calidad fisicoquímica del material inhalado. Puede variar desde 3 meses en molinos de cuarzo a más de 30 años en picapedreros. 4. - Factores individuales. Existe una clara diferencia de reacción entre individuos ante el mismo grado de contaminación ambiental. Esto dependería del estado de los mecanismos defensivos de las vías aéreas superiores y de factores inmunológicos y genéticos. Las principales ocupaciones con riesgo silicótico pueden sistematizarse en tres tipos básicos: - Excavaciones mal ventiladas en la corteza terrestre: minas, túneles. - Manipulación de cuarzo y otros materiales silíceos en polvo: fabricación de vidrios, loza, jabones abrasivos, ladrillos refractarios, moldeado de fundiciones, etcétera. - Molienda o pulverización de materiales silíceos: molinos, pulido con chorro de arena, remoción de revestimientos refractarios en hornos, esmerilado, etcétera. Patogenia Las barreras defensivas del aparato respiratorio son capaces de eliminar las partículas de sílice en las cantidades que corrientemente se inhalan en el ambiente general. Cuando la

carga es demasiado grande, muchas partículas llegan a los alvéolos donde son fagocitadas por los macrófagos, algunos de los cuales se introducen al intersticio. Por mecanismos sólo parcialmente precisados, se inicia un proceso reactivo inflamatorio con un componente inmunológico dirigido contra las proteínas del pulmón desnaturalizadas por la sílice. Este último explicaría, en parte, por qué no todos los pacientes con igual exposición desarrollan el mismo grado de reacción. Alrededor de los cristales de sílice se forman granulomas fibrosantes que confluyen formando nodulillos, que se hacen visibles en la radiografía al llegar a 2 mm de diámetro (fibrosis nodular). Si continúa la exposición, los nódulos siguen creciendo y por coalescencia llegan a formar grandes masas fibróticas (fibrosis masiva). Los ganglios regionales también se comprometen y con alguna frecuencia se calcifican en su periferia, dando a rayos el aspecto de "cáscara de huevo". A estas lesiones específicas se agregan grados variables de hipertrofia de las glándulas mucosas (bronquitis crónica) y daño bronquiolar obstructivo y enfisema, en cuyo desarrollo pesarían el hábito tabáquico concomitante y otros factores irritantes del ambiente laboral. Presentación clínica La silicosis puede ser nula o escasamente sintomática, aun en fases moderadamente avanzadas. Los síntomas dependen importantemente del grado de daño bronquial y enfisema que se agreguen, . Son corrientes la tos y expectoración mucosa o mucopurulenta y es frecuente la disnea de esfuerzo progresiva. El paciente puede magnificarla por tratarse de una enfermedad sujeta a indemnización u ocultarla cuando no desea verse obligado a abandonar su trabajo. El examen físico generalmente es negativo en cuanto a la silicosis en sí misma. Pueden constatarse signos del compromiso bronquial y enfisema concomitantes. Diagnóstico La radiografía de tórax es fundamental para el diagnóstico, ya que sus imágenes pueden ser fuertemente sugerentes, por lo cual, en conjunción con los antecedentes laborales, constituyen la base del diagnóstico clínico. Las primeras manifestaciones radiográficas son nodulillos de 1 -2 mm de diámetro, más abundantes en las zonas medias. La progresión se evidencia por aumento de su número y tamaño, así como por la formación de masas irregulares por confluencia. Pueden agregarse elementos inespecíficos de peribronquitis y

enfisema. La TBC es una complicación de alta frecuencia, que puede aparecer como una confluencia más, que llama la atención por su rápida progresión o por desarrollar excavaciones. La tomografía axial computada permite precisar los datos morfológicos ya mencionados en los casos en que la radiografía no sea bien clara. Muy ocasionalmente, la etapa nodular es inaparente, siendo el primer hallazgo una masa fibrótica aislada con aspecto tumoral, llamado silicoma, el que, por falta de una buena encuesta laboral, puede ser rotulado con el diagnóstico erróneo de cáncer. Actualmente, se sigue la nomenclatura descriptiva más compleja de la Organización Internacional del Trabajo, que es de resorte del especialista en medicina ocupacional. El estudio funcional puede ser normal en las fases nodulares, en las que hay gran cantidad de parénquima respetado. Con la confluencia aparecen trastornos de tipo restrictivo. Sin embargo, las alteraciones más frecuentes y más incapacitantes son las obstructivas, derivadas del daño bronquiolar y del enfisema. La legislación indemniza la pérdida de capacidad de ganancia, basada en la etapa radiográfica, complementada con una valoración de la incapacidad funcional. Evolución y complicaciones El ritmo de progresión de la silicosis es variable, siendo más rápida mientras más intensa haya sido la exposición. Se puede observar progresión fuera de riesgo en casos en que se retiran tardíamente en fases más avanzadas, lo que hace importante el diagnóstico precoz. La muerte se produce por insuficiencia respiratoria, cor pulmonale o sobreinfección tuberculosa. Ésta es especialmente frecuente en la silicosis de desarrollo rápido, propia de la exposición masiva. Lo característico es su rebeldía a tratamiento, lo que sugiere que el terreno alterado de estos pacientes en alguna forma protege al bacilo de Koch. Debe sospecharse la tuberculización ante sombras pulmonares con un crecimiento más rápido que el resto y buscarse su confirmación a través del estudio bacteriológico de expectoración. La eliminación de bacilos es generalmente escasa, necesitándose numerosas baciloscopías y cultivos para encontrarlo. Por su gravedad, puede recurrirse al uso de 300 mg diarios de HIN, como quimioprofilaxis, en los casos de mayor riesgo, ya sea por contactos TBC o por presentar silicosis de desarrollo rápido. Profilaxis El saneamiento ambiental es la forma más racional de evitar el problema, pero por su costo su aplicación suele ser parcial e imperfecta en empresas pequeñas. La protección individual con mascarilla resulta práctica sólo en exposiciones cortas, ya que su uso prolongado es mal tolerado. Tratamiento La silicosis en sí misma es irreversible y no tiene tratamiento, pero sí lo tiene el paciente silicótico, cuya calidad de vida puede mejorar considerablemente.

FORMULACIÓN DEL TEMA ESPECÍFICO DE LA INVESTIGACIÓN PLANTEAMIENTO DEL OBJETO ESPECÍFICO DE INVESTIGACIÓN A lo largo de las siete últimas décadas, la Oficina Internacional del Trabajo (OIT) ha fomentado el debate y publicado una serie de directrices sobre cómo clasificar las radiografías de tórax de las personas con neumoconiosis. Sus objetivos eran normalizar los métodos de clasificación y facilitar las comparaciones internacionales de los datos sobre neumoconiosis, las investigaciones epidemiológicas y los informes científicos. Con base en los principios, se refiere a imágenes radiográficas observadas en todos los tipos de neumoconiosis. La OIT inició el proceso de revisión en noviembre de 1989, en una reunión de 11 expertos de 7 países. Se solicitó a los participantes que aconsejaran sobre el tipo de modificaciones que sería deseable realizar en el esquema y que reconsideraran la idoneidad de las radiografías estándar que acompañaban a la edición de 1980. Se decidió que algunas partes de la Guía debían revisarse, pero se hizo hincapié en la importancia de mantener la continuidad en la Clasificación. Teniendo esto en cuenta, se acordó conservar la serie de radiografías estándar distribuidas con la edición de 1980, aunque se admitió que la calidad técnica de muchas de ellas era inferior a la ofrecida por los equipos y técnicas modernos. Los participantes en la reunión señalaron también que resultaría práctico reducir el número de radiografías incluidas en la serie completa de radiografías estándar (22) mediante la reproducción de las partes fundamentales de algunas de ellas en forma de cuadrantes de radiografías completas. Hubo acuerdo, no obstante, en la necesidad de verificar que esta reforma, en sí misma, no modificaría la forma de clasificar las radiografías de las personas expuestas a polvo. Por consiguiente, la OIT y la División de Estudios sobre Enfermedades Respiratorias del Instituto Nacional de Seguridad y Salud Ocupacional de los Estados Unidos (Division of Respiratory Disease Studies of the United States National Institute for Occupational Safety and Health (NIOSH)) organizaron un ensayo controlado. Participaron 40 médicos que trabajaban en clínicas y centros de investigación especializados de 10 países. Los resultados del ensayo demostraron que la modificación propuesta para las radiografías estándar de la OIT, consistente en reproducir secciones de 15 de las radiografías estándar

de la OIT (1980) en 5 nuevas radiografías de «cuadrantes» , no aumentaría la variabilidad entre lectores y quizá mejorara en algunos aspectos la reproducibilidad de la clasificación de la profusión de opacidades pequeñas, pero podría también reducir ligeramente la frecuencia con la que algunos lectores identifican las opacidades de gran tamaño. El uso de series de radiografías estándar que comprendían las radiografías de cuadrantes se asoció a un aumento de la frecuencia con la que algunos lectores describieron la forma de las pequeñas opacidades que veían como predominantemente irregulares, en lugar de redondeadas. Se concluyó, no obstante, que los efectos observados probablemente fueran indistinguibles de la variabilidad entre lectores e intralector en la mayoría de los estudios de salud laboral. En octubre de 1997, más de 200 participantes en la Novena Conferencia Internacional sobre Enfermedades Respiratorias Profesionales, celebrada en la ciudad japonesa de Kyoto, asistieron a un Grupo de Trabajo sobre la Clasificación convocado por la OIT. En esta reunión se recomendó profundizar en la preparación de radiografías compuestas por cuadrantes o secciones y en mejores técnicas para reproducir las radiografías estándar antes de incorporar las revisadas. Un grupo más reducido de expertos asistentes a esta misma Conferencia analizó detalladamente un borrador del texto revisado de la Guía para la Clasificación. El debate sobre el borrador prosiguió en una reunión celebrada en marzo de 1998 en la sede del American College of Radiology (ACR) en Reston (Virginia) y concluyó el 26 de octubre del 2000 en la Oficina de la OIT en los Estados Unidos, en Washington, D. C. Los participantes en esta última reunión compararon también dos clases de copias nuevas de varias series de radiografías estándar de la OIT (1980), de radiografías de cuadrantes utilizadas en el ensayo internacional y de una nueva radiografía compuesta para ilustrar las anormalidades pleurales. Estas copias nuevas sometidas a revisión se obtuvieron de copias anteriores por métodos convencionales de copiado de película y por técnicas mejoradas a partir de versiones digitalizadas de las copias iniciales. Los expertos prefirieron las copias obtenidas a partir de versiones digitalizadas y recomendaron utilizar esta tecnología y el proceso de reproducción asociado para generar las futuras copias de las radiografías estándar de la OIT. La Clasificación Internacional de la OIT (2000) de Radiografías de Neumoconiosis se acompaña de dos series de radiografías estándar. Ambas pueden solicitarse a la OIT. La primera serie ( «Serie Completa» ) consta de 22 radiografías. Veinte de ellas son copias nuevas obtenidas a partir de radiografías estándar de tamaño completo digitalizadas, distribuidas con la edición de 1980 de la Clasificación de la OIT. Una radiografía adicional ilustra las opacidades irregulares de tamaño u/u. Tres cuadrantes de esta radiografía reproducen las secciones de la radiografía compuesta utilizada en 1980 para ilustrar la profusión creciente de opacidades irregulares de tamaño u/u; el cuarto cuadrante ilustra la subcategoría 0/0. Se incorpora una nueva radiografía compuesta para ilustrar las anormalidades pleurales. La «Serie de Cuadrantes» consta de 14 radiografías. Nueve de ellas son las radiografías estándar más utilizadas de la Serie Completa. Las otras cinco reproducen secciones (cuadrantes) de las restantes radiografías de la Serie Completa.

Metodología 1. - Calidad de cine: En el sistema actual de clasificación de la OIT, el lector se pregunta primero a la calidad cinematográfica de grado. Hay cuatro grados técnico: bueno, aceptable, sin defectos técnicos que puedan poner en peligro la clasificación; aceptable, con algún defecto técnico, pero sigue siendo adecuada, y no aceptable. Defectos de calidad incluyen sobre o subexposición, presión baja, los artefactos, la colocación incorrecta, y otros. 2. -Las anormalidades del parénquima: Opacidades pequeñas: El lector categorizar pequeñas opacidades de acuerdo con su forma y tamaño. Las pequeñas opacidades redondeadas son p, q, r. Pequeños, opacidades irregulares se clasifican por anchura que s, t, u o. Zonas de pulmón: Cada pulmón se divide mentalmente por el lector en 3 zonas equidistantes: superior, medio e inferior. Las zonas en las que aparecen las pequeñas opacidades parenquimatosas se registran. Profusión: El uso de los rayos X estándar, la profusión de opacidades pequeñas se clasifica en una escala de las principales categorías de 4 puntos, con cada categoría principal se divide en tres, dando 12 subcategorías ordenadas de aumentar profusión: 0/-, 0/0, 0/1, 1/0, 1/1, 1/2, 2/1, 2/2, 2/3, 3/2, 3/3, y 3/+. Categoría 0 se refiere a la ausencia de pequeña opacidad y la categoría 3 representa la más profusa. La categoría principal representa la profusión sentía para adaptarse mejor a la película tema, y la categoría de menores representa la profusión considerado seriamente como una alternativa. Grande opacidades: Una gran opacidad se define como cualquier opacidad mayor que 1 cm de diámetro. Se clasifican en la categoría A, categoría B o la categoría C. 3. -Anomalías pleurales: Anomalías pleurales se presentan con respecto al tipo, la ubicación, la presencia de calcificación, anchura y extensión. 4. -Cualquier otra anomalía: Hay 29 símbolos "obligatorio" que representan aspectos importantes relacionados con las enfermedades de polvo de los pulmones y otras etiologías. Estos símbolos son: aa aorta aterosclerótica, al significativo engrosamiento pleural apical; ax coalescencia de pequeñas opacidades; bu bulla; cáncer de ca; cg granuloma calcificado o de los ganglios linfáticos; cn calcificación de pequeñas opacidades neumoconióticas; co forma cardiaco anormal o tamaño; cp cor pulmonale ; cavidad cv; di marcada distorsión de una estructura intratorácica, ef derrame pleural, em enfisema; calcificación es la cáscara de huevo, fr fractura de costilla, la ampliación de la hi linfáticos hiliares no calcificadas; ho panal de abeja; Identificación frontera diafragma no bien definida; ih mal definidos borde del corazón, las líneas septales kl; me mesotelioma. atelectasia placa pa, pb bandas parenquimatosas; pi engrosamiento pleural de una fisura interlobar; px neumotórax; ra redondeado atelectasia; rp neumoconiosis reumatoide, tuberculosis tb, y otras enfermedades od o anomalía significativa. Por último, los comentarios de los lectores sobre otras características anormales de la radiografía de tórax o de otro tipo pertinente último, los comentarios de los lectores sobre otras características anormales de la radiografía de tórax o de otra información pertinente

Pruebas de Función Pulmonar Son elementos de apoyo diagnóstico dentro de los cuales los más utilizados son: la espirometría, test de provocación con metacolina o ejercicio, y test de difusión con monóxido de carbono. Otros examenes de uso menos frecuentes son la medición de volumenes pulmonares (ej. : pletismografía), presiones respiratorias máximas y oximetría de pulso. ESPIROMETRÍA La espirometría es la prueba más accesible y reproducible para evaluar la mecánica de la respiración. Mide la cantidad de aire que un sujeto es capaz de desplazar (inhalar o exhalar) de manera forzada en función del tiempo, lo que depende del calibre de los bronquios, de las propiedades elásticas del tórax y de los pulmones, así como de la integridad de los músculos respiratorios. Las principales mediciones de la espirometría son la capacidad vital forzada (CVF), el volumen espiratorio forzado en el primer segundo (VEF 1) y el cociente VEF 1/CVF. La CVF es el mayor volumen de aire, medido en litros (L), que se puede exhalar por la boca con máximo esfuerzo después de una inspiración máxima. El VEF 1 es el volumen de aire exhalado durante el primer segundo de la maniobra de CVF. El cociente VEF 1/CVF es la proporción de la CVF exhalada en el primer segundo de la maniobra de CVF. La espirometría es el estándar de oro para medir la obstrucción bronquial y, por lo tanto, es de utilidad en el diagnóstico y seguimiento de diversas enfermedades respiratorias, como el asma o la enfermedad pulmonar obstructiva crónica (EPOC), entre otras. La espirometría permite también evaluar la respuesta a broncodilatadores o a estímulos que inducen obstrucción bronquial (ejercicio, metacolina, etc). La prueba es útil en el seguimiento de exposiciones laborales que pudieran afectar la función pulmonar, en la valoración del riesgo operatorio, para dictaminar incapacidad o impedimento y con fines de pronóstico. La restricción pulmonar no puede ser diagnosticada con precisión mediante una espirometría ya que ésta no permite medir el volumen residual (VR). A pesar de esta limitación, una vez diagnosticada apropiadamente la restricción pulmonar por los métodos adecuados (pletismografía corporal), la espirometría es de utilidad en el seguimiento de los pacientes con enfermedades restrictivas. Existen algunas contraindicaciones relativas para la realización de la espirometría dentro de las que se incluyen: enfermedad cardiovascular aguda o descompensada en los últimos tres meses (infarto agudo del miocardio, insuficiencia cardiaca, enfermedad cerebrovascular), neumotórax en los noventa días previos, riesgo de hemoptisis o ruptura de aneurisma, cirugía de tórax, abdomen, ojos u oídos en los últimos tres meses, infecciones respiratorias agudas en las últimas dos semanas, tuberculosis pulmonar activa y embarazo avanzado o complicado. La espirometría no debe ser solicitada en pacientes con traqueotomía o sonda pleural ya que los resultados que se obtendrán no serán confiables. Antes de interpretar la prueba hay que verificar que exista la información suficiente para evaluar la calidad de la misma. Esta información incluye: nombre del paciente, datos generales (edad, género, peso y estatura), origen de los valores de referencia, los valores (CVF, VEF 1/CVF) de tres maniobras aceptables y las tres gráficas de volumen-tiempo y flujovolumen. Otros parámetros opcionales son la fecha de la última calibración, datos ambientales y algoritmo de interpretación.

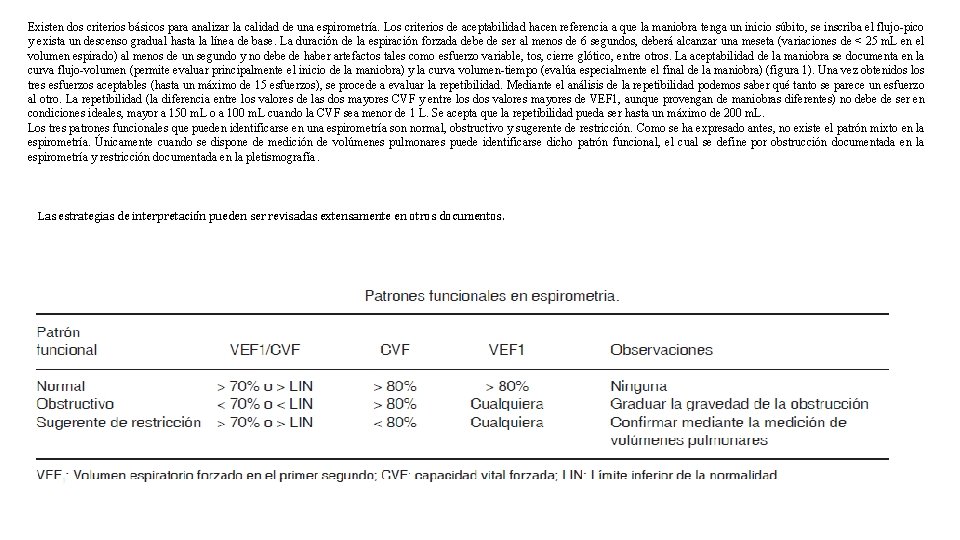
Existen dos criterios básicos para analizar la calidad de una espirometría. Los criterios de aceptabilidad hacen referencia a que la maniobra tenga un inicio súbito, se inscriba el flujo-pico y exista un descenso gradual hasta la línea de base. La duración de la espiración forzada debe de ser al menos de 6 segundos, deberá alcanzar una meseta (variaciones de < 25 m. L en el volumen espirado) al menos de un segundo y no debe de haber artefactos tales como esfuerzo variable, tos, cierre glótico, entre otros. La aceptabilidad de la maniobra se documenta en la curva flujo-volumen (permite evaluar principalmente el inicio de la maniobra) y la curva volumen-tiempo (evalúa especialmente el final de la maniobra) (figura 1). Una vez obtenidos los tres esfuerzos aceptables (hasta un máximo de 15 esfuerzos), se procede a evaluar la repetibilidad. Mediante el análisis de la repetibilidad podemos saber qué tanto se parece un esfuerzo al otro. La repetibilidad (la diferencia entre los valores de las dos mayores CVF y entre los dos valores mayores de VEF 1, aunque provengan de maniobras diferentes) no debe de ser en condiciones ideales, mayor a 150 m. L o a 100 m. L cuando la CVF sea menor de 1 L. Se acepta que la repetibilidad pueda ser hasta un máximo de 200 m. L. Los tres patrones funcionales que pueden identificarse en una espirometría son normal, obstructivo y sugerente de restricción. Como se ha expresado antes, no existe el patrón mixto en la espirometría. Únicamente cuando se dispone de medición de volúmenes pulmonares puede identificarse dicho patrón funcional, el cual se define por obstrucción documentada en la espirometría y restricción documentada en la pletismografía. Las estrategias de interpretación pueden ser revisadas extensamente en otros documentos.

DIFUSIÓN PULMONAR DE MONÓXIDO DE CARBONO CON RESPIRACIÓN ÚNICA La difusión pulmonar de monóxido de carbono (DLCO) es una prueba de intercambio gaseoso que permite evaluar el proceso de transferencia de oxígeno, desde el gas alveolar hasta su unión con la hemoglobina contendida en los glóbulos rojos. Para tal fin, el oxígeno debe cruzar la pared alveolar, la pared del capilar, el plasma, la membrana del eritrocito y finalmente unirse a la hemoglobina. La cantidad de oxígeno que puede ser transferido del gas alveolar hasta su unión con la hemoglobina está determinado por tres factores principales: el área de la membrana alveolocapilar; el grosor de la misma, y el gradiente de presión de oxígeno entre el gas alveolar y la sangre venosa. La medición de la capacidad de DLCO es simple y es una estimación válida de la capacidad de difusión de oxígeno. Así, la ecuación de DLCO podría ser expresada como DLCO = A x � PCO/G, donde DLCO es la capacidad de difusión de monóxido de carbono, A es el área, � PCO es la diferencia de presiones de monóxido de carbono entre el gas alveolar y la sangre venosa y G es el grosor de la membrana alveolocapilar. Al igual que para otras PFR, la utilidad de esta prueba es muy amplia pues sirve como prueba complementaria de diagnóstico para dar seguimiento y evaluar la respuesta terapéutica. Esta prueba, junto con una de mecánica pulmonar (espirometría simple o con broncodilatador) y con una dinámica (C 6 M), son las pruebas iniciales en la evaluación de la mayoría de los pacientes con enfermedad respiratoria. Cualquier paciente en quien sea necesario evaluar el intercambio de gases en estado de reposo, es candidato a realizar esta prueba; pero es más relevante en las enfermedades que suelen afectar inicialmente el intercambio y no la mecánica pulmonar tales como las enfermedades intersticiales de pulmón o enfermedades de la circulación pulmonar. Aunque no existen contraindicaciones absolutas para su realización, los sujetos que utilizan oxígeno suplementario no son buenos candidatos ya que es necesario suspender el oxígeno por lo menos 5 minutos antes de la prueba, lo cual no siempre es posible. Existen varios métodos para medir la tasa de transferencia de monóxido de carbono (CO) o DLCO. La técnica de respiración única (DLCOsb) es la más utilizada. Se requiere de un equipo especializado que hasta hace algunos años tenía la desventaja de ser poco portátil y prácticamente exclusivo de los laboratorios de función pulmonar. Sin embargo, recién se ha desarrollado tecnología que permite que este dispositivo sea de gran portabilidad y su manejo sumamente amigable. Para llevar a cabo la prueba de DLCOsb se utiliza una mezcla especial de gases (CO al 0. 03%, helio al 8%, oxígeno al 21% y nitrógeno para balancear la mezcla). El resultado es expresado en m. L de CO/min/mm. Hg. La maniobra que el enfermo debe realizar consiste en respiraciones a VC estable seguido de una espiración hasta VR, posteriormente, la realización de una inspiración completa. Una vez que el técnico está seguro de haber conseguido ésta, le pide al sujeto que haga una apnea de 10 segundos (tiempo durante el cual se distribuye y homogeniza la mezcla de gases en los espacios alveolares), y que finalmente lleve a cabo, otra vez, una espiración completa (figura 4). Es al inicio de la maniobra espiratoria que el analizador de gases realiza las mediciones de las concentraciones de CO exhalado. Deberán obtenerse al menos dos maniobras aceptables y repetibles entre los mejores valores de DLCO. Se permite un máximo de cuatro maniobras con un tiempo mínimo entre cada una de ellas de 4 minutos. Para considerar una prueba repetible es necesario que las mediciones de DLCO no difieran en más de tres unidades. Los resultados de DLCO obtenidos deberán ajustarse por la altitud del lugar en el que se realizó la prueba (en la Ciudad de México el factor de corrección es de 0. 87), así como por la concentración de hemoglobina. Para la interpretación de la prueba es necesario obtener el promedio de dos maniobras aceptables y repetibles. Desde un punto de vista práctico, la DLco disminuye en enfermedades que afectan a alguno de los componentes de la ecuación (DLCO = A x � PCO/G; ver arriba); p. ej. , si disminuye A como sucede en el enfisema o en pacientes con resecciones pulmonares, disminuye la DLCO; de manera inversa, si se incrementa G como sucede en las enfermedades del intersticio pulmonar, disminuye la DLCO. En diversas enfermedades, especialmente las de tipo intersticial, las alteraciones en el intercambio de gases (en este caso evaluado mediante DLCO) preceden a las alteraciones en la mecánica de la respiración (espirometría o pletismografía). La DLCO también puede estar incrementada, lo anterior se observa en pacientes con hemorragia pulmonar o asma.

JUSTIFICACIÓN DEL OBJETO DE INVESTIGACIÓN Como ya se comentó, la Clasificación OIT es un sistema de clasificación de radiografías para las personas con neumoconiosis. La intención es proporcionar un medio para describir y registrar sistemáticamente las anormalidades radiográficas en el tórax provocada por la inhalación de polvos. En 1974, después de los estudios de los programas de vigilancia de los mineros del carbón reveló grados inaceptables de variabilidad “interreader”, el Instituto Nacional para la Seguridad y Salud Ocupacional, que comenzó el programa lector de "B", con la intención de capacitar y certificar a los médicos en el sistema de clasificación de la OIT. El examen de certificación lector "B" entró en pleno funcionamiento en 1978. Un médico debe aprobar el examen de certificación para ser un lector de "B". El sistema de clasificación de la OIT incluye las Directrices impresos y dos juegos de radiografías estándar. El lector compara la radiografía sujeta el pecho con los del conjunto estándar. Las películas estándar proporcionan diferentes tipos y la gravedad de las anomalías observadas en las personas con neumoconiosis, incluyendo Neumoconiosis del minero, la silicosis y la asbestosis. El lector se clasifica la película objeto, a menudo el registro de los resultados en el formulario de interpretación radiográfico NIOSH. El sistema de clasificación de la OIT se refiere a las anormalidades del parénquima pulmonar, cambios pleurales y otras características asociadas, o confundido a veces, con enfermedad pulmonar ocupacional. El "juego completo" de películas estándar consta de 22 radiografías: dos ilustra profusión normal, quince de diferentes categoría de profusión y forma/tamaño de pequeña opacidad, que ilustra tres gran opacidad, una de "U" de tamaño pequeño opacidad, y uno de varios anormalidades pleurales. El "Quad Set" se compone de 14 radiografías, nueve de los estándares más utilizados de la serie completa, además de cinco reproducciones compuestos adicionales de las secciones de cuadrante de las otras radiografías en el juego completo. Ambos juegos son nuevos y coinciden con las nuevas directrices de la OIT. Ante la evidencia de la variabilidad que se ha presentado “usuario dependiente” al realizar una lectura, la poca practicidad al realizar el análisis y la descripción de la misma, aunado al avanze de la tecnología como auxiliar en el diagnóstico oportuno de padecimientos; surge el planteamiento del presente protocolo analizando mediante un modelo de Pruebas Diagnósticas, la utilidad actual del uso de Pruebas de Función Pulmonar, especificamente de Espirometría y DLCO frente al resultado obtenido de la lectura de radiografías con el método de la OIT, en trabajadores expuestos a factores de riesgo para desarrollar Neumoconiosis. En adición a esto, y sabiendo que las imágenes radiográficas y clínica se presentan bajo un periodo de latencia retardado, obtener pruebas funcionales compatibles con dichos procesos de manera oportuna con lo que el pronóstico y la calidad de vida del trabajador podrían mejorar sustancialmente.

PREGUNTA DE INVESTIGACIÓN Derivadas del planteamiento del objeto específico de investigación que nos ocupa, así como de la justificación de la misma investigación se derivan las siguiente interrogante: ¿CUAL ES LA UTILIDAD DE LA ESPIROMETRIA MAS DLCO PARA EL DIAGNÓSTICO OPORTUNO DE NEUMOCONIOSIS VS. TABLAS RADIOGRAFICAS DE LA OIT? OBJETIVOS DE INVESTIGACIÓN Objetivo General: Analizar mediante un modelo de Pruebas Diagnósticas, la utilidad actual del uso de Pruebas de Función Pulmonar, especificamente de Espirometría + DLCO frente al resultado obtenido de la lectura de radiografías con el método de la OIT, en trabajadores expuestos a factores de riesgo para desarrollar Neumoconiosis. Objetivos Específico: Analizar pruebas funcionales pulmonares compatibles con dichos procesos de manera oportuna previa a la presentación de patrones radiográficos. Demostrar que la Espirometría + DLCO son pruebas diagnósticas al alcanze del médico operativo, no invasiva, con pocas contraindicaciones y con la suficiente sensibilidad y especificidad para diagnosticar oportunamente Neumoconiosis con lo que el pronóstico y la calidad de vida del trabajador mejorarán. HIPOTESIS La Espirometría + DLCO son pruebas diagnósticas al alcanze del médico operativo, no invasiva, con pocas contraindicaciones y con la suficiente sensibilidad y especificidad para diagnosticar oportunamente Neumoconiosis en comparación al Gold Standard actual que son las radiografías interpretadas con el método de la OIT; con lo que el pronóstico y la calidad de vida del trabajador será mejor.

VIABILIDAD DE LA INVESTIGACIÓN En toda investigación, es fundamental comprender las limitantes y potencialidades que se tiene para desarrollar los objetivos de manera clara. El lugar donde se localiza el objeto de investigación cuenta con muestra suficiente de estudio, accesibilidad, tanto de comunicación como vías de movilidad así como equipo de cómputo; se cuenta con el apoyo del asesor y del Instituto Mexicano del Seguro Social para utilizar el laboratorio de Fisiología Pulmonar para realizar los estudios necesarios, así como el tiempo adecuado para llevarlo a cabo. Por lo que insertarse en dicho contexto es plausible. El material de la presente investigación, financiamiento y gastos correrán a cargo del investigador. Se contará, además con la participación de asesores especialistas en neumología y fisiología pulmonar con enfoque laboral.