USAGE THRAPEUTIQUE DES OPIODES Aude FERRAN 2020 Les











































- Slides: 54

USAGE THÉRAPEUTIQUE DES OPIOÏDES Aude FERRAN 2020

• Les récepteurs aux opioïdes sont A. Alpha, beta, gamma B. Delta, Mu, kappa C. À 7 domaines transmembranaires D. Des canaux ioniques

• La buprénorphine est Plus puissante que la morphine B. Plus efficace que la morphine C. Un agoniste des récepteurs mu D. Mydriatique chez le chat A.

• Le butorphanol est A. Plus analgésique sédatif B. Plus sédatif qu’analgésique C. Un agoniste des récepteurs mu D. Utilisable seul en tant qu’analgésique

• Le tramadol est A. Un agoniste des récepteurs mu B. Un bon analgésique C. Utilisable par voie orale chez le chien D. Un opioïde bien toléré

• Lors d’une association de buprénorphine et de morphine, vous verrez L’effet analgésique cumulatif des 2 molécules B. L’effet analgésique de la buprénorphine C. L’effet analgésique de la morphine D. Aucun effet analgésique A.

Plan • Rappels : physiologie de la douleur • Mode d’action des opioïdes • Effets thérapeutiques et indésirables des opioïdes • Particularités des différents opioïdes • morphine • Fentanyl • Méthadone • Buprénorphine • butorphanol • Tramadol • (Apomorphine) • Points particuliers chez le chat et le cheval • Antagonistes des récepteurs aux opioïdes • Interactions médicamenteuses

Opioïdes • Opioïdes = • opiacés dérivés de l’opium issu du pavot • + molécules synthétiques qui se lient aux récepteurs aux opioïdes (fentanyl, meperidine, …) • Opioïdes endogènes : • Endomorphine= Récepteurs mu • Enképhalines = Récepteurs delta • Dynorphine = Récepteurs kappa

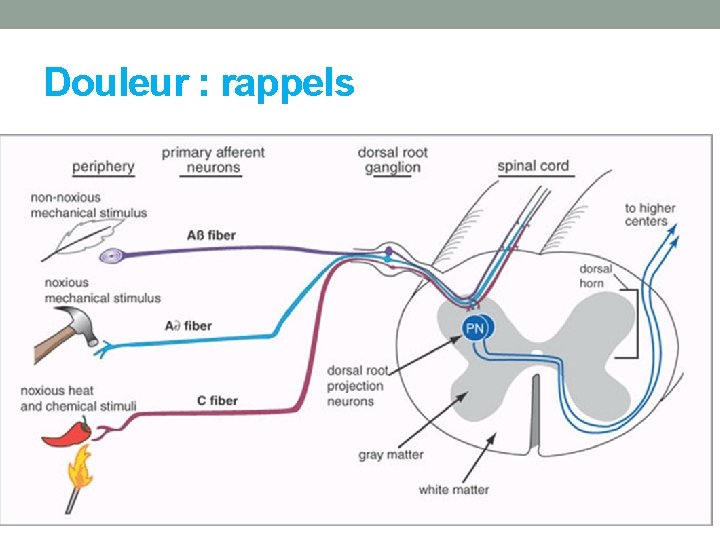
Douleur : rappels

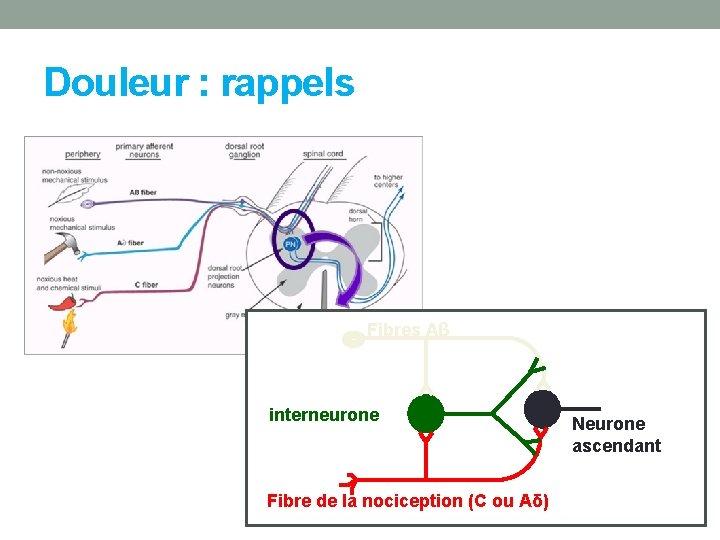
Douleur : rappels Fibres Aβ interneurone Fibre de la nociception (C ou Aδ) Neurone ascendant

Douleur : rappels • Synapses dans corne dorsale de la moelle épinière • Neurotransmetteurs au niveau de la corne dorsale • glutamate (voie rapide) et • substance P (en plus de glutamate dans la voie lente) = douleur lente et chronique • Récepteurs post-synaptiques • AMPA ionotropique (Na+) • NMDA ionotropique (Ca 2+) activés seulement si la fibre est dépolarisée de manière persistante

Douleur

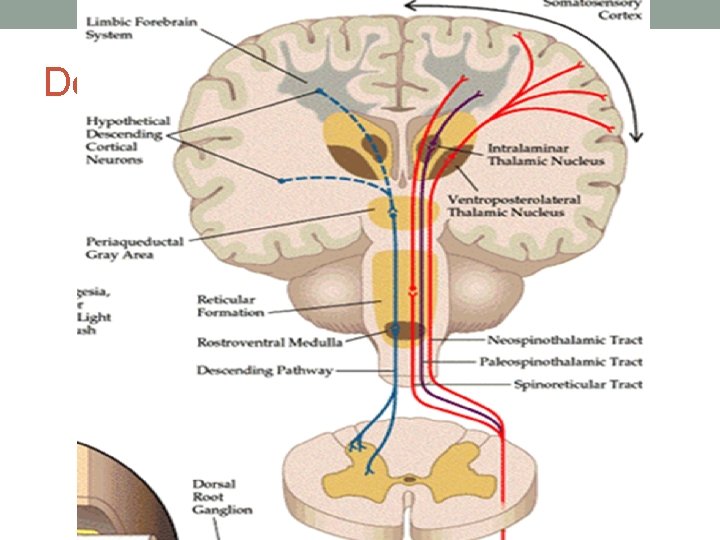
Douleur : rappels • Voies descendantes inhibitrices • Inhibition de la douleur • Origine : • Substance grise périaqueducale • Locus cœruleus • Neurotransmetteurs : • sérotonine • noradrénaline • opioïdes endogènes • glycine • GABA

Récepteurs aux opioïdes • Récepteurs • Situés au niveau de la corne dorsale de moelle épinière et cerveau (thalamus, cortex, matière grise périaqueducale) • Récepteurs couplés à la protéine G 3 types de récepteurs • Mu • Kappa • Delta

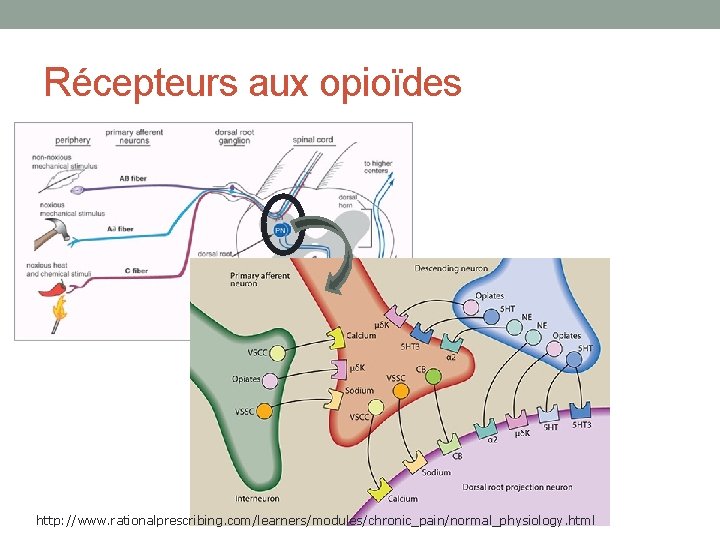
Récepteurs aux opioïdes http: //www. rationalprescribing. com/learners/modules/chronic_pain/normal_physiology. html

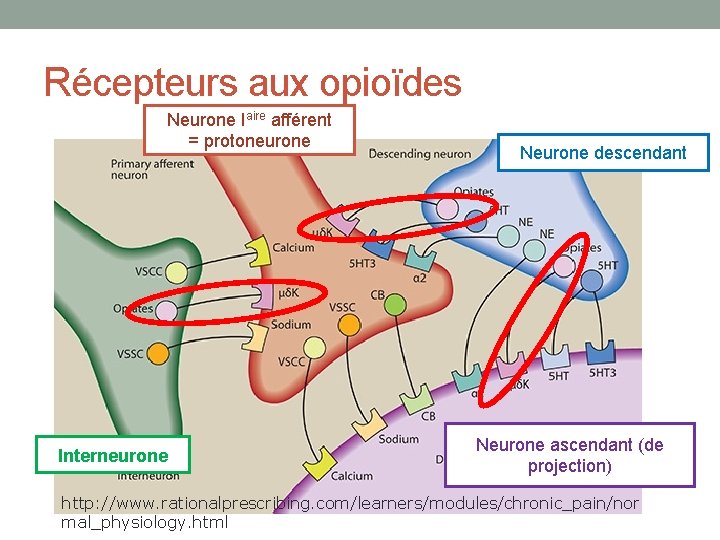
Récepteurs aux opioïdes Neurone Iaire afférent = protoneurone Interneurone Neurone descendant Neurone ascendant (de projection) http: //www. rationalprescribing. com/learners/modules/chronic_pain/nor mal_physiology. html

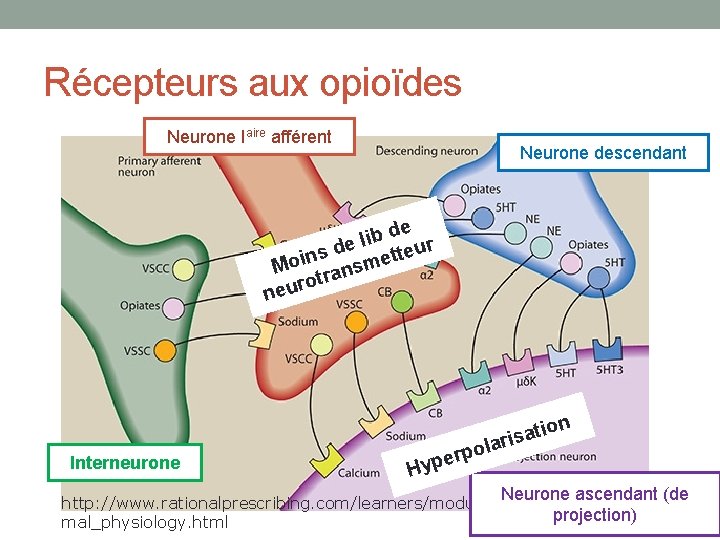
Récepteurs aux opioïdes • La liaison d’un agoniste à un récepteurs aux opioïdes • inhibe l’entrée de Ca 2+ dans le neurone présynaptique (pas de libération de neurotransmetteur) • Favorise la sortie de K+ dans le neurone postsynaptique (hyperpolarisation)

Récepteurs aux opioïdes Neurone Iaire afférent Neurone descendant de b i l r de u e s t t n Moi ransme rot u e n Interneurone on i t a laris o erp p y H Neurone ascendant (de http: //www. rationalprescribing. com/learners/modules/chronic_pain/nor projection) mal_physiology. html

Opioïdes • Effets lors de fixation d’un agoniste sur les récepteurs opioïdes • Mu : analgésie, myosis (Mydriase chat), euphorie, dépression respiratoire, dépendance • Kappa : sédation, analgésie, myosis (Mydriase chat) • Delta : analgésie, dépendance En fonction de l’affinité d’une molécule pour l’un ou l’autre des récepteurs, les effets seront différents

Pharmacocinétique • Caractéristiques générales des opioïdes • Demi-vie courte : Doses répétées ou perfusion (CRI) • Faible biodisponibilité par voie orale : premier passage hépatique souvent important • Bases faibles très lipophiles = diffusion facile au SNC

Usage thérapeutique des opioïdes • Analgésie • Sédation (en combinaison avec des anesthésiques) • Antitussif

Opioïdes / analgésie • Analgésie • Inhibition de la transmission des stimuli nociceptifs à l’encéphale • Plus importante pour des douleurs aigues que chroniques Le niveau d’analgésie possible dépend de la dose et de la molécule

Opioïdes/ sédation • Utilisation en combinaison (souvent avec des alpha-2 agonistes) • Diminution des doses • Diminution des effets indésirables • Moins de sédation chez le chat que chez le chien

Opioïdes / effets • Antitussif • Inhibition du centre de la toux par liaison d’agonistes aux récepteurs mu et kappa • Remarque : Codeine (Bronchocanis. ND) (fixation à Mu ou autres Récepteurs? ) EFFET PEU CERTAIN

Opioïdes / effets • Hémodynamique/cardiovasculaire • Très peu d’effets • Bradycardie • Vasodilatation : Ne pas utiliser si œdème cérébral • Libération d’histamine après bolus IV de morphine (surtout chez le chien) : risque d’hypotension, prurit, … • Fentanyl est le plus sûr si animal instable • Respiratoire • Dépression respiratoire due à une absence de réponse à une augmentation de la PCO 2

Opioïdes / effets • Vomissements • Stimulation de CRTZ et des récepteurs dopaminergiques D 2 • Vomissements après 1ère dose puis cessent souvent. • Vomissements moins fréquents lors de sédation car moins d’action sur le centre du vomissement • Morphine CT+++ Remarque : Apomorphine

Opioïdes / effets • Motilité intestinale • Récepteurs mu dans le plexus sous-muqueux et myentériques • Diminution de la motilité et des sécrétions. • Souvent, l’animal défèque après la première administration puis constipation quasi-systématique (possibilité d’ajouter des laxatifs chez le chien et le chat) • Diminution de la vitesse de vidange gastrique • Retard d’absorption des médications administrées par voie orale Remarque Lopéramide et diphenoxylate • substrats de Pgp et n’atteignent pas le SNC

Opioïdes / effets • Urinaire • Agonistes des récepteurs mu : action antidiurétique par augmentation du tonus du sphincter • Tendance à la rétention d’urine • Agonistes des récepteurs kappa : action diurétique

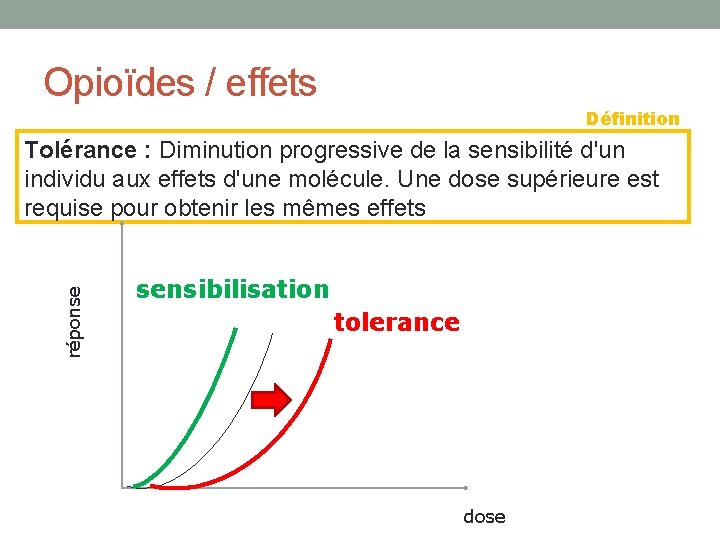
Opioïdes / effets Définition réponse Tolérance : Diminution progressive de la sensibilité d'un individu aux effets d'une molécule. Une dose supérieure est requise pour obtenir les mêmes effets sensibilisation tolerance dose

Opioïdes / effets Définition • Dépendance : envie répétée et irrépressible de reprendre le médicament. RARE en médecine vétérinaire car la plupart des usages sont courts • Se manifeste par un syndrome de sevrage (agitation, tremblements, diarrhée, vomissements) qui est possible lors • du retrait d’un agoniste des récepteurs mu ou • d’ajout d’un antagoniste mu Interactions entre opioïdes

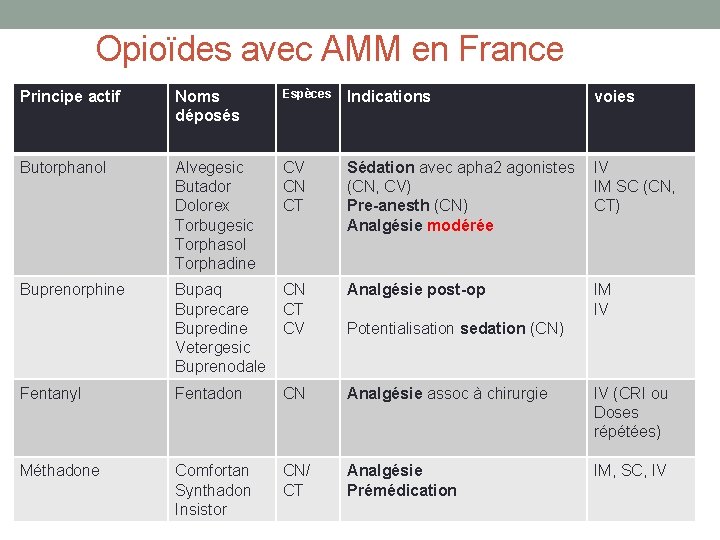
Opioïdes avec AMM en France Principe actif Noms déposés Espèces Indications voies Butorphanol Alvegesic Butador Dolorex Torbugesic Torphasol Torphadine CV CN CT Sédation avec apha 2 agonistes (CN, CV) Pre-anesth (CN) Analgésie modérée IV IM SC (CN, CT) Buprenorphine Bupaq Buprecare Bupredine Vetergesic Buprenodale CN CT CV Analgésie post-op IM IV Fentanyl Fentadon CN Analgésie assoc à chirurgie IV (CRI ou Doses répétées) Méthadone Comfortan Synthadon Insistor CN/ CT Analgésie Prémédication IM, SC, IV Potentialisation sedation (CN)

Morphine hors AMM • Agoniste sur les Rr mu +++ et kappa + • Analgésie dose-dépendante • Libération massive d’histamine après bolus IV chez le chien (ATTENTION hypotension) • Dépression respiratoire • Vomissement

Fentanyl • Agoniste sur les Rr mu • Très puissant • Analgésie dose-dépendante • Demi-vie très courte : administration en perfusion AMM) • Adaptation de la dose à la demande • Très sûr d’emploi (solution transdermique ou patch hors

Fentanyl • Patchs hors AMM • Sur 6 chats, 2 chats ont eu des concentrations de fentanyl non détectables (Lee et al; 2000 AJVR) • Sur 6 chevaux (3 patchs/cv), 2 ont eu des concentrations de fentanyl non détectables (orsini et al. 2006 J Vet pharmaco Ther) • Délai avant efficacité d’au moins 18 h • Solution transdermique chien (AMM retirée) • A appliquer 4 h avant chirurgie, effets pendant 4 j (d’après RCP) Mais concentrations à 4 h = 0. 92± 1. 02 ng/m. L!! (40 beagles) (Freise et al. 2012 J Vet Pharmaco Ther) Grande variabilité inter-individuelle Suivi obligatoire de la douleur chez l’animal traité

Methadone • Agoniste sur les Rr Mu • Antagoniste NMDA • Prévient la recapture de 5 HT et noradrénaline Effets multiples par rapport aux autres opioïdes qui permettraient une utilisation dans les douleurs chroniques • Demi-vie assez longue : 10 h CN (jusqu’à 4 h d’effet analgésique) Remarque Méthadone est commercialisée sous forme d’un mélange racémique L- méthadone et D- méthadone L-méthadone est 8 à 50 fois plus puissant

Methadone • Très bonne analgésie chirurgicale • OK pour Castration/ ovariohysterectomie CT (Slingsby et al. 2014 J feline Med and Surg) • Meilleure analgésie que buprénorphine pour chirurgie orthopédique CN (Hunt et al. 2013 J Small Anl Practice) • Sédation • Moins de vomissement et de sédation que morphine

Methadone • Diminution FC suivie d’une augmentation persistante de la résistance vasculaire (similaire à alpha-2 agonistes)

Buprénorphine • Agoniste partiel à forte affinité sur les Rr mu • Moins de vomissement • moins de dysphorie • moins de dépendance qu’avec la morphine • Antagoniste sur les Rr kappa • Demi-vie plus longue que la morphine • Possibilité de voie transmuqueuse

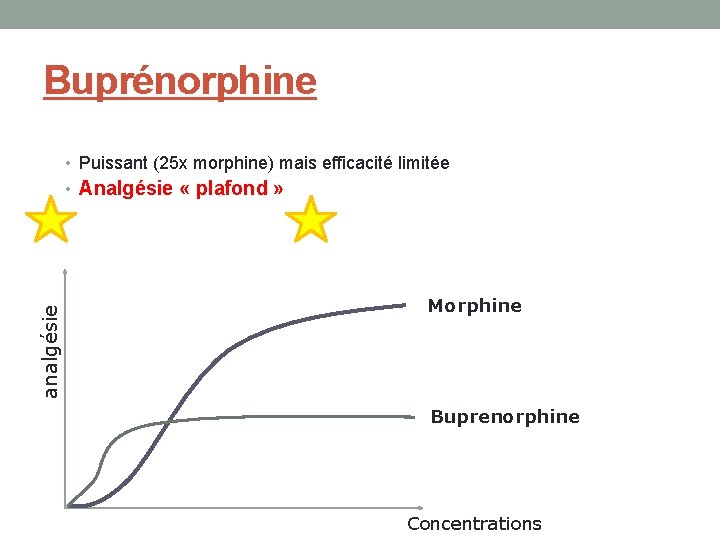
Buprénorphine • Puissant (25 x morphine) mais efficacité limitée analgésie • Analgésie « plafond » Morphine Buprenorphine Concentrations

Butorphanol • Agoniste sur les Rr kappa • Antagoniste ou agoniste partiel sur les Rr mu Possibilité de reverser une dépression respiratoire induite par la morphine en maintenant une légère analgésie sur kappa. • Puissant (5 à 7 x morphine) mais efficacité limitée • Effet court (t 1/2 cheval = 44 min, chien = 1. 5 h) • Diurétique (inhibition de la libération d’ADH)

Butorphanol • Analgésie « plafond » • Sédation à des doses inférieures à l’analgésie = NE PAS CONFONDRE SEDATION ET ANALGESIE • Cheval - Pas de différence avec placebo dans douleur post-castration (Love et al. 2009 Equine vet J) - Moins bonne analgésie post-op (0. 02 -0. 1 mg/kg) que buprenorphine (5 à 10 µg/kg) (Taylor et al. 2015 Equine vet J) - Moins bonne analgésie sur synovite (0. 1 mg/kg) que morphine et methadone (carregaro et al. 2014 BMC vet research) - Aucun effet sur les coliques JOCHLE 1989 • Chat - Analgésie insuffisante pour ovariohysterectomie (contrairement à buprénorphine) (Warne 2014 JAVMA)

Butorphanol • Augmente la pression artérielle pulmonaire et le travail cardiaque Ne pas administrer lors d’insuffisance cardiaque

Tramadol RCP des médicaments à base de tramadol est, pour la dose 2 à 4 mg/kg toutes les 6 -8 h « Réduction des douleurs aiguës et chroniques d’intensité légère au niveau des tissus mous et du système musculo-squelettique. » pour la voie orale et « Réduction des douleurs postopératoires d’intensité légère. » pour la voie injectable. Une mise en garde est « Les effets analgésiques du chlorhydrate de tramadol peuvent être variables. Cette variabilité serait due à des différences individuelles au niveau de la métabolisation du médicament qui aboutit au métabolite actif principal, le O-déméthyltramadol. Chez certains chiens (ne répondant pas au traitement), le produit peut ainsi échouer à produire une analgésie. Les chiens doivent donc faire l’objet d’une surveillance régulière afin de s'assurer que l’efficacité est suffisante. » et « si le produit ne parvient pas à produire une analgésie suffisante dans les 30 minutes suivant l’administration ou sur la durée prévue avant le renouvellement du traitement, un autre analgésique adapté devra être utilisé. »

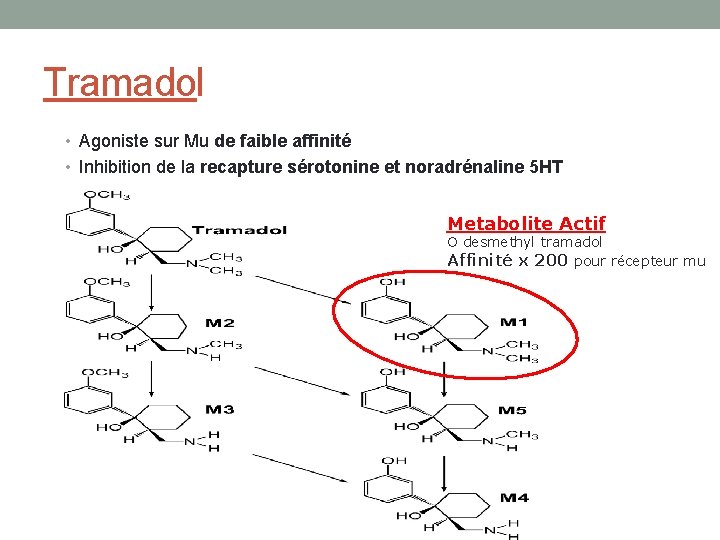
Tramadol • Agoniste sur Mu de faible affinité • Inhibition de la recapture sérotonine et noradrénaline 5 HT Metabolite Actif O desmethyl tramadol Affinité x 200 pour récepteur mu

Tramadol Chien : • Élimination du tramadol plus rapide (demi-vie=2 h) que chez l’Homme (6 h) • Très peu de métabolisation en M 1 (16% converti = concentrations indétectables dans plusieurs études) • Élimination plus rapide du M 1 (demi-vie=1. 3 h) que chez l’Homme (6 h) • Absorption par voie orale très faible et très variable • entre les chiens (65 ± 38 % chez le Beagle et 2. 5 % chez le greyhound) • pour un même chien en cours de traitement (concentrations plus de 70 % plus basses après 1 semaine)

Tramadol • Chien : très peu de métabolisation en M 1 Absence d’analgésie sur des douleurs aigües Pas de benefice clinique lors d’arthrose chronique Shutter et al. Veterinary Anaesthesia and Analgesia 2017 Budsgerg et al. JAVMA 2018 Peu de toxicité Attention interactions anti-dépresseurs (syndrome sérotoninergique) et AINS (ulcères)

Tramadol • Chat : • Conversion plus élevée en M 1 que chez le chien • Elimination plus lente de M 1 que chez le chien • Excellente absorption par voie orale = Semble fonctionner (2 mg/kg BID pour arthrose chronique) Guedes et al. JAVMA 2018 Toxicité : • Mydriase • Sédation légère • Euphorie légère (dysphorie) • Vomissements

Tramadol • Cheval : métabolisation en M 1 très inférieure à l’Homme Effet analgésique incertain Guedes et al. Equine Vet Journal 2015

Apomorphine • Pas de la famille des opioïdes • Vomissement par stimulation CRTZ ou des récepteurs dopaminergiques D 2 • Pas de VO possible • Anti-émétique à fortes doses surtout si IV ou IM>SC

Utilisation des opioïdes chez le chat • Morphine • Dysphorie/euphorie • Roulades • Ronronnement • Frottements • Pétrissage avec les membres antérieurs s a p t s lie e n’ a fo Ce e l !!! ! d • Mydriase • Hyperthermie après anesthésie • Elimination plus lente de la morphine chez le chat que chez le chien car absence de glucuronidation

Utilisation des opioïdes chez le cheval • Potentielle augmentation de l’activité locomotrice (marche) principalement sur les animaux non algiques et plutôt avec agonistes Mu • Ataxie (plutôt avec agonistes kappa) • Tremblements • Agitation • Baillements s a p x t es reu ’ n e e C ang d • Augmentation de l’appétit, …. Effets dose-dépendants principalement observés chez l’animal sans douleur Très grande variabilité inter et intra-individuelle

Antagonistes opioïdes • Naloxone • Antagoniste mu • Antagoniste kappa Diminue la dépression respiratoire • Antagoniste de GABA : risque d’épilepsie Attention : la demi-vie est courte. Il faut parfois répéter les administrations • Nalbuphine • Antagoniste mu • Agoniste kappa • Possibilité de réverser une dépression respiratoire sans enlever complètement l’analgésie.

Interactions • Morphine vs buprenorphine La buprenorphine déplace la morphine des Rr Mu et peut engendrer de la douleur et parfois des symptômes de sevrage (excitation, hyperthermie, …) • Morphine vs butorphanol Le butorphanol peut diminuer la détresse respiratoire associée à la morphine tout en maintenant une légère analgésie

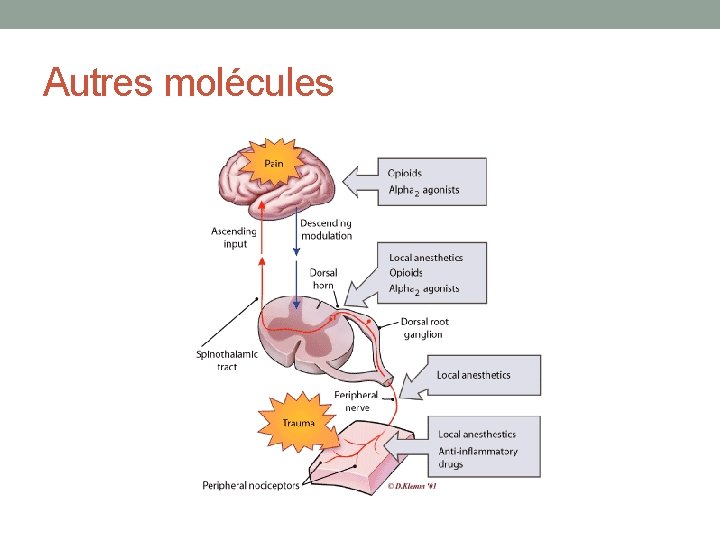
Autres molécules