Univerzita Karlova v Praze Prodovdeck fakulta Katedra uitelstv











- Slides: 17

Univerzita Karlova v Praze Přírodovědecká fakulta Katedra učitelství a didaktiky chemie Proteiny Bílkoviny Mgr. Denisa Velgová učitelství chemie 2008

Přírodní makromolekulární látky aminokyseliny peptidy - oligopeptidy (2 -10 AMK) - polypeptidy (11 -100 AMK) proteiny = polypeptidy o více než 100 AMK

Funkce • doposud není známa žádná životní forma, která by je neobsahovala • stavební, transportní (plazmatická membrána) • katalytická (enzymy) • regulační (hormony) • ochranná (protilátky) • zdroj energie (hladovění)

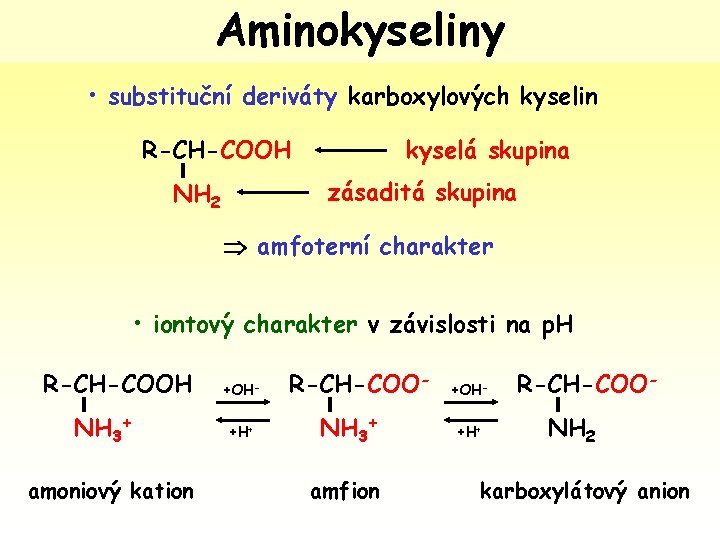
Aminokyseliny • substituční deriváty karboxylových kyselin R-CH-COOH kyselá skupina zásaditá skupina NH 2 amfoterní charakter • iontový charakter v závislosti na p. H R-CH-COOH NH 3+ amoniový kation +OH+H+ R-CH-COONH 3+ amfion +OH+H+ R-CH-COONH 2 karboxylátový anion

Aminokyseliny • 20 (22) proteinogenních geneticky kódovaných aminokyselin • -aminokyseliny • L-aminokyseliny • esenciální aminokyseliny nutno přijímat v potravě (organismus není schopen jejich syntézy) Val, Leu, Ile, Thr, Lys, Met, Phe, Trp, v dětství i His, Arg

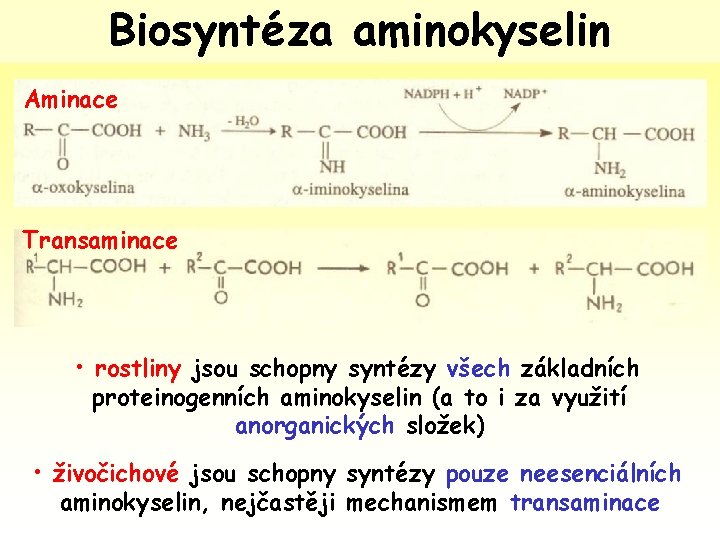
Biosyntéza aminokyselin Aminace Transaminace • rostliny jsou schopny syntézy všech základních proteinogenních aminokyselin (a to i za využití anorganických složek) • živočichové jsou schopny syntézy pouze neesenciálních aminokyselin, nejčastěji mechanismem transaminace

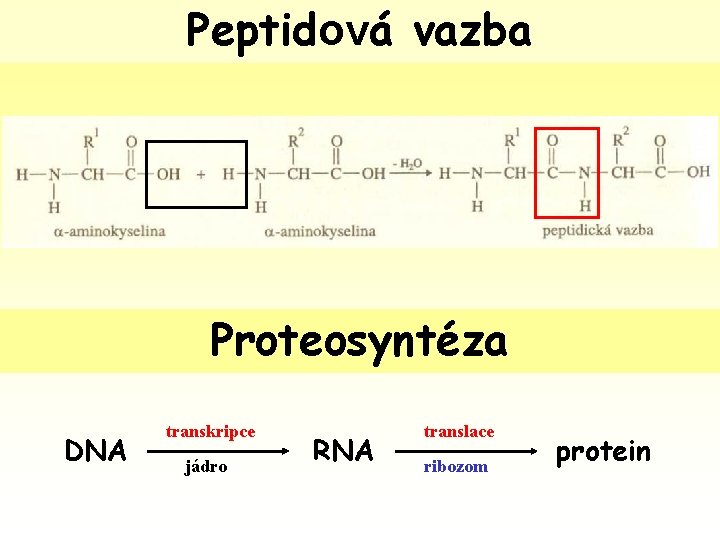
Peptidová vazba Proteosyntéza DNA transkripce jádro RNA translace ribozom protein

Peptidy • do 100 aminokyselin v řetězci • ve vodě vesměs rozpustné • podle počtu a druhu aminokyselin různé účinky • peptidová antibiotika • peptidové jedy (mykotoxiny, hadí neurotoxiny) • peptidové hormony (oxytocin, antidiuretin, inzulin, glukagon aj. )

Proteiny • vlastnosti bílkovin jsou dány jejich strukturou • pevné látky, některé rozpustné ve vodných roztocích • odolnost vůči chemickým a fyzikálním vlivům - nerozpustné bílkoviny bývají značně odolné - rozpustné (koloidní) nikoliv • koloidní bílkoviny podléhají koagulaci - vratná vysolování (např. vlivem přechodného zvýšení koncentrace Na. Cl) - nevratná denaturace (např. vlivem solí těžkých kovů, silnými kyselinami nebo zásadami, vysokou teplotou)

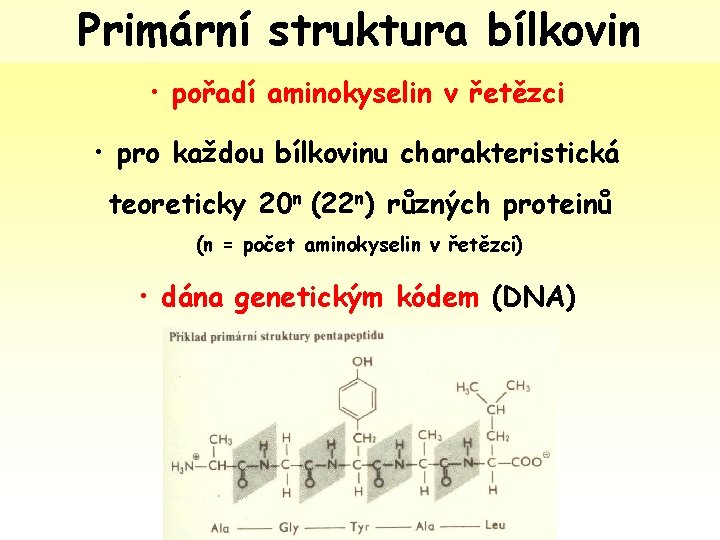
Primární struktura bílkovin • pořadí aminokyselin v řetězci • pro každou bílkovinu charakteristická teoreticky 20 n (22 n) různých proteinů (n = počet aminokyselin v řetězci) • dána genetickým kódem (DNA)

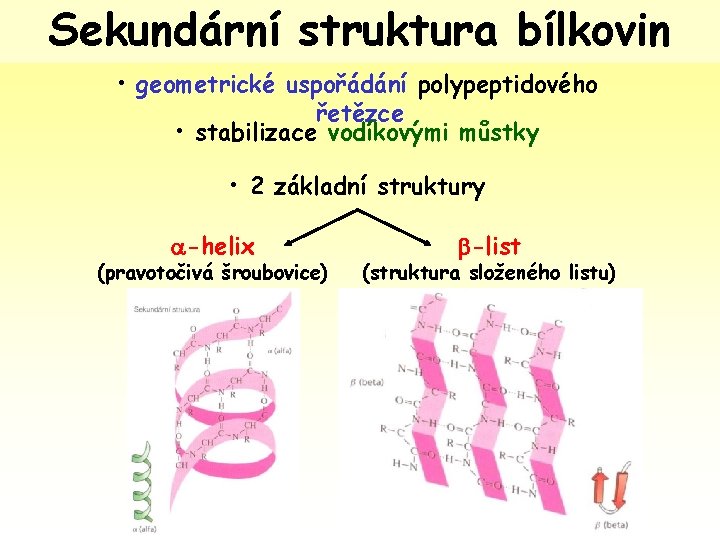
Sekundární struktura bílkovin • geometrické uspořádání polypeptidového řetězce • stabilizace vodíkovými můstky • 2 základní struktury -helix (pravotočivá šroubovice) -list (struktura složeného listu)

Terciární struktura bílkovin • uspořádání -helixu a -listu v prostoru • stabilizace slabými vazebnými interakcemi (vodíkové můstky aj. ) a zejména disulfidickými můstky (kovalentní vazba)

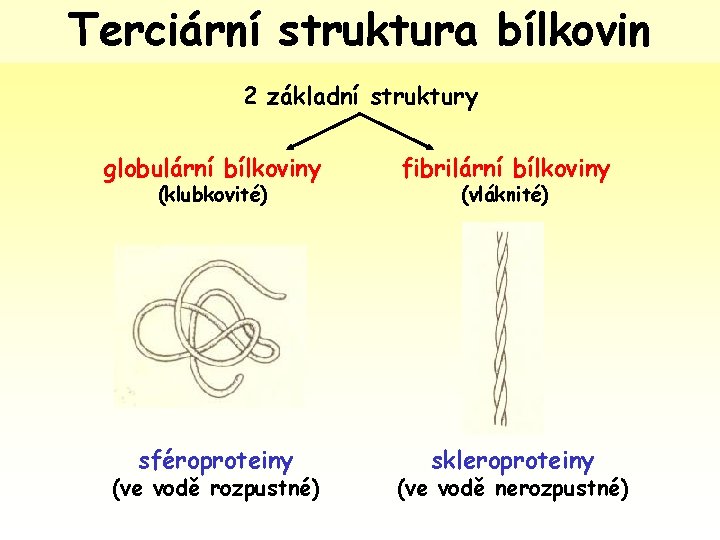
Terciární struktura bílkovin 2 základní struktury globulární bílkoviny (klubkovité) sféroproteiny (ve vodě rozpustné) fibrilární bílkoviny (vláknité) skleroproteiny (ve vodě nerozpustné)

Kvartérní struktura bílkovin • udává strukturu bílkoviny spojením několika samostatných polypeptidových řetězců (podjednotek) do funkčního celku Molekula hemoglobinu tvořená 2 páry polypeptidových řetězců (globin), ke každému z nich vázána nebílkovinná prostetická složka (hem).

Proteiny • vlastnosti bílkovin jsou dány jejich strukturou • struktura bílkovin určuje jejich funkci v organismu změna na kterékoliv úrovni má za následek větší či menší změnu funkce proteinu • příklad - odolnost vůči chemickým a fyzikálním vlivům (denaturace) - pozitivní - příprava potravin, dezinfekce, sterilizace - negativní - denaturace enzymů (i letální následky)

Jednoduché a složené bílkoviny • jednoduché - skleroproteiny - např. keratin, kolagen (vlasy, kůže …) - sféroproteiny - např. albuminy (krevní sérum), globuliny (imunoglobuliny), histony (DNA) • složené - chromoproteiny (např. hemoglobin) - metaloproteiny (např. transferin) - fosfoproteiny (např. kasein v mléce) - glykoproteiny (např. sliznice) - lipoproteiny (např. buněčné membrány) • jednoduché - obsahují ve svých molekulách pouze aminokyseliny • složené - obsahují bílkovinnou a nebílkovinnou (prostetickou) složku

Použitá literatura • Honza, J. , Mareček, A. – Chemie pro čtyřletá gymnázia, 3. díl, nakladatelství Olomouc, s. r. o. , 1. vydání, 2005 • Čársky, J. , Kopřiva, J. , Krištofová, V. , Pecháň, I. – Chemie pro III. ročník gymnázií, SPN, Praha, 1. vydání, 1986 • Benešová, M. , Satrapová, H. – Odmaturuj z chemie, nakladatelství Didaktis, s. r. o. , Brno, 1. vydání, 2002 • Rosypal, S. a kol – Nový přehled biologie, Scientia, s. r. o. , Praha, 1. vydání, 2003 • Roštejnská, M. – Trávení a metabolismus. ppt, Středoškolská biochemie, diplomová práce 2004, Katedra didaktiky chemie, PřFUK (vzdělávací kurzy pro studenty na http: //dl. cuni. cz)
 Univerzita v praze
Univerzita v praze Epizeuxis
Epizeuxis Fm vše studijní oddělení
Fm vše studijní oddělení Studentský email ujep
Studentský email ujep Uniza stavebna fakulta
Uniza stavebna fakulta Dopravní fakulta jana pernera
Dopravní fakulta jana pernera Inese karlova
Inese karlova Moodle karlova
Moodle karlova Univerzita mateja bela odbory
Univerzita mateja bela odbory Tf moodle
Tf moodle Prešovská univerzita
Prešovská univerzita Mendelova univerzita lednice
Mendelova univerzita lednice Univerzita palckého
Univerzita palckého Katedra optiky
Katedra optiky Bon uw
Bon uw Katedra psychologie ped muni
Katedra psychologie ped muni Katedra se lizbona
Katedra se lizbona Astronomija fakultet
Astronomija fakultet

































