UNIVERSITATEA POLITEHNICA TIMIOARA CURS nivel MASTER BIOINFORMATICA Prof

UNIVERSITATEA POLITEHNICA TIMIŞOARA CURS nivel MASTER BIOINFORMATICA Prof Dr George I Mihalaş UMF Victor Babeş 1

www. medinfo. umft. ro/dim/bi oinformatica. htm 2

CURSUL 3 Noțiuni de BIOCHIMIE 3

Planul cursului • Aminoacizi – Structură – Proprietăți • Proteine – Legătura peptidică – Structuri: primară, secundară, 3 D • Acizi nucleici – Nucleotide – Structura primară – Structura secundară 4
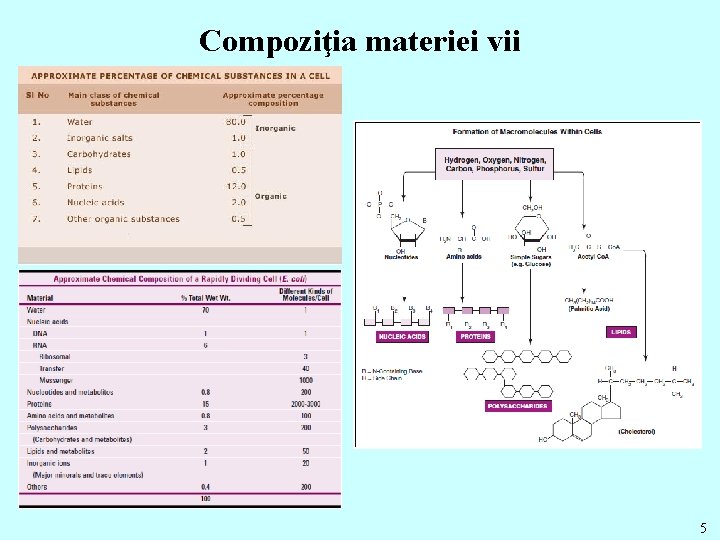
Compoziţia materiei vii 5

Amino. Acizi - Proteine 6
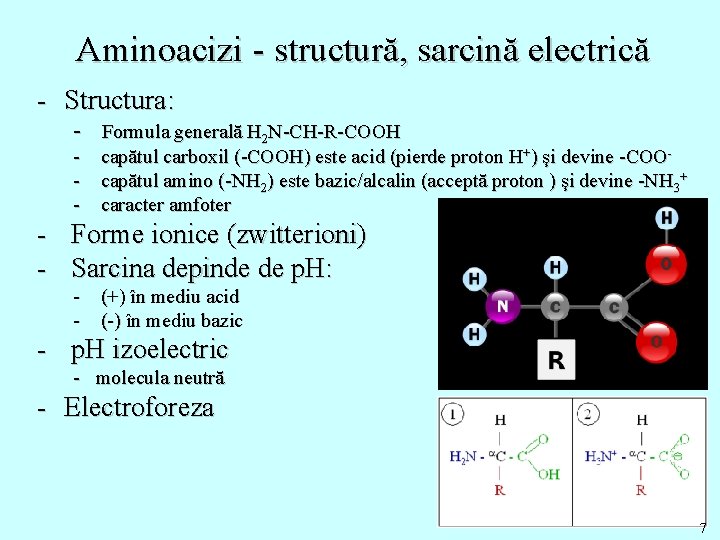
Aminoacizi - structură, sarcină electrică - Structura: - Formula generală H 2 N-CH-R-COOH - capătul carboxil (-COOH) este acid (pierde proton H+) şi devine -COO- capătul amino (-NH 2) este bazic/alcalin (acceptă proton ) şi devine -NH 3+ - caracter amfoter - Forme ionice (zwitterioni) - Sarcina depinde de p. H: - (+) în mediu acid - (-) în mediu bazic - p. H izoelectric - molecula neutră - Electroforeza 7

Structura moleculară standard 8
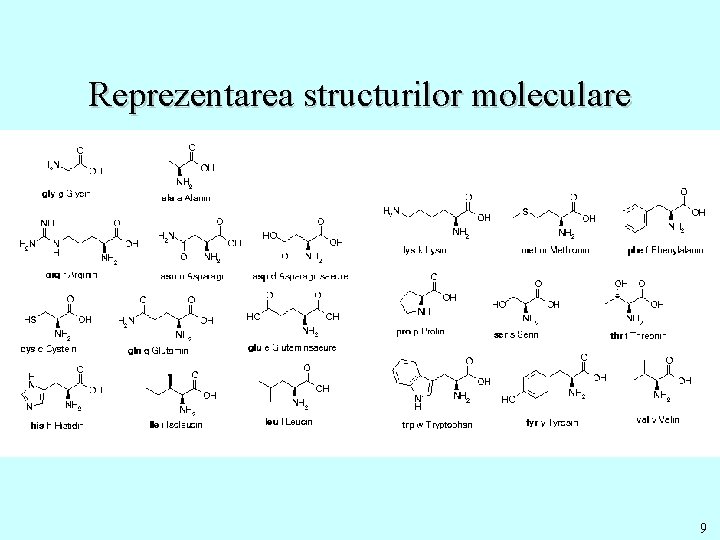
Reprezentarea structurilor moleculare 9
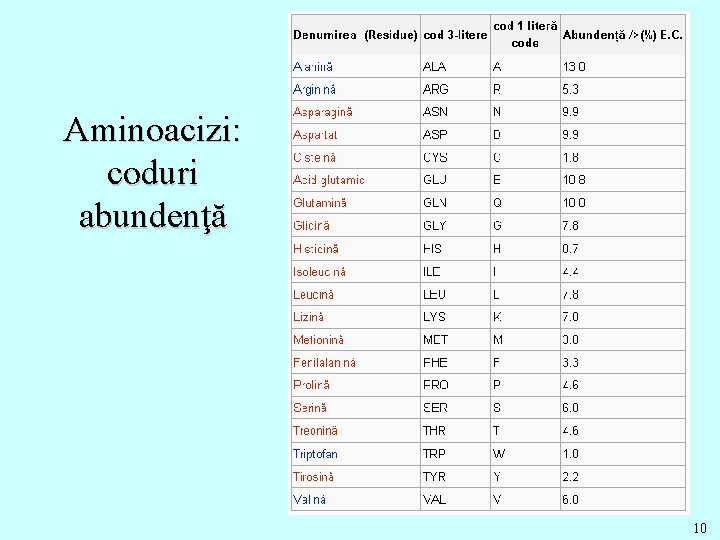
Aminoacizi: coduri abundenţă 10
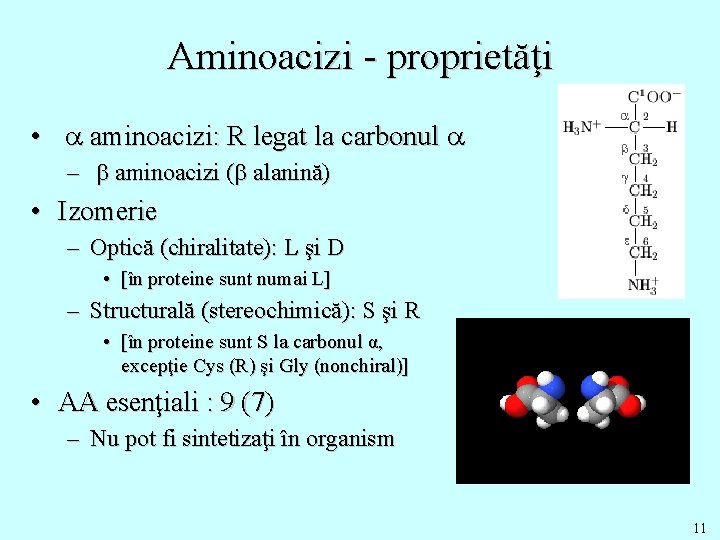
Aminoacizi - proprietăţi • a aminoacizi: R legat la carbonul a – b aminoacizi (b alanină) • Izomerie – Optică (chiralitate): L şi D • [în proteine sunt numai L] – Structurală (stereochimică): S şi R • [în proteine sunt S la carbonul α, excepţie Cys (R) şi Gly (nonchiral)] • AA esenţiali : 9 (7) – Nu pot fi sintetizaţi în organism 11
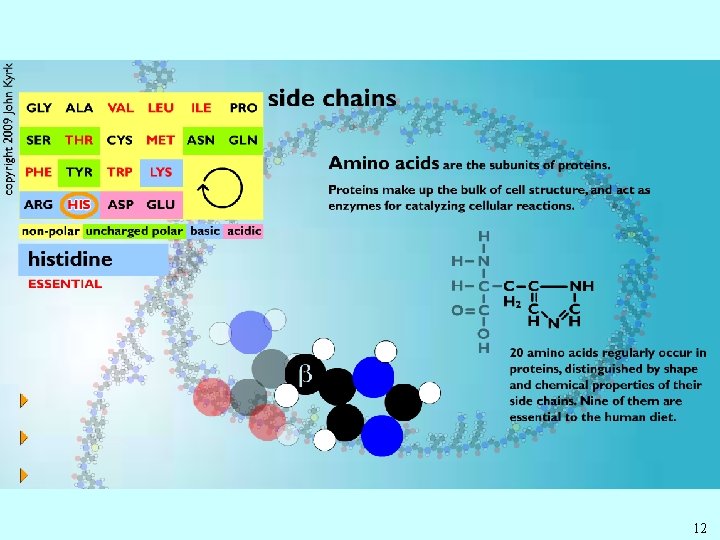
12

Proprietăţi 13
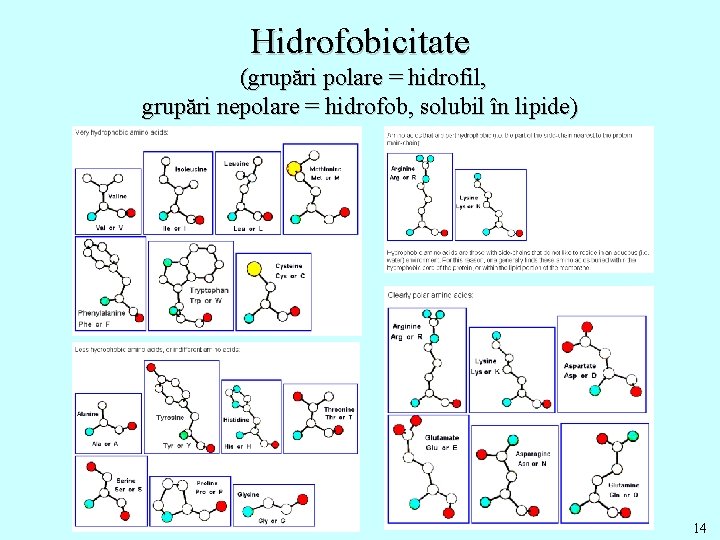
Hidrofobicitate (grupări polare = hidrofil, grupări nepolare = hidrofob, solubil în lipide) 14
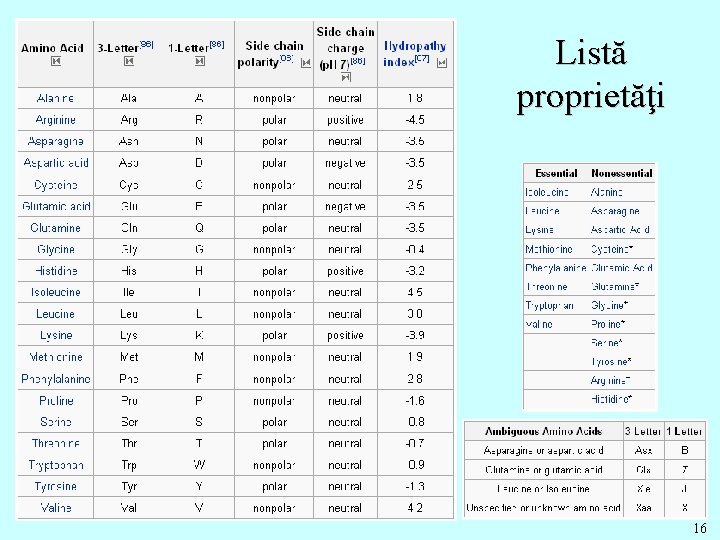
Listă proprietăţi 16
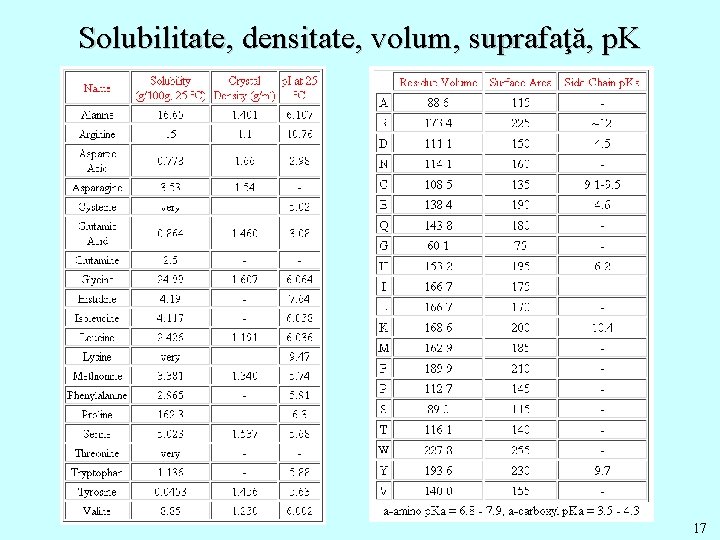
Solubilitate, densitate, volum, suprafaţă, p. K 17
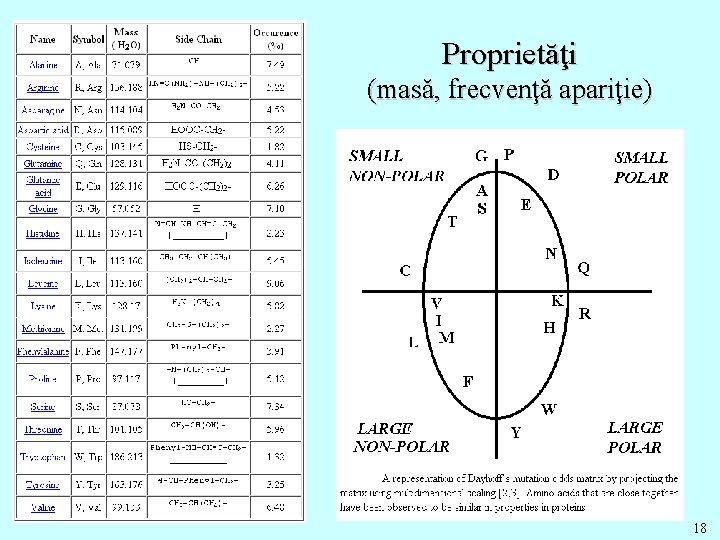
Proprietăţi (masă, frecvenţă apariţie) 18
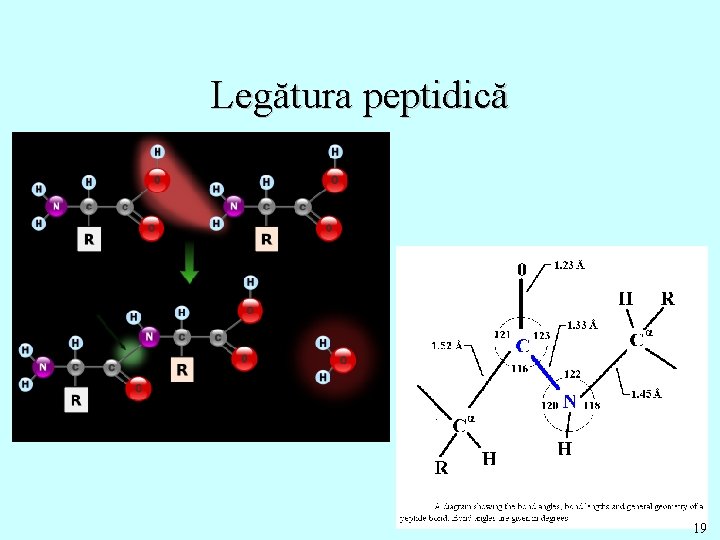
Legătura peptidică 19

Structura proteinelor - structura primară - secvenţa aminoacizilor - structura secundară - structura terţiară - structura cuaternară 20
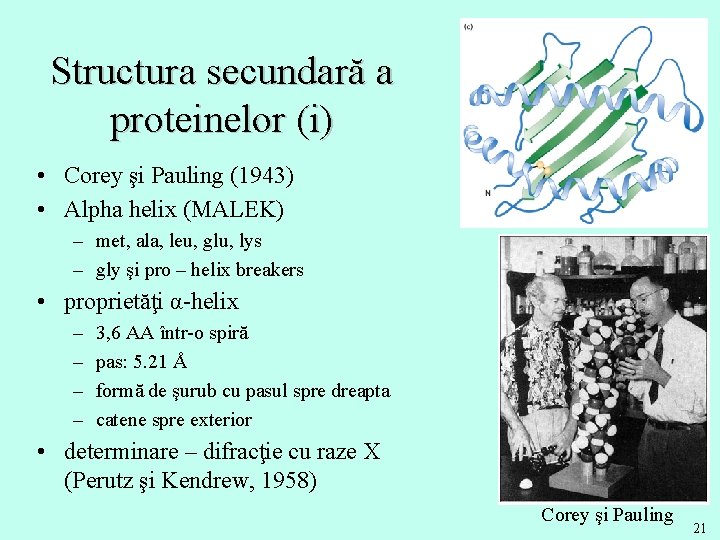
Structura secundară a proteinelor (i) • Corey şi Pauling (1943) • Alpha helix (MALEK) – met, ala, leu, glu, lys – gly şi pro – helix breakers • proprietăţi α-helix – – 3, 6 AA într-o spiră pas: 5. 21 Å formă de şurub cu pasul spre dreapta catene spre exterior • determinare – difracţie cu raze X (Perutz şi Kendrew, 1958) Corey şi Pauling 21

22
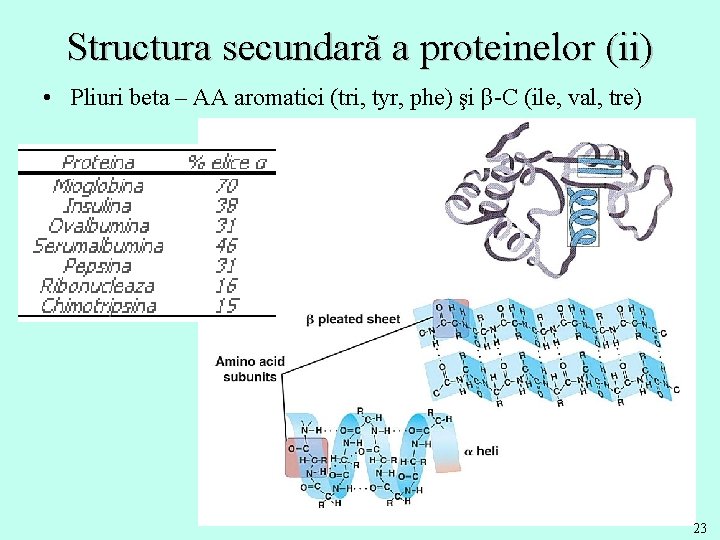
Structura secundară a proteinelor (ii) • Pliuri beta – AA aromatici (tri, tyr, phe) şi β-C (ile, val, tre) 23
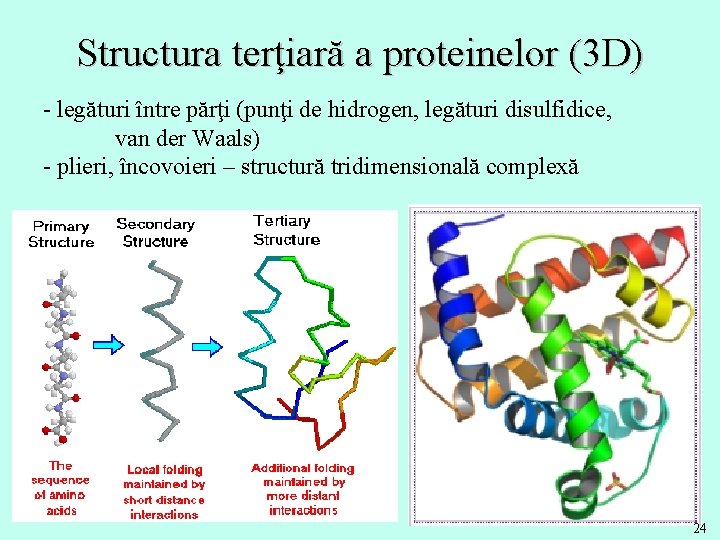
Structura terţiară a proteinelor (3 D) - legături între părţi (punţi de hidrogen, legături disulfidice, van der Waals) - plieri, încovoieri – structură tridimensională complexă 24
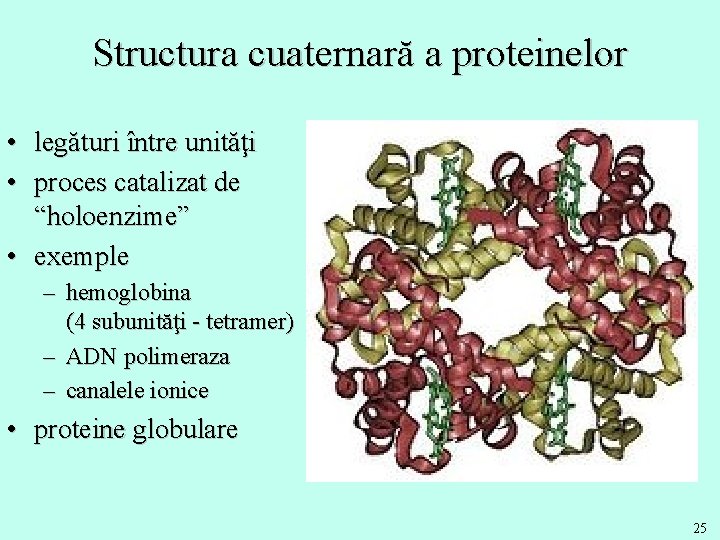
Structura cuaternară a proteinelor • legături între unităţi • proces catalizat de “holoenzime” • exemple – hemoglobina (4 subunităţi - tetramer) – ADN polimeraza – canalele ionice • proteine globulare 25
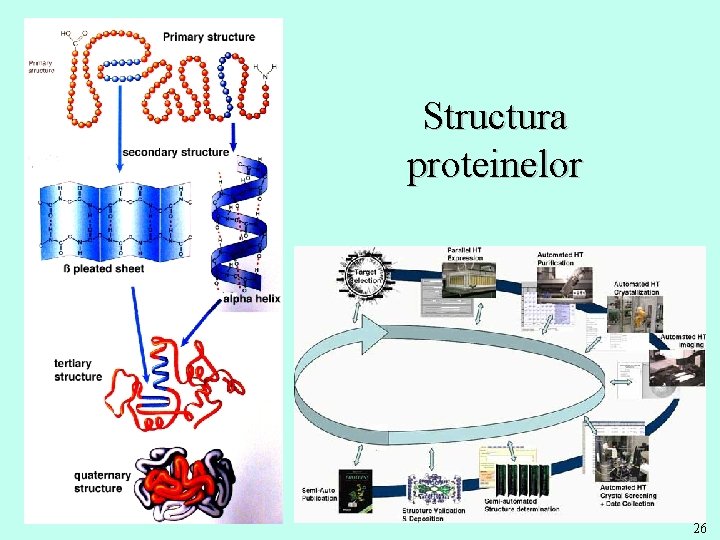
Structura proteinelor 26
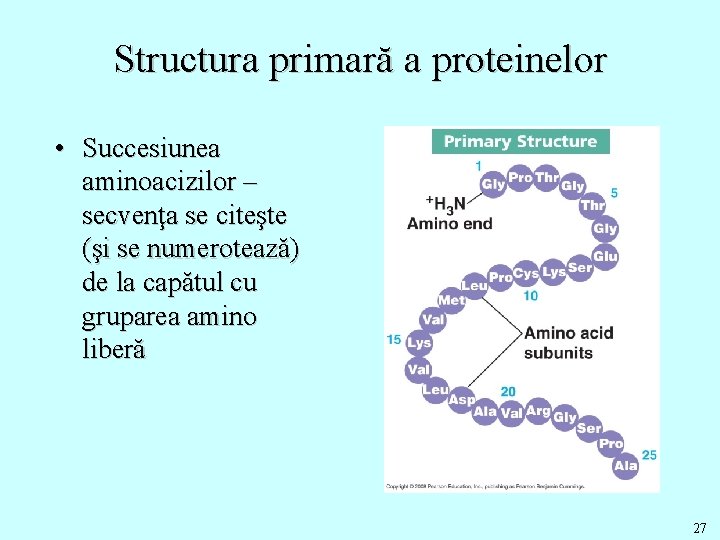
Structura primară a proteinelor • Succesiunea aminoacizilor – secvenţa se citeşte (şi se numerotează) de la capătul cu gruparea amino liberă 27
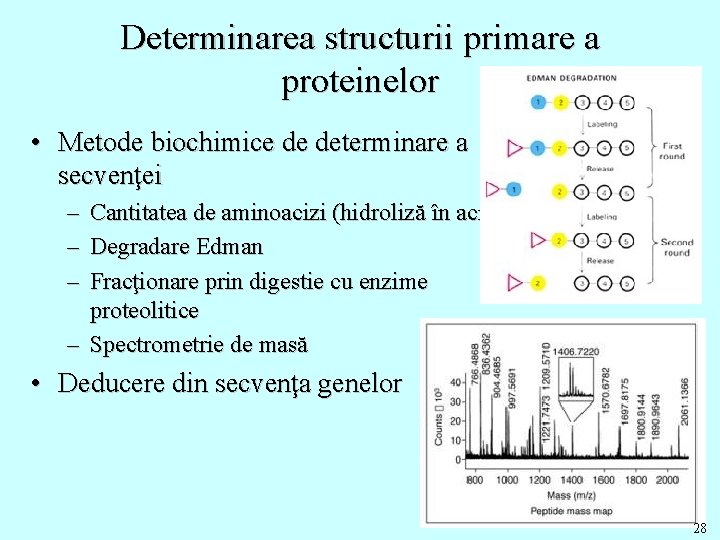
Determinarea structurii primare a proteinelor • Metode biochimice de determinare a secvenţei – – – Cantitatea de aminoacizi (hidroliză în acizi) Degradare Edman Fracţionare prin digestie cu enzime proteolitice – Spectrometrie de masă • Deducere din secvenţa genelor 28
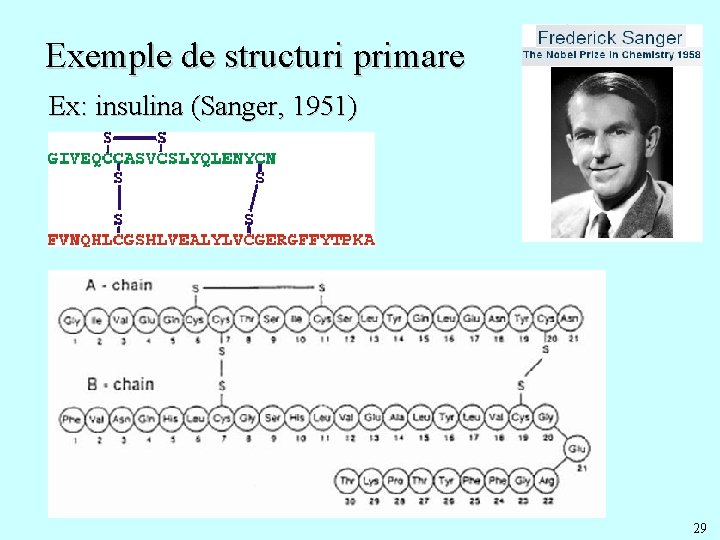
Exemple de structuri primare Ex: insulina (Sanger, 1951) 29

Acizi nucleici 30
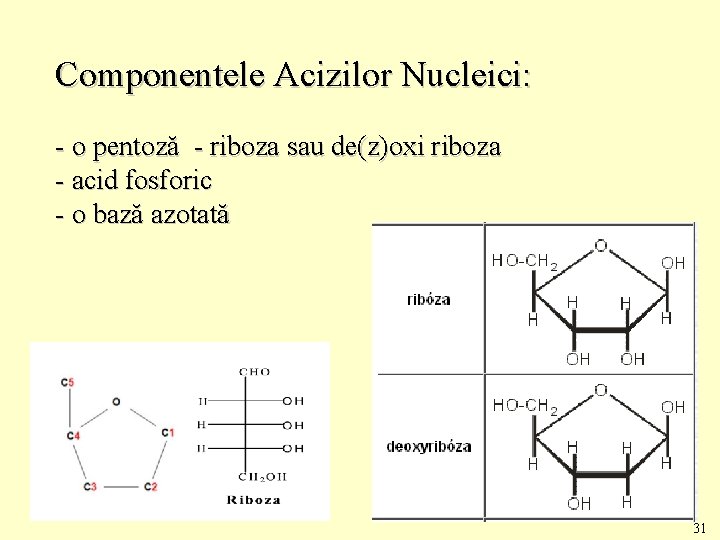
Componentele Acizilor Nucleici: - o pentoză - riboza sau de(z)oxi riboza - acid fosforic - o bază azotată 31
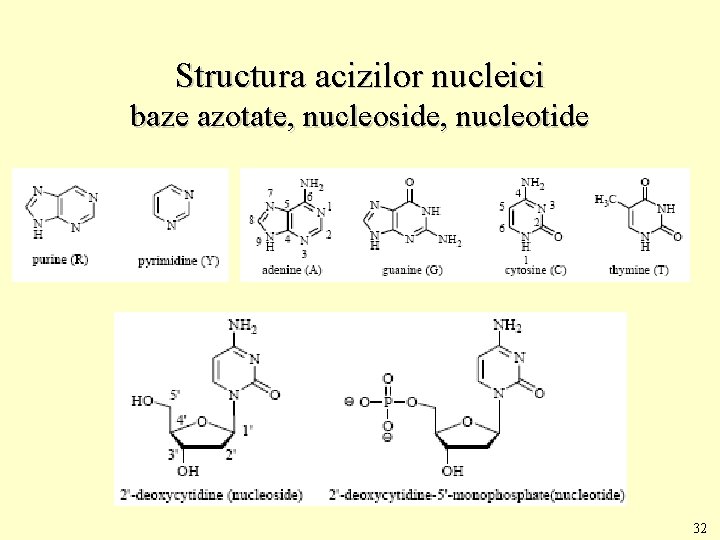
Structura acizilor nucleici baze azotate, nucleoside, nucleotide 32
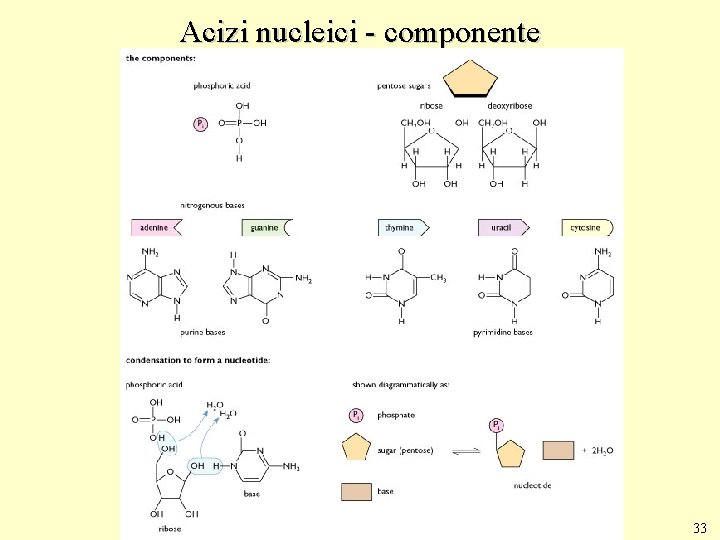
Acizi nucleici - componente 33
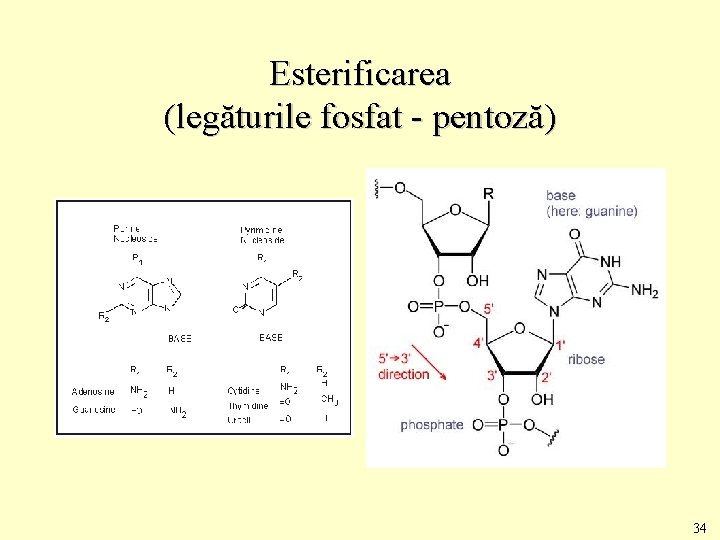
Esterificarea (legăturile fosfat - pentoză) 34
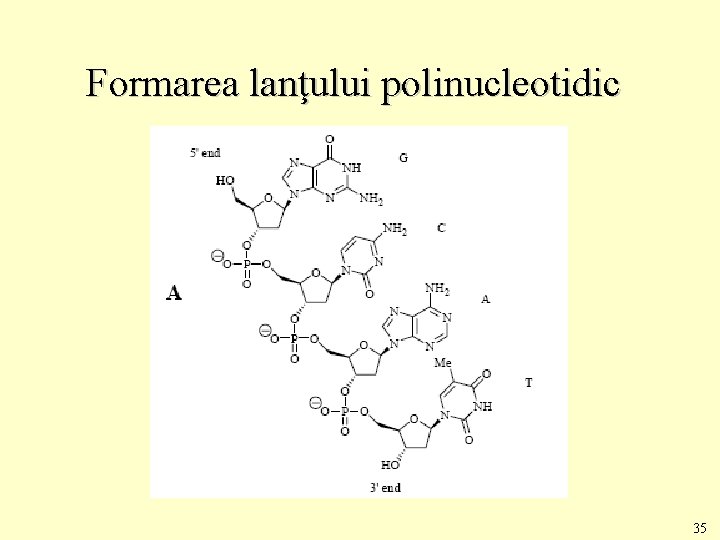
Formarea lanţului polinucleotidic 35
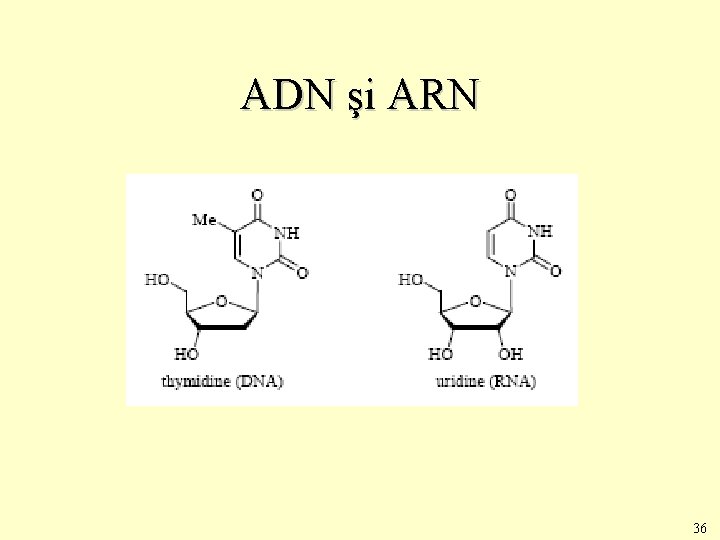
ADN şi ARN 36
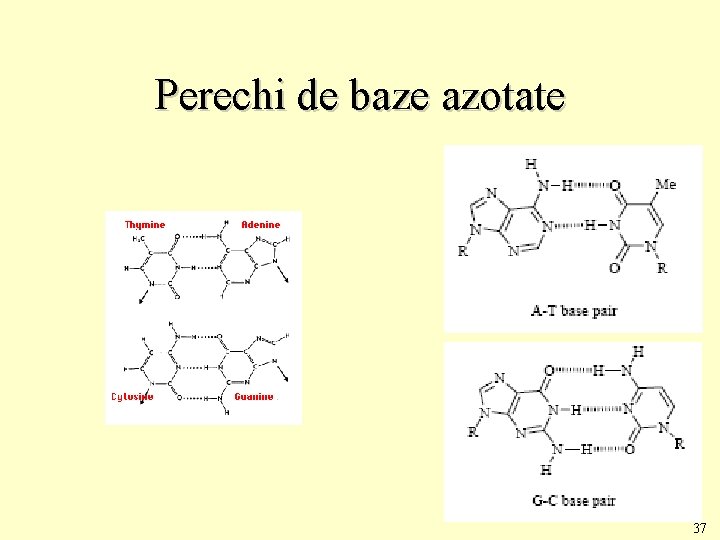
Perechi de baze azotate 37
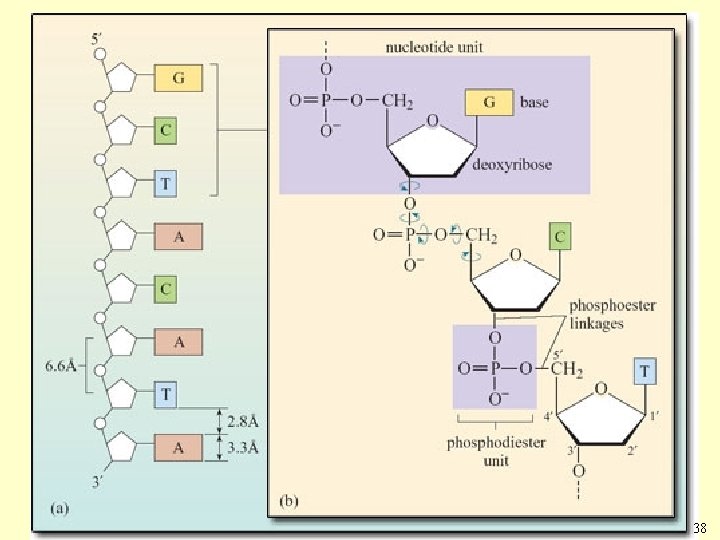
38
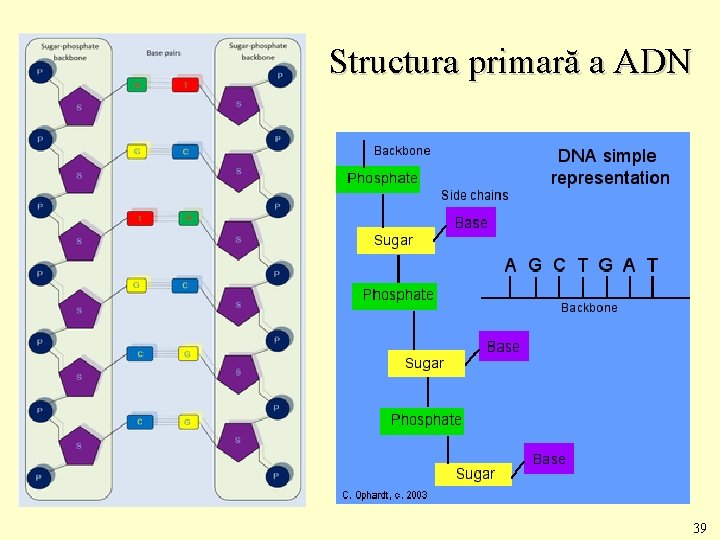
Structura primară a ADN 39
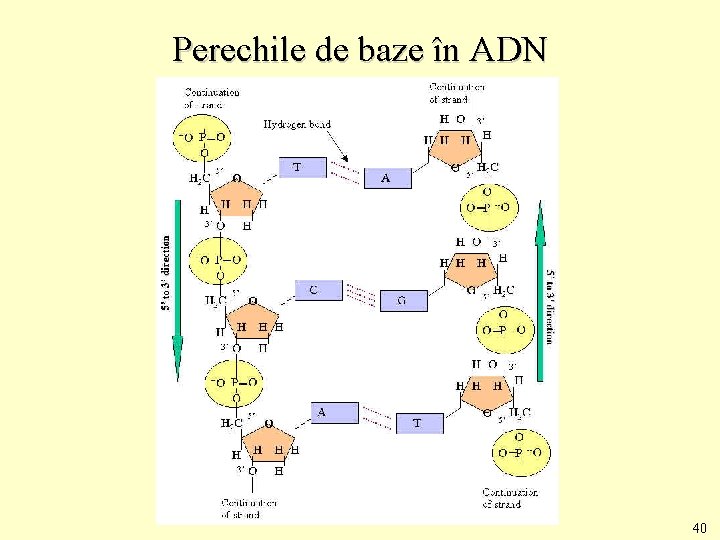
Perechile de baze în ADN 40
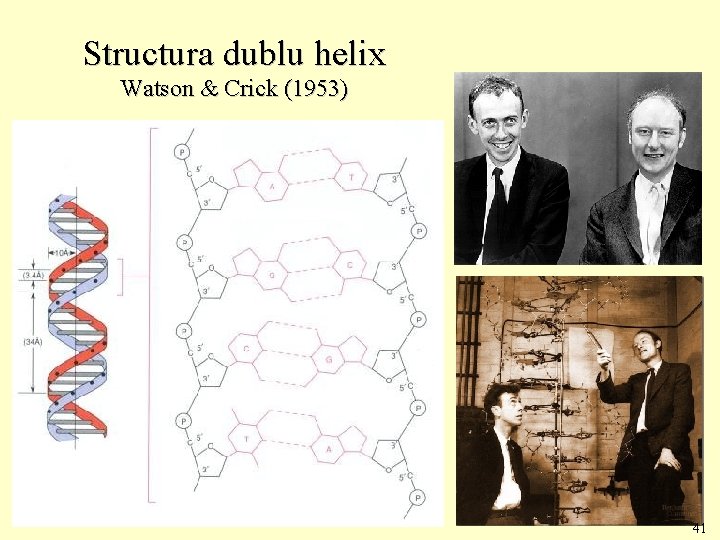
Structura dublu helix Watson & Crick (1953) 41
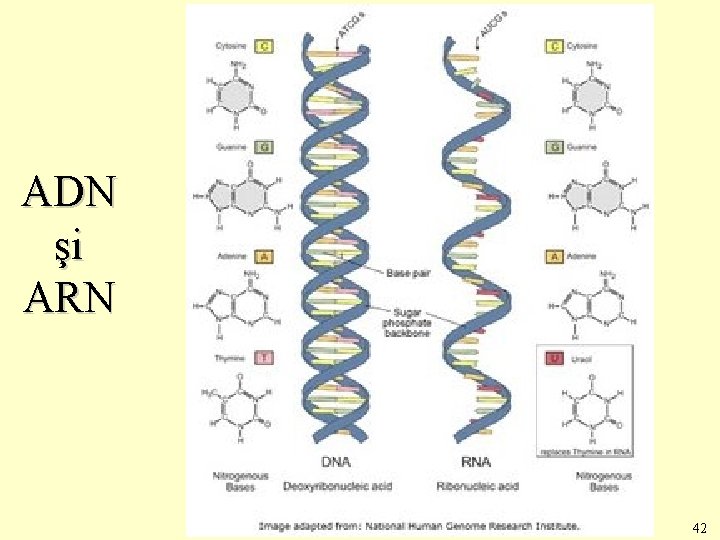
ADN şi ARN 42
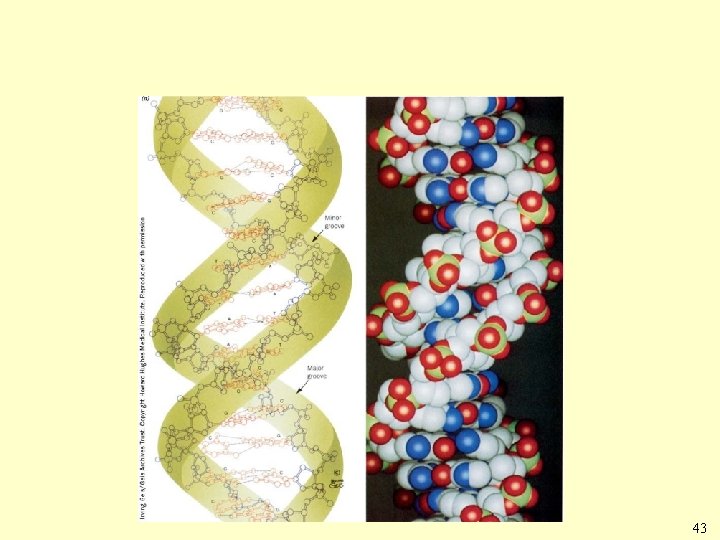
43
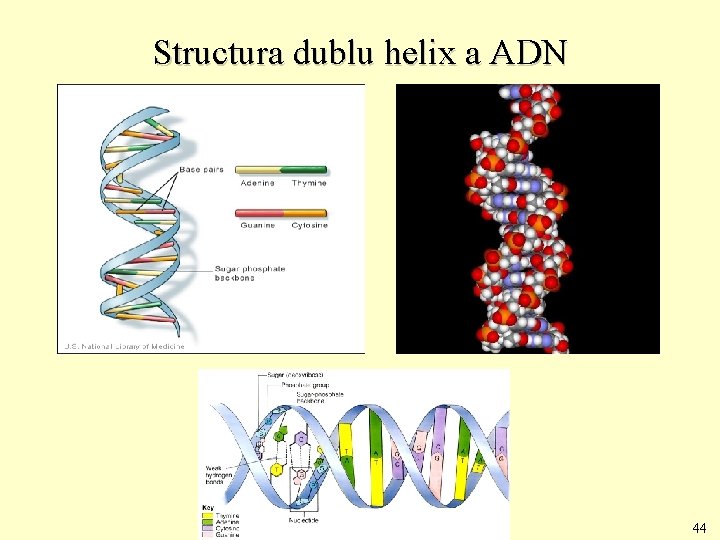
Structura dublu helix a ADN 44

PAUZA 45
- Slides: 44