Universita degli Studi dellInsubria Termodinamica Chimica Miscele di

Universita’ degli Studi dell’Insubria Termodinamica Chimica Miscele di gas ideali dario. bressanini@uninsubria. it http: //scienze-como. uninsubria. it/bressanini

Miscele di Gas Ideali n Cosa ci dobbiamo aspettare se misceliamo dei gas ideali? n Nulla di particolare! In un gas ideale, le molecole non interagiscono fra loro, e quindi la loro natura è del tutto ininfluente. n Dalton, (lo stesso del “Daltonismo”) studiò le miscele di gas nel XIX secolo © Dario Bressanini 2
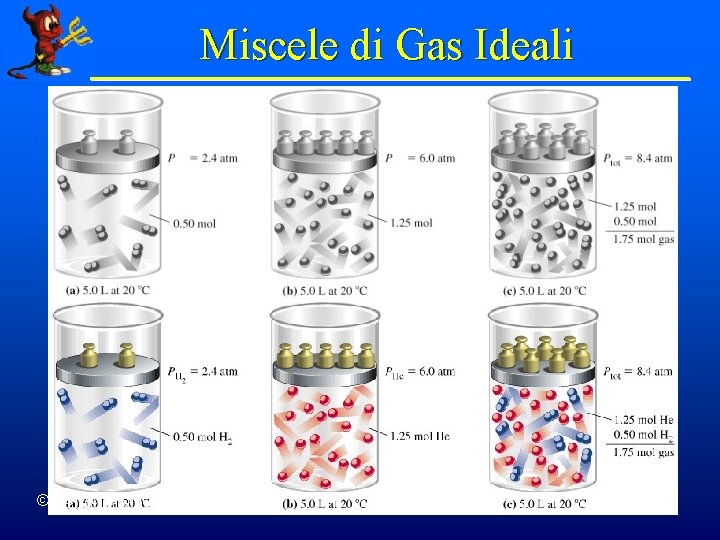
Miscele di Gas Ideali © Dario Bressanini 3
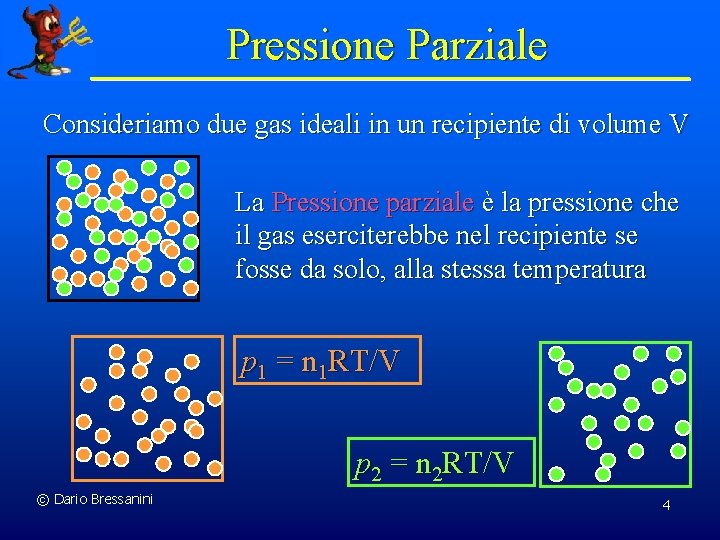
Pressione Parziale Consideriamo due gas ideali in un recipiente di volume V La Pressione parziale è la pressione che il gas eserciterebbe nel recipiente se fosse da solo, alla stessa temperatura p 1 = n 1 RT/V p 2 = n 2 RT/V © Dario Bressanini 4

Legge di Dalton In una miscela di gas ideali, la pressione totale esercitata dalla miscela è la somma delle pressioni parziali dei gas costituenti la miscela ptot = p 1 + p 2 + p 3. . . © Dario Bressanini 5
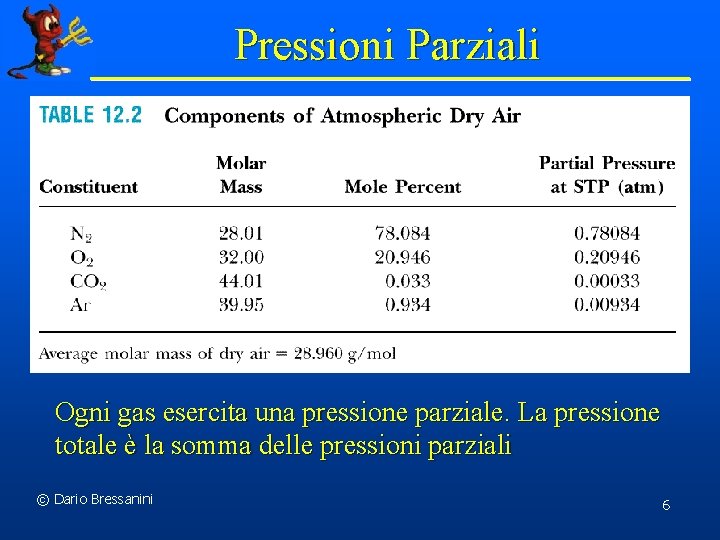
Pressioni Parziali Ogni gas esercita una pressione parziale. La pressione totale è la somma delle pressioni parziali © Dario Bressanini 6
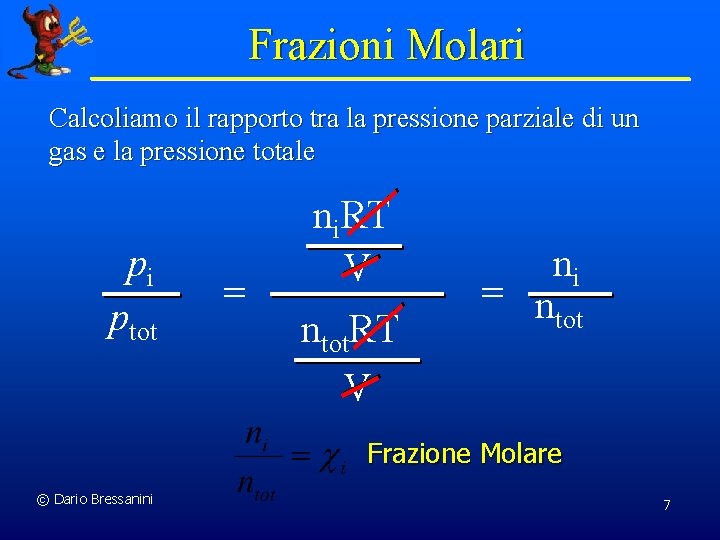
Frazioni Molari Calcoliamo il rapporto tra la pressione parziale di un gas e la pressione totale pi ptot = ni. RT V ntot. RT V ni = n tot Frazione Molare © Dario Bressanini 7
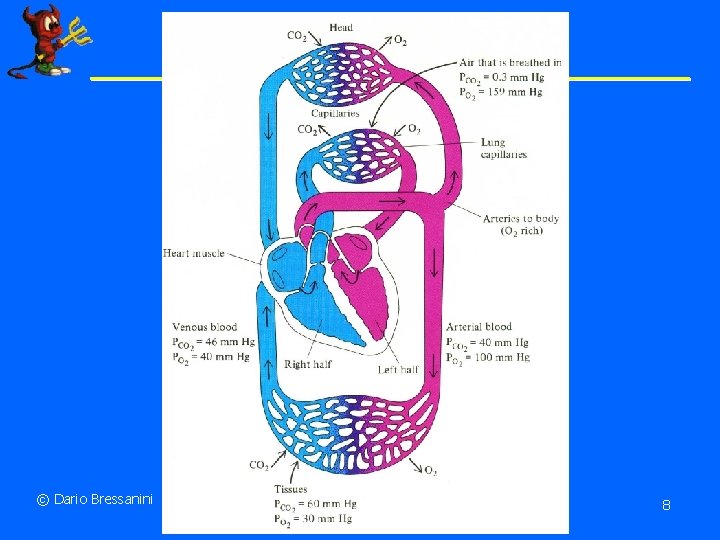
© Dario Bressanini 8

Frazioni Molari e Pressioni Parziali © Dario Bressanini 9

Esercizio Un recipiente di 10 Litri a 273 Kelvin contiene 2 grammi di H 2 e 8 grammi di N 2. Calcolare le pressioni parziali e la pressione totale 2. 00 g H 2 = 0. 992 mol H 2 8. 00 g N 2 = 0. 286 mol N 2 × 273 K 0. 992 mol 10. 0 L = 2. 22 atm × 273 K 0. 286 mol 10. 0 L = 0. 641 atm
- Slides: 10