Universita degli Studi dellInsubria Modelli in chimica ovvero

Universita’ degli Studi dell’Insubria Modelli in chimica ovvero non esiste l’elettrone 1 s Dario Bressanini dario. bressanini@uninsubria. it http: //scienze-como. uninsubria. it/bressanini

Le Basi Della Chimica © Dario Bressanini 2

Le Basi Della Chimica Atomi, Molecole, Cristalli, Materiali, . . . Meccanica Quantistica Meccanica Statistica Termodinamica Tutta la Chimica © Dario Bressanini 3

Natura e Matematica “il Grande libro della Natura e’ scritto nel linguaggio della matematica, e non possiamo capirla se prima non ne capiamo i simboli“ Galileo Galilei “In science, there is only physics; all the rest is stamp collecting” Ernest Rutherford © Dario Bressanini 4

Chimica e Matematica "We are perhaps not far removed from the time, when we shall be able to submit the bulk of chemical phenomena to calculation” Joseph Louis Gay-Lussac - 1808 “The underlying physical laws necessary for the mathematical theory of a large part of physics and the whole of chemistry are thus completely known, and the difficulty is only that the exact application of these equations leads to equations much too complicated to be soluble” P. A. M. Dirac - 1929 © Dario Bressanini 5

Scienze e Matematica 1700 1800 1940 1970 1980 – – – – Fisica Classica Elettromagnetismo Termodinamica Meccanica Quantistica Chimica Biologia Economia Non tutti la pensavano alla stessa maniera … Every attempt to employ mathematical methods in the study of chemical questions must be considered profoundly irrational and contrary to the spirit of chemistry… If mathematical analysis should ever hold a prominent place in chemistry – an aberration which is happily almost impossible – it would occasion a rapid and widespread degeneration of that science. Auguste Compte © Dario Bressanini 6

Realta’ e Modelli n La realta’ e’ spesso troppo complessa per poter essere studiata in modo semplice, preciso e accurato. n Gli scienziati ricorrono a delle semplificazioni, a volte drastiche, in modo pero’ da mantenere sempre le caratteristiche salienti del fenomeno da studiare n Si usano dei. . . © Dario Bressanini 7

…Modelli ? © Dario Bressanini 8

Modelli! n Un modello e’ una costruzione teorica che cerca di catturare, piu’ o meno fedelmente, uno o piu’ aspetti di un fenomeno n Un modello semplifica, diminuisce la complessita’ di un fenomeno, aiuta a capire, ma approssima n Scegliere un modello “buono” è difficile. . . ma NECESSARIO. © Dario Bressanini 9

Complessita’ © Dario Bressanini 10

Astrazione e Modelli © Dario Bressanini 11

Pensare per Modelli René Magritte © Dario Bressanini 12

Astrazione e Modelli n Il sole è, in prima approssimazione, una sfera piena di un Gas Ideale (p. V=n. RT). n Un cavallo da corsa è, in prima approssimazione, una sfera. n Si devono trascurare i dettagli insignificanti (il colore del cavallo), o trascurabili (la coda del cavallo). . . ma solo quelli. Una teoria scientifica deve essere la più semplice possibile. . . ma non troppo semplice (A. Einstein) © Dario Bressanini 13

Chimica: scienza dei modelli n Atomi e Molecole non sono accessibili all’esperienza quotidiana n Concetti macroscopici quali “temperatura” o “traiettoria” sono PRIVI DI SENSO a livello molecolare n Le grandezze microscopiche NON si possono misurare direttamente La Chimica ha bisogno di costruire dei modelli, sia matematici che interpretativi © Dario Bressanini 14

La Materia n Nel 17 mo secolo vi era ancora molta confusione su cosa fosse la Materia Johann Becher e Georg Stahl, medici tedeschi professori universitari, fondarono la teoria del Flogisto (dal greco ‘bruciare’) Georg Ernst Stahl (1659 -1734) © Dario Bressanini Simbolo del Flogisto 15

Il Flogisto n n La materia e’ costituita da due componenti: il Flogisto e la Cenere Bruciando, il flogisto si libera nell’aria, lasciando solamente la cenere L’aria “Flogistificata” non riesce piu’ a supportare la combusione © Dario Bressanini 16

Fatti spiegati dalla Teoria del Flogisto § I combustibili perdono peso bruciando, perche’ perdono flogisto. § La combustione cessa quando tutto il flogisto e’ fuoriuscito dalla sostanza e ha saturato l’aria § Il carbone lascia pochissimo residuo perche’ e’ flogisto quasi puro § Un topolino muore se chiuso in un ambiente sigillato perche’ l’aria si satura di flogisto § Alcune ‘calci metalliche’, scaldate con carbone si ritrasformano in metallo perche’ il carbone cede il flogisto © Dario Bressanini 17

Problemi della Teoria del Flogisto n n Tuttavia, alcune sostanze aumentano di peso dopo essere state bruciate (il magnesio ad esempio)! Joseph Priestly scopre l’ossigeno nel 1774, ma non crede alla teoria dell’ossidazione. Chiama l’ossigeno aria deflogistificata Joseph Priestly n Oggi noi sappiamo che la combustione è dovuta al processo di ossidazione. © Dario Bressanini 18

Conservazione della Massa n Antoine Lavoisier mostra come la combustione non e’ una perdita di flogisto, ma una reazione chimica con l’ossigeno. n Enuncia il principio di Antoine-Laurent Lavoisier (1743 -1794) e sua moglie © Dario Bressanini conservazione della massa: La Materia non viene nè creata nè distrutta, ma cambia solamente forma 19

Modelli per altri Fenomeni n L’elettricità è generata dal flusso di due fluidi, chiamati ‘vetroso’ e ‘resinoso’ n Il magnetismo è generato dal flusso di due altri fluidi, chiamati ‘australe’ e ‘boreale’ n Il Calore invece era il flusso di un singolo fluido, chiamato ‘calorico’ © Dario Bressanini 20

Le Nuove Forme di Energia n Nel diciottesimo secolo, il medico italiano Luigi Galvani (1737 -1798) scoprì che un conduttore bimetallico caricato elettricamente poteva far muovere le zampe di rane morte. n Si pensò che l’elettricità scorresse dentro ogni essere vivente. n Il romanzo Frankenstein, di Mary Shelley (1797 -1851) e’ basato su queste teorie © Dario Bressanini 21

Le Nuove Forme di Energia n Alessandro Volta (1745 -1827), fisico comasco, riconobbe che “l’effetto Galvanico”, il movimento delle zampette di rana, era da ricondurre al passaggio della corrente nei tessuti animali, incapaci di produrre elettricità. n Nel 1800, Volta costruì la prima pila, denominata voltaica in suo onore. Quest’apparato era in grado di produrre chimicamente corrente elettrica. © Dario Bressanini 22

Sir Francis Bacon e il Calore Francis Bacon (1561 -1626) Nato nel 1561 da una potente famiglia alla corte della Regina Elisabetta I di Inghilterra. © Dario Bressanini n Nel 1620 Bacon ebbe l’intuizione che il calore era nient’altro che “movimento, rapida e vigorosa agitazione delle particelle di cui è composta la materia “ n Mori’ di bronchite sperimentando l’idea che il freddo potesse prevenire la putrefazione della carne e permetterne la sua conservazione. n La sua teoria del calore venne dimenticata 23

La Teoria del Calorico n l’opinione prevalente (Lavoisier, Fourier, Laplace e Poisson), era che il calore fosse una sorta di fluido misterioso, il calorico, che fluiva in ogni sostanza e spontaneamente passava da un corpo caldo ad un corpo freddo. n Il calorico aveva strane proprietà. n ´ Non aveva peso. . . ´ . . ma occupava un volume Non si riusciva ad isolarlo © Dario Bressanini 24

La fine della teoria del Calorico Benjamin Thompson (1754 -1814) nato nella colonia del Massachusetts. Trasferitosi in Europa, lavorò al servizio del Duca di Baviera. Fu nominato “Conte del Sacro Romano Impero”, e scelse di chiamarsi “Conte Rumford” © Dario Bressanini Il Conte Rumford, Joule e altri dimostrarono che il calore non era una sostanza. 25
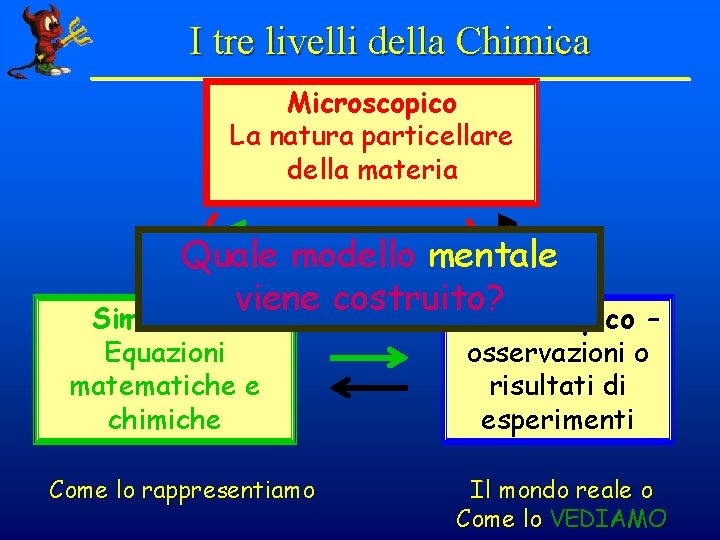
I tre livelli della Chimica Microscopico La natura particellare della materia Il livello atomico Quale modello mentale e molecolare (astratto ) viene costruito? Simbolico – Macroscopico Equazioni matematiche e chimiche Come lo rappresentiamo – osservazioni o risultati di esperimenti Il mondo reale o Come lo VEDIAMO

Concetti chimici fondamentali n Struttura e geometria molecolare n Legame Chimico ´ d- Ionico-Covalente ´ Singolo, Doppio, Triplo NON OSSERVABILI SPERIMENTALMENTE n Elettronegatività Concetti non rigorosi n d+ Numero di ossidazione n Cariche atomiche n Vibrazioni molecolari © Dario Bressanini d+ d- d- 28
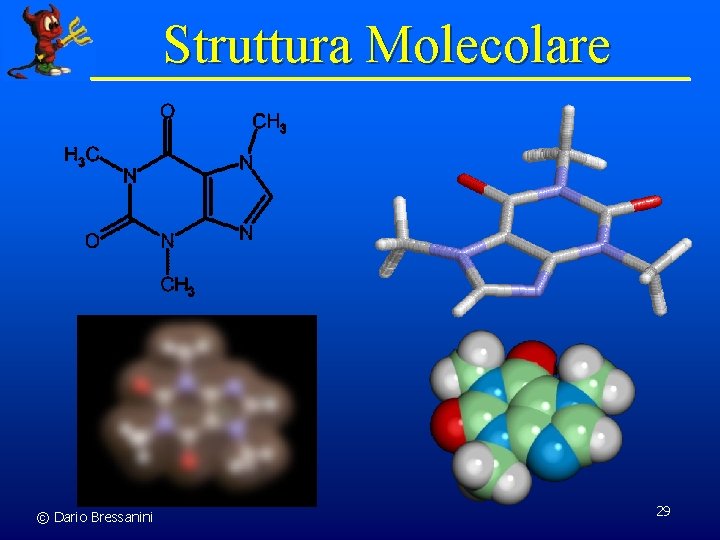
Struttura Molecolare © Dario Bressanini 29
La Chimica al Computer © Dario Bressanini 30

P l a t i n o © Dario Bressanini 31

Microscopio ad effetto tunnel © Dario Bressanini 32
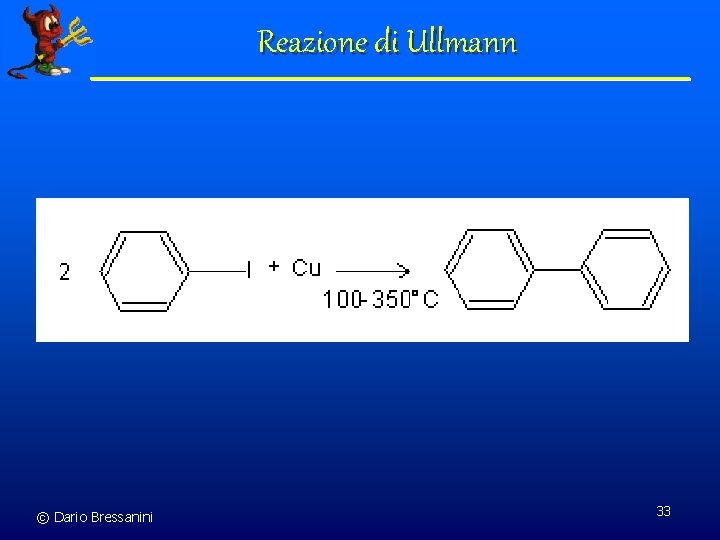
Reazione di Ullmann © Dario Bressanini 33
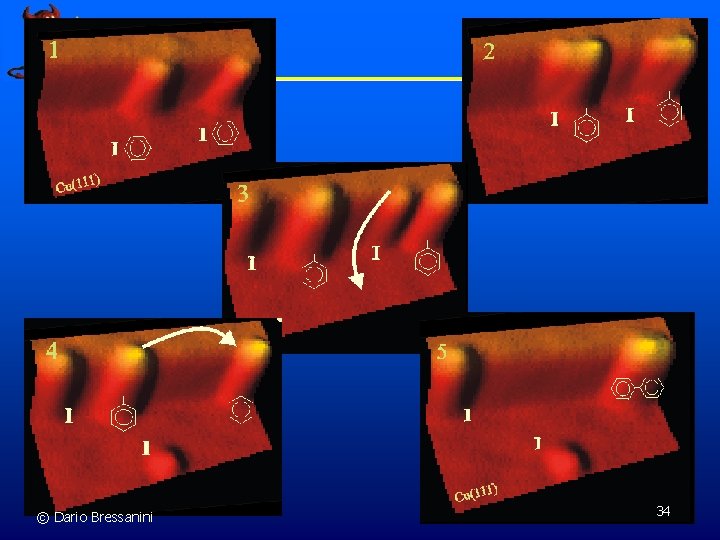
© Dario Bressanini 34

Che cos’è e come è fatta una Molecola?

Cos’è una molecola? n Na. Cl è una molecola? n Na e Cl sono contenuti in Na. Cl? n CH 2, H 2 O e He 2 sono molecole? © Dario Bressanini 36

© Dario Bressanini 37

Che cos’è una molecola? H 2 Al. F C 3 C 2 H c-C 3 H l-C 3 H C 5 C 4 H C 5 H l-H 2 C 4 C 6 H CH 3 C 3 N CH 2 CHOH CH 2 CHCN HCOOCH 3 CH 2 OHCHO Al. Cl C 2 O C 3 N C 4 Si C 2 H 4 CH 3 C 2 H CH 3 COOH? C 2 S C 3 O l-C 3 H 2 CH 3 CN HC 5 N C 7 H HCO CH 2 D+ CH CH 2 C 3 S c-C 3 H 2 CH 3 NC HCOCH 3 H 2 C 6 CH 3 SH CH 4 CH+ HCN C 2 H 2 CH 2 CN CH 3 OH NH 2 CH 3 CN c-C 2 H 4 O HC 3 NH+ HC 2 CHO CO HCO+ HCCN HC 3 N NH 2 CHO CO+ HCS+ HCNH+ HC 2 NC C 5 N CP HOC+ HNCO HCOOH CSi H 2 O HNCS H 2 CHN HCl H 2 S HOCO+ H 2 C 2 O KCl HNC H 2 CO H 2 NCN NH HNO H 2 CN HNC 3 NO Mg. CN H 2 CS Si. H 4 Molecole presenti in comete, nebulose, spazio interstellare… © Dario Bressanini 38
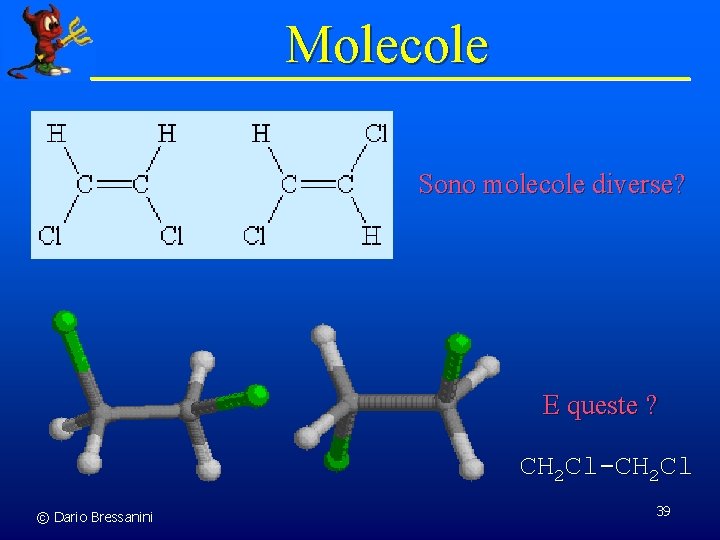
Molecole Sono molecole diverse? E queste ? CH 2 Cl-CH 2 Cl © Dario Bressanini 39

Che cos’è il Legame Chimico?

© Dario Bressanini 44
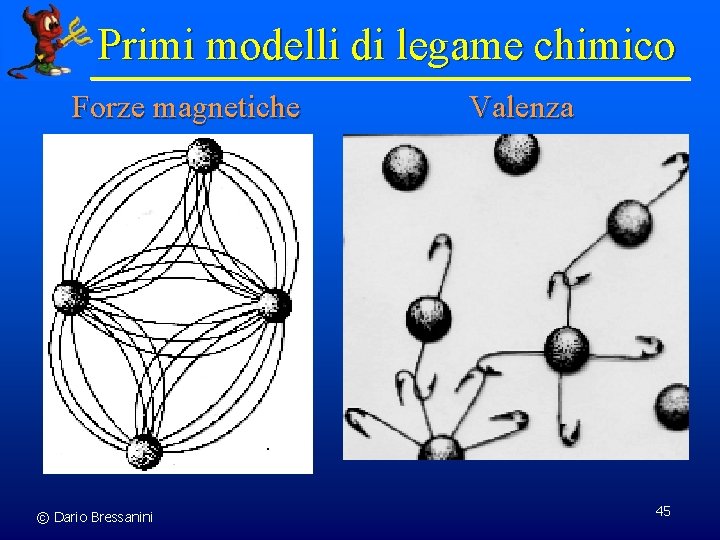
Primi modelli di legame chimico Forze magnetiche © Dario Bressanini Valenza 45

Modello di Lewis Atomo cubico © Dario Bressanini 46
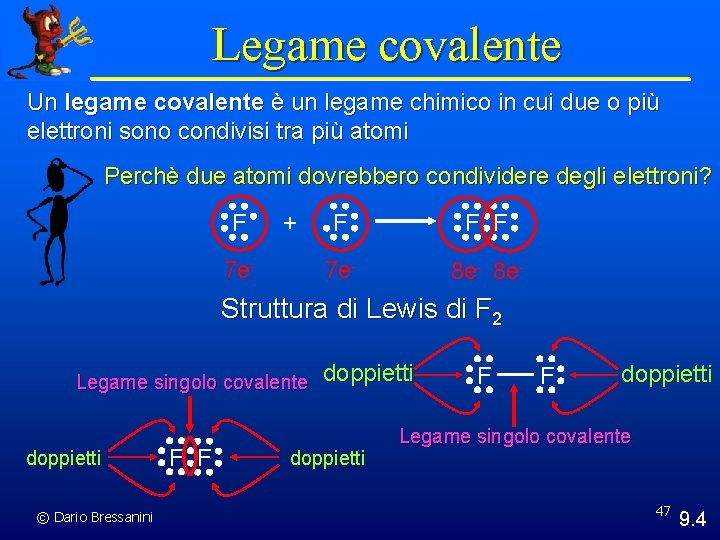
Legame covalente Un legame covalente è un legame chimico in cui due o più elettroni sono condivisi tra più atomi Perchè due atomi dovrebbero condividere degli elettroni? F + 7 e- F F F 7 e- 8 e- Struttura di Lewis di F 2 Legame singolo covalente doppietti © Dario Bressanini F F doppietti Legame singolo covalente 47 9. 4
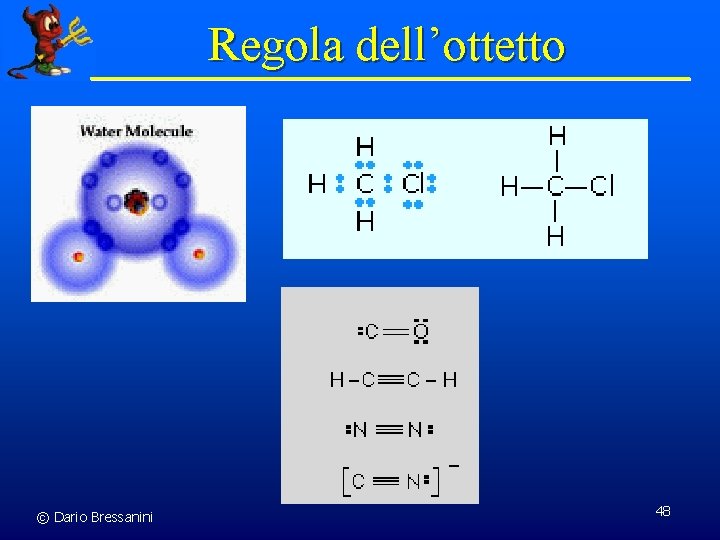
Regola dell’ottetto © Dario Bressanini 48

Problemi O H O Be NO © Dario Bressanini O 2 H N – 5 e. O – 6 e 11 e- Molecola paramagnetica ? ? Ottetto incompleto ? ? Be. H 2 N O Elettroni dispari ? ? 49
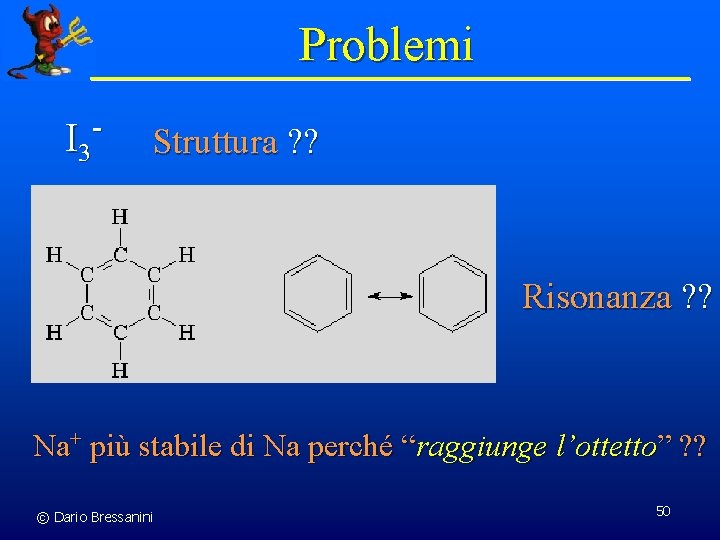
Problemi I 3 - Struttura ? ? Risonanza ? ? Na+ più stabile di Na perché “raggiunge l’ottetto” ? ? © Dario Bressanini 50

Modelli Avanzati n Il modello di Lewis ora è usato solamente come ausilio grafico n Il Legame Chimico NON è osservabile n È necessario utilizzare le leggi matematiche della Meccanica Quantistica n Come presentare delle teorie realistiche del legame chimico senza poter usufruire dell’apparato matematico? © Dario Bressanini 51
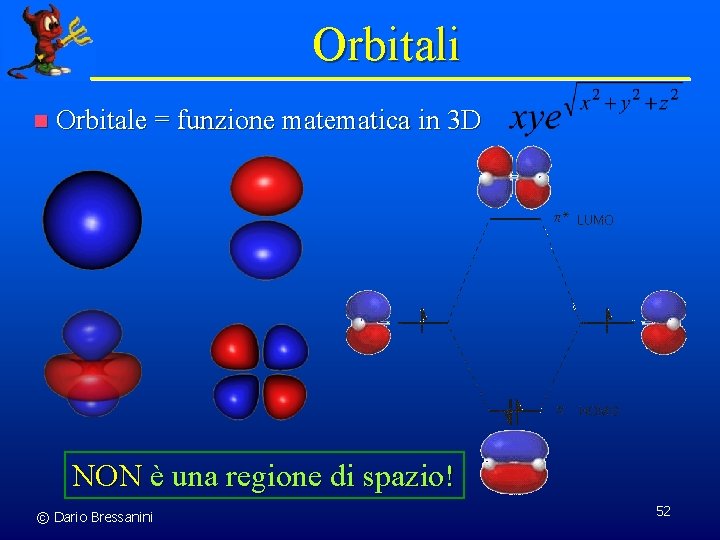
Orbitali n Orbitale = funzione matematica in 3 D NON è una regione di spazio! © Dario Bressanini 52

Teorie avanzate n n VB: Valence Bond (Legame di Valenza) ´ Orbitali ibridi ´ Risonanze MO: Molecular Orbitals (Orbitali Molecolari) ´ n LCAO, combinazione di orbitali atomici Teorie EQUIVALENTI, dal punto di vista matematico, ma che costruiscono rappresentazioni mentali diverse. © Dario Bressanini 53

Problema n Gli orbitali hanno senso fisico solamente per atomi e molecole con un solo elettrone n Non è possibile apprezzare la differenza tra le due teorie SENZA il necessario apparato matematico n Vengono spesso confusi e mischiati concetti delle due teorie n Gli studenti confondo spesso il modello con la realtà ´ Esempio: Perché il metano CH 4 è tetraedrico? ´ Risposta (sbagliata): perché il carbonio è ibridizzato sp 3 © Dario Bressanini 54

Problema: il carbonio n C: 1 s 2 2 p 2 n Anche questo è un modello! n Gli elettroni sono INDISTINGUIBILI, non esiste l’elettrone 1 s n Come costruire CH 4 con il carbonio 1 s 2 2 p 2 ? ´ n VB: costruiamo ‘orbitali ibridi’ = combinazione matematica Gli orbitali ibridi NON corrispondono ad un processo fisico, e non hanno senso nella teoria MO! © Dario Bressanini 55
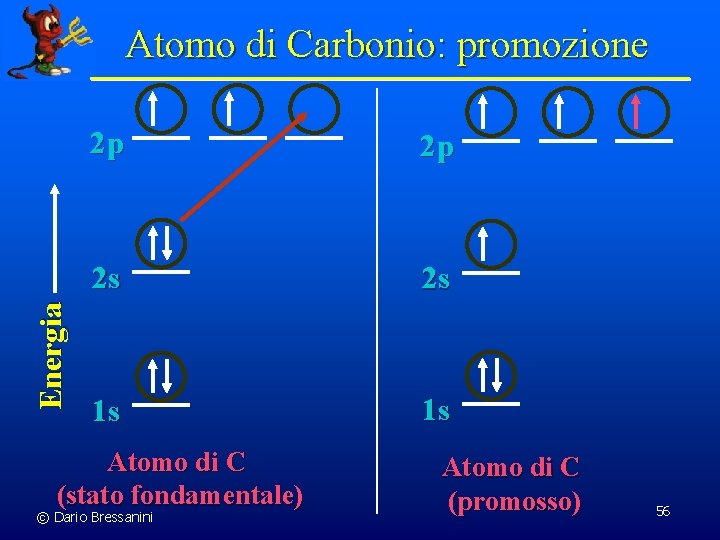
Energia Atomo di Carbonio: promozione 2 p 2 p 2 s 2 s 1 s 1 s Atomo di C (stato fondamentale) © Dario Bressanini Atomo di C (promosso) 56
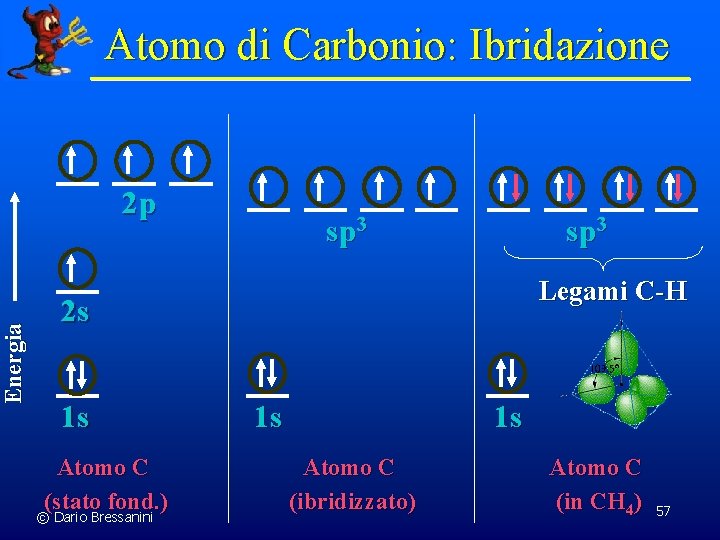
Energia Atomo di Carbonio: Ibridazione 2 p sp 3 Legami C-H 2 s 1 s Atomo C (stato fond. ) © Dario Bressanini 1 s 1 s Atomo C (ibridizzato) Atomo C (in CH 4) 57

Atomo di Carbonio: Ibridazione n Tuttavia, l’ibridazione è solamente una procedura matematica, senza significato fisico n Gli orbitali ibridi vengono costruiti appositamente per soddisfare l’immagine mentale del “legame” come “sovrapposizione di orbitali direzionali” n MO: machisseneimporta dell’orientamento degli orbitali atomici. Si ottiene lo stesso risultato anche usando gli orbitali originali px py pz e 2 s © Dario Bressanini 58
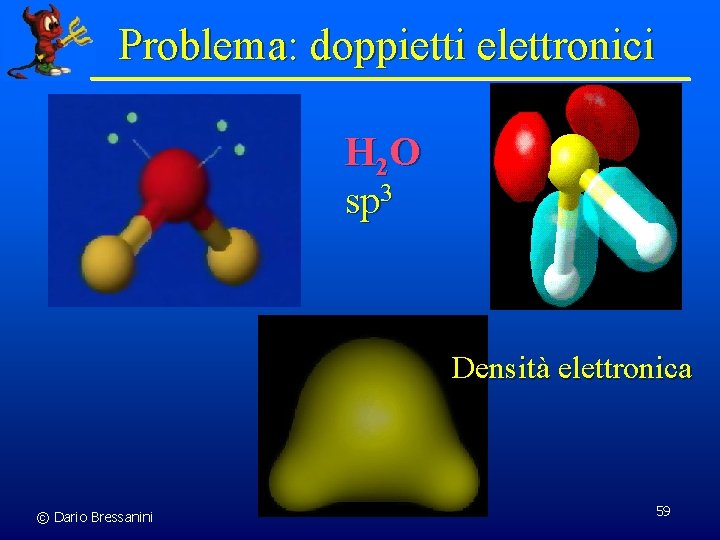
Problema: doppietti elettronici H 2 O sp 3 Densità elettronica © Dario Bressanini 59
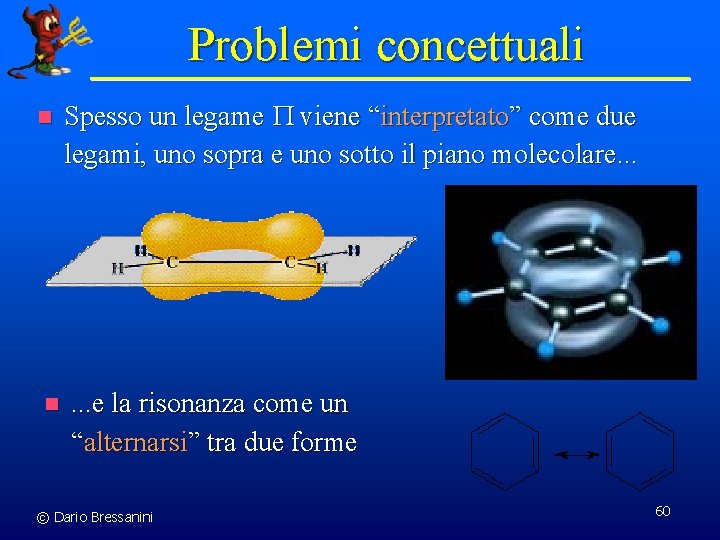
Problemi concettuali n n Spesso un legame P viene “interpretato” come due legami, uno sopra e uno sotto il piano molecolare. . . e la risonanza come un “alternarsi” tra due forme © Dario Bressanini 60

MO: Oracolo Quantistico Carbonio 1 s 2 2 p 2 Descrizione Cattiva 1 s 2 2 p 2 + 1 s 2 2 p 4 Buona 1 s 2 2 p 2 + 1 s 2 2 p 4 + 1 s 2 2 p 3 d 3 Migliore Infiniti termini. . . Perfetta Come costruire un’immagine mentale della ‘somma’ ? © Dario Bressanini 61
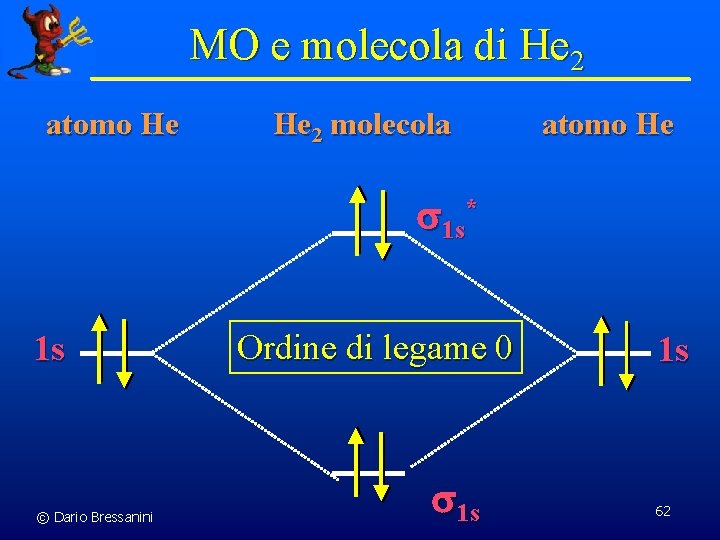
MO e molecola di He 2 atomo He He 2 molecola atomo He s 1 s* 1 s © Dario Bressanini Ordine di legame 0 s 1 s 1 s 62

MO e molecola di He 2 n Però la molecola He 2 esiste (anche se è delicatissima) nonostante il semplice modello MO affermi il contrario Perché? n Perché lo dice la matematica della Meccanica Quantistica! © Dario Bressanini 63

Atomi nelle Molecole (AIM - Bader) n Il “legame chimico” non si vede nella funzione d’onda n . . . tuttavia è troppo utile al chimico per abbandonarlo n Viene recuperato attraverso la densità elettronica © Dario Bressanini 64
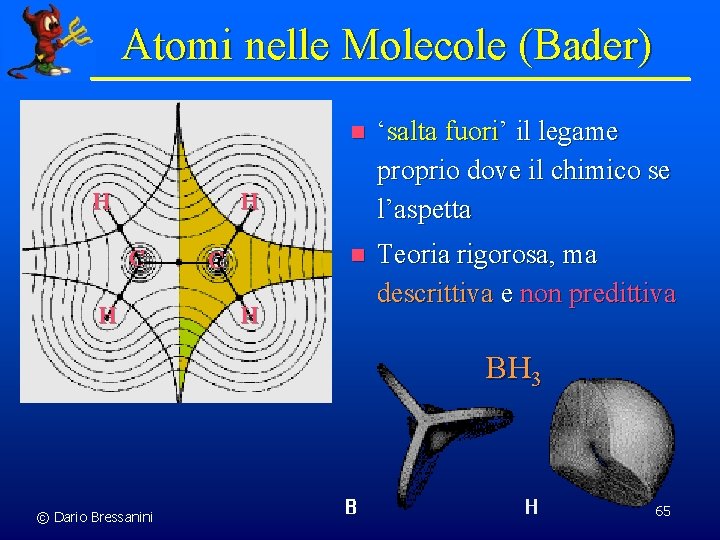
Atomi nelle Molecole (Bader) H n ‘salta fuori’ il legame proprio dove il chimico se l’aspetta n Teoria rigorosa, ma descrittiva e non predittiva H C H BH 3 © Dario Bressanini 65

Accuratezza e Rappresentazione Più si “spinge” l’accuratezza matematica per ottenere risultati confrontabili con gli esperimenti (Calori di reazione, spettri IR, UV, NMR, Costanti di velocità) MENO riesco a ritrovare i concetti di struttura, legame semplice e doppio, cariche, etc. . . © Dario Bressanini 66

Come si può fare? NON SI PUÒ! La meccanica quantistica è essenzialmente matematica, e una sua comprensione non è possibile senza una conoscenza dei metodi matematici coinvolti L. Pauling La matematica è ora così centrale, così “dentro”, che senza di essa non possiamo sperare di capire la chimica C. A. Coulson © Dario Bressanini 67

Come si può fare? n Vari studi mostrano come i concetti della MQ, introdotti senza l’apparato matematico, portano a confusione e costruzione di preconcetti negli studenti n Queste difficoltà NON derivano da un cattivo insegnamento o da scarse capacità degli studenti n Evitare di introdurre gli orbitali, e usare la teoria VSEPR per prevedere la geometria molecolare Orbitals should be left out (L. Pauling) n La chimica insegnata dovrebbe essere ‘chimica dei materiali e del mondo intorno a noi’ © Dario Bressanini 68

© Dario Bressanini 69

© Dario Bressanini 70

© Dario Bressanini 71

© Dario Bressanini 72

La Chimica intorno a noi © Dario Bressanini 73

Evoluzione della Scienza “Ho mal d’orecchio” 2000 BC “Tieni, Succhia questa radice miracolosa” 1000 AD “Quella radice e’ veleno. Recita questa preghiera” 1850 AD “Questa preghiera e’ superstizione. Bevi questa pozione” 1940 AD “Questa pozione e’ veleno. Ingoia questa pillola” 1985 AD “Questa pillola non funziona. Prendi questo antibiotico” 2000 AD “ Questo antibiotico non e’ Biologico e Naturale. Tieni, succhia questa radice ecobiodinamica” © Dario Bressanini 74

The END
- Slides: 71