Universit Mohand Akli Ouelhadj Bouira Facult des Sciences

Université Mohand Akli Ouelhadj ‐ Bouira Faculté des Sciences de la Nature et de la Vie et des Sciences de la Terre Département d’agronomie BIOCHIMIE ALIMENTAIRE Dr. MOUDACHE. M Année Universitaire : 2019/2020
Programme 1. Introduction 2. Les viandes (système protéique musculaire) 3. Le lait et produits laitiers 4. Céréales 11/02/2022
Programme 5. Les fruits et légumes 6. Les lipides alimentaire (oxydation) 7. Alterations enzymatiques et non enzymatiques (chimique) 11/02/2022
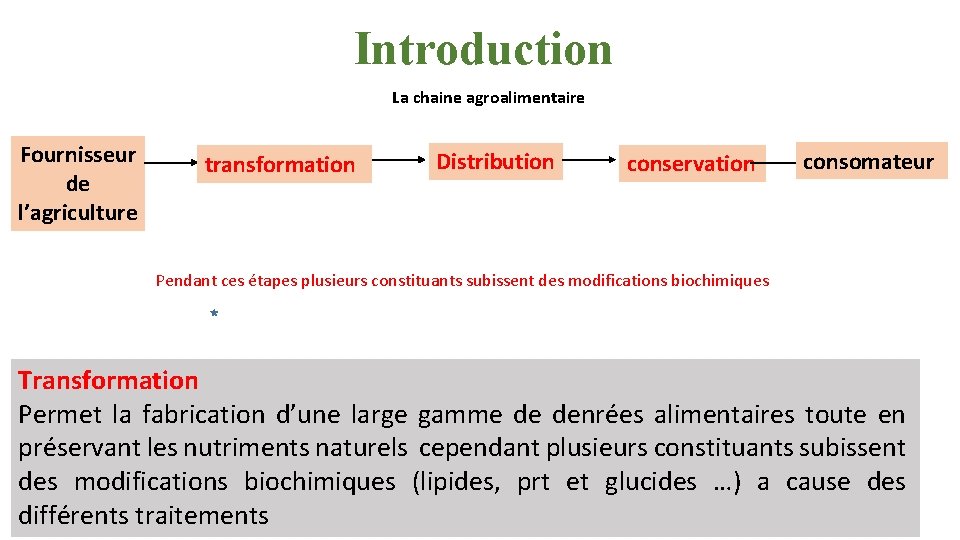
Introduction La chaine agroalimentaire Fournisseur de l’agriculture transformation Distribution conservation consomateur Pendant ces étapes plusieurs constituants subissent des modifications biochimiques Transformation Permet la fabrication d’une large gamme de denrées alimentaires toute en préservant les nutriments naturels cependant plusieurs constituants subissent des modifications biochimiques (lipides, prt et glucides …) a cause des différents traitements

Conservation: 1) Action enzymatique: tous les aliments contiennent des enzymes naturelles qui décomposent les prt lipides et glucides pour faciliter la croissance de l’animal ou de la plante Une fois un animal est tué ou une plante est récolté , si c’est enzymes ne sont pas sous controle Les enzymes continuent a travailler et dégrader les nutriment ce qui induit la détérioration de l’aliment ( modifications biochimiques)

2) Action microbienne: Tous les aliments peuvent être attaqués par des bactéries , champignon entrainant leurs pourrissement

3. Oxydation Plusieurs composants de l’aliment sont les cibles privilégiées de l’oxygéne de l’aire qui provoque des modification biochimiques de plusieurs nutriments

Distribution Transport dans des véhicules réfrigérés adaptés à un appareillage spécifique perméttant le monitoring constant de la température Eviter la détérioration des aliments

Chapitre 1 : Les viandes et poissons

- Les viandes représentent une partie importante des apports en prt chez l’adult - Elle représente une valeur nutritionnelle intéressante car elle apportent les AA indispensable en quantités équilibrées ainsi les vitamines (B 12) et le fer - Elle résulte d’une série de réactions biochimiques se déroulant dans les cellules musculaires dés la mort de l’animal ( mammifères, oiseaux)

1. Le système protéique musculaire la viande comprend des proportions variables : -du tissu musculaire - du tissu gras - des parties osseuses et cartilagineuses -dans les cas des oiseaux essentiellement la peau Power point : le muscle 11

Le tissu musculaire Est le composant le plus important et il se compose de: ‐Fibres musculaires ‐Tissu conjonctif, entoure les fibres et contient des vaisseaux et des nerfs ‐Tissu lipidique ‐Myoglobine( responsable de la couleur rouge et sert de réserve d’O 2)
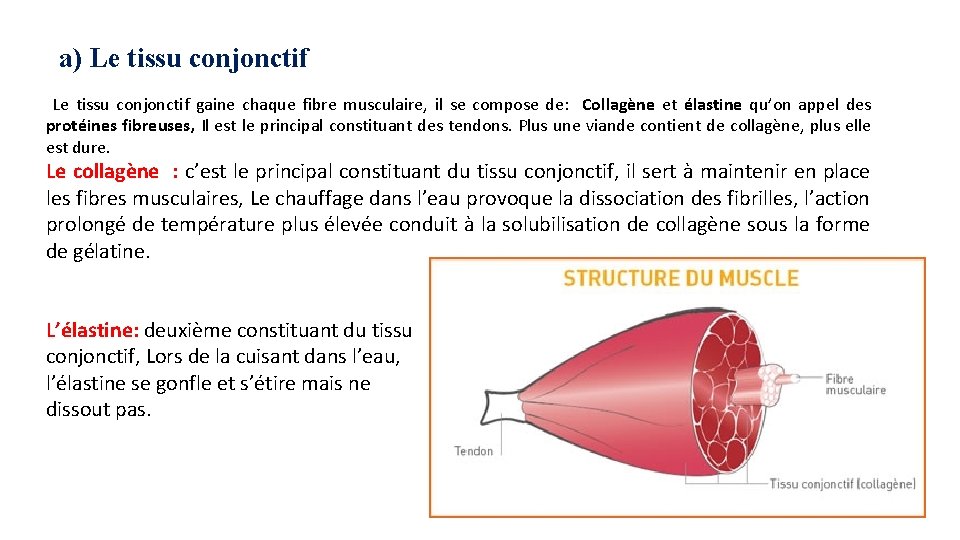
a) Le tissu conjonctif gaine chaque fibre musculaire, il se compose de: Collagène et élastine qu’on appel des protéines fibreuses, Il est le principal constituant des tendons. Plus une viande contient de collagène, plus elle est dure. Le collagène : c’est le principal constituant du tissu conjonctif, il sert à maintenir en place les fibres musculaires, Le chauffage dans l’eau provoque la dissociation des fibrilles, l’action prolongé de température plus élevée conduit à la solubilisation de collagène sous la forme de gélatine. L’élastine: deuxième constituant du tissu conjonctif, Lors de la cuisant dans l’eau, l’élastine se gonfle et s’étire mais ne dissout pas.
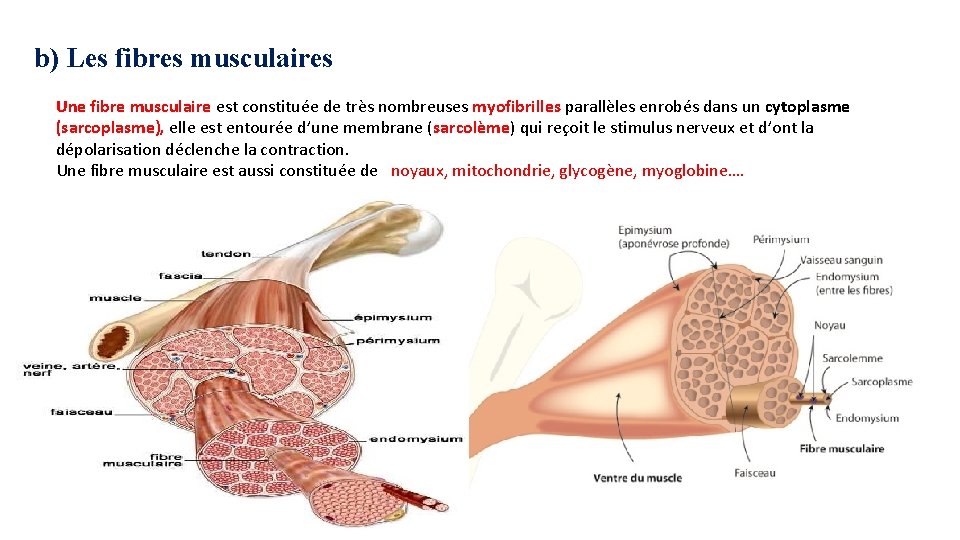
b) Les fibres musculaires Une fibre musculaire est constituée de très nombreuses myofibrilles parallèles enrobés dans un cytoplasme (sarcoplasme), elle est entourée d’une membrane (sarcolème) qui reçoit le stimulus nerveux et d’ont la dépolarisation déclenche la contraction. Une fibre musculaire est aussi constituée de noyaux, mitochondrie, glycogène, myoglobine….
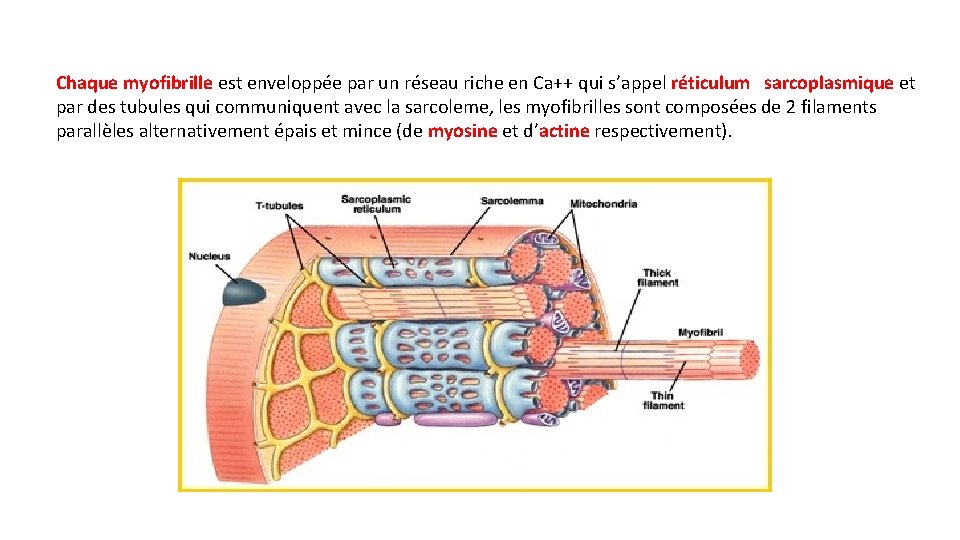
Chaque myofibrille est enveloppée par un réseau riche en Ca++ qui s’appel réticulum sarcoplasmique et par des tubules qui communiquent avec la sarcoleme, les myofibrilles sont composées de 2 filaments parallèles alternativement épais et mince (de myosine et d’actine respectivement).
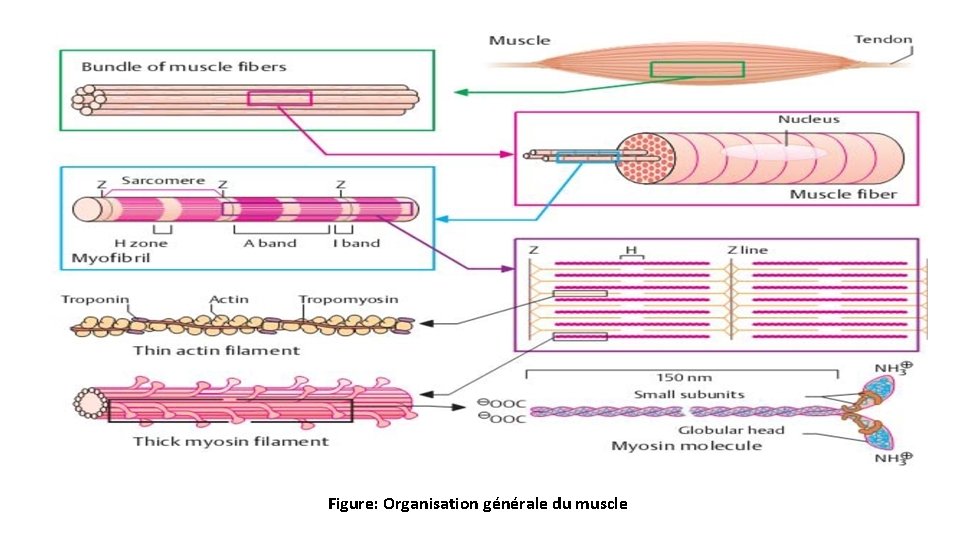
Figure: Organisation générale du muscle

2) Biochimie de la contraction Avant la contraction en présence d’ATP et d’ions Mg+2, mais aussi les ions Ca+2 qui sont retenus dans le réticulum sarcoplasmique, la myosine ne manifeste pas d’activité ATPasique et le muscle est en relaxation. Les 2 protéines seraient sous la forme de 2 complexes * Myosine‐Mg+2‐ATP • Actine‐ADP Au moment de la contraction musculaire toujours en présence d’ATP et Mg+2, lors que le réticulum sarcoplasmique relâche des ions Ca+2 en réponse au stimulé nerveux. Les ions Ca+2 se fixent sur l’actine ( exactement sur la troponine) ce qui vas entrainer une exposition des sites de fixation spécifique pour la myosine Et ainsi l’activité ATPasique de la myosine se manifeste par hydrolyse d’ATP et libération d’énergie pour une interaction temporaire entre myosine et actine (myosine‐actine et la contraction musculaire produit la formation de complexe Myosine‐Mg+2‐ATP‐Ca+2‐ADP‐acine. Au moment de la contraction musculaire : muscle contracté.
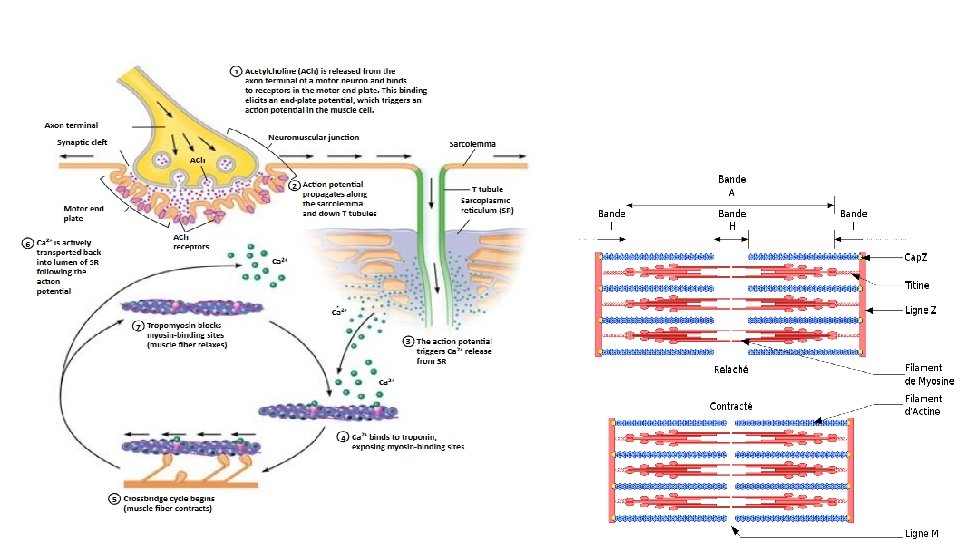

Fin de stimulation, la concentration d’ions Ca+2 diminue jusqu’au seuil de 10‐ 7 M (le Ca est récupéré par le réticulum sarcoplasmique), la contraction prend fin, relaxation de muscle ce qui aboutit à la dissociation de complexe acto‐myosine. • Voie de formation d’ATP : Normalement la teneur en ATP reste constante, ce composé se former en effet par 3 voies : ‐ ADP+ Phosphocréatine Kinase ATP+ créatine ‐ 2 ADP → ATP+AMP libéré. ‐ Quand l’apport d’O 2 par le sang est faible (lors de la contraction violente on a : Glycolyse anaérobie → glucose → 2 lactate+2 ATP.

3. MODIFICATION BIOCHIMIQUE DE SYSTÈME PROTEIQUE APRES LA MORT ü Rigidité cadavérique (rigor mortis) S’installe progressivement au fur et à mesure que la teneur en ATP décroit, elle intervient après la mort en effet : • En absence d’ATP : L’actine et la myosine se lient de façon irréversible.

3. MODIFICATION BIOCHIMIQUE DE SYSTÈME PROTEIQUE APRES LA MORT a‐ Modification dans le tissu musculaire après la mort. L’installation de la rigidité cadavérique est directement perceptible sur la carcasse : la musculature devient progressivement raide et inextensible dans les heures qui suivent la mort de l’animal. Ce phénomène résulte de l’épuisement du composé qui permet au muscle vivant de conserver son élasticité et qui par ailleurs fournit l’énergie nécessaire au travail musculaire, l’adénosine triphosphate (ATP).

• Acidification du tissu musculaire Glycolyse anaérobie → glucose → 2 lactate+2 ATP Après la mort, le turn‐over de l’ATP sera assuré tant que les réserves de phosphocréatine et de glycogène. L’amplitude de la baisse du p. H sera donc fonction des réserves énergétiques. La baisse du p. H résultant de la glycolyse anaérobie inhibe les ATPases sarcoplasmiques (pompes à Ca+2 maintenant le gradient de Ca+2) provoquant ainsi une fuite de Ca+2 dans le réticulum
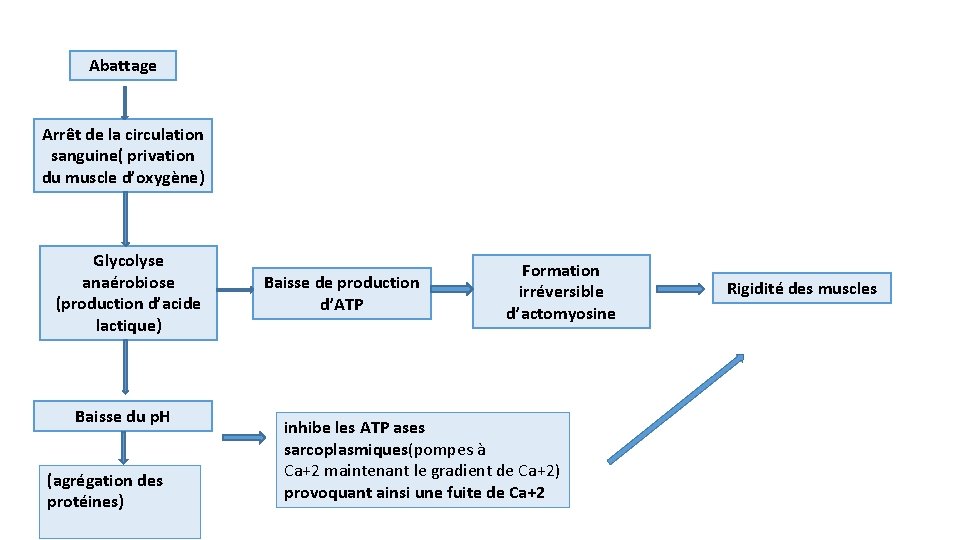
Abattage Arrêt de la circulation sanguine( privation du muscle d’oxygène) Glycolyse anaérobiose (production d’acide lactique) Baisse du p. H (agrégation des protéines) Baisse de production d’ATP Formation irréversible d’actomyosine inhibe les ATP ases sarcoplasmiques(pompes à Ca+2 maintenant le gradient de Ca+2) provoquant ainsi une fuite de Ca+2 Rigidité des muscles

b‐ Facteurs d’influence Le degré de sévérité de phénomènes accompagnants la rigidité cadavérique dépend de : ‐ Etat nutritionnel de l’animale au moment de l’abattage, animale affamé au soumis à un stress ‐ Reserve en glycogène faible ; ‐ La température à laquelle les carcasses sont entreposées.

Si la température n’est pas abaissée rapidement après l’abattage : ‐ p. H diminue rapidement ‐ Ce qui entraine une dénaturation des protéines ; ‐ Une grande partie de l’eau de gel myofibrillaire est expulsé dans les espaces intercellulaires ou exsudée hors de tissus. ‐ La texture de la viande est modifiée très défavorablement ;

‐ Lors de la mastication l’eau est expulsée rapidement et laisse un résidu fibreux et sec ; ‐ Il ya parfois aussi une perte de poids et un changement d’aspect. Si la température atteint 0 à 1 c° avant l’apparition de la rigidité cadavérique (ou congélation) : ‐ Le durcissement est rapide et intense et est précédée dune contraction de muscle

‐ En évite de congeler la viande avant qu’elle est assumée complètement la rigidité ; ‐ On ne doit jamais cuire une viande en état de rigor‐mortis. ü Résolution de la rigidité cadavérique (maturation de la viande) : Au fur et à mesure que la viande vieille : ‐ Sa dureté s’attenue ; ‐ La texture après cuisant dévient meilleur, ‐ Augmentation de la capacité de rétention d’eau.

Le mécanisme de cette maturation ne semble pas résultat d’une dissociation de complexe actomyosine, mais plutôt de détachement des filaments d’actine de la Strie Z (dénaturation progressive des différentes structures composant le muscle) sous l’influence de : ‐ Soit de modification ionique ; ‐ Soit d’enzyme : les Cathepsines provenant des lysosomes fragilisés par l’abaissement de p. H. La maturation de la viande est accompagnée d’autres réactions tel que : l’ Oxydation des lipides ;

Remarque : L’atténuation de la dureté meilleure si rigidité initiale mois sévère. Exemple 1 : Viande de boeuf, fin de la rigidité demande : 3 à 4 semaine à ‐ 15°C, ‐ 15 jours à 0°C, ‐ 2 jours à 20°C, (gain de temps et économie de volume et de locaux), ‐ 1 jour à 43°C, (à titre expérimental avec l’aide d’antibiotique)

Les poissons La structure et le comportement du muscle de poisson ne sont pas fondamentalement différent de ceux du muscle de mamiferes ‐ tissu conjonctif 3 à 10% , plus thermosensible que celui de la viande rouge ‐ muscle brin 10% Les protéines de structure représentent 65 à 75% des protéines totales :

Les poissons ‐Myosine: ‐ 40% environ ‐varie d’une espèce à l’autre ‐ plus sensible aux enzymes protéolytiques, à la chaleur, à la dessiccation, que la myosine des animaux à sang chaud ‐Actine: ‐ 15 à 20%, ‐ moins variable, ‐ plus proche de son homologue des mammifères.

La rigidité cadavérique et sa résolution interviennent très rapidement 5 à 30 heures respectivement, à 0°C. La diminution du p. H est plus faible, passe de 7, 0 à 6, 2 ‐ 6, 5 et remonte à 6, 6 ‐ 6, 7 ; inconvénient car à ce p. H la prolifération microbienne n’est pas inhibée. Les enzymes du poissons sont très actives (exp: lipases restent actives à des basses températures)
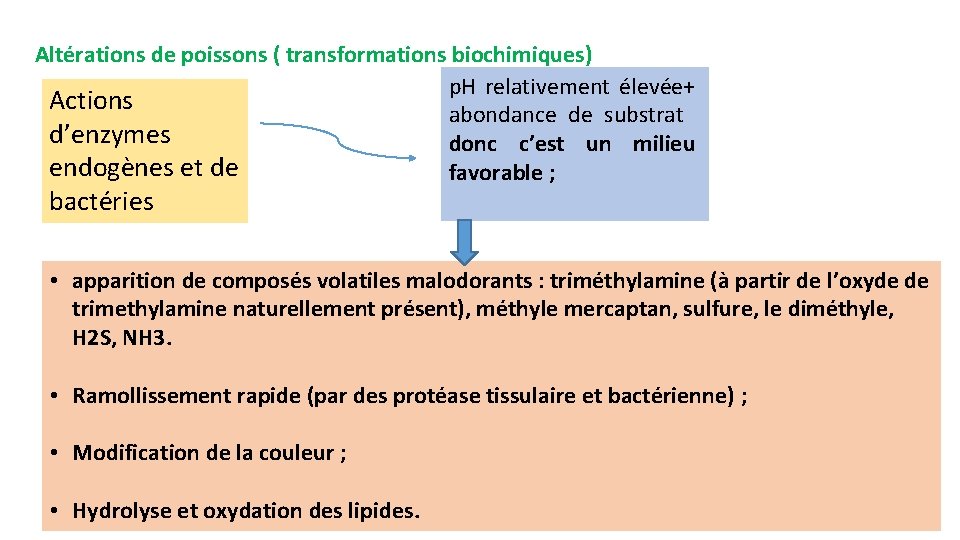
Altérations de poissons ( transformations biochimiques) p. H relativement élevée+ Actions abondance de substrat d’enzymes donc c’est un milieu endogènes et de favorable ; bactéries • apparition de composés volatiles malodorants : triméthylamine (à partir de l’oxyde de trimethylamine naturellement présent), méthyle mercaptan, sulfure, le diméthyle, H 2 S, NH 3. • Ramollissement rapide (par des protéase tissulaire et bactérienne) ; • Modification de la couleur ; • Hydrolyse et oxydation des lipides.

Réfrigération Ces transformations précédemment citées sont ralentis mais non arrêtés car: • Pseudomonas ne cesse de proliférer qu’à environ ‐ 5°C • Plusieurs enzymes lipases notamment demeurent actives même dans le poisson congelé. • Le meilleur procéder s’il est réalisable et de saigner et éviscérer dés la capture Refroidissement dans de l’eau de mer ‐ 10 à ‐ 2

Congélation • Seules températures comprises entre ‐ 25 et et ‐ 35 parviennent à une inhibition totales des enzymes • De ‐ 1 à 0°C on ne distinguent pas des modifications et le tissu musculaire garde sa souplesse, mais les couleurs de la peau peuvent changer L’entreposage prolongée a une température insuffisamment basse de poisson à l’état congelé provoque : a) Pour le poisson maigre (moin riche en matière grasse) : ‐ Dénaturation de protéine ; ‐ Durcissement de la chair (texture).

b) Pour le poisson gras (oxydation des lipides) : ‐ Une perte de poids; ‐ oxydation de lipides( formation de peroxydes, même pendant la décongélation) ; ‐ Durcissement( une perte d’eau sous forme vapeur pendant la congélation et sous forme liquide pendant la décongélation) ; ‐ Apparition des taches ‐perte des sel minéraux et vitamines hydrosolubles

Chapitre 2 : Céréales

On distingue sous l'appellation céréale différentes espèces : Blé tendre ; Blé dur; Maïs; Le riz ; Orge. Elles représentent l’apport principale de calories et de protéines dans des nombreuses régions en voie de développement (90% contre 25% seulement dans les pays industrialisés). La valeur nutritionnelle de ces protéines est cependant relativement faible (déficience en lysine).

VI. 1. 1. Utilisation : Farine: Pain (blé tendre), Semoule: Pâtes alimentaires, Kouskous, galettes (blé dur) ; VI. 1. 2. Structure : La structure des graines est semblable d’une céréale à l’autre: Une graine de céréale est constituée de 3 parties : Les enveloppes, l’albumen le germe

a‐ les enveloppes : Elles ont un rôle de protection (plusieurs couches successives), riche en cellulose indigestible, mais aussi en protéines, en vitamine B 1 et B 2. b‐ L’amande farineuse( albumen) : C’est la partie centrale de graine, elle est constituée par des grains d’amidon enchâssés dans un réseau protéique de gluten. L’amidon : pondéralement c’est le plus important (70%), sous forme de granules sphériques, il joue un rôle important durant la fermentation panaire.

Le gluten : c’est le complexe protéique « gliadine‐glutenine » , c’est une forme de matière protéique spéciale au blé, c’est lui qui confère à la pâte les propriétés élastiques. Les qualités de la pâte dépendent de la qualité et la quantité du gluten présent dans l’amande farineuse. C‐ Le germe : (l’embryon), Il est particulièrement riche en lipides

Composition La graine de blé est constituée essentiellement par : ‐ 10 à 14 % d’eau, ‐ matières organique (glucide, matière azoté, lipides), ‐ faible proportion des matières minérales (80% se trouvent dans les enveloppes contre 20% dans l’amande, les K, P, Ca, Mg possèdent les teneurs les plus élevés).

‐ Faible proportion de matière grasse( 1 à 8%) dont la majorité se trouve dans le germe et les enveloppes. ‐ Faible proportion en matière azotée (6 à 12% de protéines): localisés dans l’albumen ( glutélines (dans le cas de blé: glutenine), albumines, prolamines(dans le cas de blé: gliadine), globulines) ‐ 65 à 70 % de sucres sous forme d’amidon (sucre complexe) constitue la majeure partie de l’albumen

Dans le cas de mauvaise conditions de conservation, Ces constituants influent négativement sur la valeur boulangère par l’élévation de l’acidité grasse et sont à l’origine de phénomène de rancissement.

PANIFICATION ET BIOCHIMIE DE PAIN ‐La farine contient glucose, fructose, saccharose et lévosine, sucres directement fermentescibles et l’amidon ‐Contient des α et β amylases qui permettent la libération de sucres fermentescibles (maltose) de pâte dès le début du pétrissage.

FABRICATION DU PAIN
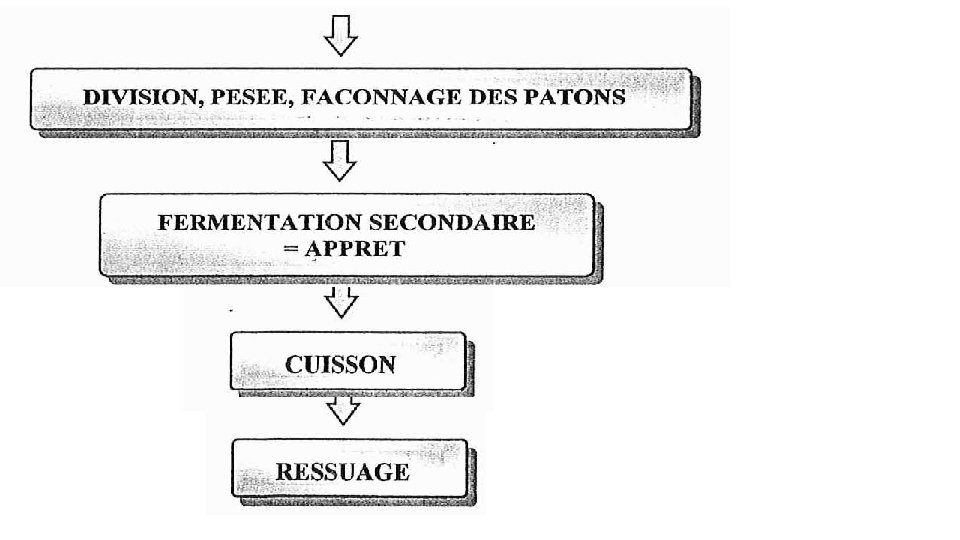

a‐ Pétrissage : il permet : ‐ Absorption de l’eau par les protéines et les granules d’amidon; ‐ Développement de l’élasticité (gluténine) et de l’extensibilité (gliadine) du gluten probablement par : • Oxydation à l’air de groupement sulfhydrile SH. • Réarrangement des ponts désulfure (SS). ‐ libération de sucres fermentescibles (maltose) par les amylases de la farine

b 1‐ Fermentation principale(Phase pointage): ‐ La levure fermente les glucides libres de la farine (préexistants) avec production de CO 2 et l’alcool, ‐ mais à ce stade, c'est l'éthanol qui joue le plus grand rôle car CO 2, se redissous dans l'eau. . ‐ pendant ce temps au fur et à mesure de la consommation des sucres, (maltose), substrat de l’activité fermentaire. les amylases (α et β) attaquent les granules d’amidon pour produire: maltose, dextrine et traces du glucose pour Renouveler le stock glucidique
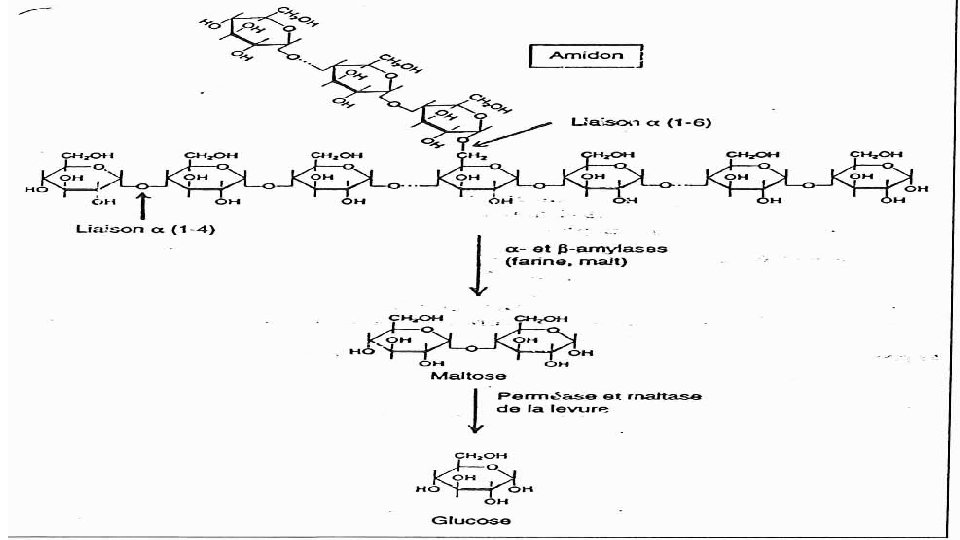
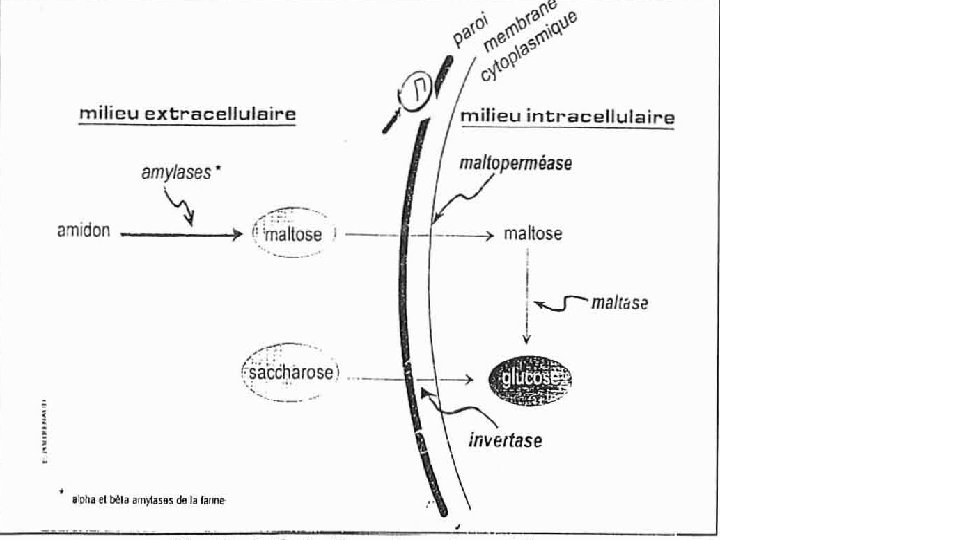

b 2‐ Phase de l'apprêt: ‐ L'amidon est dégradé en sucres simples. Ici, la libération de CO 2, a plus d'importance que la production d'éthanol car le gaz remplit les alvéoles du réseau de gluten formé au pétrissage. ‐ La pate gonfle ‐ Production de constituants secondaires, constituants de l'arome acide organique, alcool, aldéhyde, ester.

C‐ Cuisson: c. 1. Développement de pâton ( 75°C) lié à: ‐ Expansion de CO 2+ évaporation de l'alcool. c. 2. Formation de la croute: • 110 à 150 °C Dextrinisation et caramélisation. • T> 150°C Torréfaction grillage;

d‐ Rassissement de pain (ressuyage): A cours de refroidissement l'amylose (extrait des granules d'amidon pendant le pétrissage de la pate et lors de la cuisson) cristallise. En vieillissant le pain durcit et perte son élasticité, il ya cristallisation de l'amidon de la mie. la levure de boulangerie a subit une amélioration: pour avoir la capacité de dégrader l’amidon en maltose puis en glucose

Remarque Les levures: 2 types de métabolisme. • Respiration CO 2 + H 2 O + énergie (favorise biomasse: multiplication cellulaire augmente). Consommation moindre en glucose

• Fermentation( même en aérobiose; concentration> 5% de glucose: CO 2 + éthanol+ énergie faible ‐diminution de la reproduction cellulaire ‐Production (accumulation) de constituants secondaires: arôme (acide, alcool, ester, aldéhyde…) la levure de boulangerie a subit une amélioration: pour avoir la capacité de dégrader l’amidon en maltose puis en glucose( maltopanification)

Chapitre 3: Lait et produits laitiers

COMPOSITION ET VALEUR NUTRITIONNELLE: 1. Composition • Les laits secrétés par différentes espèces de mammifères présentent des caractéristiques communes et contiennent les mêmes catégories de composants : eau, protéine, lactose, matière grasse et minérale, • cependant les proportions respectives de ces composants varient largement d’une espèce à une autre (Tableau), • en outre, la composition des matières protéiques, grasses et minérales peut être très différentes selon l’espèce considéré.

cette composition varie toute fois beaucoup en fonction de l’alimentation, de la période de lactation, de la saison et de la race animale. Exemple du lait de vache: Eau: 90% MG: 3% PRT: 3% LACTOSE: 4%
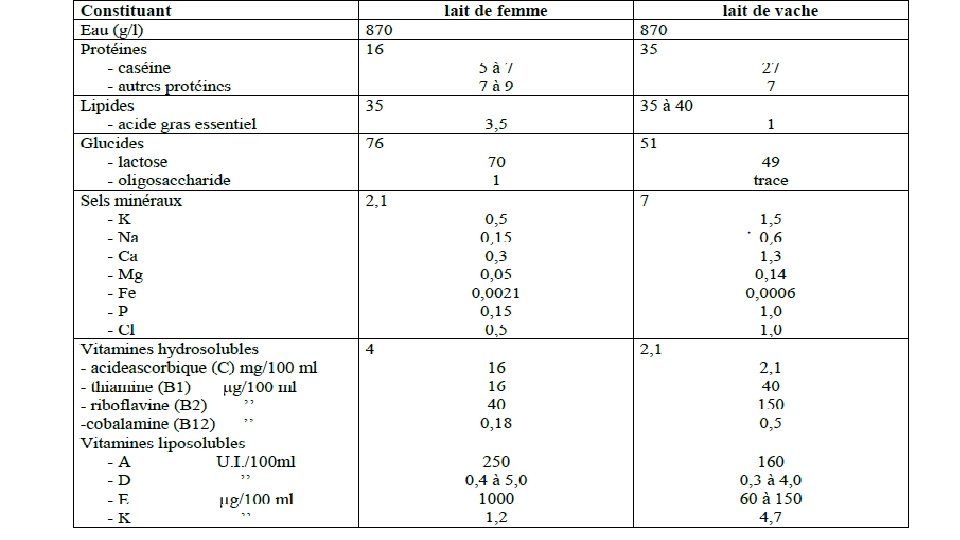

Le lait contient aussi des enzymes, des anticorps, des hormones, des particules en suspension (globules de matière grasse, micelles de caséine) et même certains cellules (macrophages), il contient inévitablement des micro‐ organismes et accidentellement les antibiotiques et antiparasitaires

D’un point de vue physique, le lait est constitué d’un système complexe, système à plusieurs phases : ‐ Phase dispersante : Lactosérum (lactose+ protéine globulaire) ; ‐ Phase particulaire 1 : Emulsion des globules de matière grasse ; ‐ Phase particulaire 2 : Suspension colloïdale des micelles protéique (caséine + sels minéraux, phosphate et calcium).
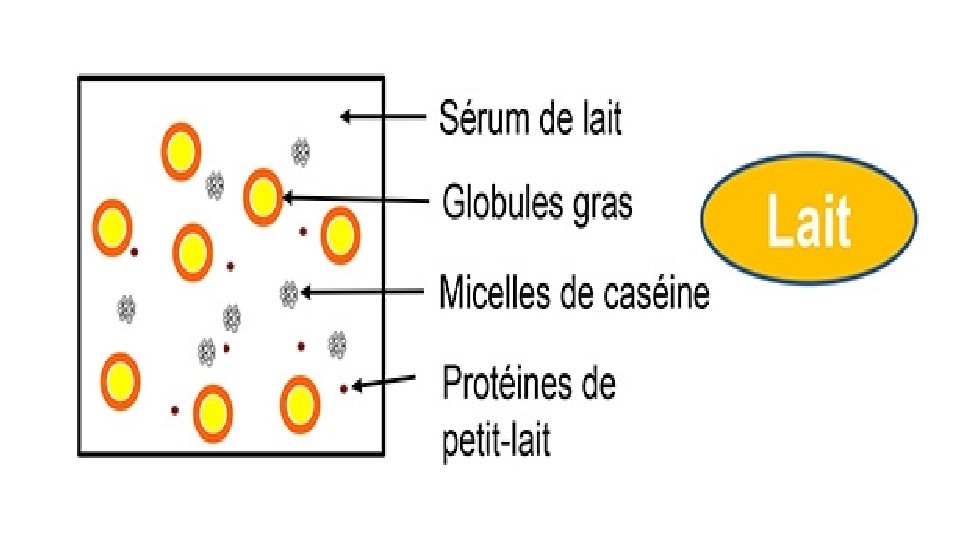

Le système protéique du lait : ‐Les caséines (phosphoprotéines), représentent 80% des protéines du lait de vache, ‐ β. lactoglobuline 10%, ‐α. lactalbumine 2%, ‐autres protéines (enzymes, immunoglobuline, . . . ).

a) Les caséines : On précipite la fraction caséinique totale par abaissement du p. H du lait jusqu’à environ 4, 7, elles comprennent plusieurs types de molécules : ‐αs. caséine 50%, ‐k‐caséine 15%, ‐ β. caséine 30%, ‐ɣ. caséine 5%.

Lorsque les caséines sont coagulées, les autres protéines restent en solution en même temps que le lactose et les sels, constituant le lactosérum.

Dans le lait frais, les lipides (insolubles dans l’eau) s’entourent de molécules de caséine, car leur partie lipophile baigne dans la matière grasse et la partie hydrophile reste dans l’eau. Il se forme donc des micelles, qui sont constituées de gouttelettes de matière grasse entourées de molécules de caséine. Le lait est une émulsion*.
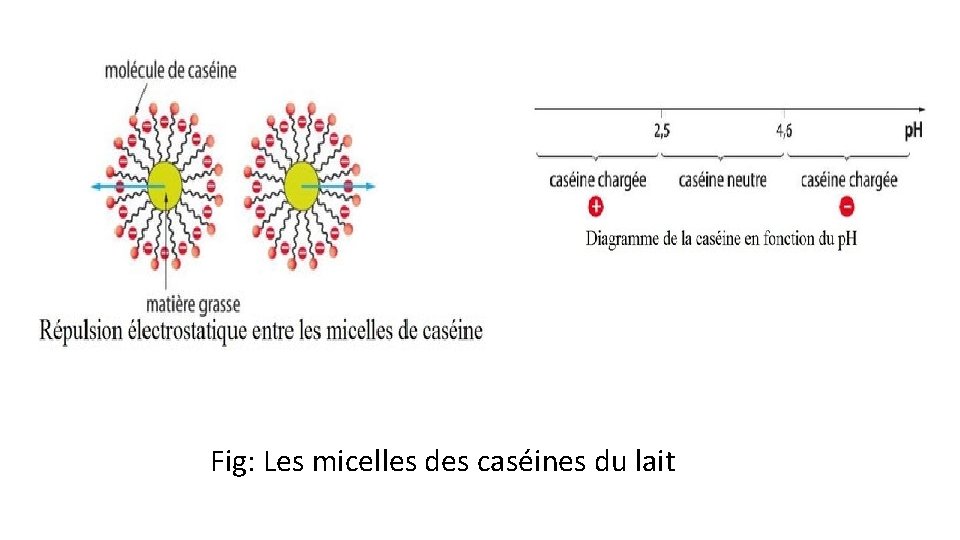
Fig: Les micelles des caséines du lait
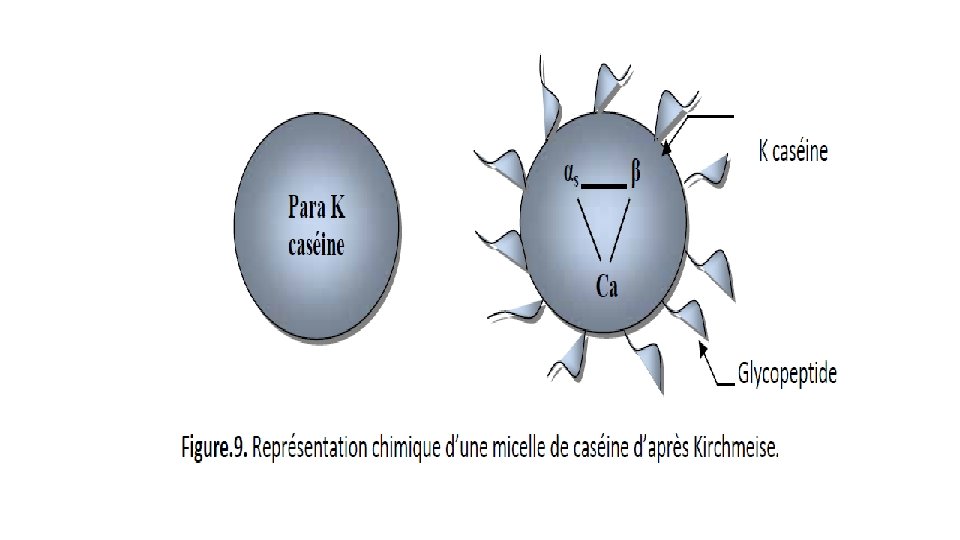

Dans la structure de la micelle, la K caséine se trouve principalement à l’extérieur, elle est très soluble dans l’eau grâce aux sucres quelle contient et qui sont hydrophiles Les caseines K possèdent des régions hydrophiles en particulier le CMP ( caseinomacropéptide qui est un glycopéptide) permet de stabiliser la micelle
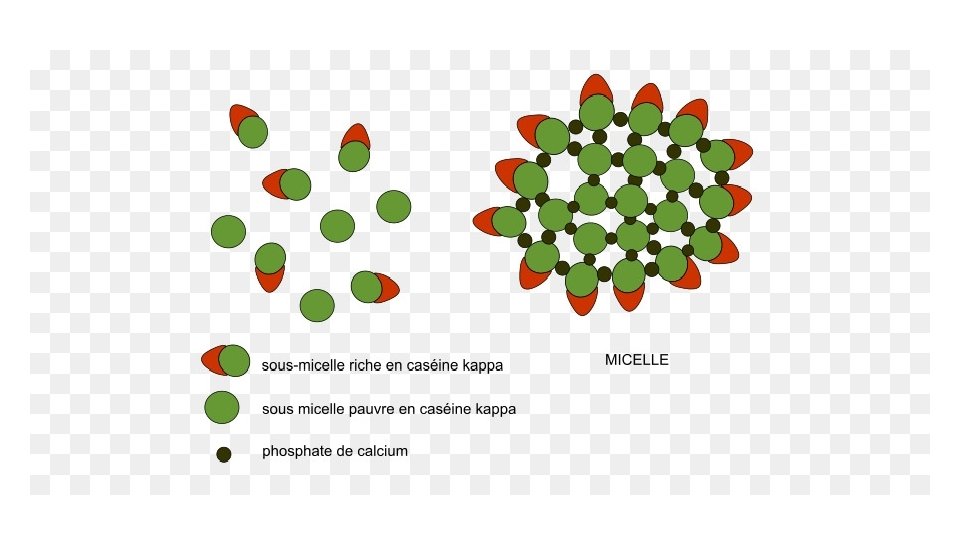

Les protéines du lactosérum (prt solubles) ü Elles représentent 20% des protéines de lait, ü elles sont de faible poids moléculaire, ü elles se trouvent dans le lait sous forme de monomère et polymère, ü elles ne se précipitent pas à leur point isoélectrique, ü elles ne contiennent pas de phosphore,

ü Elles ne se précipitent pas sous l’action enzymatique, ü elles ont une meilleur valeur nutritionnelle, riches en Aa soufrés et riches en lysine, ü elles sont divisées en : ‐ β lactglobuline = 10% ; ‐ α lactalbumine = 2% ; ‐ Immunoglobuline et sérumalbumine ; ‐ Protéose‐peptone et lactoferrine.

Les protéines solubles ne se coagule pas par la voie enzymatique mais elles sont déstabilisées par la chaleur (dénaturation) Remarque : la ‐lactoglobuline et l’‐lactalbumine forment la peau du lait bouillit.

PROCESSUS BIOCHIMIQUE DE LA COAGULATION DE LAIT Le PHi (isoélectrique) des caséines est proche de 4. 7. ‐ On précipite la fraction caséinique totale par l’abaissement de p. H de lait jusqu’à 4. 7

La coagulation de lait correspond à une déstabilisation de l’état micellaire originale de la caséine, le résultat est formation d’un caillé, cette déstabilisation est réalisée : ‐ Soit par voie acide ; ‐ Soit par voie enzymatique.

1. Coagulation par acidification lactique : Par abaissement de p. H jusqu’au environ de point isoélectrique de la fraction caséinique, l’acidification peut être effectué : ‐ Soit par addition d’acide; ‐ Soit le plus souvent par ensemencement de lait avec levains lactiques.

Cette acidification entraine : • Une neutralisation de charges négatives portées par les caséines ; • Des micelles de caséine se floculent et se soudent formants au repos un gel homogène ; • Une déminéralisation progressive des micelles qui se désintègrent en sous unités ; • Le Ca colloïdale migre dans le sérum.
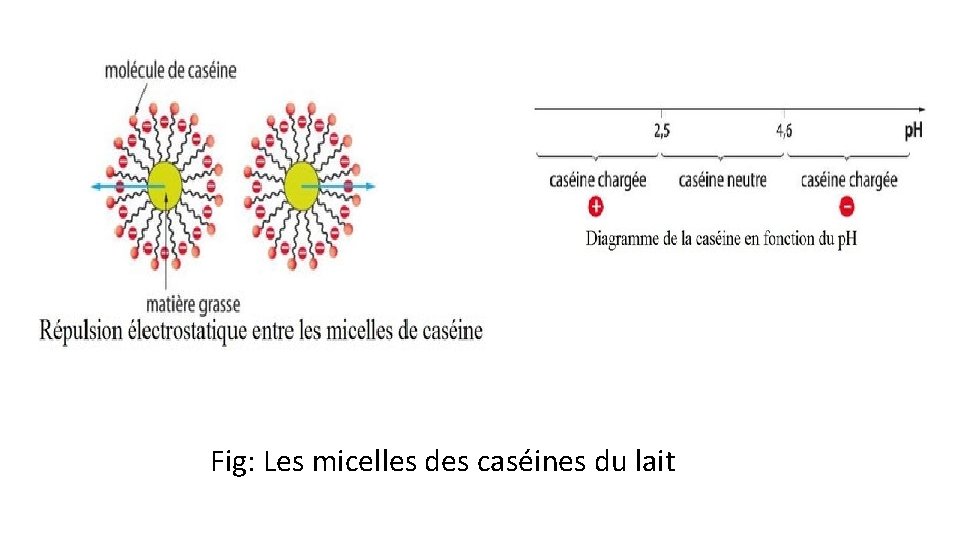
Fig: Les micelles des caséines du lait

2. Coagulation par action de la présure : Divers enzymes protéolytiques ont la propriété de coaguler de lait, elles sont d’origine : • Animal : Présure, pepsine ; • Végétale : Bromoline, fusine ; • Microbienne : Protéase fongique : Mucor pucillus, Mucor meiehei Le plus ancien et toujours très employé est la présure.

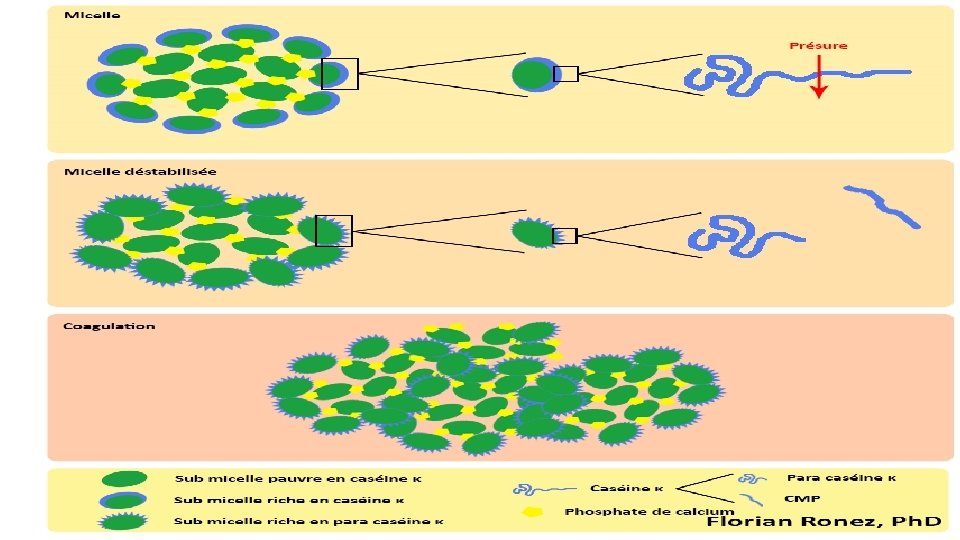
La présure : Enzyme protéolytique extraite de l’estomac des jeunes ruminants nourrit au lait, elle est constituée d’un mélange de chymosine (80%) et de pepsine (20%). L’effet de la présure sur le lait s’articule en 3 phases.

Phase primaire Le détachement de la K caséine du caséino‐glycolipides. Hydrolyse en 2 parties : • Para caséinate de K; • Gros peptide 65 Aa (caseinomacropéptide). Ce détachement cause : • Une réduction de l’état d’hydratation de la micelle même ; • Une augmentation des charges électriques négatives de la micelle.

Phase II aire : Correspond au début de rapprochement des micelles pour former un gel par (agrégation des micelles modifiés), le lait passe de l’état (liquide) à un état de gel (semi‐solide). Lorsque 80 à 90% des caseines K sont hydrolysées, les micelles de caséines perdent leur affinité pour la phase aqueuse, elles vont se rapprocher et s’accumulent entre elles sous l’effet des interactions hydrophobes donnant ainsi un cailler du lait

Phase III aire : c’est la phase d’élimination spontané du sérum ou synérèse. Dans cette phase le gel prend une consistance plus grande parceque le nombre de liaisons entre les micelles augmente, ce qui correspond à un rapprochement des micelles qui cause une contraction du gel (coagulum) qui expulse le sérum,

Chapitre 4: Les fruits et légumes

I. Composition et Propriétés Les fruits et les légumes constituent les aliments dont la consommation est la plus élevée, leur apport en calories est faible, ils sont constitués de :

‐ Faible teneur en lipides ‐ Teneur en glucides variable ‐ Faible teneur en protéines 1‐ 2%. ‐ Eléments minéraux abondant ; K(100‐ 500 mg/100 g), Na faible (5‐ 100 mg/100 g) ‐ Vitamines ; (fruits et légumes unique source de vitamine C) ‐ vitamines de groupe B ‐ Cellulose facilitant la digestion ‐ pectines ‐ Carotène,

La distinction que l’on fait couramment entre fruits et légumes est essentiellement d’ordre gastronomique, les fruits charnus ont en générale comme caractères communs : ‐ La richesse en sucre ; ‐ L’acidité relativement élevée ; ‐ Le parfum prononcé ; ‐ Ils sont les plus souvent consommés à l’état cru.

Parmi les légumes on compte : Des fruits : tomate ; Des graines : petit pois, haricot, maïs ; Des racines : betterave, carotte ; Des tiges : asperge ; Des feuilles : épinards, choux, laitue ; Des fleurs : choux‐fleurs, artichauts.

Les légumes constituent ainsi une collection hétérogène et dont la faible acidité (p. H voisin ou supérieur à 5) qui constitue une propriété commune à la plupart des légumes (abstraction faite à la tomate qui a des caractères organoleptiques d’un vrai fruit. Les fruits et légumes sont riches en eau, les fruits contiennent en générale plus d'acide organiques et moins d’amidon, de protéine et de sel minéraux que les légumes.

Les caractères organoleptiques et nutritionnelles des aliments végétaux dépendent de nombreux facteurs : • • Espèce et variétés, Conditions des cultures, Etat de maturité, Conditions et duré d’entreposage, traitement technologique

La teneur en constituants chimiques divers varie considérablement au cours de la croissance et de la maturation, de l’entreposage après récolte et des traitements La saveur et l’arôme : La saveur et l’arôme dépend du rapport de teneur en sucre et en acide, de la richesse en tannins (astringents: crispation des muqueuses buccales; assèchement(liaison amylase ‐tannin) et de la présence de composés volatils.

Couleur : Due aux piments (3 classes) : - Chlorophylles ; vertes et liposolubles, - Caroténoïdes ; jaunes, orangés et liposolubles, - Anthocyanines ; rouges, bleues et hydrosoluble (la teneur des fruits en pigments est complètement modifiée pendent la maturation. . )

Texture Résulte de la nature des cellules du parenchyme et de divers autres éléments structuraux. - Rigidité ; due au microfibrilles cristallines de cellulose (>25% du résidu sec). - Turgescence; confère aux fruits et aux légumes leur fermeté, et leurs succulence (charnue) dépend de l’eau retenue dans les cellules par osmose qui peut atteindre 96% de poids de tissus

CELLULOSE ET PECTINE ü Cellulose La cellulose est le principal polysaccharide de structure des végétaux, présente à l’état de fibre en association avec des hémicelluloses et des pectines
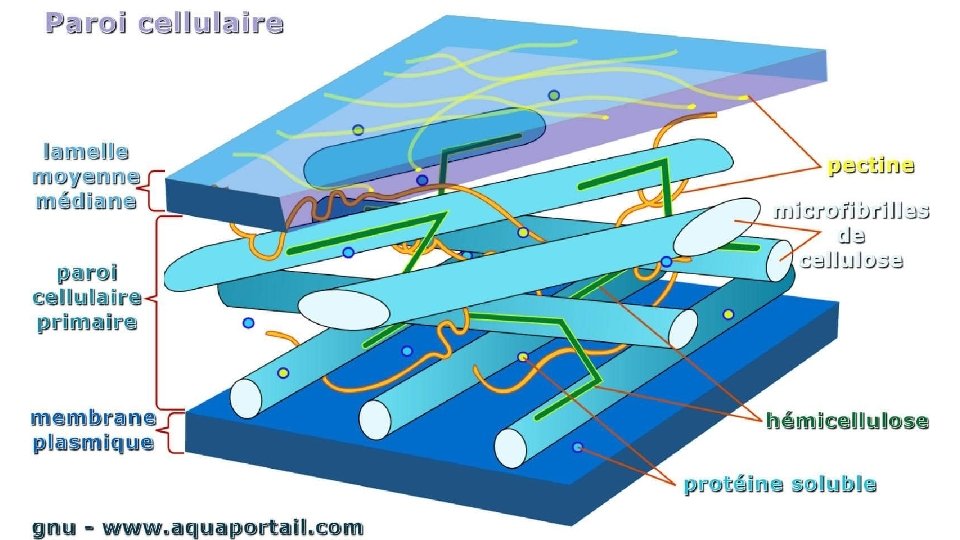

• C’est un polymère linéaire constitué de résidu de glucose relié par des laisons β(1‐ 4) (résistante) • l’hydrolyse acide rond difficilement la régularité de disposition des groupements hydroxyle ( car les chaines voisines interagissent par l’intermédiaire de nombreuses laissons hydrogène criant ainsi un taux élevée de cristallinité),
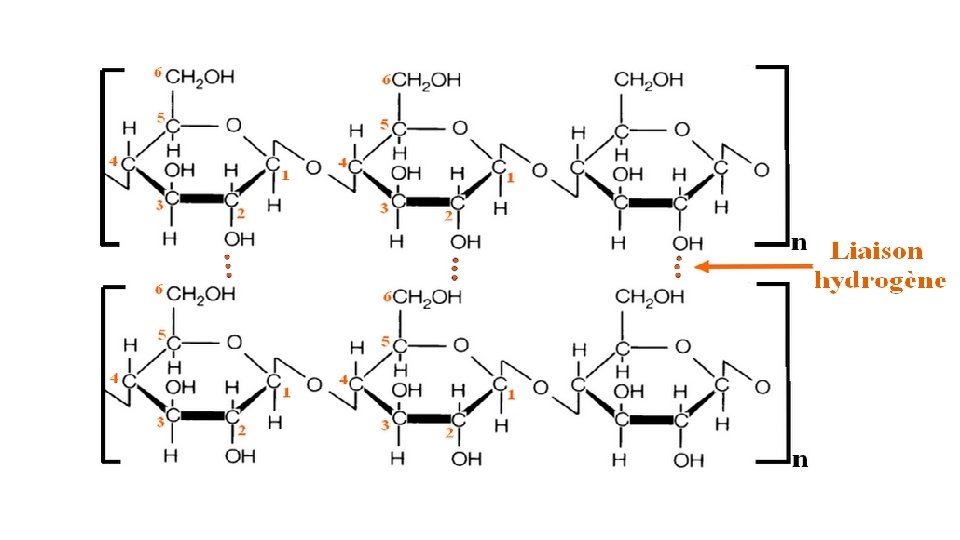

L'hémicellulose est une fibre polysaccharidique constitué de différents types de sucres. Par rapport à la cellulose, l'hémicellulose ne contient pas que des glucoses. Par exemple, en plus du glucose, les monomères de l'hémicellulose peuvent être du xylose, du mannose, du galactose, du rhamnose ou de l'arabinose.

La cellulose est insoluble dans la plus part des solvants. Une modification chimique, par la substitution d’une certaine proportion des 3 groupements OH qui sont disponibles dans chaque résidu de glucose, rend la cellulose soluble. La cellulose n’est pas digestive pour l’homme mais facilite l’évacuation d’autres matières indigestibles dans l’intestin.

Pectine Substance organique (polysaccharide), mucilagineuse, qui se rencontre dans de nombreuses cellules végétales, notamment dans les fruits mûrs, et qui, grâce à ses propriétés gélifiantes, est utilisée dans l'industrie alimentaire et dans l'industrie pharmaceutique Dans les végétaux les pectines sont souvent liés à la cellulose, notamment dans les parois cellulaires sous la forme d’un complexe insoluble dans l’eau appelés proto‐pectine, il suffit toute fois d’un bref chauffage au milieu acide telle qu’il existe naturellement dans des nombreux fruits pour libérer la pectine qui est soluble dans l’eau (matuation). Les mucilages sont des substances végétales, constituées de polysaccharides, qui gonflent au contact de l'eau en prenant une consistance visqueuse, parfois collante, semblable à la gélatine.

MODIFICATION CHIMIQUE AU COURS DE LA MATURATION 1. Généralité sur les métabolismes après récolte Lorsque un fruit ou légume est séparés de la plante il ne reçoit plus ni eau ni nutriments et la photosynthèse cesse, cependant la respiration des tissus se poursuit ainsi que divers autres réactions enzymatiques. Elle utilise de l'amidon ou des sucre stockés et s'arrête lorsque les réserves de ces éléments sont épuisées

La respiration des tissus végétaux provoque par conséquent • Une perte de matière sèche et souvent aussi une diminution de la saveur sucré ( utilisation des réserves) conduisant au vieillissement • Consomme l’oxygène faute de quoi l’anaérobiose s’installe (l’air est réduite), la fermentation peut se substituer à la respiration (Une mauvaise ventilation du produit conduit également à l'accumulation du CO 2).

• Elle dégage CO 2, • Produit de l’eau (transpiration de tissus) entraînant une perte de poids, • Elle dégage aussi la chaleur La respiration de tissus végétale après la récolte constitue ainsi le facteur limitant de la conservation les fruits et légumes à l’état frai. Les produits doivent donc être conservés dans une atmosphère à l'humidité contrôlée


2. Maturation et phénomène climactérique Schématiquement on peut considérer la vie d’un fruit comme constituer de 4 phases : Floraison Croissance Maturation La sénescence (agé) est un processus physiologique qui entraîne une lente dégradation des fonctions de la cellule Sénescence et mort

La maturation est définit comme étant la période de différenciation tissulaire accompagné d’une synthèse d’enzymes spécifiques responsables de modification biochimique et structurale rendant le fruit agréable à consommer. Un fruit (ou un légume) est dit climactérique si sa maturation est dépendante de l‘éthylène (agissant comme hormone végétale), et associée avec une augmentation de la respiration cellulaire de ses tissus.

Certains fruits notamment l’abricot, la pêche, la pomme, la poire, la tomate, l’avocat, la banane présentent un accroissement temporaire de l’activité respiratoire (plus intense) appelé pic climactérique qui coïncide en générale avec les principales modifications, Le pic climactérique survient soit sur la plante soit lors de la maturation après récolte,

D’autres notamment les raisins, cerises, fraises, figues, agrumes, ananas ainsi que la plupart des légumes ne présentent pas de pic climactérique, leurs respiration progresse plus longtemps et les laisse en générale nourrir sur la plante. Remarque Si le fruit a un pic climactérique dans ce cas on peut faire la récolte avant sa maturation

L’initiation et le déroulement de la maturation sont sous la dépendance de l’éthylène (c’est une hormone végétale produite au cours de la maturation (hormone de maturation), pour les fruits climactériques Par contre la maturation est indépendante pour les fruits non climactériques.

Lorsque les fruits sont placés dans une atmosphère contenant 1 ml d’éthylène par m 3, le déclenchement du pic climactérique se produira c’est l’activité respiratoire qui est stimulée.

3. Modification chimique La phase de maturation serait une période de différenciation de tissus accompagnée d’un ensemble de réactions qui modifient de façon notable des caractères organoleptique des fruits : • Augmentation de la teneur en oses et de la saveur sucrée, ces oses proviennent de l’hydrolyse soit de l’amidon (banane, poire, pomme) soit de hémicellulose des parois (agrume, pomme, poire). • Baisse de l’acidité : le rapport sucre sur acide (sucre/acide) s’élève qui résulte de la dégradation de l’acide organique.

• Ramollissement des fruits qui résulte de la modification des substances pectiques, la protopectine insoluble est transformée en pectine soluble et celle‐ci est partiellement déméthoxylée et dépolymérisée. • Modification des pigments: le passage du vert au jaune (agrume, abricot, pêche, certain variété de pomme. . ) ou au rouge (tomate) correspond en générale à la destruction de la chlorophylle, et la synthèse de caroténoïde ou d’anthocyanine.

La maturation donne naissance à un grand nombre de composés organiques volatiles en partie responsables de l’arome de fruit.

Chapitre 5: Les lipides alimentaires (oxydation)

I. INTRODUCTION : Les lipides qu’ils soient apparent comme dans le beurre et les huiles ou dissimulés comme dans le lait, fromage, la viande ou les œufs, jouent un rôle important dans l’alimentation : Rôle nutritionnel : apport énergétique 8. 5 cal/g acide gras essentiel vitamines liposolubles A, E, K, D. Rôle organoleptique : contribution à la texture

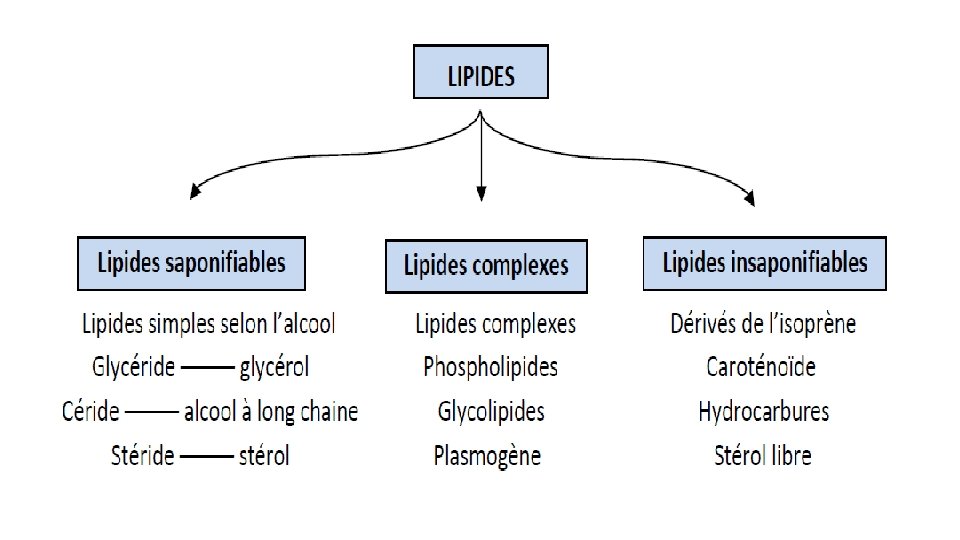
II. CLASSIFICATION ET STRUCTURE: II. 1. Classification Les lipides sont insolubles dans l’eau, solubles dans les solvants organiques: • Lipides saponifiables (simples) : Dérivés naturels résultants de combinaison d’AG (acide gras) avec un alcool ou une amine, sont des lipides ternaires uniquement constitués de C, H, et O. (Les triacylglycérols (TAG) sont très majoritaires sur le plan alimentaire (lipides neutres)) ;

• Lipides insaponifiables (isopréniques et eicosanoïdes) : Constituent un ensemble de molécules très diverses regroupées ici en raison de leur caractère hydrophobe • Ces lipides ne sont ni des acides gras, ni le resultat de l'association entre un acide gras et un alcool insaponifiables • Ils possèdent donc le caractère commun a tous les lipides: l'insolubilite en milieu aqueux.

Ils existe 2 familles chimiquement distinctes: - les isoprenoides (hydrocarbures: les terpènes; pigment (carotènes), les dérivés des stérols (cholesterol) qui sont des les dérivés d’isoprène. ‐ Les eicosanoides, dérivés des acides gras polyinsaturés ( exp: acide arachidonique): prostaglandines , leucotriènes (hormones lipophiles)

Lipides complexes ou hétérolipides : Sont constitués de C, H et O auxquels viennent s’adjoindre P et/ou N. Ces atomes (P, N) donnent des groupements polaires sur la molécule, conduisant ainsi aux lipides amphiphiles. Les phosphoglycérolipides (PGL) et les sphingolipides (SL) appartiennent à ce groupe

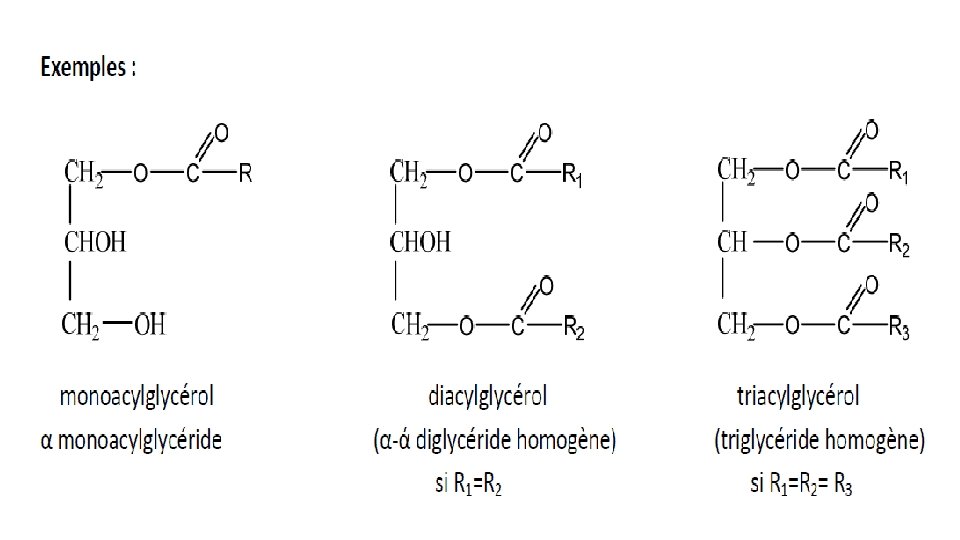
II. 2. Structure • Les acides gras possèdent tous une longue chaine hydrocarbonée et un groupement carboxylique terminal CH 3‐(CH 2)n‐COOH, • la chaine hydrocarbonique peut être saturée ou insaturée (présente une ou plusieurs doubles liaisons). • Les acides gras différent donc entre eux par la longueur de la chaine et le nombre et la localisation des doubles liaisons.



Selon : ü Nature des AG qui estérifient la fonction alcool de glycérol on parlera de : ‐ Acylglycérole homogène : Si les 3 AG sont identiques ; ‐ Acylglycérole hétérogène (mixte) : 3 AG sont différents. ü position d’estérification on parlera de : ‐ α ou β monoacylglycérol ; ‐ (α‐ά) ou (α‐β) : Diacylglycérol ; ‐ (α, β, ά) : Triacylglycérol homogène ou hétérogène.
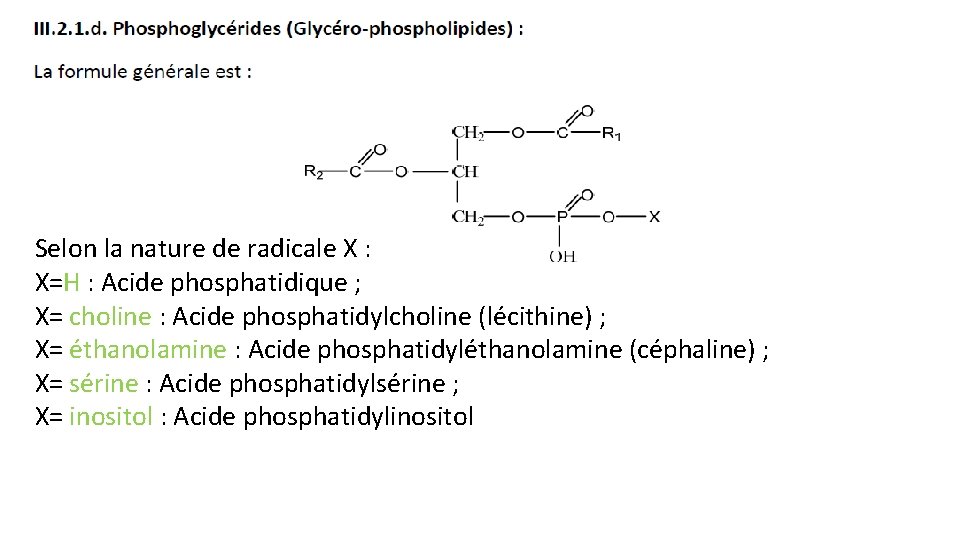
Selon la nature de radicale X : X=H : Acide phosphatidique ; X= choline : Acide phosphatidylcholine (lécithine) ; X= éthanolamine : Acide phosphatidyléthanolamine (céphaline) ; X= sérine : Acide phosphatidylsérine ; X= inositol : Acide phosphatidylinositol
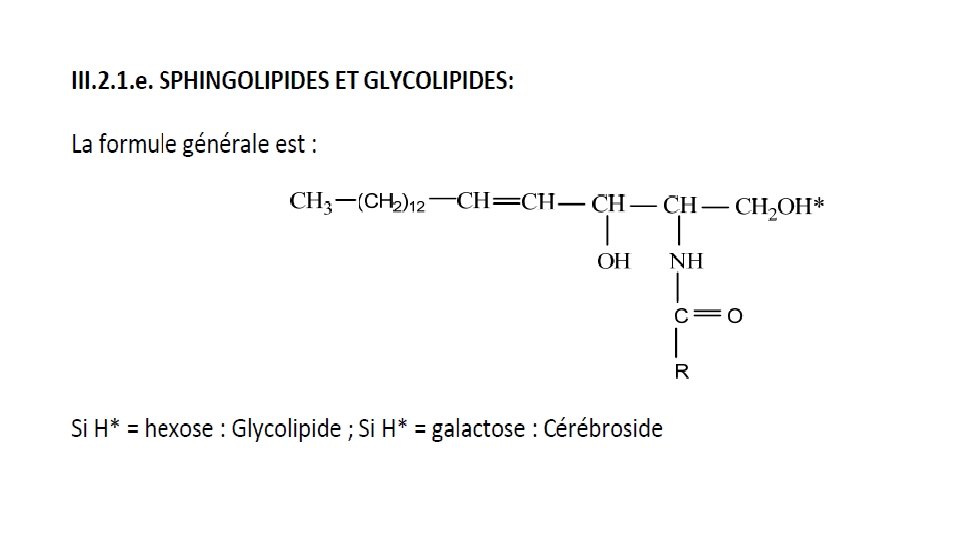
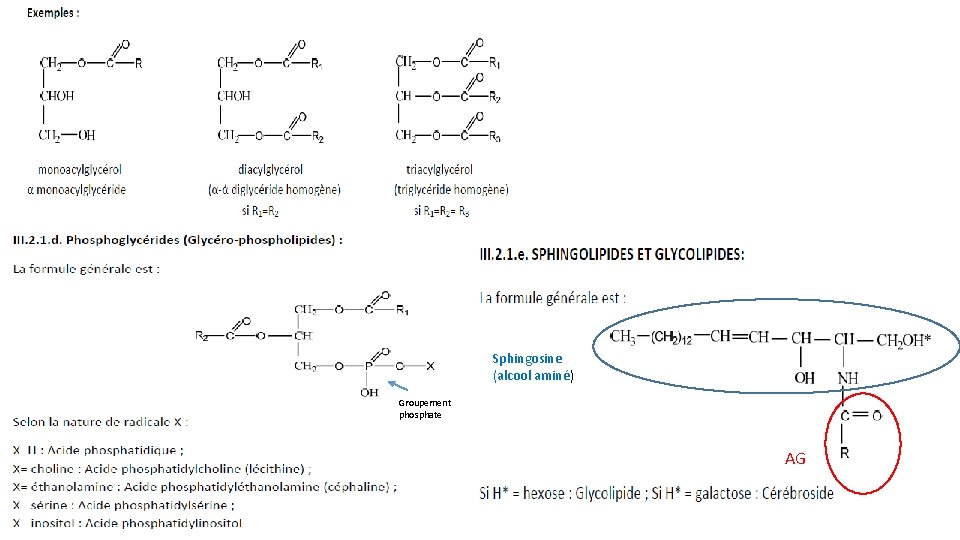
Sphingosine (alcool aminé) Groupement phosphate AG

PROPRIETÉS PHYSICO‐CHIMIQUES : • Le point de fusion de l’AG s’élever avec la longueur de la chaine Hydrocarbonée • L’hydrophobie croit avec l’augmentation de nombre de carbone • Seuls les AG à courte chaine n= C 4–C 10 sont dits volatiles, et seuls les C 4 et C 6 sont solubles dans l’eau.

Le point de fusion d’un triglycéride dépend de plusieurs paramètres : ü La présence d’acides gras à chaînes courtes ou d’acides gras insaturés, abaisse le point de fusion. Ce qui donne des triglycérides liquides à température ordinaire ü Les isomères (Cis ou Trans). Exemple C 18. 4 = 44°c (Trans) forme Cis = 13. 4°c Toute graisse ou huile naturelle contient divers triglycérides. Donc il n’y a pas de point de fusion net mais zone de fusion.


OXYDATION DES LIPIDES Substrat : Les substrats de ces réactions sont principalement les: • AG non saturés libres (ils s’oxydent plus vite lorsqu’ils sont estérifiés), • Le degré d’insaturation influence la vitesse d’oxydation. • Les AG saturés ne s’oxydent qu’à une température supérieure à 60°C, tandis que les AGP s’oxydent même lors de l’entreposage de l’aliment à l’état congelé.

Autres substrats non saturés peuvent subir des réactions d’oxydation analogues: exp ‐ Vitamine A et les pigments caroténoïdes ; ‐ Vitamine E (α tocophérol).

L’auto-oxydation Elle est catalysée par la température, les ions métalliques et l’oxygène La température - Une élévation de température favorise l’oxydation des lipides (cuisson qui a un effet pro-oxydant). - Au contraire, la congélation est un bon moyen pour augmenter la durée de conservation des aliments, (vitesse d’oxydation des réduite).

Ø Ions métalliques La décomposition des lipides peut être accélérée de manière significative par la présence des métaux lourds tels que le cuivre, le fer et le cobalt. Ø Oxygène ‐ Son incidence est donc à la fois sur la durée de conservation du produit et sur la nature des odeurs perçues quand le produit est oxydé. ‐ Plus l’huile est aérée c'est‐à‐dire, une surface de contact accrue, plus la réaction d’oxydation est avancée.

- L'oxygène réagit avec de nombreux substrats organiques (RH) pour donner des hydro-peroxydes et autres composés oxygénés. Cette oxydation est un enchaînement de réactions radicalaires se déroulant en trois étapes

1. Initiation • Production d’un radical libre par élimination d’un hydrogène de l’acide gras ( Ki: O 2, chaleur, lumière, métaux)

2. Propagation les radicaux libres formés fixent l'oxygène et forment des peroxyles instables qui réagissent avec d'autres molécules d'acides gras et conduisent à des radicaux libres et des hydro-peroxydes

3. Terminaison - Couplage entre deux radicaux libres instables pour aboutir à des produits stables. - Globalement, ce processus conduit à des hydrocarbures, des aldéhydes, des cétones (Responsables de l’odeur de rance), des acides, des esters et des peroxydes

Brunissement enzymatiques et non enzymatiques

I. Brunissement enzymatique (BE) , ( Fruits et légumes) De nombreuses réactions de détérioration des aliments sont causées par des enzymes, qui sont: - des constituants naturels de l’aliment, - ou provenant de bactéries présentes dans l’aliment.

Ø Le BE enzymatique s’observe chez les végétaux qui sont riches en composés phénoliques, il n’intervient pas dans les aliments d’origine animale. Ø Le BE cause d’important problèmes de couleur avec certains fruits et légumes (pomme, poire, banane, pomme de terre, champignon) en particulier lorsque le tissus de ces végétaux sont malades ou endommagés. Ø Cependant un certain degré de brunissement est en effet recherché lors de la maturation (ex. les dattes).

Le BE (de pêches, pommes, abricots, . . . ) est dû aux transformations enzymatiques(l’oxydation enzymatique) de substances phénoliques en quinones très réactives qui se polymérisent pour donner des composés bruns
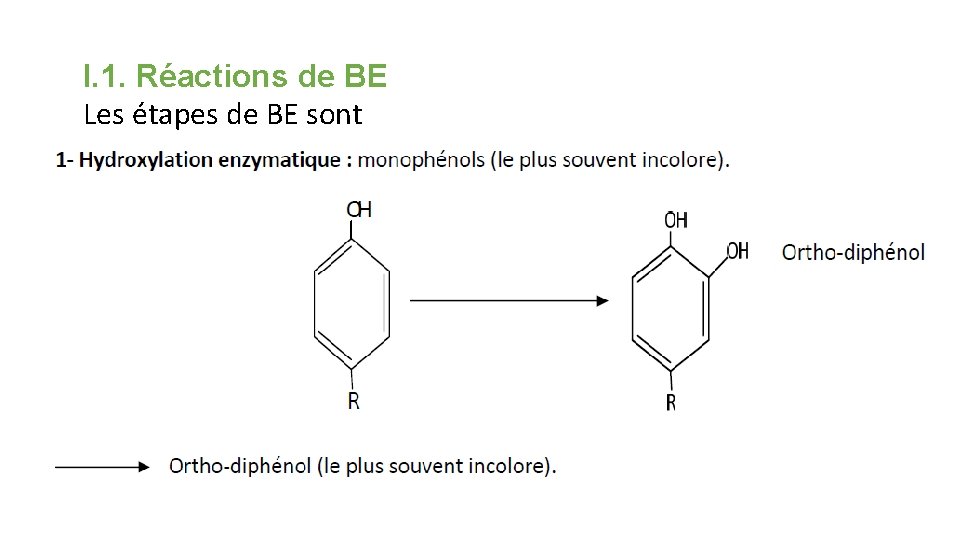
I. 1. Réactions de BE Les étapes de BE sont
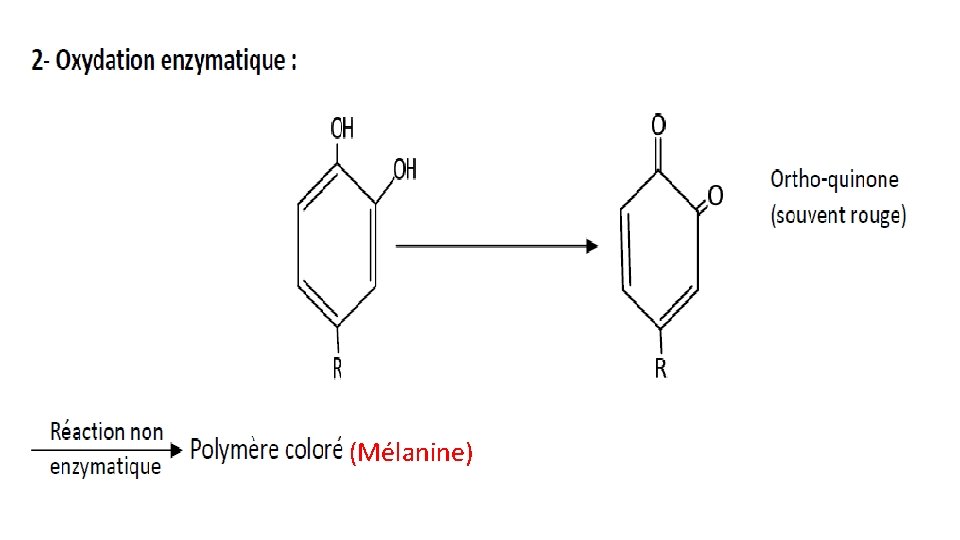
(Mélanine)

Les pigments qui se forment par BE sont désignés par le terme générale de mélanines Ø Les enzymes impliquées sont : Monophénolase (crésolase) ; Polyphénoloxydase (ou polyphénolase ou catecholase)

Conditions de BE : Substrat + enzyme + O 2, sont les conditions de BE, si l’un des facteurs est absent la réaction n’aura pas lieu.

Prévention • Sélection de variétés pauvres en substrat phénolique. • Eviter d’endommager les tissus. • Inactivation des enzymes par la chaleur (Blanchiment par l’eau bouillante ou vapeur) • Addition des composés réducteurs (acide ascorbique).

• Abaissement du p. H par addition d’acide citrique ou de citron. • Enlèvement d’O 2 (désoxygénation, exp: vide ). • Traitement avec le SO 2 ou sulfite (Réaction avec les quinones en les bloquant, Réaction avec les polyphénols oxydases)

II. Brunissement non enzymatique (BNE) ou caramélisation (exp du lait) Définition : Le brunissement non enzymatique (BNE) appelé aussi ’’ réaction de Maillard ’’ ou ’’ Caramélisation ’’ (formation de mélanoïdines), désigne un ensemble très complexe de réactions aboutissant dans divers aliments à la formation de pigments bruns divers et souvent aussi à des modifications de l’odeur et de la saveur.
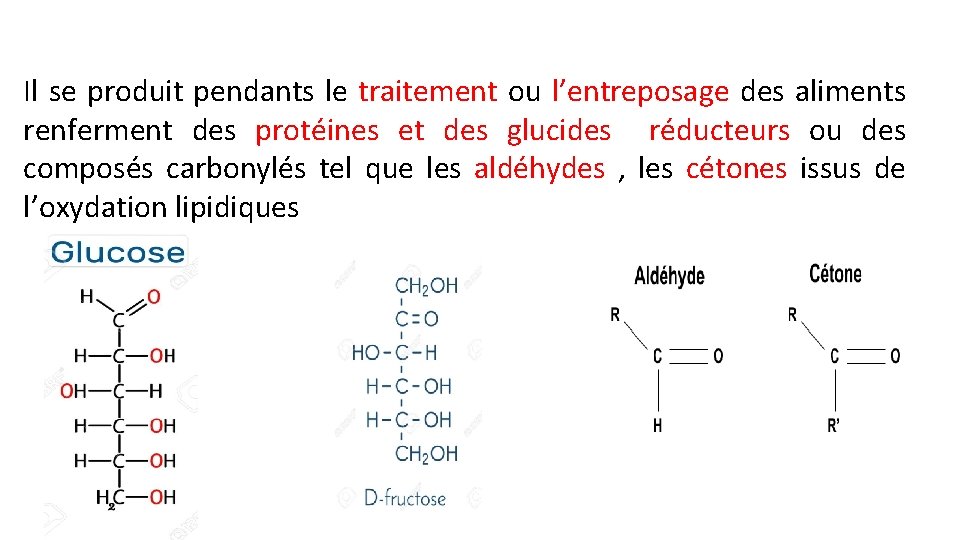
Il se produit pendants le traitement ou l’entreposage des aliments renferment des protéines et des glucides réducteurs ou des composés carbonylés tel que les aldéhydes , les cétones issus de l’oxydation lipidiques

Les facteurs responsables des réactions de BNE : - Composés carbonylés et sucres réducteurs - Acides aminés libres ou protéines ( groupement amine). - Certaines vitamines (C et K , porteurs de fonctions carbonylées). Selon l’aliment le BNE peut être désirable ou non:

• Effets favorable : Croute de pain, viande rotie, caramel ; • Effets défavorable : Lors de la préparation ou de l’entreposage d’aliments liquides ou concentrés (laits, jus de fruit…sirop) ou d’aliments déshydratés (lait, œufs, viande…). Cela entraine: ‐ une diminution de la disponibilité des AA ‐ diminution de la digestibilité des protéines ‐ Perte de valeur vitaminique quand les vitamines sont impliquées

-l’apparition de composés mutagènes ou génotoxiques comme l’acrylamide Remarque: Le BNE est accéléré par la chaleur (traitements thermiques: pasteurisation, stérilisation, …)
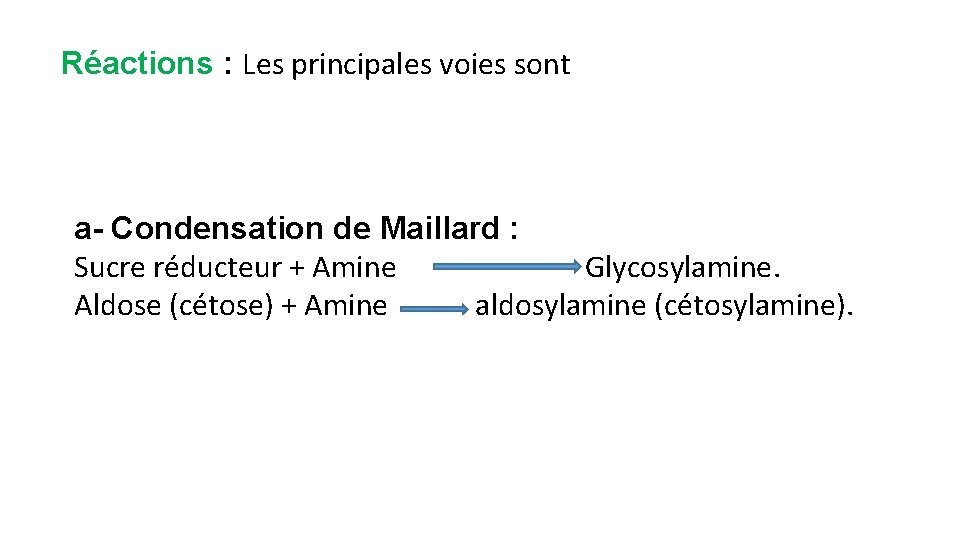
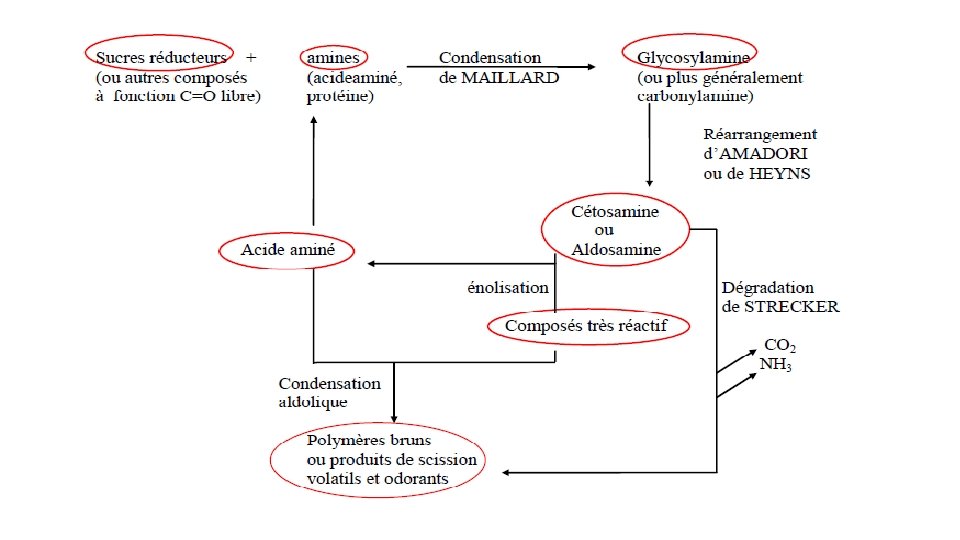
Réactions : Les principales voies sont a- Condensation de Maillard : Sucre réducteur + Amine Glycosylamine. Aldose (cétose) + Amine aldosylamine (cétosylamine).

b) Réarrangement (d’Amadori ou de Heyns) Aldosylamine Cétosylamine cétosamine (Amadori) aldosamine (Heyns). • Les cétosamines résultent de réarrangement des aldosylamine selon Amadori, • Tandis que les cétosylamines donnent des aldosamines selon Heyns • Ces deux composés sont stables et peu colorés
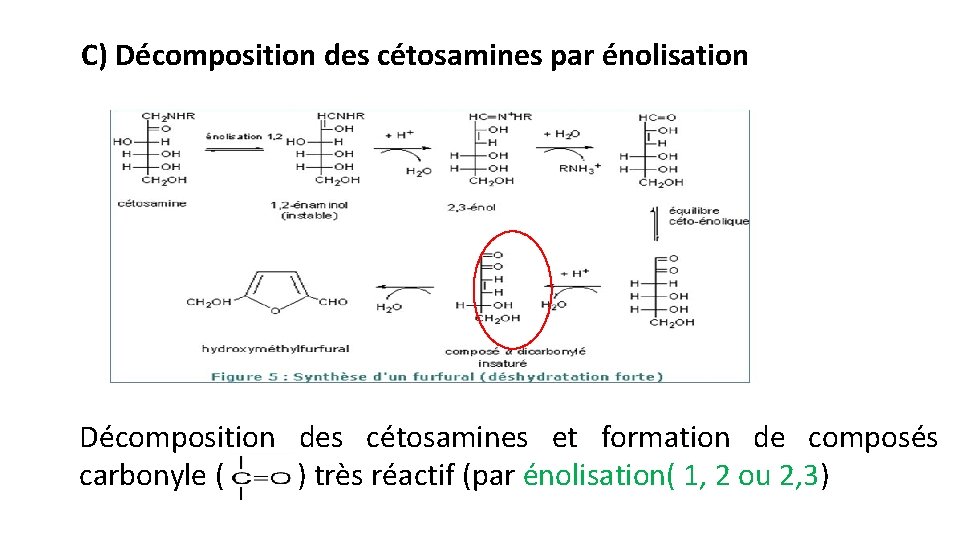
C) Décomposition des cétosamines par énolisation Décomposition des cétosamines et formation de composés carbonyle ( ) très réactif (par énolisation( 1, 2 ou 2, 3)

d) Dégradation de Strecker : Les composés α dicarbonylés résultants de la décomposition des cétosamines peuvent réagirent avec un acide aminé et entrainent la dégradation de ce dernier, le résultat est : • Formation d’un aldéhyde à 1 atome de C de moins que l’acide aminé initiale. • Apparition de divers composés carboniques nouveaux. Condensation aldolique Polymères bruns

Facteurs influençant les réactions de BNE : a) Natures des sucres réducteurs : ‐ Pentoses plus réactifs, ‐ Hexoses moins réactif, b) La température : Des hautes températures accélèrent le BNE. c) a. W : la réaction de BNE se situe dans l’intervalle 0, 55 ‐ 0, 80
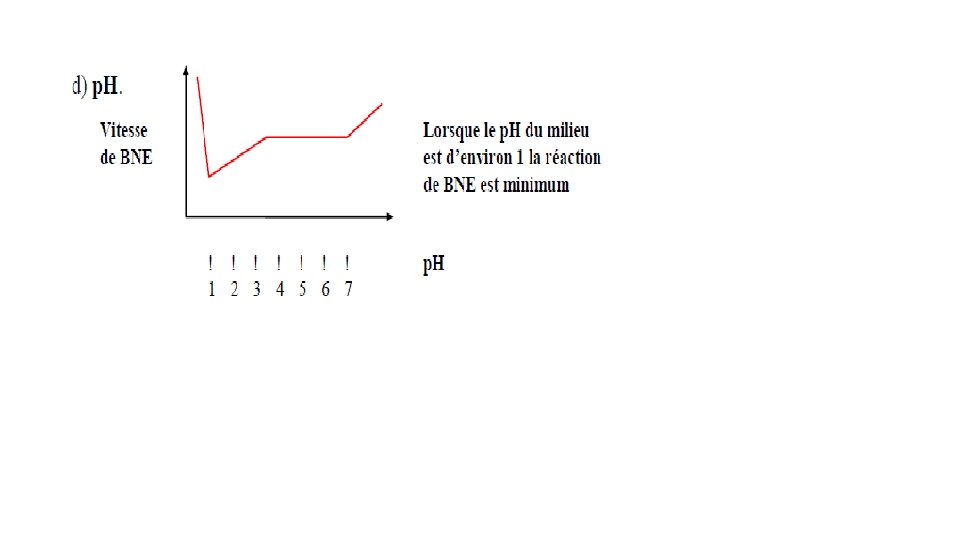

Prévention
- Slides: 164