UNIVERSIT IBN TOFAIL FACULT DES SCIENCES DE KENITRA

UNIVERSITÉ IBN TOFAIL FACULTÉ DES SCIENCES DE KENITRA MASTER NEUROCOGNITION HUMAINE ET SANTÉ DE LA POPULATION Bisphénol A Présenté par: Laaraychi Mohamed Coulibaly Sidi Med Talhaoui Abdeljalil Nassiri Abdeljabbar Cheikhani Tourad Encadré par Dr: Azzaoui Année universitaire : 2012/2013

PLAN I. Introduction générale I. 1. Historique du Bisphénol A (BPA) I. 2. Formule chimique I. 3. Implications industrielles I. 4. Facteurs d’exposition au BPA II. Toxicité générale II. 1. Métabolisme II. 2. Elimination du BPA II. 3. Mode d’action du BPA II. 4. Toxicité aiguë II. 5. Toxicité subaiguë, subchronique et chronique II. 6. Reprotoxicité et embryotoxicité III. Neurotoxicité

I. INTRODUCTION GÉNÉRALE

I. 1. HISTORIQUE DU BISPHÉNOL A (BPA) � Le bisphénol A (2, 2 -bis-(4 -Hydroxyphenyl)-propane (C 15 H 16 O 2) un composé chimique issue de la réaction entre phénol et acétone, il a été produit pour la première fois en 1891 par le chimiste Russe Alexander P. DIANIN.
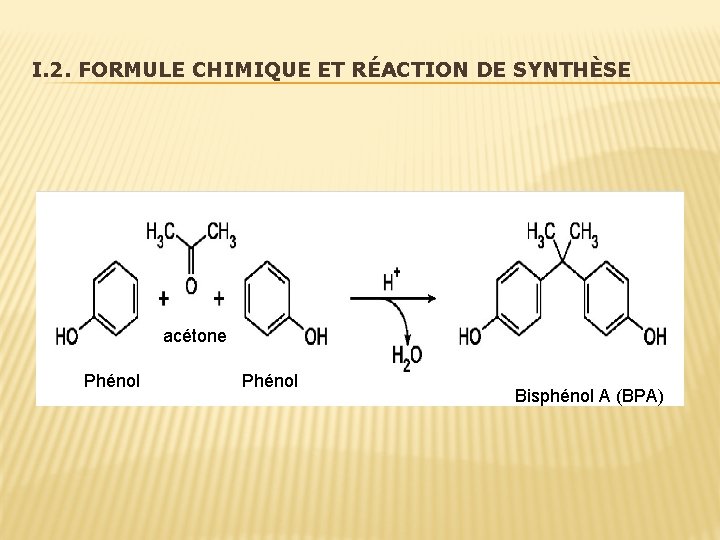
I. 2. FORMULE CHIMIQUE ET RÉACTION DE SYNTHÈSE acétone Phénol Bisphénol A (BPA)

I. 3. IMPLICATIONS INDUSTRIELLES � utilisé comme un monomère dans la fabrication industrielle plastique de type polycarbonates et de résines époxy et notamment présent dans 90% des biberons plastiques vendus au canada (santé au canada, 2008). C’est à ce titre que les risques éventuels encourus par les nourrissons liés à leurs expositions à cette substance , ont été fortement médiatisés depuis fin 2008.

I. 3. IMPLICATIONS INDUSTRIELLES � on le retrouve dans les emballages alimentaires (revêtements internes des boites de conserves et bouteilles d’eau par exemple*) et les mastics dentaires notamment. Il est aussi utilisé dans la composition des retardateurs de flamme, de certains pesticides, des CD et DVD, des téléphones portables, des jouets pour enfants, des verres de lunettes de soleil, des équipements médicaux et de nombreux matériaux de construction… (Staples et al, 1998).

FACTEURS D’EXPOSITION AU BPA Deux principales sources d’exposition humaine au BPA: - l’alimentation (exposition par voie orale): Ø Migration du BPA de l’emballage vers l’aliment. Ø Du lait maternel vers le nourrisson. Ø Amalgames dentaires. - l’environnement(eaux de surface, l’air, soles et sédiments).

II. Toxicité générale

II. 1. MÉTABOLISME � Glucurono-conjuguaison: Voie principale chez toutes les espèces Ø Rat: catalysée par UGT 2 B 1 (Uridine diphosphate-Glucuronyl. Transférase 2 B 1). Ø Homme: catalysée par les isoformes UGT 2 B 15 et UGT 2 B 7 Ø Formation du BPA glucuronide (Hanioka et al. , 2011; Inserm, 2011). � Sulfo-conjuguaison: catalysée par une sulfotransférase et donne BPAsulfate (Pottenger et al, 2000).

II. 2. ELIMINATION DU BPA � Homme: élimination rapide du BPA-glucuronide principalement par les urines(temps de demi-vie inférieur à 6 h). � Rat: élimination du BPA-AG par cycle entérohépatique ( plus lente que celle chez l’Hommme)
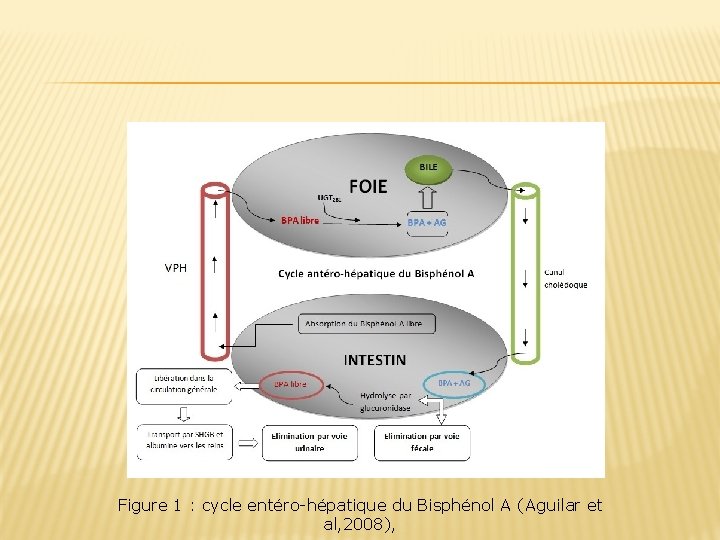
Figure 1 : cycle entéro-hépatique du Bisphénol A (Aguilar et al, 2008),
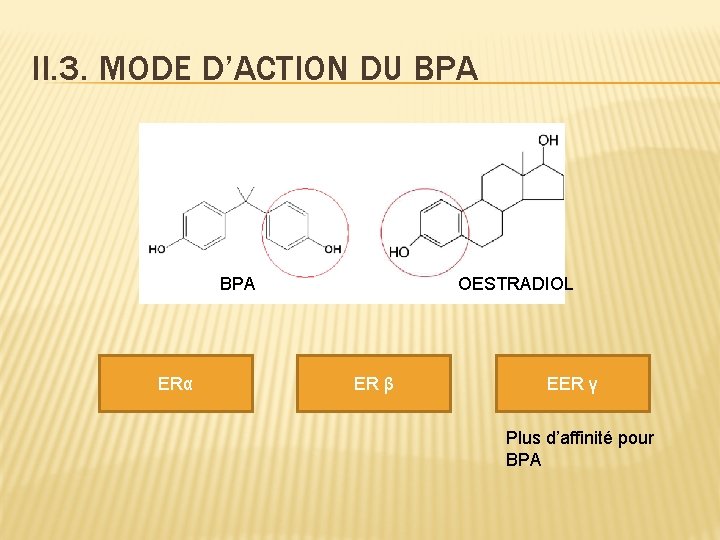
II. 3. MODE D’ACTION DU BPA ERα OESTRADIOL ER β EER γ Plus d’affinité pour BPA

II. 4. TOXICITÉ AIGUË � Seule la forme libre du BPA peut avoir un effet toxique. � par inhalation: relativement faible chez le rat, où la CL 50 est supérieure à 170 mg/m 3 (Nitshke et al. , 1985 a cité dans EU risk assessment report, 2003). � voie orale: faible aussi avec DL 50 comprise entre 3, 3 g/kg et 5 g/kg chez le rat, avec une sensibilité plus grande des femelles. � Voie dermique: faible chez le lapin avec DL 50 > à 2 g/kg.

II. 5. TOXICITÉ SUBAIGUË, SUBCHRONIQUE ET CHRONIQUE � Toxicité subaiguë: Une étude d’inhalations répétées chez le rat a révélé une légère inflammation de l’épithélium du tractus respiratoire supérieur, avec une NOAEL mesurée de 10 mg/m 3. � subchronique : baisse du poids du foie, de la prostate et des glandes séminales, en particulier pour la plus forte dose chez des rats mâles. F 344 exposés à 466 et 950 mg/kg/jour pendant 44 jours via l’alimentation(Takahashi et Oishi, 2001). � Chronique: Une NOAEL de 74 mg/kg a été établie à partir d’une étude de deux ans chez le rat (EU risk assessment report, 2003).

II. 6. REPROTOXICITÉ ET EMBRYOTOXICITÉ Embryotoxicité Ø Rate: exposition unique au BPA par voie orale à une dose élevée 1 g/kg, après 20 min, BPA atteint le fœtus, après 40 min sa concentration dépasse celle du sang maternel ( causes ? ? ) (INERIS, 2010). Ø Humains: selon Benachour et Aris (2009), exposition in vitro de 24 h des cellules du trophoblaste au BPA à différentes concentrations augmentation de la production des TNF, l’apoptose et nécrose = passage du BPA au fœtus (Nishikawa et al, 2010).

II. 6. REPROTOXICITÉ ET EMBRYOTOXICITÉ Reprotoxicité � baisse de la fertilité et de la fécondité a été observée chez des rates dont la mère a été exposée au BPA à la dose de 25 μg/kg/jour pendant la gestation (à partir du 8ème jour) et la lactation (jusqu’au 16ème jour) (Cabaton et al, 2011). � De même, sur le modèle rongeur, une exposition in utero à la dose de 20μg/kg/jour pendant 7 jours a entraîné un avancement de la puberté (Honma et al, 2002).

� Une association inverse entre les concentrations urinaires de BPA et les concentrations plasmatiques de FSH a aussi été observée chez des ouvriers appliquant les résines époxy sur les contenants alimentaires (Hanaoka et al, 2002)

III. Neurotoxicité du Bisphénol A

� Les perturbateurs endocriniens tels que le bisphénol A, peuvent interagir avec le développement fœtal et en particulier celui du cerveau. � Il est encore impossible de dire avec certitude que le contact avec le bisphénol A à une influence sur le développement du cerveau et sur le comportement humain. O. kebir, M, O, Krebs, Médecine & Longévité, June 2011

Des études sur les modèles humains ont montré quelques complications résultantes de l’effet du Bisphénol A

� Le bisphénol A affecterait le cerveau même à des doses respectant les limites fixées par les autorités de santé, selon une nouvelle étude américaine publiée dans la revue Proceedings of the National Academy of Sciences. � d’après une récente étude de santé publique de l’université d’Harvard, le BPA provoquerait des troubles comportementaux (anxiété, dépression, hyperactivité) chez les fillettes dont les mères ont été exposées pendant leur grossesse.

� En avril 2008, le rapport d’évaluation de Santé Canada sur le BPA, tient totalement compte de « la possibilité d’altérations du développement neurologique et du comportement au cours de la période de croissance de l’organisme et ce, à des doses très inférieures à la dose considérée comme sans effet. Le BPA pourrait être associé à des changements neurologiques et à des altérations comportementales affectant notamment le dimorphisme sexuel.

D’autres études portées sur les modèles animaux, ont prouvé les complications neurologiques et comportementales liées à l’effet du Bisphénol A

� l’évaluation de l’Institut national de l’alimentation de l’Université technique du Danemark (DTU Food) inclue une étude sur le développement du système nerveux et du comportement des rats nouveau-nés exposés à de faibles doses de BPA. � Les résultats font état également de troubles de l’apprentissage. Résultant des données montrent des changements biochimiques dans le cerveau.

� L'équipe de Leranth a soumis, pendant 28 jours, des jeunes singes à des doses de BPA de 50 microgrammes/kg de poids corporel, ce qui correspond aux normes de l'Agence américaine de protection de l'environnement. � Ils leur ont aussi administré de l'œstradiol, une forme d'estrogène qui est impliquée dans le contrôle des connections entre les cellules du cerveau.

� Les graphes suivants montrent la diminution des formations synaptiques dans le stratum radiatum (structure dans l’hippocampe) et le cortex préfrontal, pour les singes ayant consommé le Bisphénol A par la voie orale ou la voie sous-cutanée vis-à-vis le groupe de contrôle.
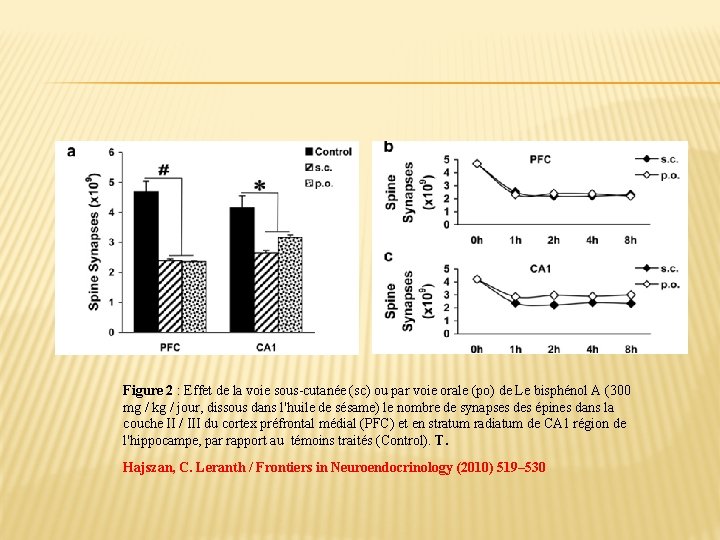
Figure 2 : Effet de la voie sous-cutanée (sc) ou par voie orale (po) de Le bisphénol A (300 mg / kg / jour, dissous dans l'huile de sésame) le nombre de synapses des épines dans la couche II / III du cortex préfrontal médial (PFC) et en stratum radiatum de CA 1 région de l'hippocampe, par rapport au témoins traités (Control). T. Hajszan, C. Leranth / Frontiers in Neuroendocrinology (2010) 519– 530

MERCI DE VOTRE ATTENTION
- Slides: 29