Universit Ibn Tofail Anne Universitaire 2018 2019 Facult

Université Ibn Tofail Année Universitaire 2018 -2019 Faculté des sciences Département de chimie Kenitra La Catalyse Section : SMC-S 5 Pr. Omar BENALI 1

Historique Si le terme Catalyse fut bien introduit dans la Science par Berzelius en 1836, les phénomènes qu’il recouvre avaient été observés bien avant lui. (Parmentier 1781, Kirchoff 1812) Hydrolyse de l’amidon* en dextrine puis en glucose sous l’action des acides minéraux. Le premier cas de catalyse hétérogène par un métal: (Dobereiner 1822): La combustion de l’hydrogène en présence de platine divisé, Il faut cependant arriver à la fin du siècle dernier pour voir apparaitre une étude systématique de tels effets, avec Sabatier (1897) et et Ipatieff (1901). Les premières grandes applications industrielles coïncident sensiblement avec cette phase. (synthèse de l’anhydride sulfurique par Kuhlman 1838), synthèse de l’amoniac par Haber 1910) *Les dextrines sont des glucides amorphes de formule brute approximative (C 6 H 10 O 5)n. Elles sont obtenues par chauffage de l'amidon vers 160°C ou par son hydrolyse acide vers 100°C. Des dextrines se forment dans la croûte du pain lors de la cuisson, ce qui lui confère sa couleur et son parfum. On les trouve sous forme de poudre blanche, jaune ou brune. Elles sont plus ou moins solubles dans l'eau et donnent les solutions incolores et dextrogyres. 2

Un catalyseur est une substance qui accélère la vitesse d’une réaction thermodynamiquement possible. Il participe aux mécanismes réactionnels sans altérer les produits. 3

La catalyse est une branche de la cinétique chimique. Alors que la catalyse homogène rentre assez facilement dans le cadre de l’étude générale, des mécanismes des réaction à étapes, la catalyse hétérogène touche à la science encore imparfaite de l’état solide, ce qui justifie un traitement particulier. Deux facteurs interviennent spécifiquement au niveau des lois de vitesse pour une transformation chimique : le facteur pré-exponentiel, A, et l’énergie d’activation, Ea L’expression classique de la constante de vitesse est : k = A e-Ea/RT Cette constante n’est valable que pour un système donné. À partir d’un ensemble de réactifs, via un chemin réactionnel approprié, le système évolue vers la formation des produits. Ea mesure la hauteur de la barrière de potentiel (cf. figure ci-dessous). Contrairement à la thermodynamique qui ne tient pas compte du chemin suivi (principe de l’état initial et de l’état final), la cinétique chimique en est largement dépendante. En modifiant ce chemin, on modifiera la barrière de potentiel. Si Ea augmente, la barrière s’élève et la constante de vitesse décroît et inversement. 4
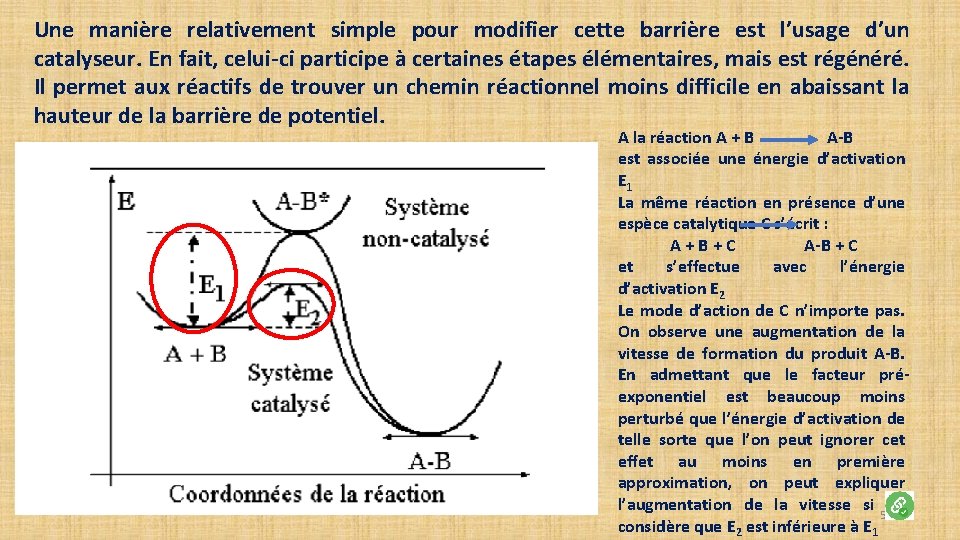
Une manière relativement simple pour modifier cette barrière est l’usage d’un catalyseur. En fait, celui-ci participe à certaines étapes élémentaires, mais est régénéré. Il permet aux réactifs de trouver un chemin réactionnel moins difficile en abaissant la hauteur de la barrière de potentiel. A la réaction A + B A-B est associée une énergie d’activation E 1 La même réaction en présence d’une espèce catalytique C s’écrit : A + B + C A-B + C et s’effectue avec l’énergie d’activation E 2 Le mode d’action de C n’importe pas. On observe une augmentation de la vitesse de formation du produit A-B. En admettant que le facteur préexponentiel est beaucoup moins perturbé que l’énergie d’activation de telle sorte que l’on peut ignorer cet effet au moins en première approximation, on peut expliquer l’augmentation de la vitesse si 5 on considère que E 2 est inférieure à E 1

Un catalyseur est une substance qui accélère la vitesse d’une réaction thermodynamiquement possible. Il participe aux mécanismes réactionnels sans altérer les produits. 6

Les différents types de catalyse La catalyse homogène Une réaction catalytique est homogène, lorsque le catalyseur et le réactif constituent une phase unique. Les premières recherche en catalyse homogène, datant du début du 20ème siècle, sont étroitement liées à celle sur la catalyse acido-basique. Mode d’action des catalyseurs acido-basiques Dans la transformation de molécules neutres de réactifs, la catalyse par des acides et des bases est essentiellement régie par le proton qui du fait de sa nature particulière, permet d’obtenir aisément des espèces franchement ionisés: · Soit par transfert du proton sur un substrat neutre, en catalyse acide. · Soit part extraction du proton à partir du substrat (HS) par l’intermédiaire d’une base en catalyse basique. 7
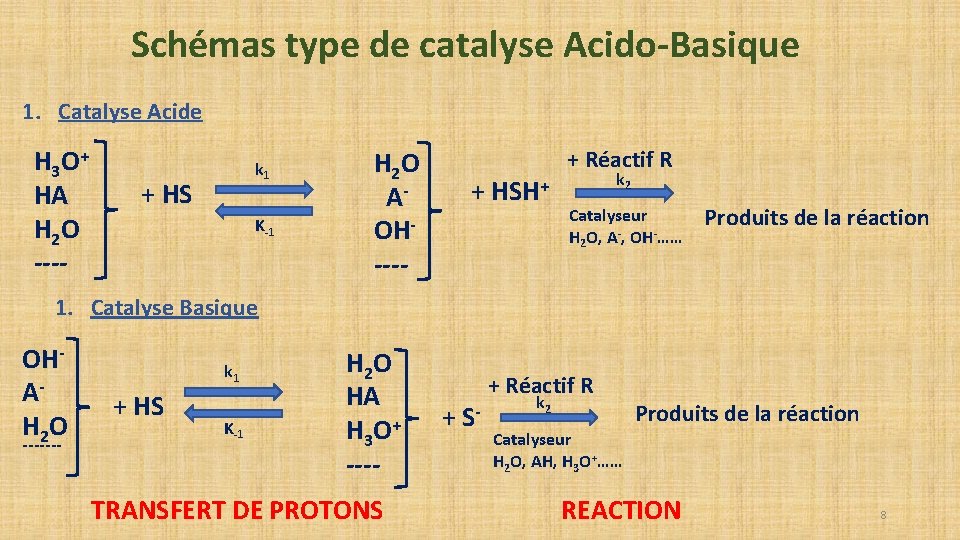
Schémas type de catalyse Acido-Basique 1. Catalyse Acide H 3 O+ HA H 2 O ---- k 1 + HS K-1 H 2 O AOH---- + HSH+ + Réactif R k 2 Catalyseur H 2 O, A-, OH-…… Produits de la réaction 1. Catalyse Basique OHAH 2 O ------- k 1 + HS K-1 H 2 O HA H 3 O+ ---- TRANSFERT DE PROTONS + Réactif R + S- k 2 Produits de la réaction Catalyseur H 2 O, AH, H 3 O+…… REACTION 8

Le processus fondamental est donc constitué d’au moins deux étapes comme le montre la figure: 1°) La production par transfert de proton de la forme réactionnelle intermédiaire, ionisée positive ou négative. 2°) La transformation de celle-ci intramoléculairement ou avec un corréactif, dans une seconde étape. 9

La catalyse enzymatique Les transformations chimiques opérées par les microorganismes s’appellent des fermentations. Les produits de fermentation les plus anciennement obtenus étaient des petites molécules ( éthanol, acide acétique, acide lactique, acide citrique). Mais un brusque changement est apparu après la seconde guerre mondiale, avec l’essor des antibiotiques (pénicilline, streptomycine), En effet les antibiotiques qui sont souvent des molécules très complexes, sont obtenues industriellement par fermentation. D’une manière générale, les fermentations qu’elles soient réalisées à l’échelle industrielle ou artisanale (fabrication de vin, de fromages, de la bière) sont le résultat d’un ensemble de réactions catalysées par des enzymes: Substance protéiques contenues dans les microorganismes utilisées. En biologie, dans les cellules, les enzymes, très nombreux, jouent ces rôles d'accélérateur, de catalyseurs, dans les processus biochimiques : métabolisme digestif, de la reproduction, de la transcription de l'information génétique, les sciences du génome, le yaourt, la pâte à pain 10

Une enzyme est une protéine catalysant une réaction biochimique. Une enzyme est un catalyseur organique colloïdale, soluble dans l’eau. Les enzymes constituent la classe des protéines la plus vaste. Substance organique produite par des cellules vivantes, qui agit comme catalyseur dans les changements chimiques. Structure des enzymes Les enzymes sont le plus souvent des protéines, et sont donc constituées de chaînes d'acides aminés. Parfois, les activités enzymatiques sont portées par des ARN, et sont dans ce cas appelées des ribozymes. La partie importante de l'enzyme est constituée du site actif. C'est dans ce site, qui prend souvent la forme d'une cavité, que se fixe le substrat qui pourra alors être soumis à l'action de l'enzyme afin de le transformer en produit. Chaque enzyme protéique possède une structure adaptée à sa fonction, et peut être sous forme monomérique, alors que certaines au contraire sont actives sous formes dimériques, voire plus. Elles peuvent alors s'associer à plusieurs chaînes protéiques codées par le même gène (homodimère) ou codées par des gènes différents (hétérodimère). 11

Fonctions des enzymes Les enzymes ont pour mission d'accélérer (catalyser) des millions de fois les réactions chimiques dans les organismes vivants. Il existe un grand nombre d'enzymes spécifiques qui jouent un rôle important dans les processus physiologiques (digestion, conduction nerveuse, synthèse d'hormones, etc. ). On peut toutefois classer les enzymes en six catégories suivant la réaction biochimique qu'elles réalisent : les oxydoréductases, qui catalysent des réactions d'oxydoréduction (comme la peroxydase) ; les transférases, qui transfèrent un groupement fonctionnel d'une molécule à l'autre (comme les méthyltransférases qui transfèrent un groupement méthyle) ; les hydrolases, qui hydrolysent des liaisons chimiques (comme les nucléases qui coupent l'ADN ou l'ARN) ; 12

les lyases, qui rompent des liaisons mais en produisent de nouvelles simultanément (comme l'adénylate cyclase qui produit l'AMP cyclique à partir d'ATP) ; les isomérases, qui réarrangent les groupements fonctionnels d'une molécule pour former des isomères (comme les topoisomérases qui enroulent l'ADN) ; les ligases ou synthétases, qui permettent la jonction de deux molécules (comme les ADN ligases). Seuls les substrats et les produits varient d'une enzyme à l'autre. 13
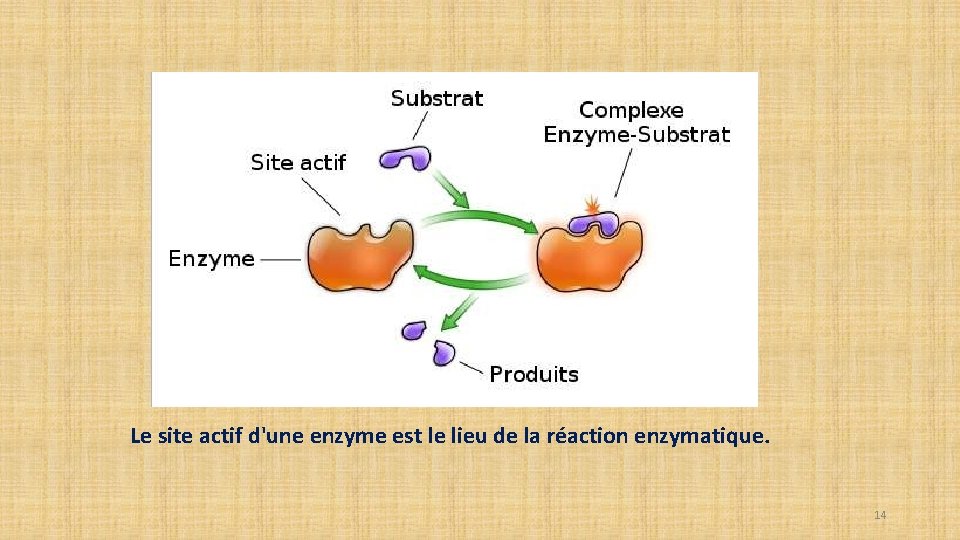
Le site actif d'une enzyme est le lieu de la réaction enzymatique. 14

LA CATALYSE HETEROGENE Si le catalyseur se trouve dans une autre phase que les réactifs et les produits, on parle de la catalyse hétérogène. Dans le cas où le catalyseur se trouve à l'état solide, il catalyse donc une réaction en phase gazeuse ou en phase liquide. La catalyse hétérogène a été pendant longtemps traitée indépendamment de la catalyse homogène. L'ignorance de la nature physicochimique exacte d'un solide et de sa structure ajoutait à la difficulté. Les applications industrielles de la catalyse par les solides ont été développées, bien avant que leurs études scientifiques aient abouti à des résultats positifs. 15
le catalyseur est insoluble et donc facilement éliminable par filtration en fin de réaction. Un autre avantage notable est que l'on peut chauffer à des températures très élevées , bien au- delà de ce que peuvent supporter les catalyseurs homogènes, et donc effectuer des réactions cinétiquement beaucoup plus difficiles sans affecter le catalyseur (synthèse de NH 3 , oxydation de CH 4 en CH 3 OH, réduction de CO). Ces deux atouts font de la catalyse hétérogène un type de catalyse efficace et, par conséquent, beaucoup utilisé dans la pétrochimie (craquage, isomérisation, augmentation de l’indice d’octane de l’essence), les synthèses minérales (H 2 SO 4 , HNO 3 , NH 3, les engrais (phosphatés et azotés), les polymères et la chimie fine (par exemple, la réaction de Friedel- Crafts). 16

D’autres procédés très connus en catalyse hétérogène sont la réduction de CO par H 2 ( Fischer-Tropsch ), la réaction du gaz à l’eau, les synthèse de H 2 SO 4, HNO 3 , NH 3 , des phosphates, des engrais à l’azote et des polymères et la chimie de l’environnement (pots d’échappements). Le problème majeur est la sélectivité, et les approches modernes impliquent les catalyseurs à site unique avec un contrôle de plus en plus moléculaires. Leur mode d’action est contrôlé par l’affinement de la taille et de la forme des nanoparticules actives et de leurs supports y compris avec l’aide des systèmes modèles et de la chimie organométallique de surface. La chimie verte s’impose de plus en plus impérativement dans l’aspect environnemental afin de maitriser la toxicité des nanoparticules polluantes et leur rejet dans l’atmosphère, et cet aspect restera un pôle majeur de recherche au XXIème siècle, 17

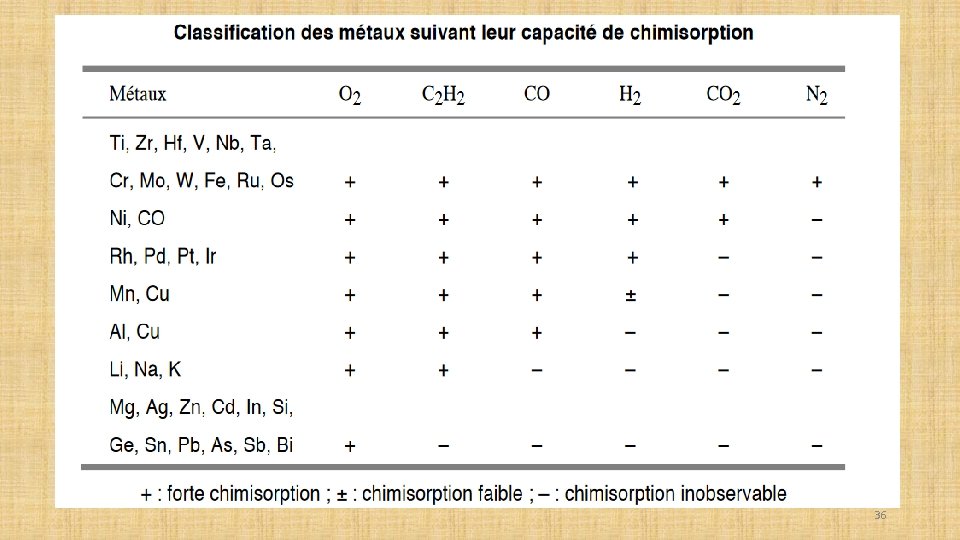
CONCEPTS DE LA CATALYSE HÉTÉROGÈNE La catalyse hétérogène est basée sur les phénomènes de surface : les atomes disponibles à la surface d’un solide sont ceux qui activent les substrats. L’activité d’un catalyseur hétérogène ne dépend pas de sa masse propre, mais de sa surface de contact avec les réactifs fluides. Cette activité est plus grande quand le rapport surface/masse (surface spécifique en m 2. g– 1 ) croît, c’est- à- dire quand le solide est plus poreux et divisé. Par exemple, le noir de platine a une surface de 20 à 30 m 2. g– 1 et celle de l’alumine activée de 100 à 300 m 2. g– 1. Une surface possède plusieurs types de domaines élémentaires, chacun d’entre eux étant capable de former une liaison avec un atome ou une molécule de différentes façons : par conséquent, habituellement les sites d’une surface ne sont pas du tout identiques. Cette distribution des sites actifs de surface avec des propriétés différentes représente une distinction importante entre la catalyse homogène et la catalyse hétérogène. 18

Les étapes impliquées dans l’activation moléculaire sur une surface sont : Très employée industriellement, notamment en pétrochimie (reformage, isomérisation des alcanes, …), elle concerne les réactions dans lesquelles réactifs ne sont pas dans la même phase que le catalyseur, en général solide. La séparation est donc concrètement facilitée. On peut distinguer trois réactions chimiques du cycle catalytique : 1. Chimisorption : il s’agit en fait d’une véritable réaction avec formation de liaisons chimiques entre les réactifs et les sites actifs de la surface du catalyseur. 2. Réaction c’est à dire transformation des espèces chimisorbées. 3. Désorption du ou des produits et régénération du catalyseur. Le fait que la réaction se produise à la surface du catalyseur (interface solide – fluide) complique le cycle puisque des étapes de transport de matière interviennent : diffusion des molécules de réactifs vers la surface du solide et des produits de la surface vers la 19 phase fluide.

Les transferts de chaleur sont aussi à considérer puisque la réaction chimique (exothermique ou endothermique) se produit très ponctuellement : les différences de température au sein du milieu ont des conséquences sur l’activité et surtout la sélectivité des catalyseurs. L’activité du catalyseur (qui est une expression de la vitesse de réaction) s’exprime en quantité de réactif transformé par unité de masse du catalyseur et par unité de temps. Elle dépend donc étroitement de la surface du catalyseur et plus précisément de la densité des sites actifs. Cela explique les surfaces spécifiques très élevées des catalyseurs employés, qui s’étendent de 50 à 1000 m 2/g. De telles surfaces ne peuvent être obtenues que par la création de pores au cours de la préparation ; on distingue suivant la taille des pores des solides macro, méso ou microporeux. 20

Si l’on considère l’ensemble du processus entre une molécule en phase gazeuse et un solide poreux, il est possible de distinguer 7 étapes élémentaires : Diffusion externe dans la phase fluide entourant le grain : en régime permanent un gradient de concentration existe au voisinage du grain. Diffusion dans les pores du catalyseur : le transport des molécules doit tenir compte des chocs entre molécules et avec les parois solides. Adsorption, c'est-à-dire rétention des molécules à la surface : dans le cas de l’acte catalytique, nous avons vu qu’il s’agit de l’établissement de liaisons chimiques : si on considère la réaction d’hydrogénation sur platine, la molécule gazeuse de dihydrogène est dissociée et des liaisons H-Pt se forment. 21

La transformation représente l’acte chimique désiré : la compréhension de cet acte élémentaire nécessite l’identification des intermédiaires. Dans l’exemple simple de l’hydrogénation catalytique des alcènes sur platine, seule la molécule de dihydrogène est chimisorbée, l’autre réactif restant dans la phase fluide. Le cas se complique quand les deux molécules sont adsorbées sur le catalyseur ; il faut alors considérer les différents sites actifs possibles et l’intervention des méthodes de modélisation est indispensable. Désorption du (ou des) produit(s) des sites actifs. Diffusion dans les pores jusqu’à la frontière du grain. Diffusion externe à travers la couche gazeuse qui entoure le grain. 22

Les caractéristiques physiques essentielles des solides employés en catalyse hétérogène sont le volume poreux, la répartition des pores et la surface spécifique. Ces grandeurs sont mesurées expérimentalement à partir des isothermes d’adsorption de l’azote. Définition de la surface spécifique N : nombre d’Avogadro ; σ : surface occupée par une molécule adsorbée ; m : masse de solide utilisé pour l’adsorption ; VB : volume adsorbé nécessaire pour obtenir une monocouche d’adsorbat sur toute la surface. Pour l’azote : σ = 0, 162 nm 2 la température d’adsorption est 77 K. 23

La qualité d’un catalyseur est définie par son activité, sa sélectivité et sa stabilité ; les fabricants et utilisateurs évaluent ces grandeurs par des tests représentatifs du procédé industriel. L’activité estimée à partir des courbes d’évolution du taux de conversion en fonction du temps de travail. La sélectivité est en fait le caractère primordial du choix du catalyseur. En effet, il est rare qu’une transformation ne mène qu’à un seul produit ; les réactions secondaires imposent la mise en œuvre de procédés de séparation très coûteux économiquement et écologiquement. La sélectivité est chiffrée simplement par le rendement en produit désiré par rapport au réactif. La connaissance des mécanismes est ici importante pour connaître l’origine des produits indésirables (transformation directe du réactif, réaction secondaire du produit sur le réactif, sur le catalyseur, …) et agir sur les conditions opératoires pour trouver le meilleur compromis. 24

Enfin la stabilité, c'est-à-dire la durée de vie du catalyseur détermine le temps d’utilisation avant régénération ou changement du matériau. La désactivation d’un catalyseur provient principalement : · de la dégradation thermique, · de l’empoisonnement dû à la présence dans le fluide réactionnel de composés réagissant et occupant les sites actifs, de l’encrassement par des impuretés organiques piégées dans le catalyseur. 25

Par exemple, lors de la formation d’eau à partir de H 2 et O 2 , comment le catalyseur Pt fonctionne- t-il ? En dépit de la très grande énergie libre de la réaction ( ∆ G° = – 232 k. J. mol– 1 ), le mélange de H 2 et O 2 dans un récipient en verre est parfaitement stable, car H 2 et O 2 possèdent chacun une très forte énergie de liaison (respectivement 412 k. J. mol– 1 et 418 k. J. mol– 1 ). Cependant, si du Pt est introduit, une explosion a lieu immédiatement. Ceci s’explique par le fait que, en présence d’une grande surface de Pt, les réactions d’addition oxydante H 2 + 2* → 2 H et O 2 + 2*→ 2 O ont lieu avec une énergie d’activation quasiment nulle. Le résultat global est que la surface de Pt est capable de dissocier des molécules ayant de fortes énergies de liaisons entre leurs atomes et implique de très faibles énergies d’activation pour les recombinaisons des atomes ainsi liés à la surface. 26

Réaction à route unique Considérons à titre d’illustration, l’exemple de de l’oxydation de SO 2 sur un catalyseur au platine. On peut écrire la séquence catalytique constitué par les deux étapes élémentaires équilibrées suivantes, selon le mécanisme: adsorption dissociative de l’oxygène suivie de la réaction du SO 2 phase gazeuse avec l’oxygène adsorbé. O 2 + 2*→ 2 O* (x 1) SO 2 + 2 O*→ SO 3 + * (x 2) 2 SO 2 + O 2 → SO 3 Ou SO 2 + 1/2 O 2 → SO 3 Les deux équations stœchiométriques résultantes sont équivalentes et on voit qu’il n’y a qu’une seule route unique de la réaction. 27

Réaction à route multiple Elle conduit à une seule réaction globale, mais par des séquences différentes. Considérons la synthèse catalytique de l’eau à partir de H 2 et O 2. 28

29

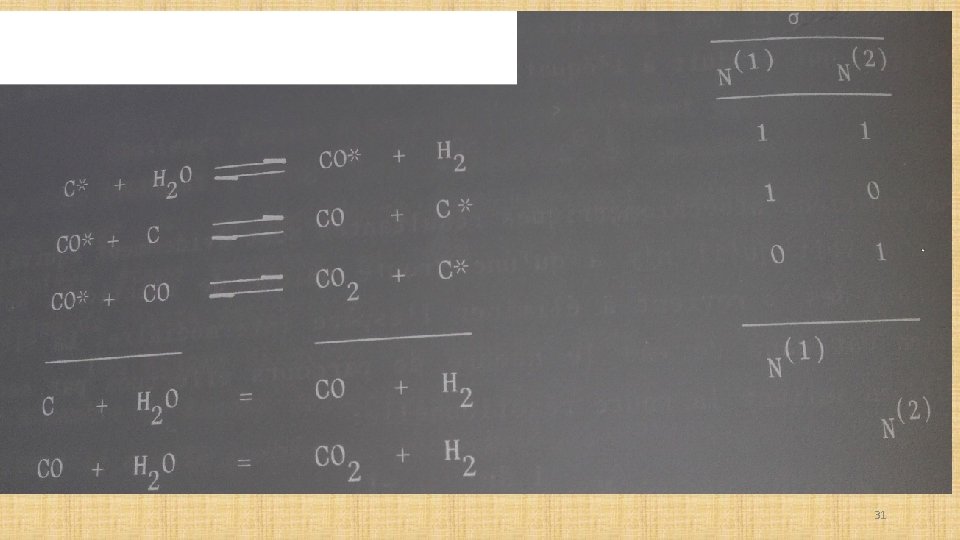
Réseau de réaction: Il s’agit du dernier cas qui met en jeu des séquences réactionnelles différentes selon les routes N(i) dont les équations stœchiométriques sont aussi différentes, Citons la synthèse du gaz à l’eau: 30
31

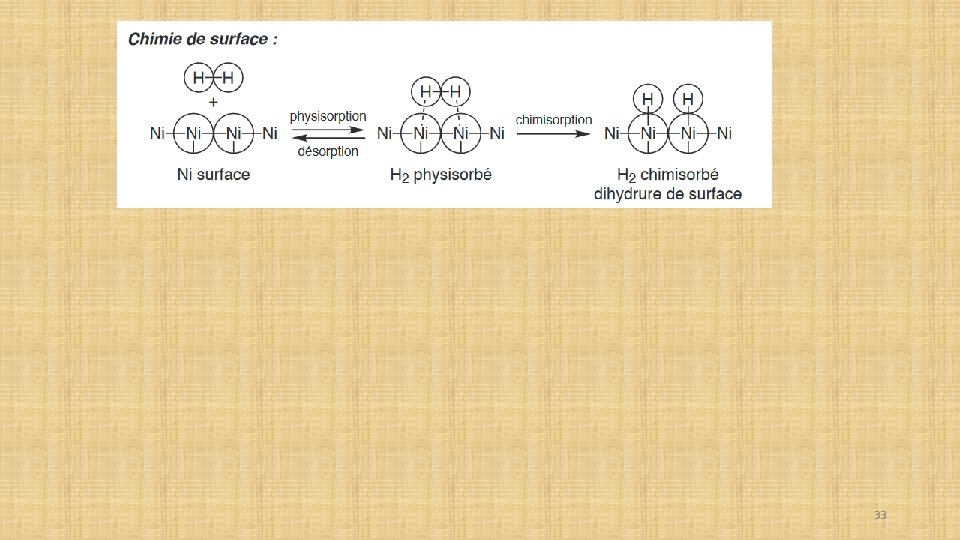
PHYSISORPTION ET CHIMISORPTION Quand une molécule diffuse près de la surface métallique, elle est d’abord physisorbée, c’est- à- dire qu’elle se lie sur la surface sans dissociation. Les forces impliquées sont de type van der Waals, c’est- à- dire inférieures à 20 k. J. mol – 1. Cette étape est réversible, et la désorption peut intervenir rapidement. Avec H 2 , par exemple, on peut comparer cette liaison à la formation d’un complexe de H 2 sur le site métallique vacant d’un complexe à 16 électrons. L’addition oxydante peut éventuellement se produire sur la surface suivant la nature du métal. Dans le cas d’un complexe monométallique, le complexe de H 2 peut souvent être stable et isolable (c’est- à- dire dans lequel H 2 est quand même plus fortement lié au métal que lorsqu’il est physisorbé). Alternativement, cette entité peut être fugitive et rapidement former le dihydrure par addition oxydante. La différence est que, sur la surface, l’addition oxydante est bimétallique alors qu’en chimie organométallique elle est souvent (mais pas toujours) monométallique : 32
33

La synthèse de NH 3 à partir de N 2 et H 2 catalysée par Fe (avec de petites proportions d’additifs Al 2 O 3 et K 2 O) autour de 300 °C constitue l’un des grands classiques de la catalyse hétérogène. La très forte liaison entre les deux atomes d’azote de la molécule N 2 (∆G°=1120 k. J. mol– 1) empêche toute dissociation de la molécule non-complexée. La physisorption réversible a lieu à température ambiante, mais pas la dissociation. 34

Les molécules qui entrent en contact avec la surface et réagissent ne se décomposent pas instantanément. Elle forme avec le catalyseur une combinaison labile qui peut Soit restituer la molécule originelle soit se transformer par une suite d’étapes en produits qui ne seront pas non plus restitués instantanément réaction chimique en phase adsorbée B A Bads Aads Equilibre d’adsorption des réactifs C D Cads Dads Equilibre de désorption des produits
36

CINÉTIQUE : L A FRÉQUENCE DE ROTATION ℜ La fréquence de rotation F se définit par le nombre de molécules de produits formées par seconde. Son inverse, 1/F, est le temps de rotation, c’est- à- dire le temps nécessaire à la formation d’une molécule de produit. En divisant la fréquence de rotation F par la surface du catalyseur ℘ , on obtient la vitesse de rotation spécifique (mol. cm– 2. s– 1 ) : ℜ = F/℘. ℜ est souvent appelé fréquence de rotation. 37

En multipliant ℜ par le temps total t, on obtient le nombre de rotations, c’est -à- dire le nombre de molécules formées par site de surface (qui doit être supérieur à 100 pour que l’on puisse utiliser le terme de catalyse). ℜ peut être formulé comme le produit de la constante de vitesse par un terme relié à la pression P : ℜ = k. f(Pi), dans lequel Pi est la pression partielle du réactif. La constante de vitesse, k, peut être exprimée en utilisant l’équation d’Arrhénius : k = A exp (– ΔE*/RT) dans laquelle A est un facteur préexponentiel et ΔE* est l’énergie d’activation apparente de la réaction dans les conditions catalytiques. Les transformations d’hydrocarbures (isomérisation, cyclisation, déhydrocyclisation, et hydrogénolyse) ont souvent des valeurs de Δ E* de l’ordre de 140 à 180 k. J. mol– 1 , mais les réactions d’hydrogénation ont des valeurs de Δ E* de seulement 24 -48 k. J. mol– 1 à température ambiante. L’hydrogénation a lieu dans des conditions beaucoup plus douces que les transformations d’hydrocarbures ci –dessus. 38

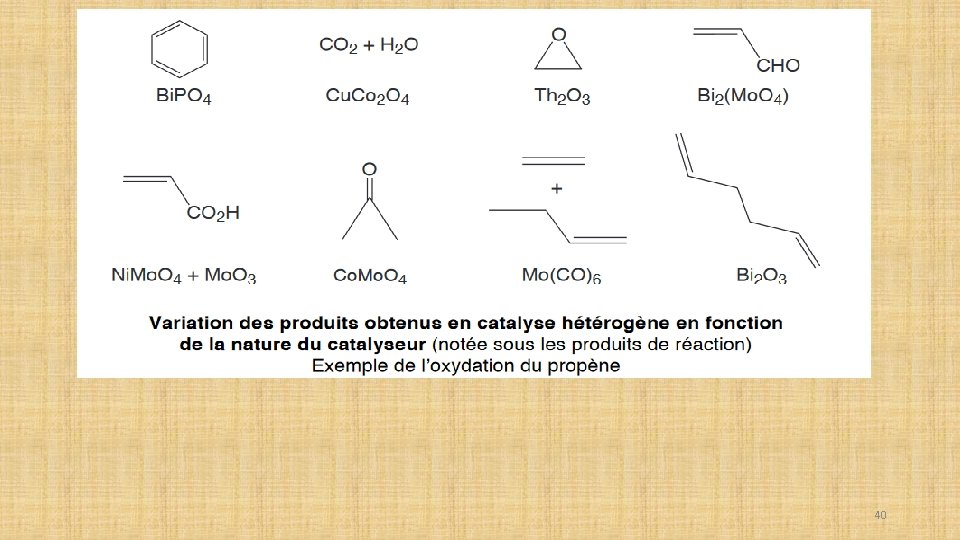
LA SELECTIVITÉ La sélectivité est un problème majeur en catalyse hétérogène car beaucoup de procédés hétérogènes ne sont pas sélectifs et par conséquent produisent des mélanges de produits. La sélectivité du catalyseur est définie pour une réaction 1 par rapporrt à une réaction 2, par le quotient de leur vitesse : S=V 1/V 2 Des progrès considérables ont été réalisés dans l’amélioration des sélectivités des catalyseurs, particulièrement en variant les matériaux catalytiques et du fait du développement des zéolithes*. Une grande gamme de produits peut être obtenue sélectivement en changeant la nature du catalyseur, comme dans l’exemple de l’oxydation du propène : *Une zéolithe, ou zéolite, est un cristal formé d'un squelette microporeux d'aluminosilicate, dont les espaces vides connexes sont initialement occupés par des cations et des molécules d'eau. Les ions et les molécules d'eau sont mobiles au sein de la structure, ce qui permet d'une part des échanges ioniques, d'autre part une déshydratation partielle réversible, et la possibilité de remplacer l'eau par une autre phase adsorbée. Le caractère cristallin du squelette implique les porosités de la structure sont toutes de même taille. Ces porosités peuvent autoriser ou non le passage de molécules, avec un pouvoir discriminant inférieur à 100 picomètres (10− 10 m). C'est pourquoi l'on qualifie 39 les zéolithes de tamis moléculaires.
40
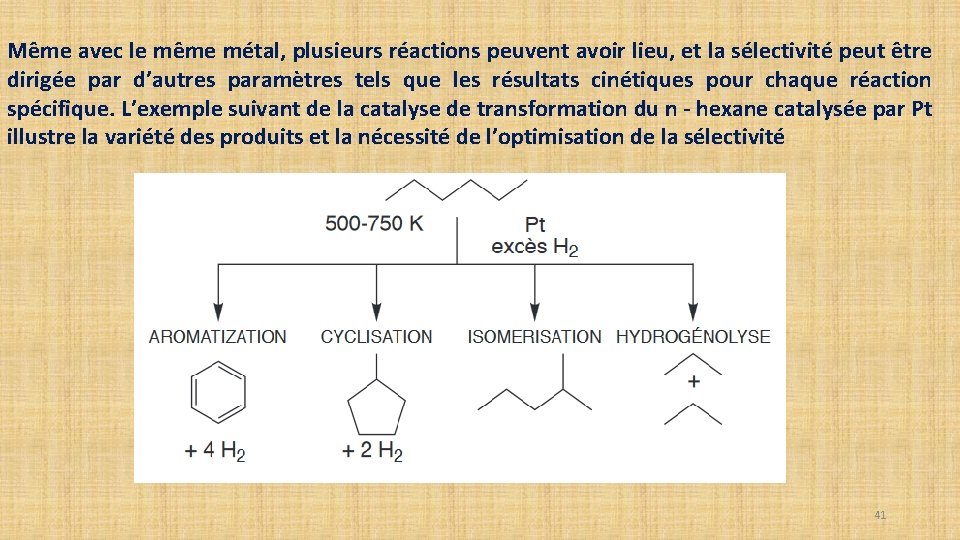
Même avec le même métal, plusieurs réactions peuvent avoir lieu, et la sélectivité peut être dirigée par d’autres paramètres tels que les résultats cinétiques pour chaque réaction spécifique. L’exemple suivant de la catalyse de transformation du n - hexane catalysée par Pt illustre la variété des produits et la nécessité de l’optimisation de la sélectivité 41

On sait aussi que la sélectivité dépend de la face particulière du Crystal du catalyseur. Par exemple, avec Mo. O 3 , la face {010} n’est pas sélective pour l’oxydation du propène, mais la face {100} donne l’acroléine sélectivement. Avec le méthanol, la face {010} de Mo. O 3 conduit sélectivement à la déhydrogénation en formaldéhyde, et la face {100} donne H 2 C(OCH 3)2 42

PRÉPARATION , DÉSACTIVATION ET RÉGÉNÉRATION DU CATALYSEUR Préparation Etant donné que l’activité d’un catalyseur hétérogène est directement reliée à sa surface, il est important d’utiliser des catalyseurs métalliques aussi finement divisés que possible. A cet effet, les catalyseurs sont préparés à partir d’alumine , de silice et d’autres supports oxydes (de Mg, Zr, Ti, V), carbone (graphite ou nanotubes), phosphate, sulfure ou carbonate. 43

Habituellement, la surface atteint 100 à 400 m 2. g– 1 sur de tels supports. Le support microporeux est imprégné dans les micropores avec un ou plusieurs sels de métaux qui sont réduits en nanoparticules (NP) métalliques de 1 à 10 nm par chauffage. Avec de telles dimensions, la majorité des atomes des NPs se trouvent en surface et la polydispersité est supposée être proche de 1. Un autre oxyde tel que Ti. O 2 est fréquemment dispersé à la surface de l’oxyde primaire de façon à accroître la sélectivité. Les additifs peuvent inclure des métaux alcalins agissant comme donneurs d’électron ou des halogènes agissant comme des accepteurs d’électron. 44

Les catalyseurs hétérogènes sont produits sous forme de palets, sphères, anneaux, tablettes, granules et autres extraits. Leurs tailles varient de quelques fractions de mm à plusieurs cm. Les plus gros sont utilisés dans des lits fixes parcourus par le fluide, liquide ou gaz, tandis que les plus petits sont suspendus dans le fluide duquel ils sont séparés par décantation où filtration. Les propriétés requises sont l’activité, la sélectivité et la longévité. De tels systèmes peuvent fonctionner à de grandes vitesses jusqu’à plusieurs milliers d’heures avec plusieurs millions de rotations. Désactivation- Les catalyseurs utilisés dans l’industrie pétrolière pour le reformage produisent habituellement de l’ordre de 10 5 litres par kilo de catalyseur ; puis le catalyseur doit être remplacé ou régénéré. Les raisons de la désactivation sont celles qui provoquent la diminution de la surface du catalyseur : e formation d’une couche de carbone lors de la décomposition des hydrocarbures à la température ( voir § 3), e empoisonnement des sites actifs, un processus chimique qui change leur réactivité, par exemple avec le soufre 20. 5 , e coalescence des grains à des températures excessivement élevées, un processus physiquement irréversible. 45

46

47
- Slides: 47