Universit hassan II Casablanca Facult des Sciences An

Université hassan II - Casablanca Faculté des Sciences Aïn Chock Travaux pratiques de Chimie descriptive SMC 3 Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Manipulation N° 2 : Dosage du calcium dans l’eau d’alimentation d’une ville. Manipulation N° 3 : Préparation et analyse du sel de Mohr.

Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Expérience Burette Dosage des ions Ba 2+ Solution So contenant du Ba 2+ et du Fe 3+. 20 ml = volume précis Solution So Pipette, burette 20 ml

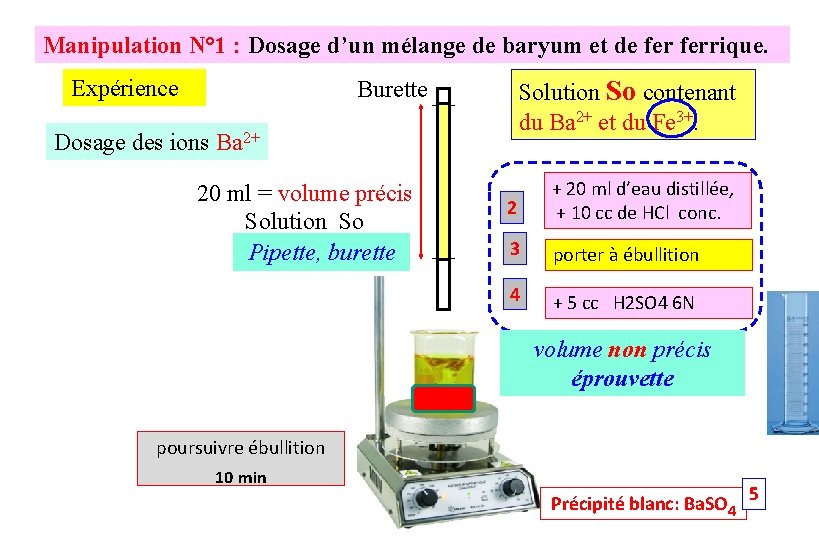
Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Expérience Solution So contenant du Ba 2+ et du Fe 3+. Burette Dosage des ions Ba 2+ 20 ml = volume précis Solution So Pipette, burette 2 + 20 ml d’eau distillée, + 10 cc de HCl conc. 3 porter à ébullition 4 + 5 cc H 2 SO 4 6 N volume non précis éprouvette poursuivre ébullition 10 min Précipité blanc: Ba. SO 4 5
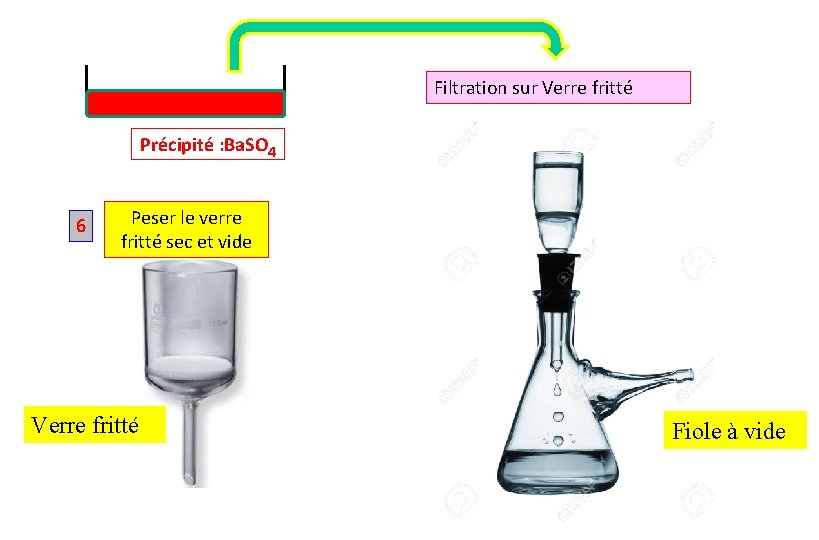
Filtration sur Verre fritté Précipité : Ba. SO 4 6 Peser le verre fritté sec et vide Verre fritté Fiole à vide
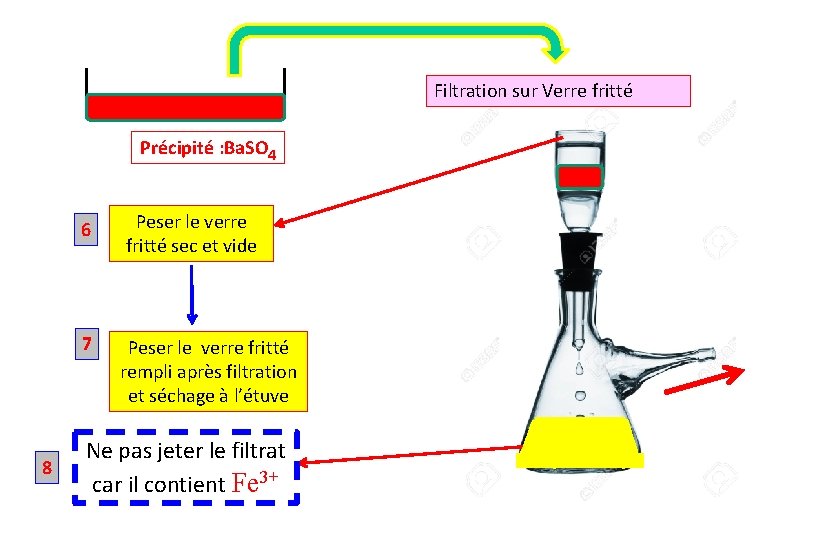
Filtration sur Verre fritté Précipité : Ba. SO 4 8 6 Peser le verre fritté sec et vide 7 Peser le verre fritté rempli après filtration et séchage à l’étuve Ne pas jeter le filtrat car il contient Fe 3+
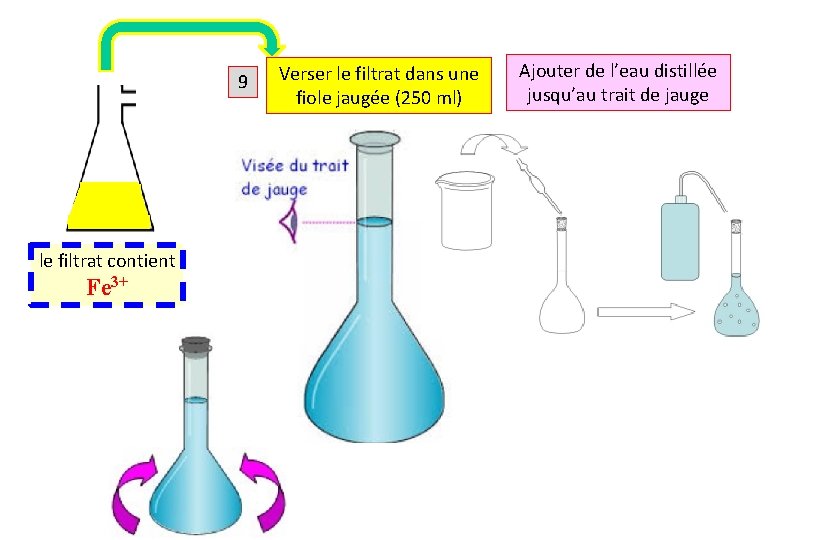
9 le filtrat contient Fe 3+ Verser le filtrat dans une fiole jaugée (250 ml) Ajouter de l’eau distillée jusqu’au trait de jauge
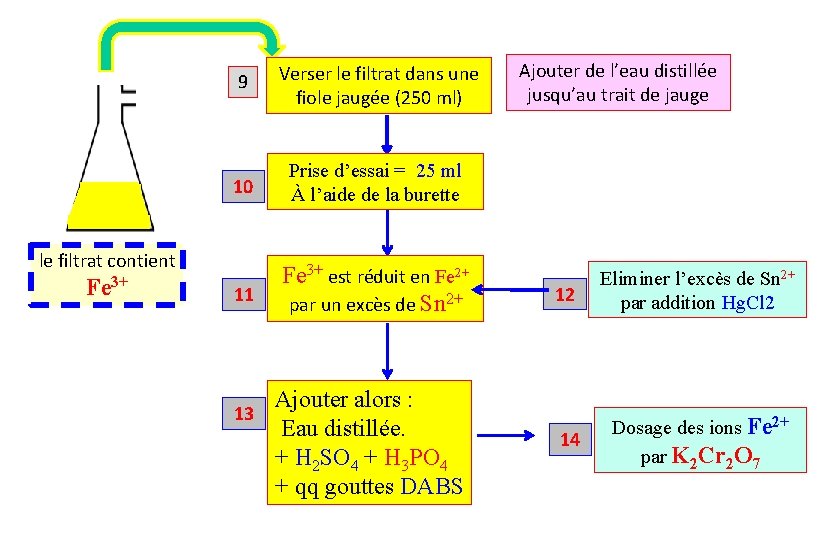
9 Verser le filtrat dans une fiole jaugée (250 ml) 10 Prise d’essai = 25 ml À l’aide de la burette 11 Fe 3+ est réduit en Fe 2+ par un excès de Sn 2+ le filtrat contient Fe 3+ 13 Ajouter alors : Eau distillée. + H 2 SO 4 + H 3 PO 4 + qq gouttes DABS Ajouter de l’eau distillée jusqu’au trait de jauge 12 Eliminer l’excès de Sn 2+ par addition Hg. Cl 2 14 Dosage des ions Fe 2+ par K 2 Cr 2 O 7
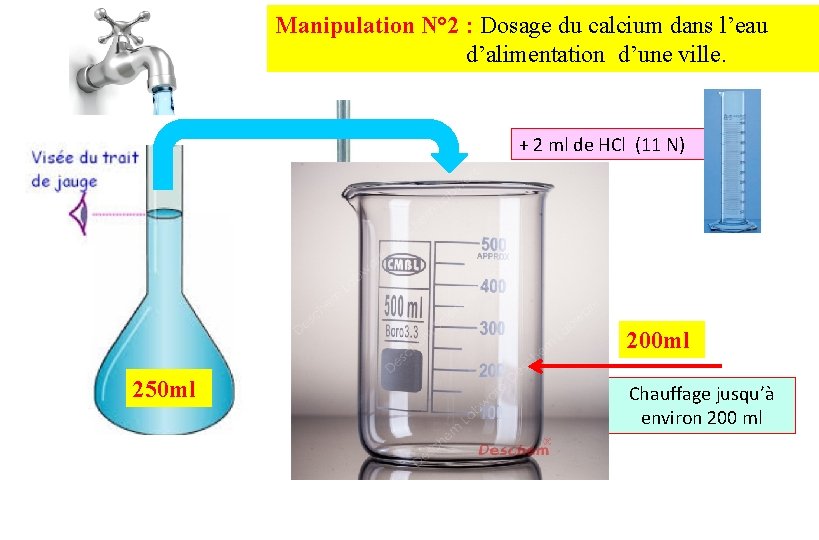
Manipulation N° 2 : Dosage du calcium dans l’eau d’alimentation d’une ville. + 2 ml de HCl (11 N) 200 ml 250 ml Chauffage jusqu’à environ 200 ml

2 gouttes d’héliantine Coloration rouge + 5 ml NH 4 Cl à 25% + NH 3 jusqu’au virage au jaune + 40 ml oxalate d’ammonium Maintenir l’ébullition 2à 3 min Acidifier la solution en ajoutant l’acide acétique CH 3 COOH Laisser déposer le précipité blanc Oxalate de Ca Faire bouillir le mélange
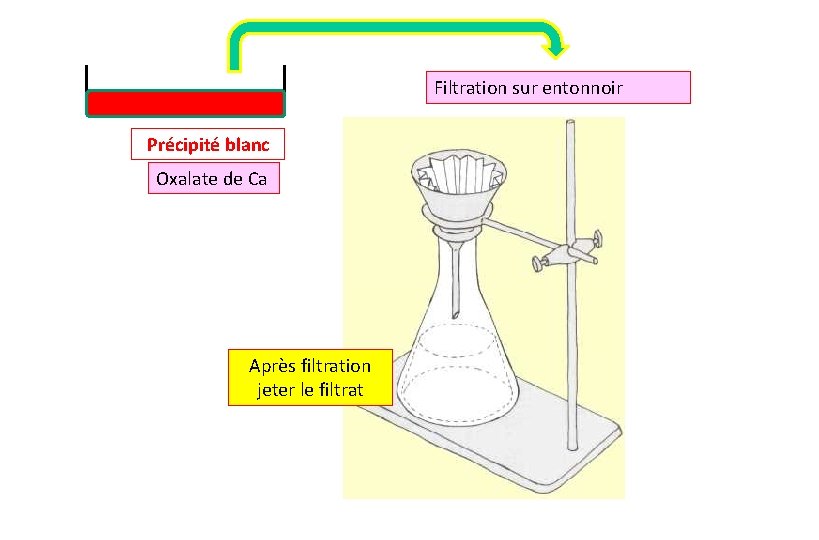
Filtration sur entonnoir Précipité blanc Oxalate de Ca Après filtration jeter le filtrat
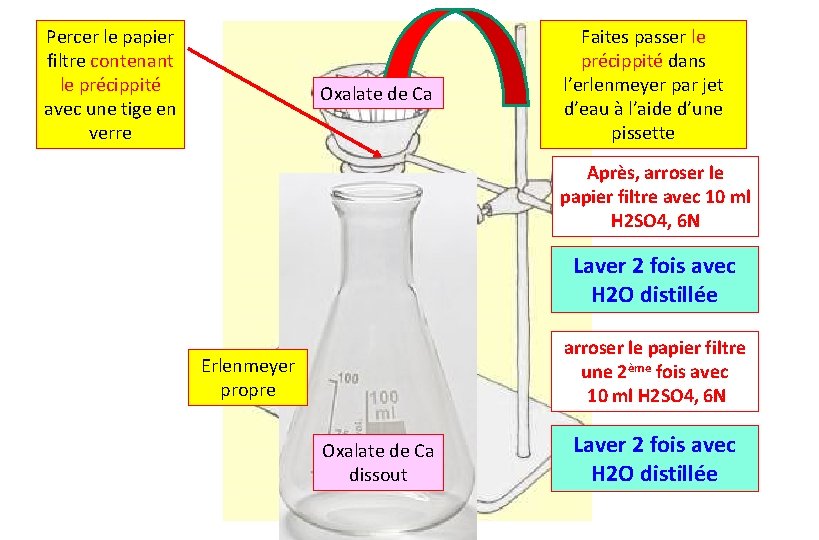
Percer le papier filtre contenant le précippité avec une tige en verre Oxalate de Ca Faites passer le précippité dans l’erlenmeyer par jet d’eau à l’aide d’une pissette Après, arroser le papier filtre avec 10 ml H 2 SO 4, 6 N Laver 2 fois avec H 2 O distillée arroser le papier filtre une 2ème fois avec 10 ml H 2 SO 4, 6 N Erlenmeyer propre Oxalate de Ca dissout Laver 2 fois avec H 2 O distillée
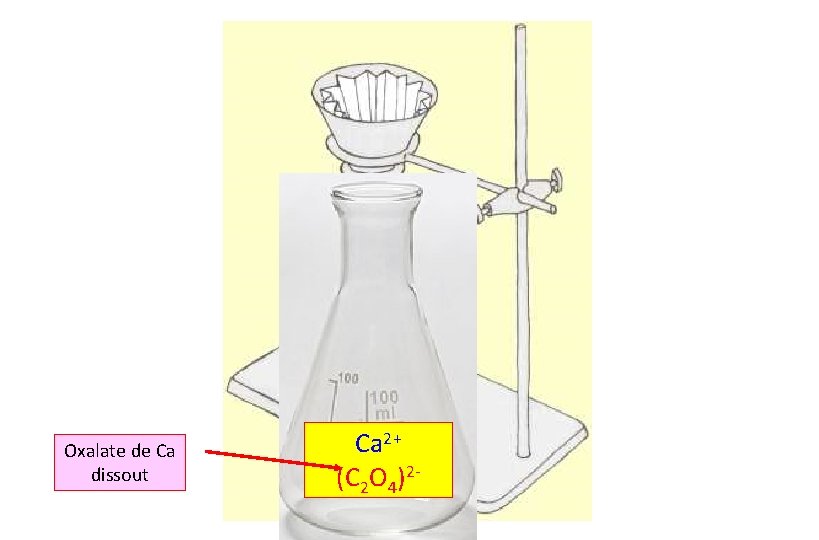
Oxalate de Ca dissout Ca 2+ (C 2 O 4)2 -
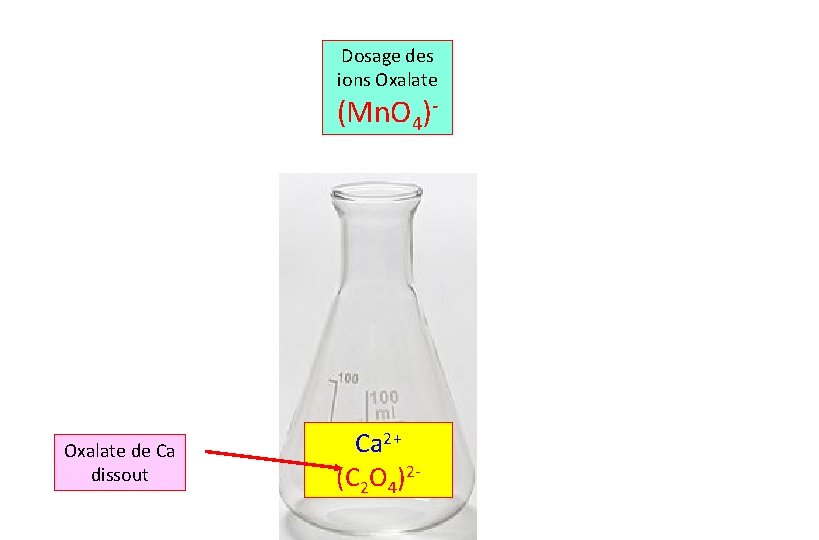
Dosage des ions Oxalate (Mn. O 4)- Oxalate de Ca dissout Ca 2+ (C 2 O 4)2 -
- Slides: 14