Universit hassan II Casablanca Facult des Sciences An

Université hassan II - Casablanca Faculté des Sciences Aïn Chock Travaux pratiques de Chimie descriptive SMC 3 Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Manipulation N° 2 : Dosage du calcium dans l’eau d’alimentation d’une ville. Manipulation N° 3 : Préparation et analyse du sel de Mohr.

Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Expérience Burette Dosage des ions Ba 2+ Solution So contenant du Ba 2+ et du Fe 3+. 20 ml = volume précis Solution So Pipette, burette 20 ml

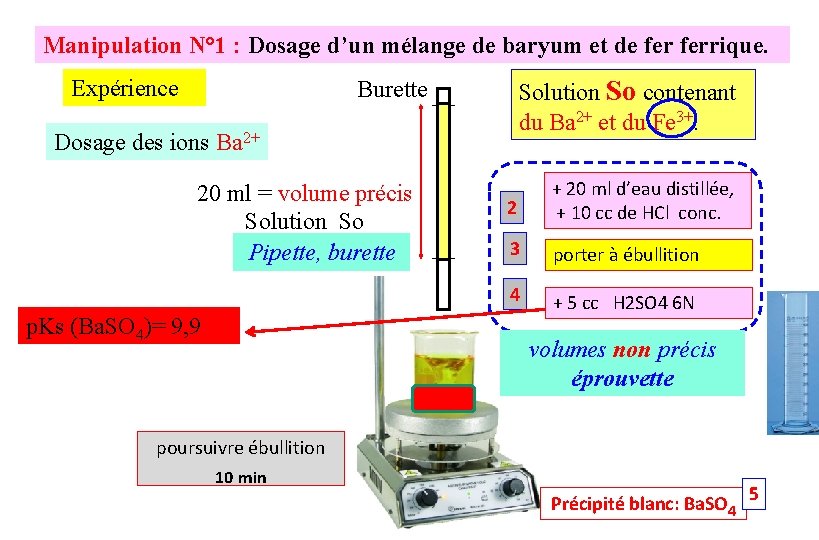
Manipulation N° 1 : Dosage d’un mélange de baryum et de ferrique. Expérience Solution So contenant du Ba 2+ et du Fe 3+. Burette Dosage des ions Ba 2+ 20 ml = volume précis Solution So Pipette, burette p. Ks (Ba. SO 4)= 9, 9 2 + 20 ml d’eau distillée, + 10 cc de HCl conc. 3 porter à ébullition 4 + 5 cc H 2 SO 4 6 N volumes non précis éprouvette poursuivre ébullition 10 min Précipité blanc: Ba. SO 4 5
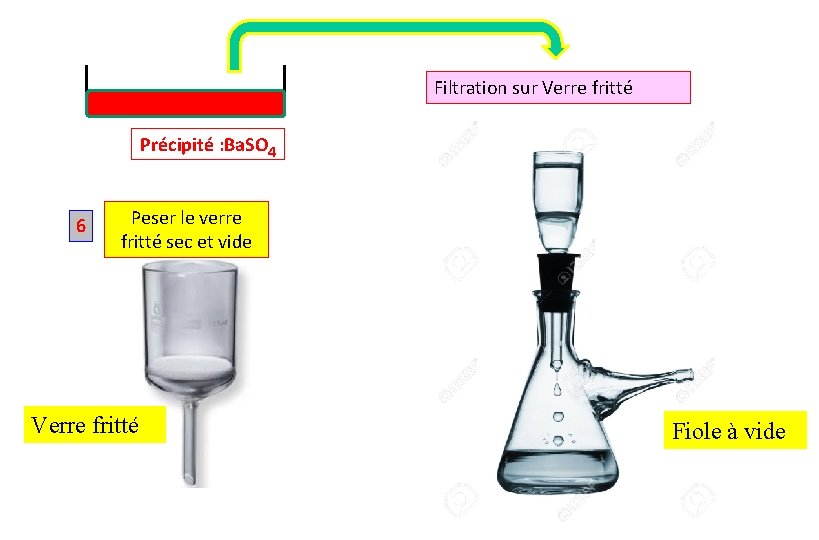
Filtration sur Verre fritté Précipité : Ba. SO 4 6 Peser le verre fritté sec et vide Verre fritté Fiole à vide
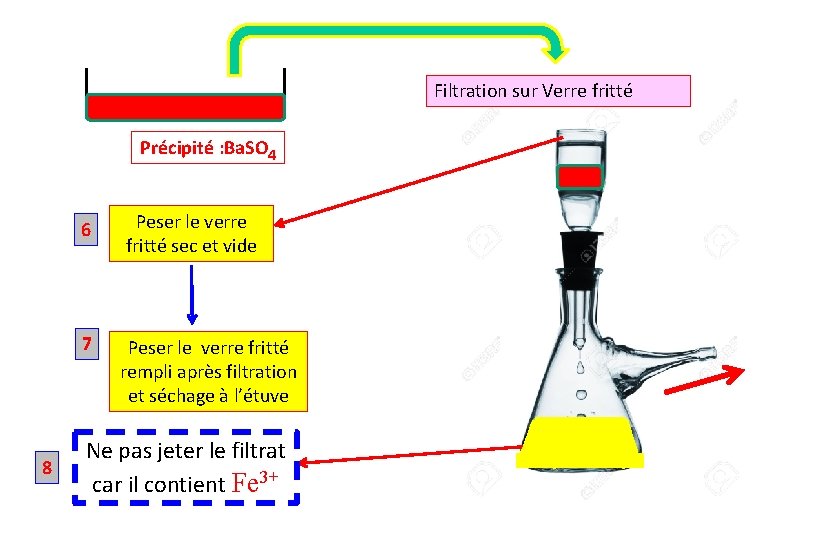
Filtration sur Verre fritté Précipité : Ba. SO 4 8 6 Peser le verre fritté sec et vide 7 Peser le verre fritté rempli après filtration et séchage à l’étuve Ne pas jeter le filtrat car il contient Fe 3+
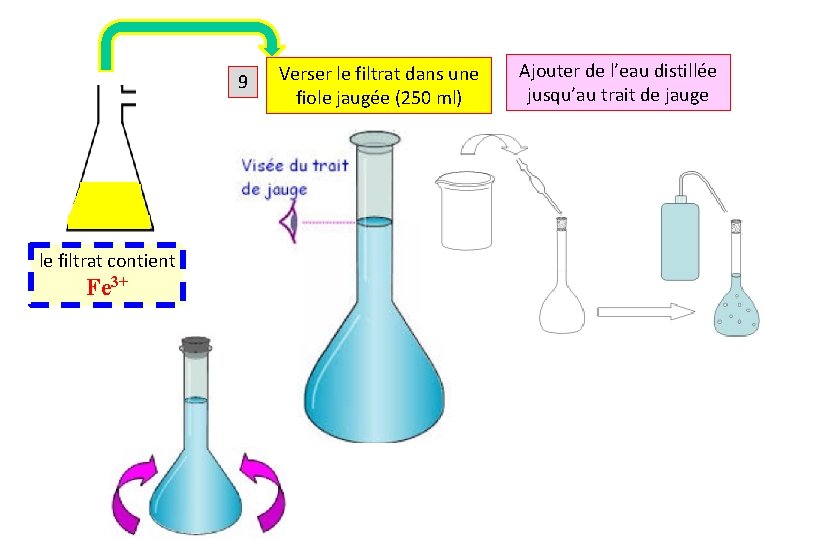
9 le filtrat contient Fe 3+ Verser le filtrat dans une fiole jaugée (250 ml) Ajouter de l’eau distillée jusqu’au trait de jauge
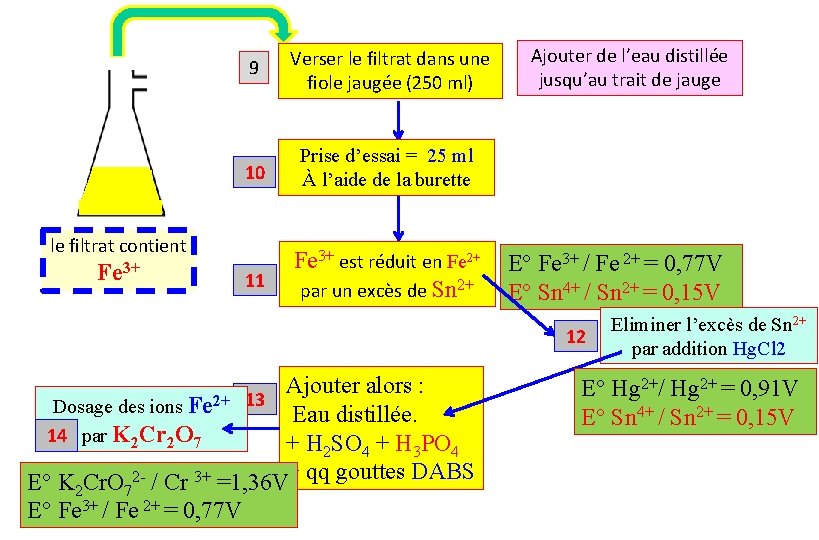
9 Verser le filtrat dans une fiole jaugée (250 ml) 10 Prise d’essai = 25 ml À l’aide de la burette 11 Fe 3+ est réduit en Fe 2+ par un excès de Sn 2+ le filtrat contient Fe 3+ Ajouter de l’eau distillée jusqu’au trait de jauge E° Fe 3+ / Fe 2+ = 0, 77 V E° Sn 4+ / Sn 2+ = 0, 15 V 12 Ajouter alors : 2+ 13 Dosage des ions Fe Eau distillée. 14 par K 2 Cr 2 O 7 + H 2 SO 4 + H 3 PO 4 E° K Cr. O 2 - / Cr 3+ =1, 36 V+ qq gouttes DABS E° 2 7 Fe 3+ / Fe 2+ = 0, 77 V Eliminer l’excès de Sn 2+ par addition Hg. Cl 2 E° Hg 2+/ Hg 2+ = 0, 91 V E° Sn 4+ / Sn 2+ = 0, 15 V
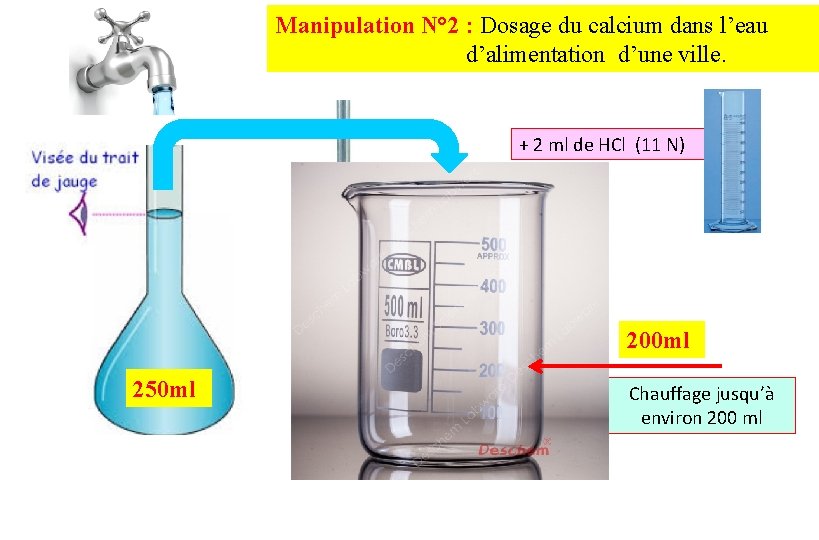
Manipulation N° 2 : Dosage du calcium dans l’eau d’alimentation d’une ville. + 2 ml de HCl (11 N) 200 ml 250 ml Chauffage jusqu’à environ 200 ml

2 gouttes d’héliantine + 40 ml oxalate d’ammonium Coloration rouge + 5 ml NH 4 Cl à 25% + NH 3 jusqu’au virage au jaune Maintenir l’ébullition 2à 3 min Acidifier la solution en ajoutant l’acide acétique CH 3 COOH Laisser déposer le précipité blanc Oxalate de Ca p. Ks (Ca. C 2 O 4)= 8, 7 p. Ka (CH 3 CO 2 H/CH 3 CO 2 -) = 4, 75 Faire bouillir le mélange
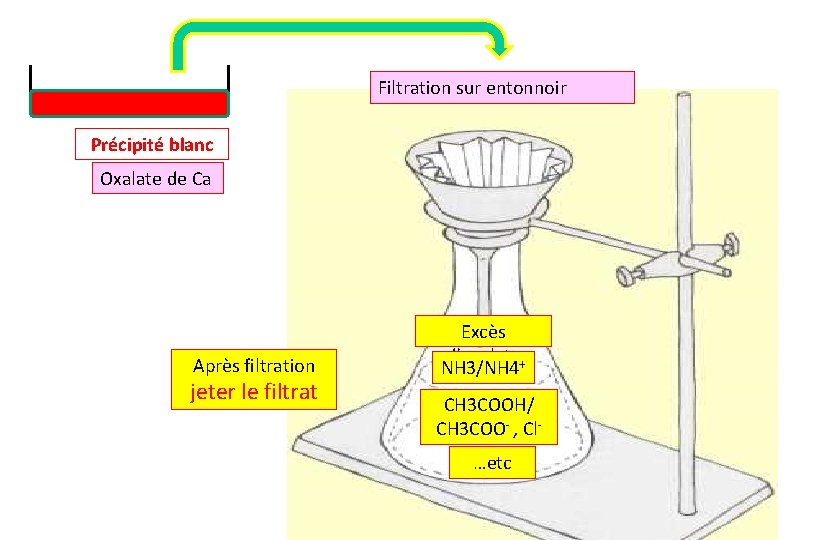
Filtration sur entonnoir Précipité blanc Oxalate de Ca Après filtration jeter le filtrat Excès d’oxalate NH 3/NH 4+ CH 3 COOH/ CH 3 COO- , Cl…etc
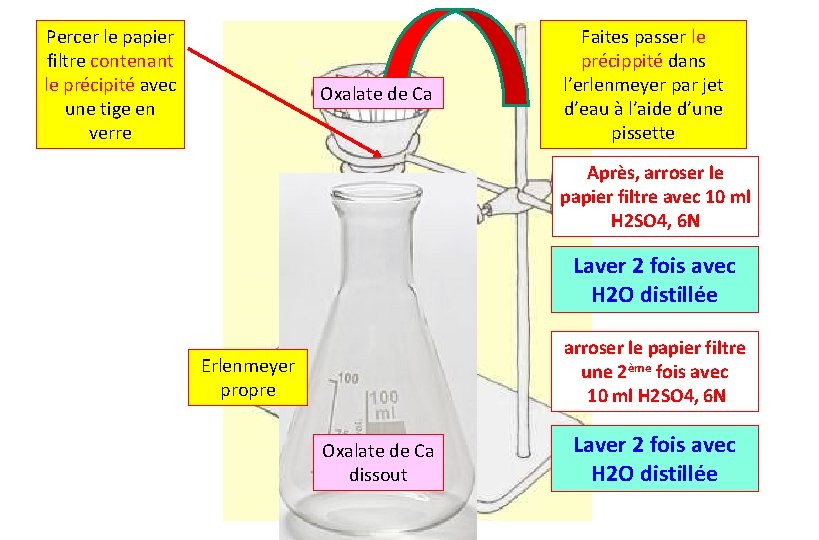
Percer le papier filtre contenant le précipité avec une tige en verre Oxalate de Ca Faites passer le précippité dans l’erlenmeyer par jet d’eau à l’aide d’une pissette Après, arroser le papier filtre avec 10 ml H 2 SO 4, 6 N Laver 2 fois avec H 2 O distillée arroser le papier filtre une 2ème fois avec 10 ml H 2 SO 4, 6 N Erlenmeyer propre Oxalate de Ca dissout Laver 2 fois avec H 2 O distillée
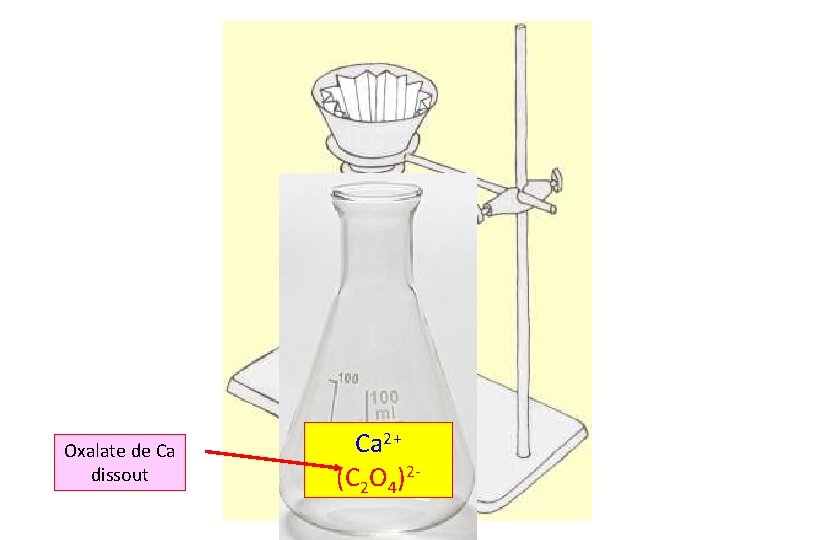
Oxalate de Ca dissout Ca 2+ (C 2 O 4)2 -
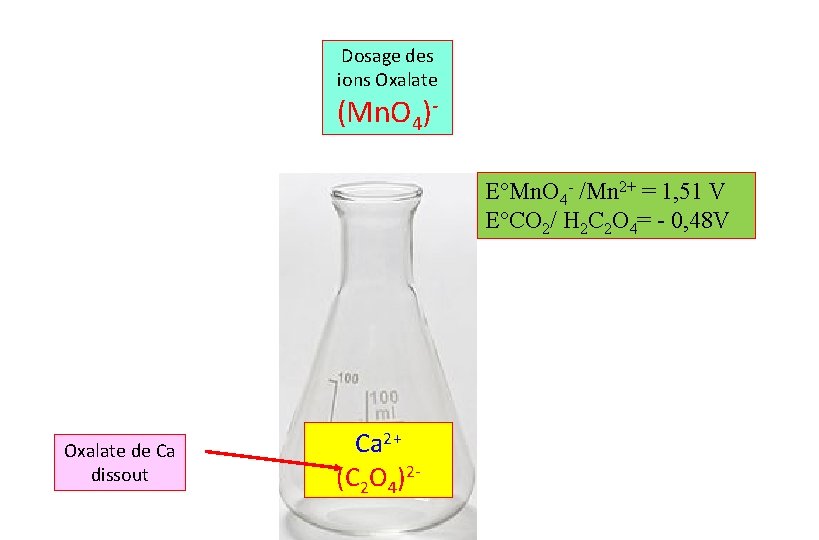
Dosage des ions Oxalate (Mn. O 4)E°Mn. O 4 - /Mn 2+ = 1, 51 V E°CO 2/ H 2 C 2 O 4= - 0, 48 V Oxalate de Ca dissout Ca 2+ (C 2 O 4)2 -

Manipulation N° 3 : Préparation et analyse du sel de Mohr. Une masse m 1 de sulfate ferreux Fe. SO 4, 7 H 2 O) et une masse m 2 (sulfate d'ammonium (NH 4)2 SO 4) sont dissoutes dans un minimum d'eau. Le sel de Mohr est alors précipité par addition d'un volume conséquent d'alcool. Après filtration et lavage à l’alcool, on recueille le sel de Mohr. + (NH 4) 2 Fe 2+ 2 - (SO 4)2, x H 2 O
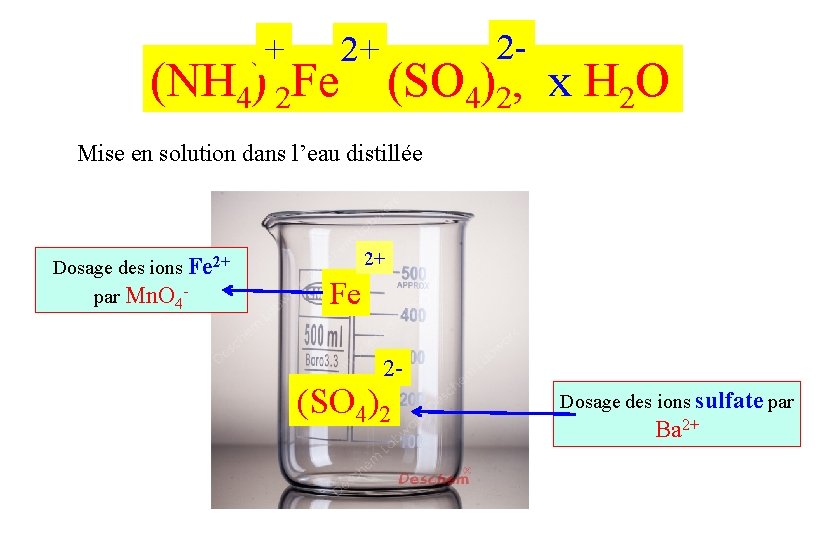
+ (NH 4) 2 Fe 2 - 2+ (SO 4)2, x H 2 O Mise en solution dans l’eau distillée Dosage des ions Fe 2+ par Mn. O 4 - 2+ Fe 2 - (SO 4)2 Dosage des ions sulfate par Ba 2+
- Slides: 16