Universit di Roma TOR VERGATA CL in Medicina





















- Slides: 30

Università di Roma TOR VERGATA CL in Medicina Biochimica (Prof L. Avigliano) GENERALITA’ SUL METABOLISMO DIGESTIONE ED ASSORBIMENTO DEI CARBOIDRATI GLICOLISI

ENERGIA per Ø gradiente elettrochimico (Na/K ATPasi) Ø processi biosintetici (es. sintesi proteica) Ø trasporto di molecole transmembrana Ø trasduzione del segnale Ø lavoro meccanico (respirazione, contrazione cardiaca, contrazione muscolare) FONTI DI ENERGIA - carboidrati GLUCOSIO - trigliceridi ACIDI GRASSI - scheletro carbonioso degli amminoacidi RESA ENERGETICA ~ 35 % “SOTTOPRODOTTI” calore, CO 2, H 2 O, NH 3 ( urea)

UTILIZZAZIONE D’ENERGIA A RIPOSO organo consumo ATP fegato Na/K ATPasi sistema nervoso sintesi proteine 3% peso corporeo muscolo miosina ATPasi stomaco e intestino calcio ATPasi cuore ciclo dei substrati rene polmoni altro alltro

METABOLISMO VIA METABOLICA - METABOLITA - ENERGIA CATABOLISMO - REAZIONI ESOERGONICHE DEGRADAZIONE DEIDROGENAZIONE (NAD+, NADP+, FAD) PRODUZIONE DI ATP ANABOLISMO - REAZIONI ENDOERGONICHE SINTESI IDROGENAZIONE (NADPH + H+) CONSUMO DI ATP § Metaboliti in comune § Meccanismi di controllo regolano il flusso metabolico § Diversa localizzazione cellulare e d’organo

DEIDROGENASI NAD+ NADH + H+ NON LEGATO COVALENTEMENTE OSSIDA: ALCOL ALDEIDE/CHETONE ACIDO NADP+ NADPH + H+ FADH 2 LEGATO COVALENTEMENTE ( enzima di membrana, esempio Complesso II) OSSIDA: IDROCARBURO saturo IDROCARBURO insaturo (+ H 2 O ALCOL)

Ø DIETA Ø BIOSINTESI Ø RISERVE Componenti della DIETA NUTRIENTI: glucidi, lipidi, proteine, vitamine, minerali NUTRIENTI ESSENZIALI L’organismo è incapace di sintetizzarli e devono essere assunti con la dieta acidi grassi 6 ed 3, alcuni amminoacidi, minerali, quasi tutte le vitamine

Il nutriente per essere utilizzato deve prima subire i processi di - Digestione Polimero monomero - per scissione idrolitica - Assorbimento lume intestinale enterocita circolo (plasma, linfa) MALASSORBIMENTO Difetti digestione /assorbimento

DIGESTIONE BOCCA saliva: digestione amido ( -amilasi) STOMACO digestione proteine (e trigliceridi) - HCl - zimogeni ed enzimi (pepsinogeno) - fattore intrinseco (assorbimento vit B 12) INTESTINO TENUE digestione proteine, carboidrati, lipidi Ø bile - funzione digestiva, HCO 3 -, sali biliari -funzione escretoria ( sostanze lipofile, quali pigmenti biliari, farmaci) Ø secrezione pancreatica: HCO 3 -, zimogeni ed enzimi COLON fermentazione batterica

ALTERAZIONI secrezione conseguenze ————————————— HCl assorbimento ferro (anemia) fattore intrinseco assorbimento vit B 12 sali biliari assorbimento lipidi e vit liposolubili enzimi pancreatici digestione di tutti gli alimenti

glucosio vs acido grasso unica fonte energetica utilizzabile in assenza di O 2 fonte obbligata per eritrocita fonte di energia per il sistema nervoso strettamente aerobica fonte energetica di riserva scarsa rispetto ai trigliceridi ma prontamente utilizzabile -glicogeno epatico (50 -100 g sufficienti per 8 -12 h, a riposo) -glicogeno muscolare (400 g totali) facilita il metabolismo lipidico con scarso glucosio (es digiuno) si formano i corpi chetonici risparmia le proteine in assenza di glucosio si ha biosintesi di glucosio - gluconeogenesi -da glicerolo ed amminoacidi

FONTI DI GLUCOSIO DIETA AMIDO, saccarosio, lattosio RISERVE Glicogeno epatico BIOSINTESI Gluconeogenesi epatica

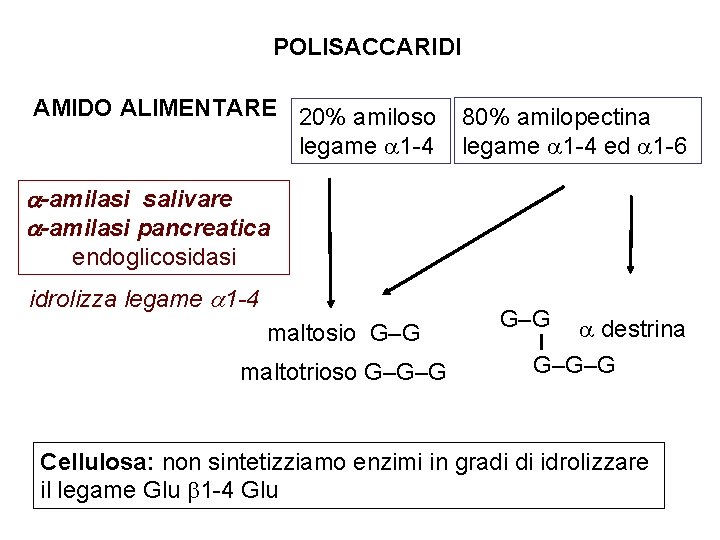
POLISACCARIDI AMIDO ALIMENTARE 20% amiloso legame 1 -4 80% amilopectina legame 1 -4 ed 1 -6 -amilasi salivare -amilasi pancreatica endoglicosidasi idrolizza legame 1 -4 maltosio G–G maltotrioso G–G–G destrina G–G–G Cellulosa: non sintetizziamo enzimi in gradi di idrolizzare il legame Glu 1 -4 Glu

DISACCARIDI: idrolizzati da enzimi sintetizzati dall’enterocita e siti sulla membrana plasmatica -glicosidasi maltasi scinde legame Glu 1 -4 Glu saccarasi scinde legame Glu 1 -2 Fru isomaltasi scinde legame Glu 1 -6 Glu -galattosidasi lattasi scinde legame Gal 1 -4 Glu IPOLACTASIA: Polimorfismo genetico porta a Fenotipo “non persistente”: adulto cala al 10%, stato ancestrale normale nei mammiferi Fenotipo “persistente”: stessi livelli nell’adulto -popolazione nord Europa e area mediterranea - (mutazione 6. 000 -9. 000 anni fa con la pastorizia; per favorire assorbimento di calcio nei popoli nordici)

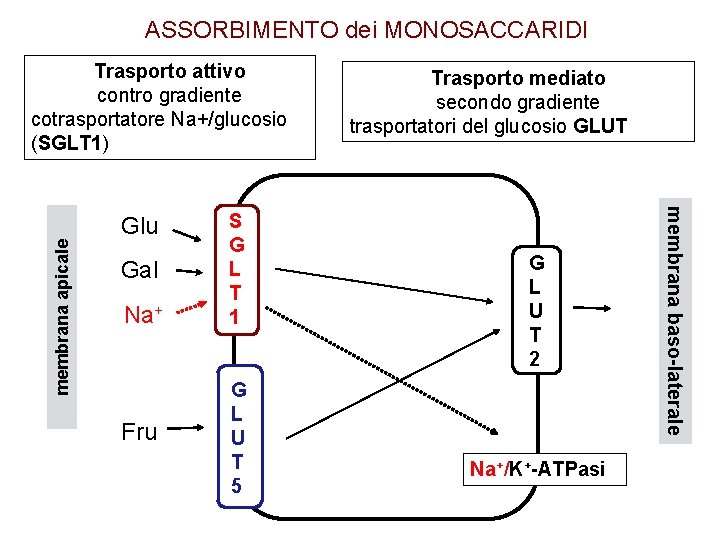
ASSORBIMENTO dei MONOSACCARIDI Glu Gal Na+ Fru S G L T 1 G L U T 5 Trasporto mediato secondo gradiente trasportatori del glucosio GLUT G L U T 2 Na+/K+-ATPasi membrana baso-laterale membrana apicale Trasporto attivo contro gradiente cotrasportatore Na+/glucosio (SGLT 1)

glicemia dopo digiuno notturno ~ 5 m. M (80 mg/d. L) 3, 5 m. M (digiuno prolungato) 7, 2 m. M (ricco pasto glucidico) glicosuria 9 -10 m. M Metabolismo glucidico regolato da ormoni insulina: ipoglicemizzante glucagone, cortisolo, adrenalina: iperglicemizzanti

danno da eccesso di glucosio il gruppo aldeidico è un gruppo reattivo che porta a - glicazione non enzimatica di proteine il gruppo aldeidico reagisce con il gruppo amminico di proteine il livello di Hb glicosilata è un indice del controllo glicemico - autoossidazione e formazione di ROS (specie reattive dell’ossigeno)

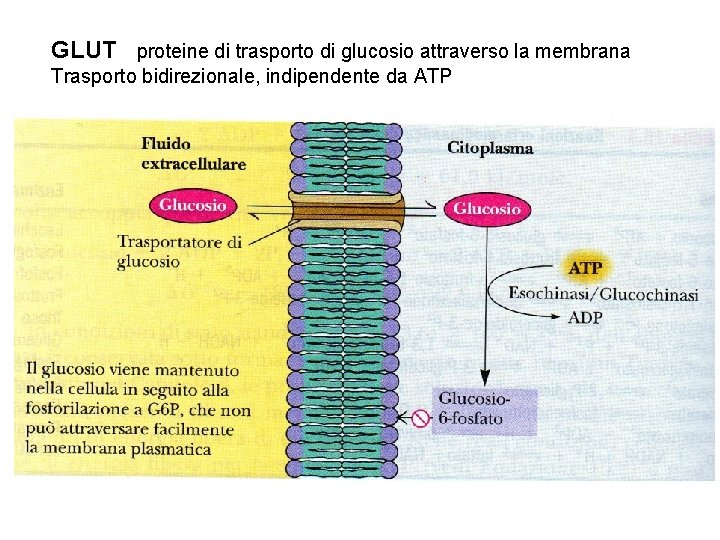
GLUT proteine di trasporto di glucosio attraverso la membrana Trasporto bidirezionale, indipendente da ATP

finora identificate 12 isoforme (GLU 1 GLUT 12 da geni diversi) GLUT 1 eritrocita, ubiquitario GLUT 2 intestiono, fegato, isole pancreatiche GLUT 3 cervello GLUT 4 muscolo, tessuto adiposo GLUT 5 intestino (specifico per fruttosio) insulina indipendente regolato dall’insulina Isoforme diverse per specificità di substrato e parametri cinetici GLUT 1 Km 3 m. M GLUT 2 Km 17 m. M - bassa affinità mai saturo, flusso lineare concentrazione di Glu GLUT 3 Km 1, 7 m. M - alta affinità, saturo anche a basse conc Glu GLUT 4 Km 5 m. M GLUT 4 - riserva intracellulare. In seguito allo stimolo dell’insulina, GLUT 4 va incontro a rapida traslocazione sulla membrana, con aumento dell’attività di trasporto

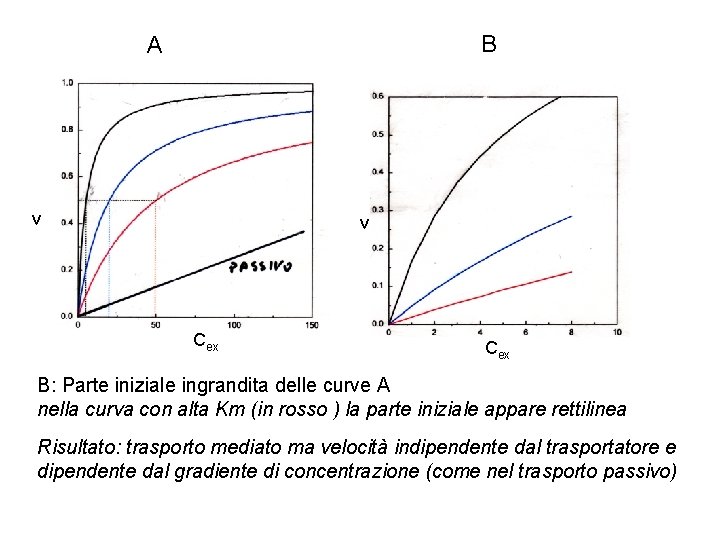
Trasporto descritto da una funzione Michaelis - Menten Gex + T Gint + T con una cinetica di saturazione Gex V = Vmax –––– Km + Gex Vmax = kcat T specifico e dipende da Livello del trasportatore Affinità del trasportatore per il glucosio Capacità di turnover del trasportatore

B A v v Cex B: Parte iniziale ingrandita delle curve A nella curva con alta Km (in rosso ) la parte iniziale appare rettilinea Risultato: trasporto mediato ma velocità indipendente dal trasportatore e dipendente dal gradiente di concentrazione (come nel trasporto passivo)

qualunque sia il destino metabolico G + Mg-ATP G 6 P (glicogenosintesi, glicolisi, via dei pentosi. P, ac glucuronico) ESOCHINASI alta affinità (Km = 0, 1 m. M) cervello, muscolo, ubiquitaria - funziona in presenza di bassa disponibilità di glucosio - non specifica - inibita dal prodotto G 6 P GLUCOCHINASI epatica bassa affinità (Km = 5 m. M) - funziona in presenza di alta disponibilità di glucosio - specifica per il glucosio - non inibita dal prodotto G 6 P - inducibile (ormoni, dieta) insulina glucosio digiuno diabete (conseguente alta glicemia) G 6 P punto di arrivo di glicogenolisi e gluconeogenesi G 6 P FOSFATASI epatica G 6 P + H 2 O G + Pi CONTROLLO GLICEMIA

GLICOLISI

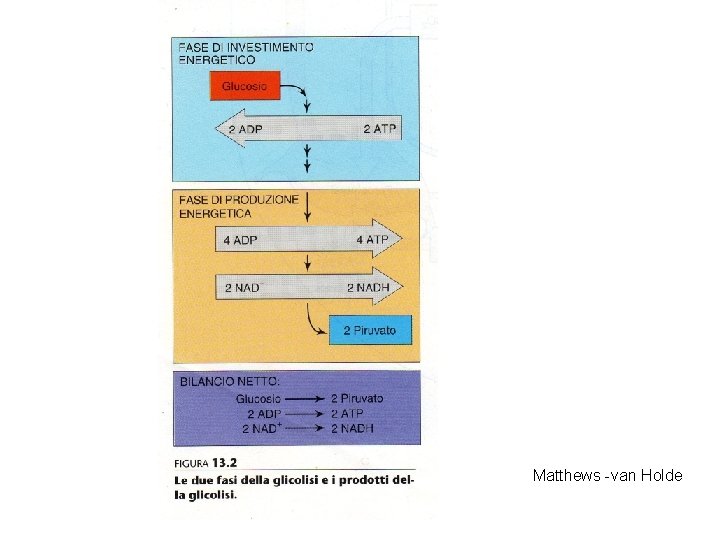
GLICOLISI unica via in grado di produrre ATP in assenza di O 2 tramite FOSFORILAZIONE A LIVELLO DEL SUBSTRATO Resa energetica della glicolisi anaerobica: 5% rispetto alla fosforilazione ossidativa ma più rapida

Matthews -van Holde

ESISTONO DUE MECCANISMI PER LA SINTESI DELL’ATP MITOCONDRIALE fosforilazione ossidativa: richiede gradiente di membrana CITOPLASMATICA fosforilazione a livello del substrato: avviene in soluzione, pertanto il legame ad alta energia deve essere trasferito direttamente da un composto ad un altro

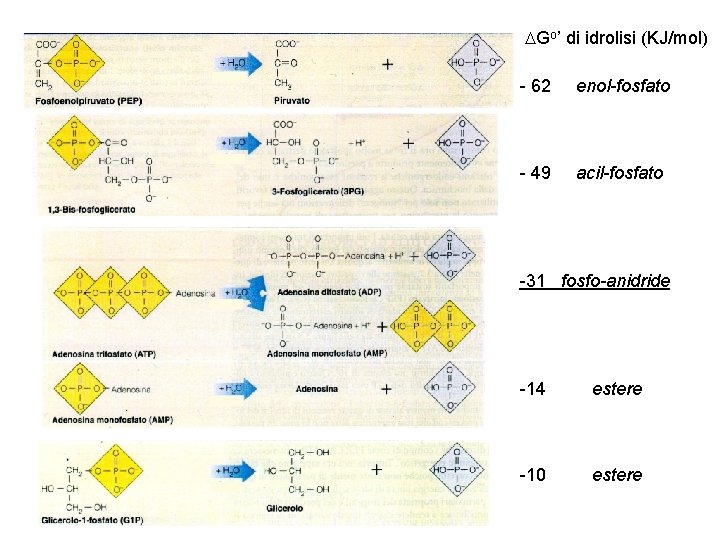
LEGAMI AD “ALTA ENERGIA” legami la cui idrolisi è fortemente esoergonica > 25 k. J/mol Fosfo anidride Fosfo guanidina Acil fosfato Enol fosfato Intermedi della glicolisi sono 2 composti fosforilati con Go’ di idrolisi più esoergonico del legame fosfoanidridico presente nell’ ATP ( -31 KJ/mol) fosfo enolpiruvato ( Go’ di idrolisi = - 62 KJ/mol) 1 -3 bis fosfoglicerato ( Go’ di idrolisi = - 49 KJ/mol)

Go’ di idrolisi (KJ/mol) - 62 enol-fosfato - 49 acil-fosfato -31 fosfo-anidride -14 estere -10 estere

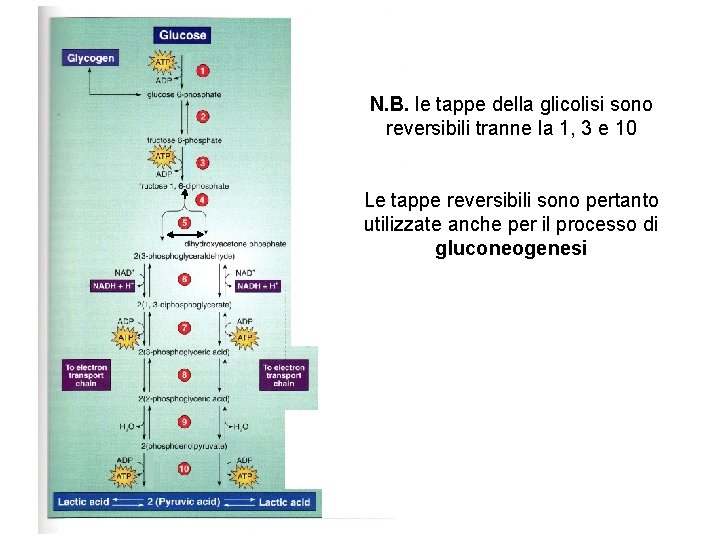
N. B. le tappe della glicolisi sono reversibili tranne la 1, 3 e 10 Le tappe reversibili sono pertanto utilizzate anche per il processo di gluconeogenesi

