Universit degli Studi di Bari scuola di Medicina

Università degli Studi di Bari – scuola di Medicina e Chirurgia Polo Scientifico Didattico di Tricase Corso di Laurea in Infermieristica Anno Accademico: 2018 -19 Corso integrato: oncologia medica Docente: Dr. Emiliano Tamburini Farmaci antiblastici ed effetti tossici
Timeline dello sviluppo dei farmaci oncologici 2
Timeline dello sviluppo dei farmaci oncologici 3

Storia della chemioterapia • Primi anni ‘ 900 ricerca antibiotici • Sviluppo primi agenti chemioterapici 1940 -1960 • Agenti alchilanti sviluppati dalle armi chimiche (mostarde azotate) usate nella 1° e 2° guerra mondiale L’iprite: struttura chimica e i suoi effetti acuti – Osservazione casi ipoplasia linfoide e midollare – Prime osservazioni trattamento linfomi con risposte sorprendenti ma temporanee • 1950: scoperta effetto antiproliferativo inibitori acido folico – Remissioni complete alcune forme leucemia 4

Terapia medica antitumorale • Chemioterapia antiblastica: chemioterapici citotossici • Ormonoterapia: ormoni, antagonisti di ormoni o loro recettori • Terapia target: farmaci diretti con bersagli molecolari. Interagiscono con fattori di crescita e di trasmissione dei segnali proliferativi. • Immunoterapia: farmaci che stimolano il sistema immunitario • Radioterapia e terapia radiometabolica: radiazionizzanti • Terapie di supporto e citoprotettori: farmaci per ridurre sintomi ed effetti collaterali dei trattamenti 5

Terapie antitumorali Chemioterapia Ormonoterapia Farmaci citotossici antiblastici Ormoni ed anti-ormoni che antagonizzano meccanismi endocrini di crescita cellulare Radioterapia Impiego di radiazionizzanti per colpire il tumore Immunoterapia Agenti stimolanti la reazione del sistema immunitario contro il tumore Agenti target o terapie biologiche Terapie di supporto e citoprotettori Interagiscono con fattori di crescita, meccanismi molecolare e di trasmissione dei segnali proliferativi Farmaci collaterali atti a ridurre sintomi o effetti collaterali dei trattamenti antitumorali: 6

Storia della chemioterapia • • • Anni ‘ 60 aumento del numero di farmaci attivi alcuni estratti da piante (vincristina e dalla pervinca, taxolo dalla corteccia del tasso ) o di sintesi. Grande programma di ricerca di molecole ad azione antitumorale )NCI-USA). Iniziale utilizzo delle combinazioni di farmaci (polichemioterapia) Anni ‘ 70: neoplasie come il Linfoma di Hodgkin e del testicolo diventano malattie potenzialmente curabili Anni ‘ 80 primi risultati sulle terapie adiuvanti del tumore mammario, osteosarcoma , colon, iniziale introduzione di terapie biologiche (interferoni ed altre) Anni ’ 90: ottimizzazione farmaci noti, nuovi farmaci, integrazione diverse modalità terapeutiche, impiego citochine, modificatori risposta biologica, fattori di crescita e terapie di supporto Anni 2000: terapie biologiche Pervinca Taxus brevifolia e baccata 7

Farmaci citotossici o antiblastici • Molecole di sintesi, prodotti naturali o loro derivati semisintetici • Interferiscono con la sintesi o la funzione di macromolecole biologicamente rilevanti, e conseguentemente con la proliferazione cellulare, inibendola • Cellule attivamente proliferanti maggiormente colpite 8

Farmaci citotossici: effetti indesiderati • Cellule in continua replicazione presenti in molti tessuti normali, oltre che neoplastici – Ciò è all’origine degli effetti terapeutici e collaterali per limitata specificità degli effetti della chemioterapia. • Tessuti con rapido turn-over a maggior rischio di eventi tossici: – – Midollo osseo Mucose gastrointestinali Cute e follicoli piliferi Cellule germinali • Intervallo di dose all’estremo dei quali si ottengono effetti benefici e tossici è generalmente piccolo 9

Il ciclo cellulare • G 0: fase di quiescenza: le cellule non si dividono; permane la sintesi proteica a velocità ridotta. • G 1: fase postmitotica o interfase. Vengono prodotti proteine, RNA ed enzimi per la sintesi di DNA. • S: fase di sintesi del DNA • G 2: fase di premitosi. Ulteriore sintesi di proteina ed RNA, produzione di precursori del fuso mitotico. • Mitosi: divisione cellulare. 10

Classificazione di farmaci • In base al meccanismo d’azione • In base all’origine (naturale o di sintesi) • In base alla struttura chimica • In base all’attività in rapporto al ciclo cellulare – Farmaci ciclo specifici (fase non specifici): efficaci su cellule proliferanti indipendentemente dalla fase – Farmaci ciclo specifici-fase specifici: più attivi su cellule in particolari fasi del ciclo. – Farmaci non ciclo specifici: attivi sia su cellule quiescenti che in divisione • Talora i farmaci appartengono a più classi o a nessuna (miscellanei) 11

Farmaci antiblastici • • Alchilanti Derivati del platino Antimetaboliti Alcaloidi della vinca, epipodofillotossine, taxani • Antibiotici tumorali • Miscellanei 12

Alchilanti: farmaci e meccanismo d’azione • Effetti correlati alla capacità di formare legami covalenti con gruppi nucleofilici dei DNA (N 7 guanina) e gruppi reattivi proteici – Formazione di legami di inter ed intracatenari (DNA), sia legami con proteine, con rigidità, rotture delle catene di DNA, ostacolo della divisione cellulare. • Considerati come attivi su cellule in proliferazione, durante tulle le fasi del ciclo (preferenzialmente in tarda fase G 1 -S). • Spesso necessità di attivazione metabolica, in genere epatica. 13

Alchilanti: classificazione • Mostarde azotate – – – Mecloretamina Chlorambucil Ciclofosfamide Ifosfamide Melphalan • Etilenimine – Thiotepa • Melamine – Esametilmelamina • Alchilsulfonati • Triazeni – Dacarbazina • Nitrosouree – – – Carmustina (BCNU) Lomustina (CCNU) Semustina (Me-CCNU) Streptozocina Fotemustina, Estramustine Bendamustina • Imidazotetrazine – Temozolamide – Busulfano 14

Principali alchilanti: ciclofosfamide • Agente alchilante con ampie indicazioni di impiego: – Ematologia (linfomi, leucemie, ) – Oncologia (neoplasie mammarie, ovariche, microcitoma polmonare, sarcomi, ecc – Patologie autoimmuni (sclerosi multipla, patologie recumatiche ecc. ). • Disponibile in compresse rivestite (50 mg) o polvere per soluzione iniettabile, da ricostituire (200, 500 e 1000 mg) – Con soluzione fisiologica in caso di immediata iniezione parenterale (im/ev), o con acqua per preparazioni iniettabili e aggiunta a soluzioni per infusione ev: fisiologica, glucosata ed altre (utilizzo prevalente). Soluzione conservabile per 2 -3 ore. • Dosi standard: 600 -1200 mg/m 2 ogni 1 -3 settimane (ev), 100 mg/m 2 (os) per 14 gg (dosi metronomiche 50 mg/d continuative), alte dosi mobilizzazione cellule staminali emopoietiche (dosi intermedie = 2 -3 g/m 2 fino a 7 g/m 2). 15

Principali alchilanti: ifosfamide • Derivato della ciclofosfamide, particolarmente attivo nei sarcomi e tumori del testicolo. • Disponibile come polvere per infusione (1 g e 2 g) con acqua per PI per ricostituzione (25 e 50 ml) • Dosi 1200 mg/m 2/die per 3 -5 giorni ogni 21 o 5 g/m 2 in 24 ore • Per l’infusione raccomandata diluizione in SG 5%, SF o Ringer Lattato: 250 ml per infusione in 30 -60 minuti o -500 ml in 1 -2 ore; 3 litri per infusione in 24 (5 g/m 2) 16

Principali alchilanti: ifosfamide • Dopo ricostituzione del medicinale, non si devono superare le 24 ore di conservazione a temperature comprese tra 2 e 8 °C (in frigorifero). • Generalmente associato a MESNA (2 mercaptoetano-sodio-N-acetil-cisteina, Uromitexan® per prevenire tossicità urinaria da acroleina (metabolita): 20% della dose di Ifosfamide al tempo zero 20% a distanza di 4 e 8 ore (anche per os a dose doppia). Con infusioni di 24 ore dose al tempo 0 poi dose fino al 100% della dose di ifosfamide, in infusione congiunta 17

Altri alchilanti: indicazioni terapeutiche • Melphalan: mieloma multiplo (ma registrato anche per tumori ovarici, melanoma e sarcomi delle estremità) • Dacarbazina: Linfoma di Hodgkin e Melanoma • Fotemustina: nitrosuurea. Caratteristica liposolubilità. Melanoma, tumori cerebrali primitivi. • Streptozocina: carcinoidi e tumori endocrini del tubo digerente • Temozolamide: glioblastoma multiforme, da solo in combinazione con radioterapia • Estramustine: carcinoma prostatico • Chlorambucil e Bendamustina: linfomi e leucemie croniche linfatiche 18

Alchilanti: principali effetti tossici • Per meccanismo d’azione potenziale teratogeni e mutagenicancerogeni. • Rischio tossicità gonadica con sterilità ed amenorrea. • Tossicità ematologica con leucopenia e piastrinopenia: nadir a 7 -10 giorni, recupero entro 10 giorni circa. – mielo-tossicità ritardata e cumulativa: nitrosouree e melphalan. Rischio agranuolocitosi con chlorambucil • • Effetto immunosoppressore (Ciclofosfamide) Nausea, vomito, ed alopecia Mucosite Ciclofosfamide a dosi elevate e ifosfamide: rischio di cistite emorragica. 19
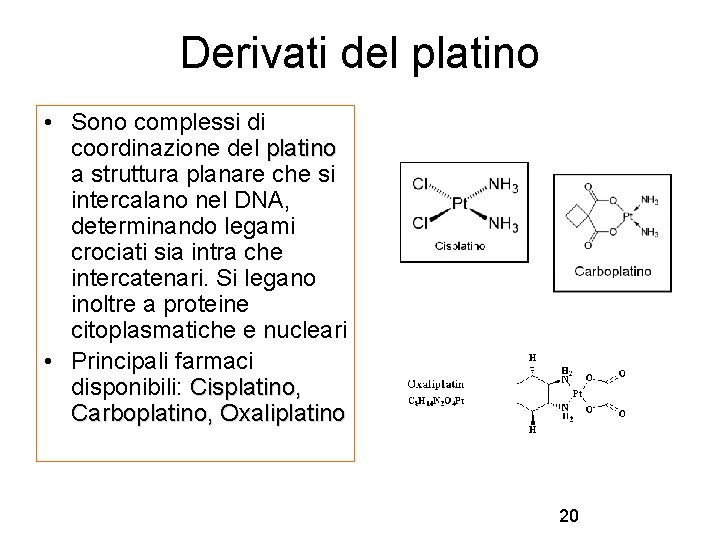
Derivati del platino • Sono complessi di coordinazione del platino a struttura planare che si intercalano nel DNA, determinando legami crociati sia intra che intercatenari. Si legano inoltre a proteine citoplasmatiche e nucleari • Principali farmaci disponibili: Cisplatino, Carboplatino, Oxaliplatino 20

Derivati del Platino: cisplatino • Ampie indicazioni di impiego: neoplasie polmonari, ovariche, endometrio, vescica, testa e collo, testicolo ecc. Effetto radiosensibilizzante • Dosi standard: 50 -75 mg/m 2/ev in 250 ml di SF ogni 3 -4 settimane • Richiede abbondante idratazione e diuretici osmotici (glicerolo, mannitolo) per prevenire al tossicità renale. 21

Derivati del platino • Carboplatino: Carboplatino ha uno spettro di attività simile al Cisplatino, ma presenta minor rischio di danno renale e richiede minor idratazione – Dosi usuali 4 -6 mg/m 2/min (AUC) in 250 ml SF ogni 3 -4 settimane • Oxaliplatino: Oxaliplatino indicato nei tumori del colonretto, stomaco, pancreas. – Dosi standard: 85 (135) mg/m 2 ogni 2 (3) settimane, infusione in glucosata al 5%. 22

Derivati del Platino: tossicità • Nausea e vomito sono preminenti con il Cisplatino, come pure il rischio di tossicità renale (insufficienza renale acuta) • Tossicità neurologica periferica, soprattutto per dosi elevate e trattamenti prolungate – Tipica la neurotossicità da oxaliplatino scatenata dal freddo • Tossicità ematologica – Più marcata con il Carboplatino che peraltro è meglio tollerato del cisplatino, con acufeni ed ipoacusia • Allergia, possibile con tutti i 3 farmaci 23

Antibiotici antitumorali • Si tratta di una classe eterogenea di farmaci provenienti da muffe e lieviti – Antracicline (Adriamicina, Epirubicina, Daunomicina, Idarubicina): • inducono danni al DNA attraverso produzione di radicali liberi, blocco Topoisomerasi, azione intercalante fra le catene di DNA. Non ciclo specifiche. – Antracenedioni (Mitoxantrone): meccanismo simile alle antracicline 24

Antibiotici antitumorali • Mitramicina ed Actinomicina D – agenti intercalanti il DNA, legano preferenzialmente guanina e citosina, con inibizione della sintesi di RNA messaggero • Mitomicina – Attivata metabolicamente si comporta come alchilante bifunzionale, ciclo specifico ((fasi G 1 -S) • Bleomicina – Induce rottura del DNA e ne impedisce la riparazione (inibizione DNA ligasi) 25

Antibiotici antitumorali: indicazioni • Daunorubicina ed idarubicina: leucemie acute • Adriamicina: impiegata generalmente alla dose di 6070 mg/m 2/3 settimane. (Epirubicina 100 -120/mg/m 2). – Ampio spettro d’azione: linfomi, sarcomi, carcinomi mammari, polmonari, tiroidei. • Actinomicina D: utilizzata nel trattamento del coriocarcinoma e tumori pediatrici • Mitomicina: neoplasie gastriche e della mammella • Bleomicina: in regimi polichemioterapici per linfomi, neoplasie del testicolo, spinocellulari genitali, della cute, e testa e collo. 26

Antibiotici antitumorali: tossicità • Tossicità ematologica con nadir dopo 10 -14 giorni (ma più tardivo per la mitomicina). Scarsa mielotossicità per la bleomicina • Nausea-vomito • Cardiotossicità: antracicline. Necessità esclusione cardiopatici e monitoraggio. – Precoce (Anomalie del ritmo ed ECG) – Tardiva e dose dipendente • Bleomicina: fibrosi polmonareinterstiziale dosedipendente (dose cumulativa max 200 mg/m 2), iperpigmentazione cutanea ed iperpiressia 27

Formulazioni di antracicline liposomiali • Prodotti con lo scopo di – Migliorare la distribuzione del farmaco – Modificarne la farmacocinetica – Ridurne la tossicità • Esempi: – Doxorubicina liposomiale pegilata (Caelix®) – Doxorubicina liposomiale non pegilata (Myocet®) – Daunorubicina liposomiale (Daunoxome®) 28

Antimetaboliti • Analoghi dell’Acido folico – Methotrexate – Raltritrexed – Pemetrexed • Analoghi delle Purine – 6 -mercaptopurina (6 MP) – 6 -Thioguanina (6 -TG) • Analoghi delle Pirimidine – – – – – 5 -Fluorouracile Capecitabina 5 -Fluorodesossiuridina UFT TS-1 TAS-102 Azacitidina Citosina arabinoside Fludarabina Gemcitabina 29

Antimetaboliti: meccanismi d’azione • Effetto antitumorale conseguente a somiglianza a metaboliti essenziali per la sintesi di molecole chiave per l’omeostasi cellulare (soprattutto DNA ed RNA) – Methotrexate (specifico per fase S): analogo dell’acido folico, blocca l’enzima Deidrofolato-reduttasi (DHFR). Blocco conversione acido deidrofolico in tetraidrofolico. • L’acido folinico è un antidoto – Raltitrexed inibisce la timidilico sintetasi (TS) – Pemetrexed: inibisce simultaneamente DHFR, TS, e glicil. ribonucleotiltransformilasi 30
Antimetaboliti: meccanismi d’azione • Gli analoghi delle Purine competono con adenina e guanina per la biosintesi degli acidi nucleici e possono provocare rotture dei filamenti. • Gli analoghi delle pirimidine vengono incorporate in DNA ed RNA interferendo con la loro sintesi – Il 5 -Fluorouracile, dopo trasformazione metabolica, inibisce la timidilico-sintetasi, azione potenziata dall’acido folinico (sfruttata in clinica come biomodulazione) – Altri derivati del fluorouracile sono stati prodotti con l’obiettivo di somministrazione orale o associazione con altre molecole per potenziarne l’efficacia • L’azacitidina è un farmaco che agisce inibendo la metil-trasferasi, enzima responsabile della metilazione del DNA 31

Antimetaboliti: indicazioni • Il Methotrexate è uno dei farmaci impiegati da più tempo in oncologia. – Ampie indicazioni: sarcoma dell’osso, carcinoma mammario, del testa e collo, leucemie acute linfoblastiche, Linfomi. – Somministrato per os, im, ev, ed anche per via intratecale ed intracavitaria – Dosi variabili da 20 -40 mg/m 2 ogni 1 -2 settimane ad oltre 3 g/m 2 (intermedie-alte, possono superare la barriera emato-encefalica e richiedono rescue con acido folinico) • Il Pemetrexed ha oggi indicazione nell’adenocarcinoma polmonare e nel mesotelioma: richiede somministrazione profilattica di vitamina B 12, acido folico e cortisonici. • I Raltitrexed nei tumori del colon e mesotelioma, ma è utilizzato più raramente. 32

Antimetaboliti: indicazioni • 6 -MP e 6 -TG oggi sono più raramente impiegati (patologie ematologiche) • Il 5 -Fluorouracile è ampiamente impiegato in molte neoplasie: mammarie, gastroenteriche, cutanee e del testa e collo, talora con biomodulazione con acido folinico – Infusione rapida – Infusione continua – Spesso sostituito da capecitabina o altre fluoropirimidine orali. • Citosina arabinoside e Azacitadina in combinazione nelle leucemie acute mieloidi, mielodisplasie e linfomi • Fludarabina: Fludarabina nei linfomi non Hodgkin a basso grado • Gemcitabina: Gemcitabina tumore del polmone, pancreas, mammella, vescica. 33

Antimetaboliti: tossicità • Il Methotrexate, Methotrexate eliminato per via renale, richiede controllo della funzione renale, idratazione e talora alcalinizzazione delle urine. Può indurre severe mucositi, diarrea, nausea/vomito e mielotossicità. • La Citosina arabinoside determina soprattutto una mielosoppressione, ma la tossicità può essere diversa con le alte dosi • Le Fluoropirimidine possono indurre soprattutto mucosite, diarrea, mielosoppressione, nausea e vomito, talora tossicità cutanea. • La Gemcitabina può indurre mielosoppressione, nausea, vomito, tossicità epatica, febbre, allergia. 34

Alcaloidi della vinca, taxani, eribulina: veleni del fuso: fase M specifici • Sono farmaci di origine naturale o semisintetica (oggi tutti prodotti per sintesi), ciclo specifici ed agiscono inibendo il funzionamento del fuso mitotico – Alcaloidi della vinca: vinca si legano alla subunità β della tubulina, determinano depolimerizzazione o destabilizzazione del fuso mitotico – Taxani: Taxani si legano alla tubulina determinandone la polimerizzazione, stabilizzando il fuso mitotico – Eribulina: lega la tubulina a livello di un sito diverso da taxani e alcaloidi della vinca e blocca la crescita e la polimerizzazione dei microtubuli e favorisce la formazione di aggregati tubulinici non funzionali. 35

Alcaloidi della vinca: indicazioni terapeutiche • Vincristina e vinblastina inizialmente estratti dalla Pervinca del Madagascar – Vindesina e vinorelbina derivati semisintetici della vinblastina • Vincristina: Vincristina Linfomi e leucemie linfoblastiche; tumori pediatrici. Dose convenzionale < 2 mg • Vinblastina: Vinblastina linfoma di Hodgkin, tumori germinali del testicolo, leucemie (citoriduzione) • Vinorelbina (disponibile anche in formulazione orale): carcinoma polmonare non a piccole cellule e mammario 36

Alcaloidi della vinca: tossicità • Sono farmaci scarsamente alopecizzanti, vescicanti, modicamente emetizzanti. – Vincristina: poco mielotossica, ma fortemente neurotossica. Neuropatia periferica sensitiva (parestesie e ipoestesia), autonomica con ileo paralitico, riduzione riflessi. – Vinblastina : più rilevante tossicità ematologica con leucopiastrinopenia. – Vinorelbina: più rilevante tossicità ematologica con leucopiastrinopenia. 37

Taxani: paclitaxel, docetaxel • Paclitaxel: originariamente estratto dalla corteccia del Taxus Brevifolia, albero della costa americana del Pacifico, (molecola molto idrofobica) • Docetaxel: semisintesi dagli aghi della Taxus baccata, arbusto europeo molto diffuso, molecola più idrosolubile. • Richiedono solventi diversi (soluzioni di olio di ricino ed etanolo e etanolo/acqua nel secondo caso) Taxus brevifolia e baccata – Nab-Paclitaxel prodotto nanotecnologico contenente paclitaxel coniugato ad albumina, più solubile, e in grado di raggiungere più selettivamente le cellule tumorali (proteina SPARC) 38 • Nuovi taxani o composti correlati ancora non commercializzati in Italia 38

Taxani: dosi e indicazioni • Taxolo (175 mg/m 2 ogni 3 settimane o 60 -100 mg settimanale: mammella, ovaio, polmone, ed altri. – Nab-Paclitaxel: 260 mg/m 2 ogni 21 gg nel tumore mammario; in associazione con gemcitabina 125 mg/m 2 , nei giorni 1, 8 e 15 di ciascun ciclo di 28 giorni pancreas 1° linea (via endovenosa nell’arco di 30 minuti), polmone 1° linea. • Docetaxel (70 -100 mg ogni 3 settimane 25 -30 mg/m 2 ogni settimana): mammella, prostata, stomaco, ovaio, polmone. • Effetti avversi: alopecia e distrofie ungueali, mielo-soppresione (più marcata con docetaxel), neurotossicità, ipersensibilità (più frequenti con il paclitaxel per il diverso solvente, oleoso – cremoforo – premedicazione corticosteroidea sempre necessaria, < rischio Nab-paclitaxel), modesto effetto emetizzante, ritenzione liquidi (docetaxel). 39

Eribulina (Eribulina mesylato) • Analogo sintetico dell’Halicondrina H – Origine da spugne marine, veleno del fuso. • Indicazioni: carcinoma mammario metastatico dopo 1 o più linee CHT, liposarcoma inoperabile o metastatico pretrattato con antracicline • Dose: 1, 23 mg/m 2, ev in 2 -5 minuti, giorni 1 e 8 ogni 21. – Riduzione dose se compromissione epatica – Infuso in 2 -5 min previa diluizione in SF (max 100 ml; NO Sol. glucosata) • Tossicità: mielosoppressione, neurotossicità, tossicità epatica 40

Inibitori delle topoisomerasi II: Epipodofillotossine (Etoposide e Teniposide): CSFS (G 2) • Derivati semisintetici estratti dalla mandragola, pianta simile alla borragine, ma velenosa – Tagli intracatenari del DNA x stabilizzazione complesso DNAtopoisomerasi II • Indicazioni: neoplasie polmone, prostata, sarcomi, linfomi (Teniposide ormai abbandonato) – Dose 50 -125 mg/m 2 • Tossicità: leucopenia, alopecia, modesto potere emetizzante. 41

Inibitori delle Topoisomerasi I: Topotecan e Irinotecan • Alcaloidi semisintetici, derivati dalla Campotheca Acuminata, pianta endemica in Cina – Inibitori della Topo-I enzima che determina tagli monocatenari del DNA • Indicazioni – Topotecan: microcitoma polmonare, carcinoma ovarico e della cervice uterina – Irinotecan: neoplasie colorettali e gastroenteriche • Tossicità: – Topotecan: soprattutto ematologica, alopecia – Irinotecan: elatologica, diarrea, sindrome colinergica ed effetti simpatico mimetici (atropina), nausea-vomito 42

Miscellanei: Trabectadina: (ET-743) • • Farmaco originato dall’ascidia, tunicato marino, oggi prodotto per sintesi. Meccanismo complesso: legame al solco minore del DNA, interferenza meccanismi riparazione DNA, modulazione della trascrizione, effetti sul microambiente tumorale Indicazioni: sarcomi dei tessuti molli dopo fallimento antracicline e Ifosfamide (1, 5 mg/m 2/infusione 24 ore ogni 21 gg), carcinoma dell’ovaio in recidiva platino sensibile (con Caelix (dopo) alla dose di 1, 1 mg/m 2 in 3 ore: dose iniziale velocità < 1 mg/minuto). – Dopo ricostituzione diluizione SF o SG-5%. Lavare sempre via venosa con SG 5% prima di infondere dopo il Caelix (rischio precipitazione Caelix nella via venosa) • Effetti collaterali: nausea/vomito, epatotossicità (corticosteroidi), tossicità ematologica, astenia, ipersensibilità, disfunzione cardiaca, rabdomiolisi (CPK), reazione locale (CVC) 43

Miscellanei: altri • Idrossiurea: inibitore della ribonucleotide-reduttasi (fase S). – Farmaco orale S. mieloproliferative croniche, anemie falciformi, altri tumori solidi • Procarbazina: inibisce la sintesi degli acidi nucelici, di proteine e determina metilazione aberrante del DNA – Farmaco orale linfoma di Hodgkin (MOPP) oggi poco usato • Mitotane: analogo del DDT, agisce selettivamente su cellule della corteccia del surrene – Tumori della corticale del surrene • Asparaginasi: enzima derivato da E-Coli, che inibisce la sintesi proteica (oggi disponibile da DNA ricombinante e PEGilata). – Leucemie linfoblastiche. Rischio allergie (anafilassi), alterazioni coagulative con trombosi, pancreatiti, iperglicemia. 44
Miscellanea: PARPi • Inibitori della Poli-ADP-Riboso Polimerasi, enzima che si lega a DNA danneggiato consntendone la riparazione – In tumori con deficit di BRCA -1 e 2 la riparazione del DNA è meno efficiente e l’impiego dei PARPi causa un danno irreversibile letalità sintetica BRCA: Breast Related Cancer Antigens: geni oncosoppressori, intervengono nel controllo del ciclo cellulare e codificano per la "proteina per la suscettibilità al carcinoma mammario (BRCA 1: cr 17 e BRCA 2: Cr. 13) • Olaparib e Iniparib – Tumori della mammella, dell’ovaio, ma potenzialmente pancreas e prostata in pz con mutazioni BRCA – Tossicità: soppressione ematologica, astenia, cefalea, inappetenza. 45

CHT: mono-CHT vs poli-CHT Monochemioterapia: 1 solo farmaco • Vantaggi – – Ridotti effetti collaterali Maggiore maneggevolezza Utilizzo di dosi piene Più adatta a situazioni di malattia avanzata (es tumore mammario) • Svantaggi – Potenziale minore efficacia – Aumentata possibilità resistenza Polichemioterapia: combinazioni di più farmaci • Vantaggi – Possibile maggiore efficacia – Maggiore controllo di cloni cellulari resistenti o eterogenei – Potenziali sinergie fra farmaci – Combinazione di farmaci con diverse tossicità – Combinazione con farmaci biologici con sinergie e talora effetti tossici • Svantaggi – – Maggiore tossicità Possibili interferenze farmacologiche Riduzione dosi singoli farmaci Ridotte opportunità in caso di ripresa malattia 46

Obiettivi delle terapie antitumorali • Intervento sulla sopravvivenza – Curativa: guarigione di una malattia altrimenti letale – Controllo della malattia con prolungamento della vita e miglioramento qualità di vita. • Terapia con intento palliativo – Controllo dei sintomi • Improponibile ricercare il solo effetto antalgico, ma controllo dolore spesso insufficiente, sintomi spesso multipli per alcuni dei quali non esistono rimedi sintomatici efficaci – Miglioramento della qualità di vita intesa come benessere fisico, psichico e sociale del paziente 47

Modalità di impiego della CHT • Primaria o neoadiuvante – Viene applicata prima di un trattamento locale (chirurgia, radioterapia) ad intento curativo. Può consentire la riduzione di volume e agevolare il trattamento successivo • Adiuvante – Viene somministrata dopo il trattamento locale con l’intento di eliminare eventuali micrometastasi e aumentare le possibilità di cura • Chemioterapia della fase avanzata – Con intento curativo: neoplasie altamente chemiosensibili – Con intento palliativo: neoplasie a minor chemiosensibilità 48

Fattori influenzanti la risposta alla terapia • • Sede del tumore Dimensione tumorale e tumor-burden Velocità di crescita (attività proliferativa) Caratteristiche di resistenza: intrinseca o acquisita. Coinvolta multidrug resistance (MDR): biotrasportatori o pompe di efflusso per i farmaci. • Caratteristiche molecolari (es. recettori ormonali nel carcinoma mammario) • Adeguata irrorazione del tumore. • Caratteristiche paziente: performance, età, precedenti terapie 49
La decisione di intraprendere la CHT • Chemio-sensibilità del tumore • Trattamento precedenti • Performance status del paziente • Età e comorbidità • Desiderio / compliance del paziente e dei familiari 50
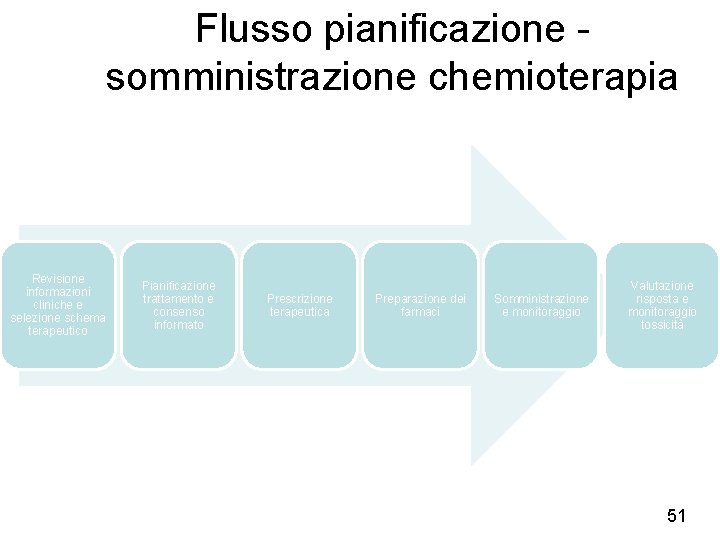
Flusso pianificazione somministrazione chemioterapia Revisione informazioni cliniche e selezione schema terapeutico Pianificazione trattamento e consenso informato Prescrizione terapeutica Preparazione dei farmaci Somministrazione e monitoraggio Valutazione risposta e monitoraggio tossicità 51

Chemioterapia: fattori critici • • • Farmaco giusto Dose congrua Corretta preparazione e diluizione Paziente giusto: identificazione! Condizioni clinico-laboratoristiche adeguate • Lo schema terapeutico • Modalità di somministrazione appropriata – Via di somministrazione – Tempi di infusione – Sequenza dei farmaci • Adeguata terapia di supporto • Adeguato follow-up successivo 52

Chemioterapia: la dose • Il calcolo della dose – In base al peso – In base alla superficie corporea – In base alla clearance della creatinina (AUC) • Dosi – Standard: dosi usuali somministrate alla maggior parte dei pazienti. – Alte: richiedono supporto di fattori di crescita e/o cellule staminali emopoietiche – Ridotte: in base a precedente tossicità, alterazioni funzionalità epatica o renale, alterazioni metaboliche individuali (farmacogenomica), performance status scaduto 53

Le via di somministrazione della CHT • • Orale Sottocutanea o intramuscolare Topica Endovena – Periferica – Centrale: mid-line, PICC-line, Port a cath • Chemioterapia regionale in specifiche sedi: – Intra-arteriosa: es arteria epatica, perfusione arti. – Intratecale: rachicentesi medicate, Ommaha reservoir. – Intracavitaria (intrapleurica, intraperitoneale, intrapericardica, intravescicale) 54

Somministrazione orale della CHT • Orale: facilità di somministrazione e disponibilità crescente di farmaci orali – Chemioterapici: ciclofosfamide, capecitabina, clorambucil, melphalan, vinorelbina, idarubicina – Nuovi farmaci target. • Inconsistenza dell’assorbimento, interferenza con il cibo o altri farmaci • Problemi di aderenza non sempre controllabile • Necessità di istruire paziente e caregiver su come maneggiare i farmaci al domicilio (uso di guanti) 55

Somministrazione della CHT: via endovenosa • E’ la più comune via di somministrazione della chemioterapia. Assorbimento è certo • Consente la somministrazione in sequenza di farmaci ancillari e chemioterapici, con velocità dipendente dal tipo di farmaco e idratazioni se necessarie • Adatta alla somministrazione di farmaci irritanti e vescicanti con precauzioni apposite. Può determinare flebite e sclerosi delle vene nel tempo: richiede spesso inserimento di cateteri venosi centrali • Push, infusioni brevi, infusioni continue, modalità combinate. 56

Somministrazione sottocute o im della chemioterapia • • Facilità di somministrazione Richiede massa muscolare adeguata Assorbimento variabile Non applicabile per alcuni farmaci irritanti o vscicanti • Rischio di infezione o sanguinamento • Nel complesso impiegata raramente: Citosina arabinoside, Methotrexate • Disponibili formulazioni sottocutanee di farmaci biologici: (Trastuzumab, Rituximab). • Vantaggio di breve durata di somministrazione e limitato impegno del DH 57

Somministrazione della CHT: via intra-arteriosa • Consente di far giungere dosi elevate di farmaci direttamente alle sedi tumorali con ridotta esposizione sistemica al farmaco stesso • Richiede spesso procedure chirurgiche per l’inserimento di speciali cateteri (es in arteria epatica per neoplasie o metastasi epatiche) 58
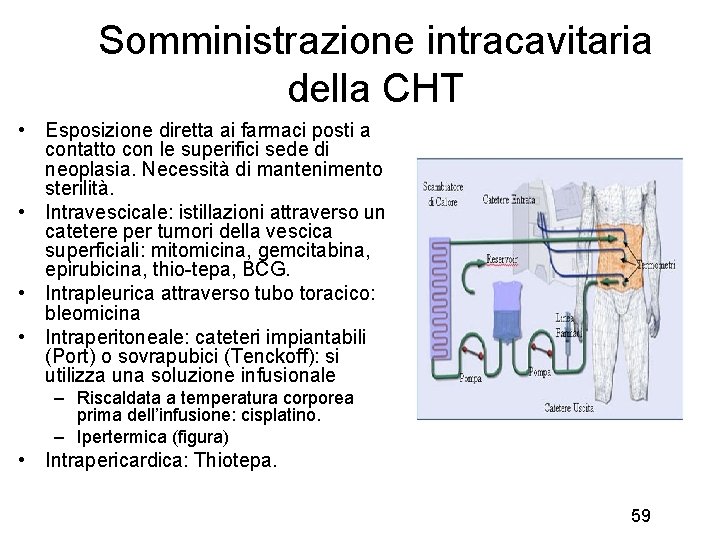
Somministrazione intracavitaria della CHT • Esposizione diretta ai farmaci posti a contatto con le superifici sede di neoplasia. Necessità di mantenimento sterilità. • Intravescicale: istillazioni attraverso un catetere per tumori della vescica superficiali: mitomicina, gemcitabina, epirubicina, thio-tepa, BCG. • Intrapleurica attraverso tubo toracico: bleomicina • Intraperitoneale: cateteri impiantabili (Port) o sovrapubici (Tenckoff): si utilizza una soluzione infusionale – Riscaldata a temperatura corporea prima dell’infusione: cisplatino. – Ipertermica (figura) • Intrapericardica: Thiotepa. 59

Meningosi neoplastica • Localizzazione neoplastica metastatica alle meningi • Complicanza che si verifica nel 3 -5% delle neoplasie (in particolare leucemie, linfomi, neoplasie mammarie), caratterizzata da segni neurologici multifocali, cefalea e vari sintomi neurologici. Possibilità di ostruzione alla circolazione del liquor • Diagnosi non sempre agevole: – RMN dell’encefalo e spinale – Esame citologico del liquido cerebrospinale ottenuto con rachicentesi • Trattamento: – Terapia intratecale – Chemioterapia sistemica con farmaci ad alte dosi (Methotrexate, ARA-C) – Radioterapia: in particolare su sedi di ostacolo alla circolazione liquorale 60
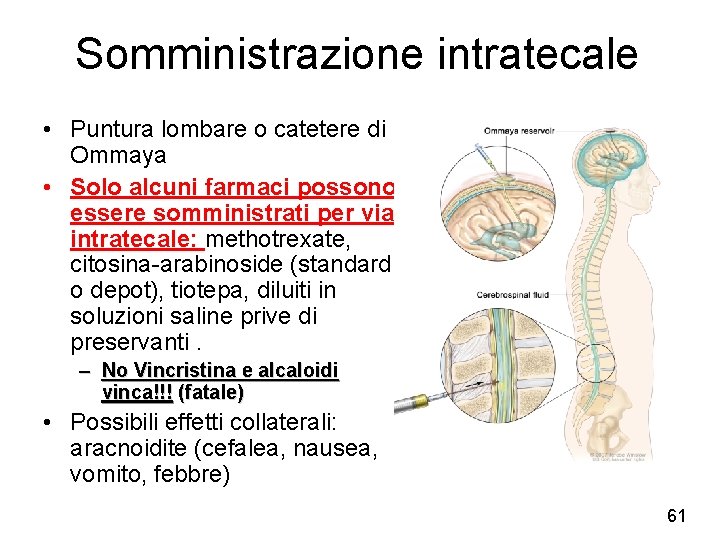
Somministrazione intratecale • Puntura lombare o catetere di Ommaya • Solo alcuni farmaci possono essere somministrati per via intratecale: methotrexate, citosina-arabinoside (standard o depot), tiotepa, diluiti in soluzioni saline prive di preservanti. – No Vincristina e alcaloidi vinca!!! (fatale) • Possibili effetti collaterali: aracnoidite (cefalea, nausea, vomito, febbre) 61

Speciali attenzioni per le terapie intratecali • Preparare solo insieme ad altri farmaci da iniettare per via intratecale (non con altri farmaci da iniettare attraverso altre vie di somministrazione) • Una volta preparati conservare in contenitore isolato con un etichettatura evidente che indichi l’utilizzo intratecale • Somministrare al paziente solo con altri farmaci intesi per somministrazione intratecale 62
Modalità infusione chemioterapici • Poco utilizzate infusioni troppo rapide (bolo) • Infusioni brevi • Infusioni prolungate per alcuni farmaci o continue di alcuni giorni • Seguire l’ordine prestabilito dei farmaci, in genere non miscelare, eseguire (con fisiologica o talora glucosata) fra un farmaco e l’altro 63

Le opzioni terapeutiche disponibili • Regimi chemioterapici a somministrazione diurna in DH – Eventuale impiego di pompe infusionali per la somministrazione continua, anche domiciliare – Le chemioterapie orali • Regimi chemioterapici complessi che richiedono l’ospedalizzazione 64

Prima della prescrizione di un nuovo programma chemioterapico • Verifica della diagnosi istopatologica: referto del Patologo • Definizione dello stadio clinico • Storia clinica completa ed esame fisico – Peso, altezza, superficie corporea – Storia di allergie – Funzione d’organo • Valutazione laboratoristica – Emocromo » Neutrofili > 1500/mmc » Piastrine > 100. 000/mmc – Funzionalità renale – Funzionalità epatica e bilirubina • ECG (+ ecocardiogramma per alcuni farmaci) 65

Il programma Chemioterapico • Definire chiaramente: – Scopo della terapia e durata • Produrre un programma di chemioterapia indicante – Scopo terapia – Durata – Schema: farmaci e loro dosi, vie di somministrazione (e dosi cumulative da non superare) – Terapie di supporto – Programma di rivalutazione e monitoraggio del trattamento • Informare il paziente e verificare la comprensione: diagnosi, significato terapia, effetti collaterali previsti. Consenso informato datato e firmato • Verificare la necessità di un supporto psicosociale 66

Le prescrizioni chemioterapiche • Devono essere sempre scritte, datate, firmate da un oncologo/ematologo con esperienza nella terapia antitumorale – mai accettare ordini orali, in particolare per la chemioterapia antitumorale • I farmaci chemioterapici orali o parenterali devono essere preparati da un farmacista, tecnico di farmacia o infermiere con adeguato training • La somministrazione deve essere effettuata da medici o infermieri qualificati • Mantenimento di competenza nel tempo e BLS 67

Prescrizioni chemioterapia • Schemioterapici pre-stampati o computerizzati • Nome e cognome del paziente ed altri elementi utili all’identificazione • Data e N° del ciclo • Farmaci, dosaggi, via di somministrazione, volume e velocità di infusione. • Chiara definizione della sequenza dei farmaci citostatici, e collaterali (premedicazioni: anti-istaminici, cortisonici, antiemetici, idratazione se necessaria) • Prima della somministrazione adeguata identificazione del paziente e valutazione infermieristica del pz. 68

Valutazione infermieristica per la somministrazione di CHT • Stato delle vene • Stato del cavo orale • Stato dell’apparato gastro-intestinale: persistenza di diarrea o incompleta canalizzazione • Stato ematologico • Prescrizione e verifica dell’assunzione di eventuali premedicazioni • Aspetti psico-sociali • Necessità educazionali.

Pratica di manipolazione sicura degli antiblastici • Diluizione, e allestimento in unità attrezzate di preparazione antiblastici. • Uso di dispositivi di protezione individuale: abiti, guanti, visiera, ecc. • Contenitori approvati per lo smaltimento • Kit per gli spandimenti disponibile.

Linee guida per il paziente e caregiver • Per 48 ore dopo la chemioterapia: – Risciacquare il water 2 volte dopo l’uso – Risciacquare il water con la candeggina una volta al giorno – Il Caregiver dovrebbe utilizzare guanti quando viene a contatto con qualsiasi liquido biologico. • Utilizzare un preservativo in caso di attività sessuale

Linee guida per il paziente e caregiver • Fra le sessioni di chemioterapia – Controllo dell’emocromo – NADIR (punto più basso della conta dei granulociti neutrofili) – Informazione sugli effetti collaterali attesi e sul loro timing – Indicare ciò che è importante riportare – Terapie domiciliari: antiemetici, antidiarroici, collutori, ecc.

Principali effetti collaterali della CHT • • • • Nausea/vomito Cute e annessi: alopecia, alterazioni ungueali, hand-foot syndrome Anoressia Gastro-intestinale: mucosite e diarrea Mielodepressione Azospermia, amenorrea Neurotossicità Astenia Nefrotossicità Epatotossicità Cardiotossicità Allergie Febbre Effetti da stravaso • Come li misuriamo e valutiamo? 73

Alopecia da chemioterapia: CIA • Effetto collaterale comune della CHT stimata globalmente intorno al 65% dei casi, con prevalenza e severità variabile • Pochi effetti collaterali generano tanta trepidazione come l’improvvisa e sostanziale caduta dei capelli – – Impatto psicologico potenzialmente importante Possibile causa di rifiuto del trattamento Strategie per management ancora insoddisfacenti Meccanismi patobiologici complessi Paus R, et al. Lancet Oncol 2013; 14: 50

Variabilità dell’entità dell’alopecia per farmaci alopecizzanti • Farmaco, dose, durata, regime chemioterapico con più farmaci, protocollo di chemioterapia (curativo vs regimi frazionati palliativi), presenza di Gv. HD in pazienti sottoposti a trapianto allogenico di midollo, radioterapia • Età, comorbidità, stato nutrizionale e ormonale, altri fattori individuali. • Presenza e progressione di alopecia androgenica Paus R, et al. Lancet Oncol 2013; 14: 50. (#1288. pdf), Shin H, et al. Int J Cancer 2015; 136(5): E 442 (1302. pdf#)
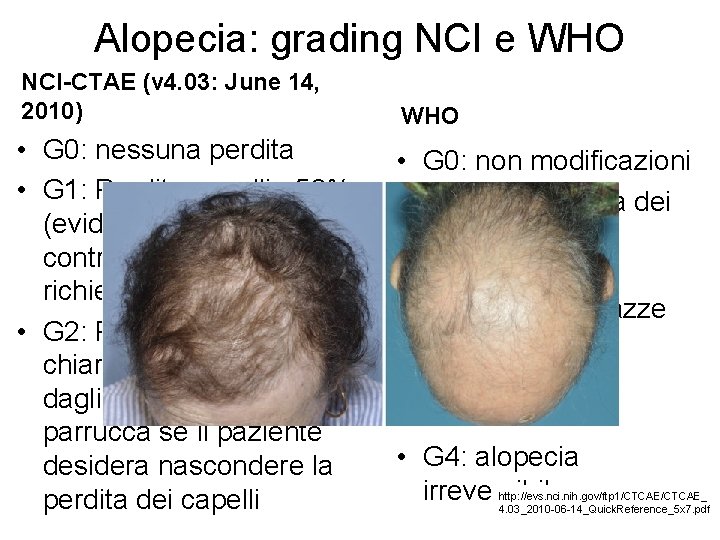
Alopecia: grading NCI e WHO NCI-CTAE (v 4. 03: June 14, 2010) WHO • G 0: nessuna perdita • G 1: Perdita capelli <50% (evidente solo controllo ravvicinato), non richiede parrucca. • G 2: Perdita ≥ 50%, chiaramente riconoscibile dagli altri e richiede una parrucca se il paziente desidera nascondere la perdita dei capelli • G 0: non modificazioni • G 1: lieve perdita dei capelli • G 2: alopecia moderata a chiazze • G 3: alopecia completa, ma reversibile • G 4: alopecia irreversibile http: //evs. nci. nih. gov/ftp 1/CTCAE_ 4. 03_2010 -06 -14_Quick. Reference_5 x 7. pdf
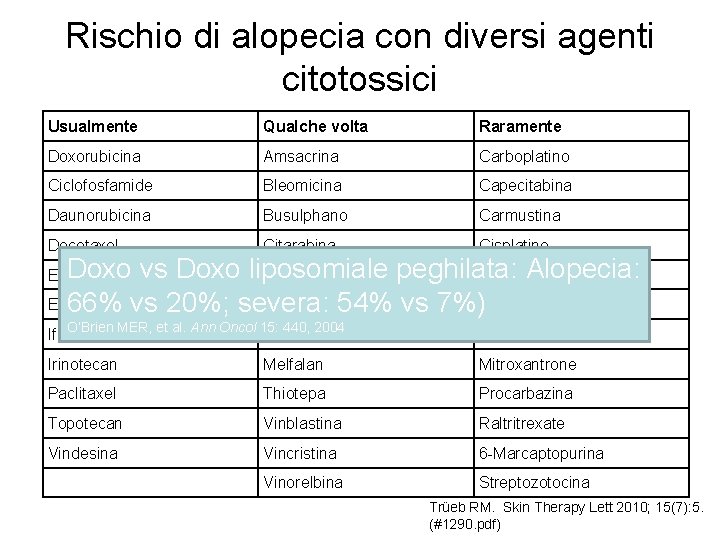
Rischio di alopecia con diversi agenti citotossici Usualmente Qualche volta Raramente Doxorubicina Amsacrina Carboplatino Ciclofosfamide Bleomicina Capecitabina Daunorubicina Busulphano Carmustina Docetaxel Citarabina Cisplatino Doxo vs Doxo liposomiale peghilata: Alopecia: 5 -Fluorouracile Fludarabina Etoposide Gemcitabina 66% vs 20%; severa: 54% vs 7%)Metotrexate Epirubicina O’Brien MER, et al. Ann Oncol 15: 440, 2004 Ifosfamide Lomustina Mitomicina C Irinotecan Melfalan Mitroxantrone Paclitaxel Thiotepa Procarbazina Topotecan Vinblastina Raltritrexate Vindesina Vincristina 6 -Marcaptopurina Vinorelbina Streptozotocina Trüeb RM. Skin Therapy Lett 2010; 15(7): 5. (#1290. pdf)
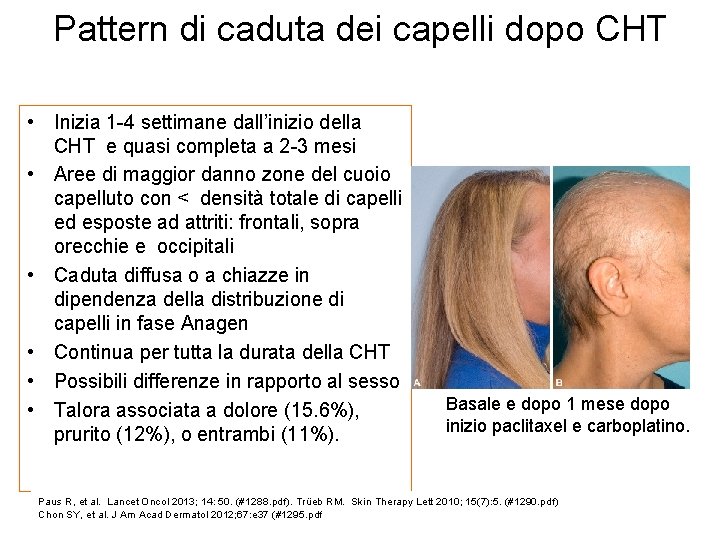
Pattern di caduta dei capelli dopo CHT • Inizia 1 -4 settimane dall’inizio della CHT e quasi completa a 2 -3 mesi • Aree di maggior danno zone del cuoio capelluto con < densità totale di capelli ed esposte ad attriti: frontali, sopra orecchie e occipitali • Caduta diffusa o a chiazze in dipendenza della distribuzione di capelli in fase Anagen • Continua per tutta la durata della CHT • Possibili differenze in rapporto al sesso • Talora associata a dolore (15. 6%), prurito (12%), o entrambi (11%). Basale e dopo 1 mese dopo inizio paclitaxel e carboplatino. Paus R, et al. Lancet Oncol 2013; 14: 50. (#1288. pdf). Trüeb RM. Skin Therapy Lett 2010; 15(7): 5. (#1290. pdf) Chon SY, et al. J Am Acad Dermatol 2012; 67: e 37 (#1295. pdf

Scalp-cooling • Prevalentemente utilizzata in Europa occidentale Il raffreddamento dello scalpo viene generalmente applicato continuamente iniziando 30’ prima e fino a 90’ dopo la fine dell’infusione • Temperatura circa 22°C (range 12 -25 C) • Molti studi (52 dal 1973 al 2003), ma di bassa qualità (solo 7 randomizzati: in 6 con un significativo vantaggio, più evidenti in pz trattati con antracicline o taxani) – Prevenzione alopecia severa in circa il 50%

Meccanismi di azione dei dispositivi di «scalp-cooling» • Vasocostrizione con ridotto flusso ematico ai follicoli piliferi durante l’infusione della CHT con ridotto «uptake» agenti citotossici da parte dei follicoli piliferi • Rallentamento dell’attività biochimica a livello dei follicoli, con minor possibilità di danno biologico da parte dei citotossici
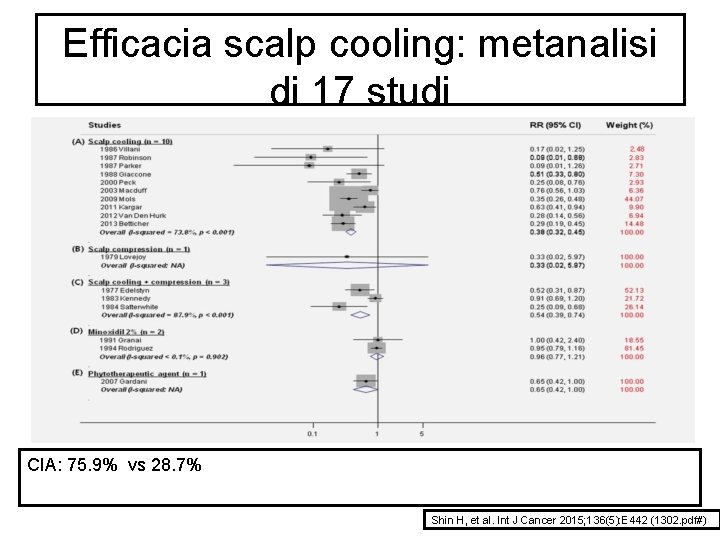
Efficacia scalp cooling: metanalisi di 17 studi CIA: 75. 9% vs 28. 7% Shin H, et al. Int J Cancer 2015; 136(5): E 442 (1302. pdf#)

Sicurezza e tollerabilità dello scalp cooling • Intolleranza al freddo , cefalea o dolore frontale, cervicalgie, capogiri o sensazione di testa vuota – AE: 4 -33% – Eventi non seri e transitori, ma causa di abbandono procedura per molti pz • Controindicazioni: – Orticaria da freddo: reazione allergica all’esposizione al freddo con comparsa di ecchimosi e rischio ipotetico di anafilassi – Malattia da crioagglutinine, crioglobulinemia, criofibrinogenemia, Malattia di Raynaud – Alcune neoplasie: leucemie, mieloma multiplo, linfomi, melanoma. Trüeb RM. Skin Therapy Lett 2010; 15(7): 5. (#1290. pdf), Shin H, et al. Int J Cancer 2015; 136(5): E 442 (1302. pdf#)
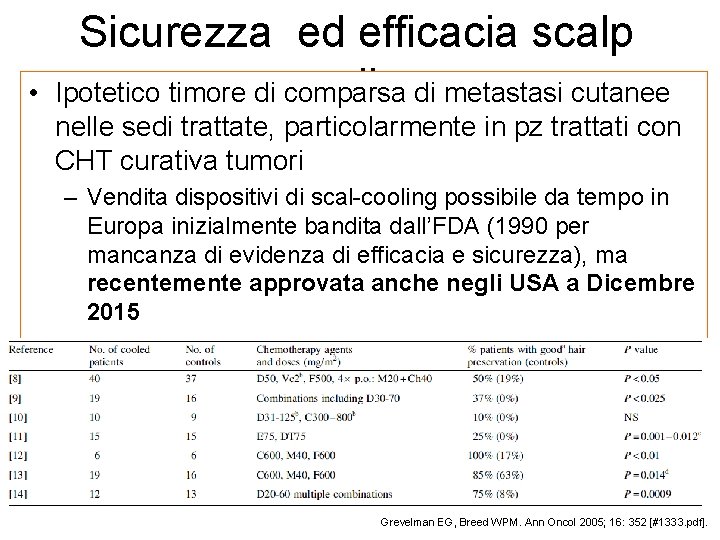
• Sicurezza ed efficacia scalp coolingdi metastasi cutanee Ipotetico timore di comparsa nelle sedi trattate, particolarmente in pz trattati con CHT curativa tumori – Vendita dispositivi di scal-cooling possibile da tempo in Europa inizialmente bandita dall’FDA (1990 per mancanza di evidenza di efficacia e sicurezza), ma recentemente approvata anche negli USA a Dicembre 2015 • Revisione sistematica di Grevelman (Ann Oncol 2005 • 56 studi: circa 2, 500 pz (1973 -2003) • Metastasi al cuoio capelluto: 0. 36% (follow-up 2 -63 mesi) Grevelman EG, Breed WPM. Ann Oncol 2005; 16: 352 [#1333. pdf].

Metastasi cutanee in pz con neoplasia mammaria • Incidenza variabile negli studi cliniciautoptici • Per la maggior parte rilevata a livello del tronco e vicino alla cicatrice chirurgica • Rare le metastasi a livello del cuoio capelluto van den Hurk CJG, et al. The Breast 2013; 22: 1001 (#1392. pdf)
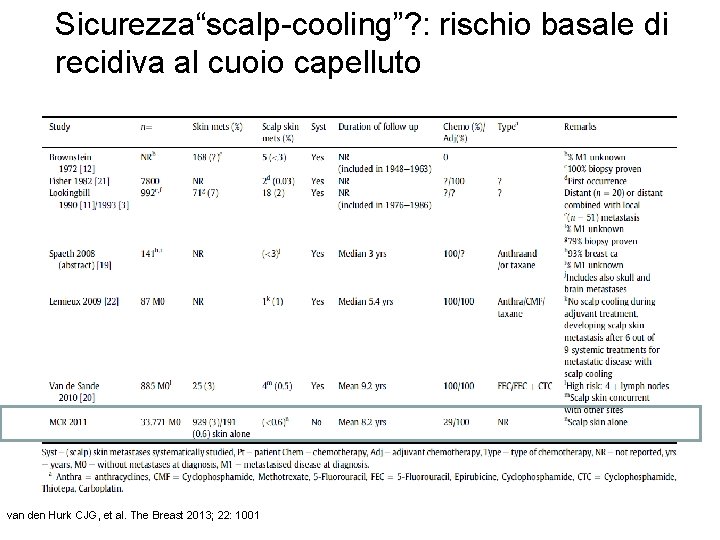
Sicurezza“scalp-cooling”? : rischio basale di recidiva al cuoio capelluto van den Hurk CJG, et al. The Breast 2013; 22: 1001

Sicurezza: rischio recidiva cuoio capelluto dopo “scalp-cooling” * # * Con o senza # FU attivo van den Hurk CJG, et al. The Breast 2013; 22: 1001
![Lemieux J, et al Breast Cancer Res Treat (2015) 149: 263 [#1310. pdf] Lemieux J, et al Breast Cancer Res Treat (2015) 149: 263 [#1310. pdf]](http://slidetodoc.com/presentation_image/31be5f67efc14a96a7257ad246e7330a/image-87.jpg)
Lemieux J, et al Breast Cancer Res Treat (2015) 149: 263 [#1310. pdf]

Fattori influenzanti l’efficacia dello scalp cooling • • Età giovane, sesso maschile, tipo di capello Caucasico. Spessore dello strato di capelli: correla con la temperatura cute Farmaci e dosaggi Temperatura sottocutanea: < 22°C (corrispondente ad una temperatura epicutanea < 19°C) – Assicurare un buon contatto cuffia refrigerante-scalpo – Umidificazione dei capelli può migliorare i risultati • Durata dello scalp-cooling – Preinfusion cooling time : 45’ ottimale se cuffia non pre-raffreddata – Post-infusion cooling time: durata ottimale più incerta (15’-4 h) • Dispositivi diversi: pochi dati da studi comparativi Komen MMC et al. The Oncologist 2013; 18: 885. [#1331. pdf]

Penguin cold caps, Paxman, Dignicap, Chemocoldcaps ecc. https: //penguincoldcaps. com/ , http: //www. paxman-coolers. co. uk/, http: //www. dignicap. com/ http: //www. chemocoldcaps. com/index. ht

Pro e contro diversi dispositivi • Ice cap, gel cap, “Cold Cap”: – devono essere cambiate parecchie volte durante una sessione (nursing time!) – possono essere pesanti – hanno una durata relativamente limitata – Non limitiano la mobilità del pz – Requisiti tecnici e costi limitati (è sufficiente in freezer). Betticher DC, et al. Support Care Cancer (2013) 21: 2565. [#1312. pdf]

Pro e contro diversi dispositivi • I dispositivi come Paxman e Dignicap sono provvisti di un sistema di refrigerazione connesso a cuffie leggere di silicone. • Temperatura del cuoio capelluto mantenuta a temperatura di circa 18°C grazie a refrigerante fatto circolare a -4°C entro le cuffie • Alcuni dispositivi consentono una regolazione a feed-back della temperatura sulla base di misurazione diretta della T dello scalpo Betticher DC, et al. Support Care Cancer (2013) 21: 2565. [#1312. pdf]
Tossicità gastroenterica • Nausea e vomito • Alterazione della mucosa orale e gastrointestinale per effetto antiproliferativo dei farmaci ed eventuale sovrapposizione infettiva – Mucosite – Diarrea • Tossicità epatica 92

Nausea e vomito da chemioterapia • Sono effetti collaterali molto disturbanti • Importante impatto – Capacità di alimentarsi e assumere liquidi, con possibilità di idratazione. Possono aggiungersi ad una preesistente inappetenza e nausea correlata alla malattia – Qualità di vita – Vita di relazione 93
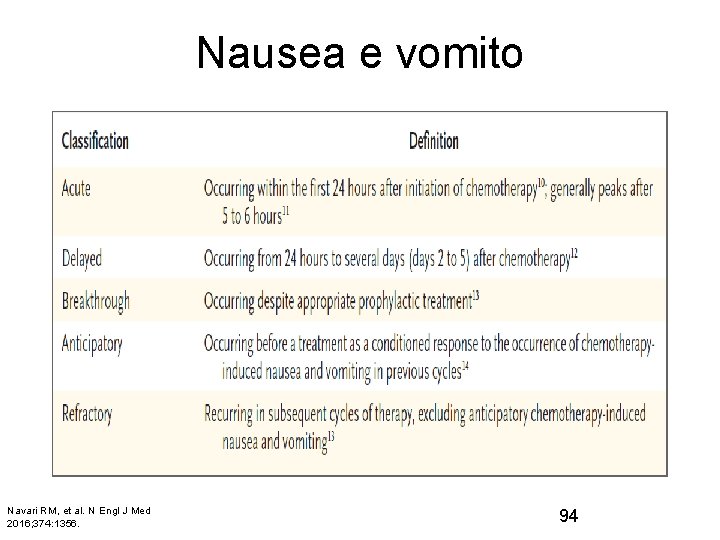
Nausea e vomito Navari RM, et al. N Engl J Med 2016; 374: 1356. 94

95
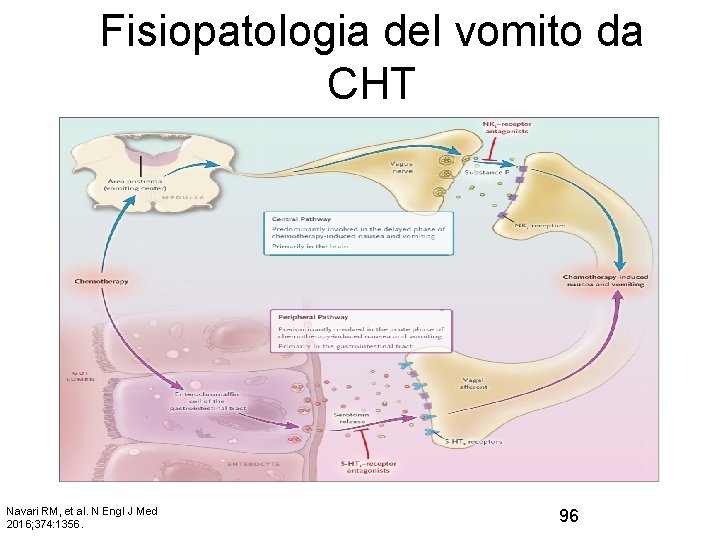
Fisiopatologia del vomito da CHT Navari RM, et al. N Engl J Med 2016; 374: 1356. 96

Vomito e nausea: determinanti principali • Chemioterapia – – Potenziale emetizzante dei farmaci impiegati Dose Schedula somministrazione Via di somministrazione • Paziente – – Età (giovane) Sesso (femminile >) Uso di alcool Controllo dell’emesi nei cicli precedenti • Antiemetici impiegati – Farmaci, dose, schedula, combinazioni, ecc. 97

Potenziale emetizzante dei farmaci Hesketh PJ. N Engl J Med 2008; 358: 2482. 98

99

Potenziale emetizzante dei farmaci a somministrazione orale 100
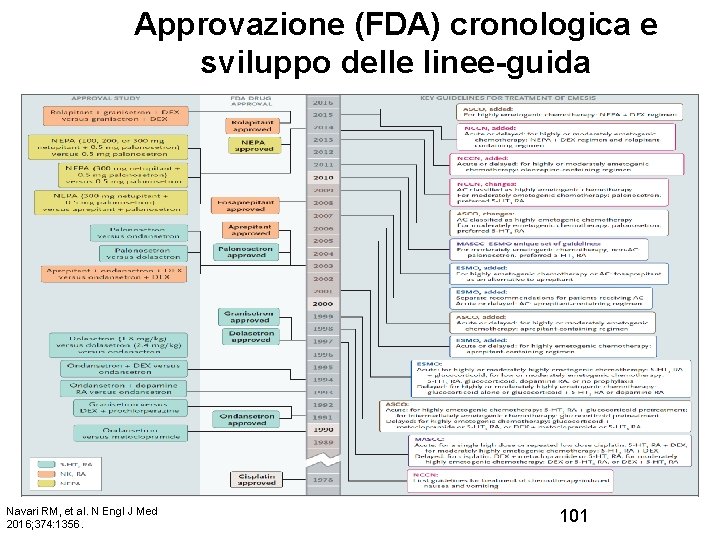
Approvazione (FDA) cronologica e sviluppo delle linee-guida Navari RM, et al. N Engl J Med 2016; 374: 1356. 101

I farmaci antiemetici in rapporto alla previsione di entità dell’emesi e della fase Navari RM, et al. N Engl J Med 2016; 374: 1356. 102

Rappresenta il più serio effetto della mielosoppressione indotta dai chemioterapici a causa del suo rischio di mortalità connesso alla Neutropenia febbrile, infezioni e sepsi. Nonostante lo sviluppo dei fattori di crescita grannulocitari circa 15 anni fa abbia significativamente cambiato la possibilità dell’oncologo di prevenire la neutropenia, ci sono stati meno risultati nel management della neutropenia febbrile. Questa rimane un’emergenza oncologica che richiede una stretta osservazione e spesso l’ospedalizzazione con somministrazione di antibiotici per via ev. NEUTROPENIA 103

Neutropenia • Riduzione dei globuli bianchi generalmente con nadir dopo 7 -14 giorni (più tardivo per nitrosouree, melphalan e mitomicina). • Il rischio è variabile con i diversi farmaci e aumenta con la dose e trattamenti precedenti • Recupero generalmente entro 8 -10 giorni • Può ritardare le terapie successive • Può comportare rischio infettivo • Management: controllo emocromo, temperatura, profilassi e terapia antibiotica, impiego oculato fattori di crescita granulocitari, esami colturali in caso di febbre ed infezioni 104

Perché CHT = fattore rischio x infezioni? • Neutropenia • Danno alle barriere anatomiche: mucose • Impiego di CVC • Profilassi e terapia antibiotica • Colonizzazione intestinale e cutanea da germi nosocomiali e funghi • Linfocitopenia e deficit immunitario • Malattia neoplastica. 105
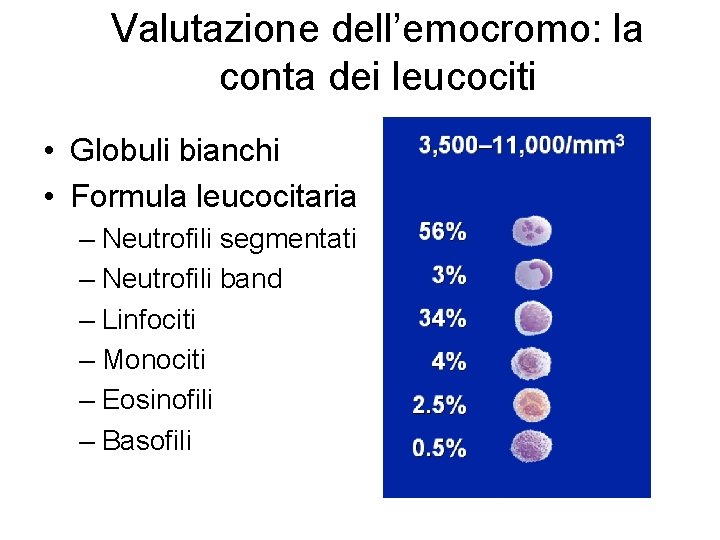
Valutazione dell’emocromo: la conta dei leucociti • Globuli bianchi • Formula leucocitaria – Neutrofili segmentati – Neutrofili band – Linfociti – Monociti – Eosinofili – Basofili
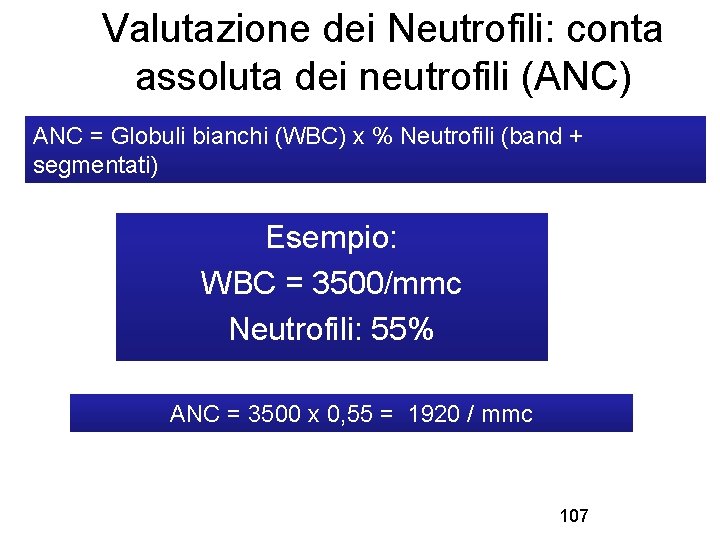
Valutazione dei Neutrofili: conta assoluta dei neutrofili (ANC) ANC = Globuli bianchi (WBC) x % Neutrofili (band + segmentati) Esempio: WBC = 3500/mmc Neutrofili: 55% ANC = 3500 x 0, 55 = 1920 / mmc 107
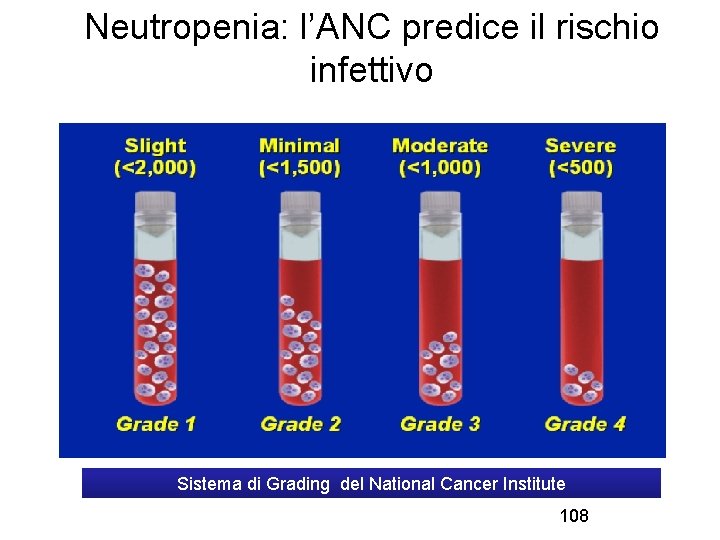
Neutropenia: l’ANC predice il rischio infettivo Sistema di Grading del National Cancer Institute 108

Rilevare segni di infezione nel paziente in chemioterapia • La neutropenia è una alterazione ematologica spesso silente • L’unico segno di infezione può essere la comparsa di FEBBRE – Controlla la temperatura ogni 4 -6 ore (pz ricoverati) – Istruisci il paziente a controllare la temperatura a casa (es ogni 6 -12 ore) – Istruisci il paziente a riportare la cmparsa di febbre, soprattutto se > 38°C

Definizione neutropenia febbrile • T ascellare 38. 5°C • T ascellare 38°C per più di 1 h o in 2 determinazioni entro 12 h 110

Neutropenia e rischio infettivo standard alto Neutropenia > 500/ mm 3, <7 gg <100/mm 3, >gg Mucosite non severa Malattia Emopatie tranne LA Leucemia acuta Trattamento convenzionale Sovramassimale 111
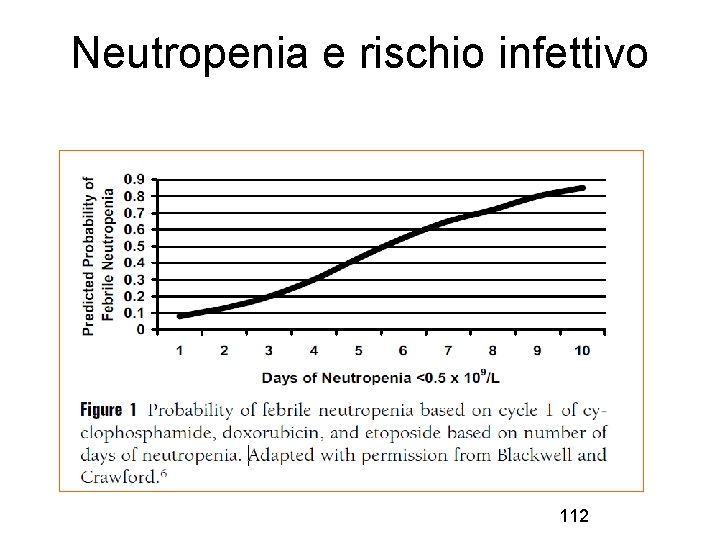
Neutropenia e rischio infettivo 112
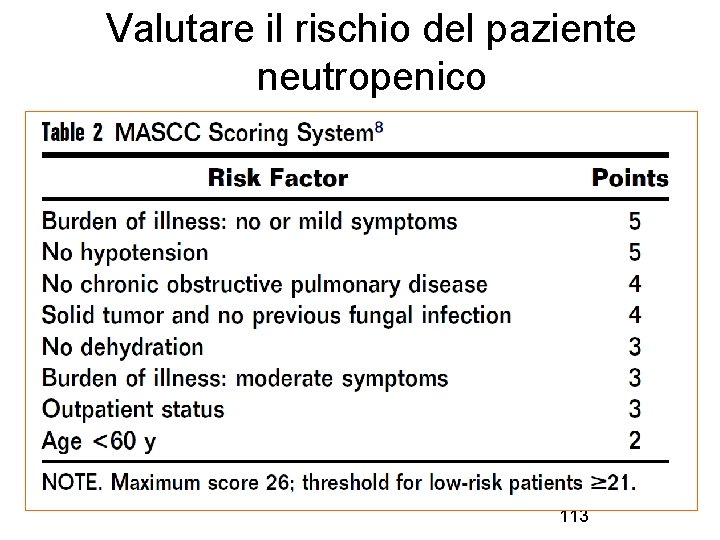
Valutare il rischio del paziente neutropenico 113
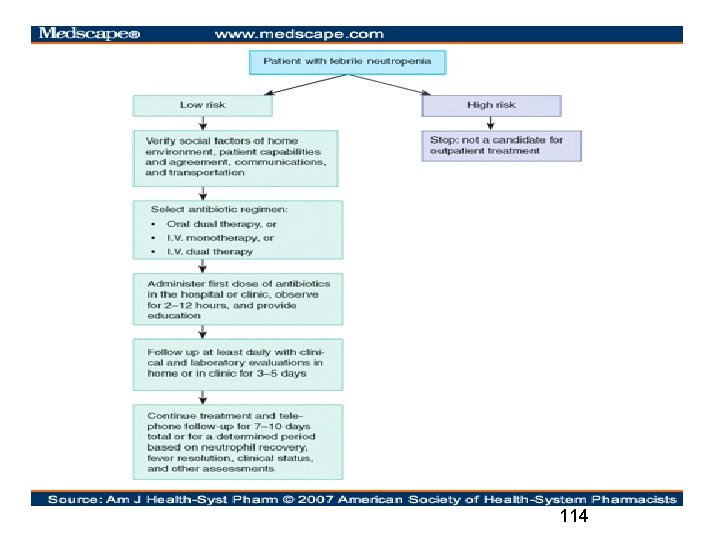
114

Impiego profilattico dei fattori di crescita granulocitari 115

Siti ad alto rischio di infezione Polmone orofaringe esofago tratto gastrointestinale CVC SNC seni paranasali regione perineale e pararettale 116

Shock settico: complicanza temibile Sintomi premonitori • • • Febbre con brivido Nausea/vomito Ipotensione Tachipnea Tachicardia Oliguria Sintomi conclamati • Grave ipotensione (PA < 90 mm. Hg) • Obnubilamento del sensorio • Tachipnea • Tachicardia • Ipotermia • Cianosi • Anuria 117

Prevenzione delle infezioni • Pz. Ricoverati o a domicilio – – Frequente igiene delle mani Doccia giornaliera Frequente cura della bocca Adeguata igiene regione perineale. – Igiene dei visitatori e operatori (mani!) – Deambulazione – movimento – Profilassi riattivazione di virus epatite B in pz HBs. Ag positivi. 118

Prevenzione delle infezioni • Pz ricoverati: – dieta a bassa carica microbica e isolamento in camere a bassa carica microbica in caso di neutropenia protratta (leucemie e trapianti) Profilassi antibiotica e con fattori di crescita granulocitari – Profilassi antivirale (anti CMV, Herpes) , antifungina e anti-pneumocistis /Bactrim): leucemie e linfomi – Adeguata cura del CVC • Pz al domicilio – Norme comportamentali (evitare luoghi affollati in fase di neutropenia, oggi meno enfatizzato del passato) passato – Restrizione contatto con fiori recisi, piante escrementi animali 119

Approccio al pz con neutropenia febbrile • Informazione preliminare del paziente riguardo ai rischi della neutropenia febbrile • Valutazione clinica adeguata con valutazione delle sedi possibili di infezione • Valutazione di accessi venosi • Esami colturali: sangue (periferico e CVC se presente), urine, orofaringe, cavità nasali. In caso di diarrea feci e ricerca tossina da Clostridium difficilis • Rx torace • Emocromo ed esami ematochimici • Terapia empirica precoce; eventuale impiego di G-CSF • In base al quadro clinico e fattori di rischio (entità sintomi, ipotensione, disidratazione ecc) decidere eventuale ospedalizzazione con possibile isolamento protettivo 120
Altre tossicità ematologiche: Anemia • Definizione: riduzione della concentrazione di emoglobina sotto i valori normali (< 12 g%) – Lieve 10 -12 g% (G 1) – Moderata 8 -10 g% (G 2) – Severa < 8 g% (G 3) • Sintomi correlati a ridotta ossigenazione tissutale • Entità dei sintomi correlata a: severità dell’anemia, velocità di comparsa, meccanismi di compenso, comorbidità, meccanismi fisiopatologici, ecc. – Ridotta produzione, emolisi, ecc. • Talora impatto significativo sul PS. 121

Altre tossicità ematologiche: Anemia • Correzione rapida dell’anemia. • Limitazioni correlate a: – – Costi Rischio infettivo Limitata disponibilità del sangue Reazioni trasfusionali e comparsa di anticorpi irregolari nel politrasfuso – Sovraccarico di liquidi – Rifiuto della trasfusione per convinzioni personali o religiose • Indicazioni – Anemia severa (< 8 g%) o con sintomi importanti correlati a ridotta capacità di compenso o manifestazioni ischemiche. • Tipi: emazie concentrate, filtrate, lavate, irradiate 122

Altre tossicità ematologiche: Anemia • • Eritropoietina: ormone prodotto dal rene e fegato in risposta all’ipossiemia Eritropoietina ricombinante – Farmaco ottenuto con metodologia del DNA ricombinante con produzione del farmaco in quantità necessarie per gli scopi terapeutici e commerciali – Iniezione sottocutanea a dì alterni, con schedula settimanale o diversa. • Sospetto che un uso estensivo abbia possibili effetti negativi – Rischio trombotico – Rischio stimolazione tumorale? – Aplasie eritroidi selettive • • Impiego eritropoietine con stretta aderenza alle linee guida di utilizzo Linee guida ASCO per uso eritropoietina – – Solo CHT concomitante Hb < 10 g% Livello target Hb: 10 -12 g%: titolazione della dose Supplemento di Ferro 123
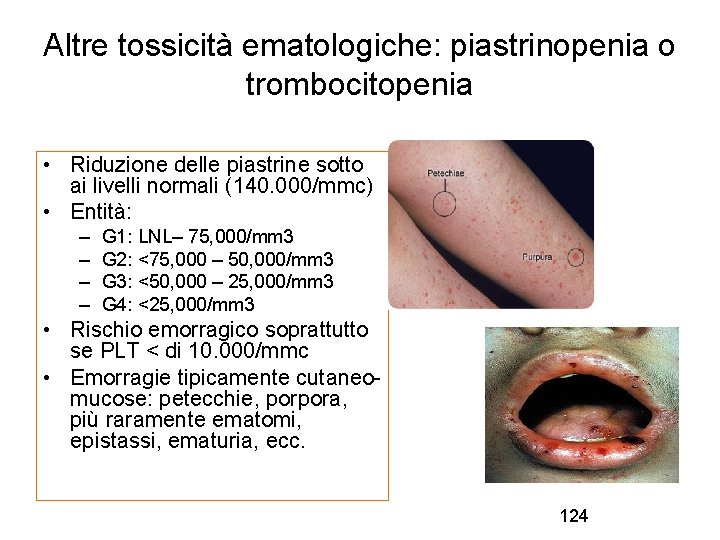
Altre tossicità ematologiche: piastrinopenia o trombocitopenia • Riduzione delle piastrine sotto ai livelli normali (140. 000/mmc) • Entità: – – G 1: LNL– 75, 000/mm 3 G 2: <75, 000 – 50, 000/mm 3 G 3: <50, 000 – 25, 000/mm 3 G 4: <25, 000/mm 3 • Rischio emorragico soprattutto se PLT < di 10. 000/mmc • Emorragie tipicamente cutaneomucose: petecchie, porpora, più raramente ematomi, epistassi, ematuria, ecc. 124

Altre tossicità ematologiche: piastrinopenia o trombocitopenia • Evitare traumatismi, procedure a rischio, uso FANS, aspirina, limitazione dell’attività fisica, ecc. • Terapia trasfusionale profilattica se PLT < 5. 00010. 000/mmc • Situazioni di maggior rischio che richiedono trasfusione con cut-off superiori: • In caso di Sindrome emorragica • Pz con necessità di procedure invasive o chirurgiche • Pz settico o febbrile • Problemi della terapia trasfusionale: limitata disponibilità, rischio infettivo, ridotta durata, reazioni, immunizzazione con ridotta efficacia in seguito. 125

Tossicità epatica • Epatite con aumento delle transaminasi e bilirubina, talora asintomatica, colestasi con ittero, malattia venoocclusiva epatica (trapianto e terapie ad alte dosi) – Favorita da patologia epatica precedente (virale o alcolica), compromissione epatica, uso contemporaneo farmaci epatotossici • Farmaci: methotrexate, gemcitabina, alchilanti e altri. • In caso di aumento delle transaminasi: dilazionare / ridurre le dosi – Monitoraggio enzimi epatici; esclusione preliminare epatopatia HBV e HCV • Profilassi con antivirali in caso di HBV 126

Neurotossicità • • Fattori di rischio: farmaci, dosi, durata della terapia Derivati del platino, alcaloidi della vinca, taxani, fluorouracile. Cause: danno neuronale. Più frequentemente periferica e sensitiva, talora motoria e centrale. In genere solo parzialmente reversibile. • Parestesie, dolori urenti alle estremità, paresi intestinale, difficoltà ai movimenti fini, iporeflessia, deficit di forza, atassia, alterazioni della deambulazione, encefalopatia. Con l’oxaliplatino tossicità acuta evocata dal freddo. • Attenzione ai sintomi: riduzione delle dosi o sospensione dei farmaci prima di grave tossicità. Protezione dal freddo con oxaliplatino. • Vitamine gruppo B, acetil carnitina: poco efficaci. Farmaci analgesici, antidepressivi, antiepilettici (Gabapentin). 127

Tossicità cutanee: chemioterapia • • • Alopecia Hand-foot syndrome Eruzioni acneiformi e dermatiti Rash maculo-papulare (taxani) Alterazioni ungueali: distrofie, discromie (iperpigmentazioni o strie verticali/orizzontali) o depressioni/irregolarità, infezioni micotiche, distacco della lamina ungueale (antracicline e taxani!) • Iperpigmentazione: alchilanti (busulfano, ciclofosfamide, tio-TEPA), antibiotici antitumorali (antracicline, bleomicina), antimetaboliti (fluorouracile, methotrexate), nitrosouree 128
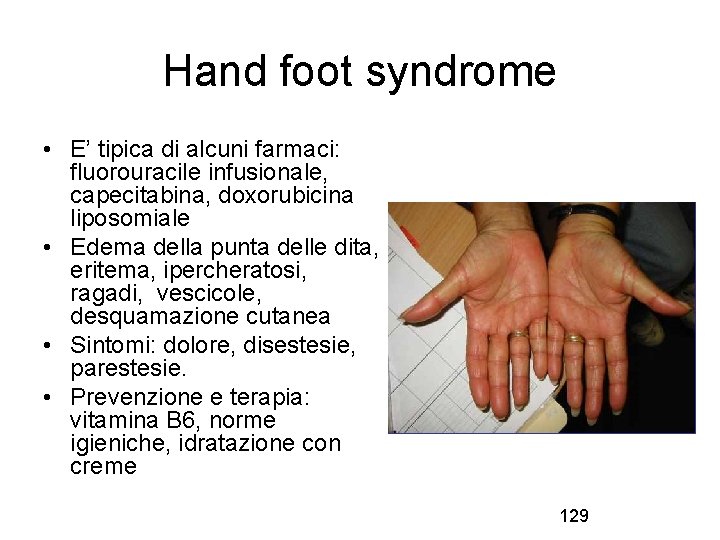
Hand foot syndrome • E’ tipica di alcuni farmaci: fluorouracile infusionale, capecitabina, doxorubicina liposomiale • Edema della punta delle dita, eritema, ipercheratosi, ragadi, vescicole, desquamazione cutanea • Sintomi: dolore, disestesie, parestesie. • Prevenzione e terapia: vitamina B 6, norme igieniche, idratazione con creme 129

Tossicità oculare e ototossicità • Tossicità oculare: – Irritazione congiuntivale, lacrimazione, dolore, fotofobia, stenosi dei dotti lacrimali (epifora) – Riduzione o annebbiamento del visus, neuropatia ottica (rara) • Antimetaboliti: ARA-C ad alte dosi (profilassi cortisonica topica), fluorouracile (possibile applicazione di compresse fredde), capecitabina • Cisplatino e carboplatino • Nitrosouree e alchilanti • Tamoxifen (retinopatia, cataratta) • Ototossicità – Cisplatino e carboplatino • Attenzione ai primi sintomi: acufeni, iniziale deficit uditivo 130

Tossicità gonadica • Cause: effetto tossico sulle cellule germinali • Effetti: Azoospermia nel maschio, amenorrea nella femmina con sterilità; alterazioni della libido; disturbi eiaculazione ed impotenza. • Agenti: alchilanti, nitrosouree, derivati del platino, • Fattori di rischio per sterilità: – – Dosi soprattutto cumulative Radioterapia Malattia tumorale (maschio) Età • Prevenzione nel giovane: prelievo e criopreservazione seme e ovociti. Soppressione ormonale nella donna (effetto limitato) 131

Tossicità cardiaca • Tossicità cumulative con antracicline (doxorubicina 450 mg/m 2). Meno tossiche le antracicline liposomiali. • Ciclofosfamide • Paclitaxel • Trastuzumab (anticorpo monoclonale anti. HER 2) • Attenzione agli effetti addittivi: antracicline, taxani e trastuzumab, radioterapia. • Anamnesi, esame obiettivo, ecg, ecocardiogramma basale e monitoraggio • Sintomi: tachicardia, dispnea, turgore giugulare, edemi declivi, aritmie • Sospensione farmaci cardiotossici. Terapia con ACE inibitori, diuretici, ecc. 132
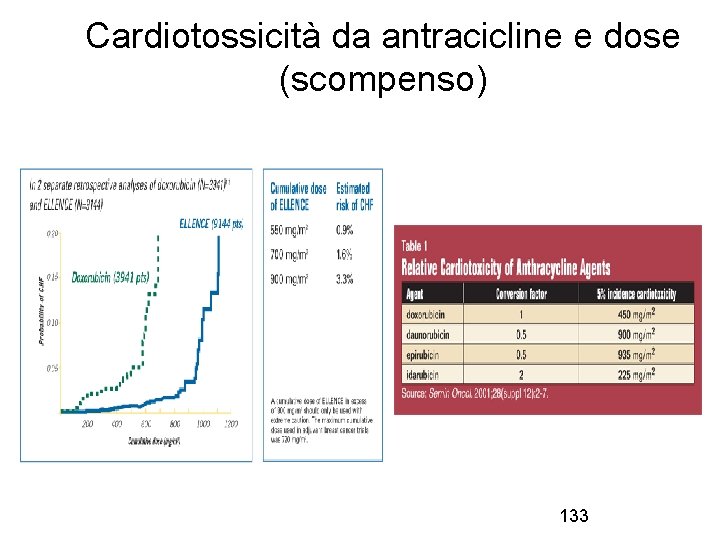
Cardiotossicità da antracicline e dose (scompenso) 133
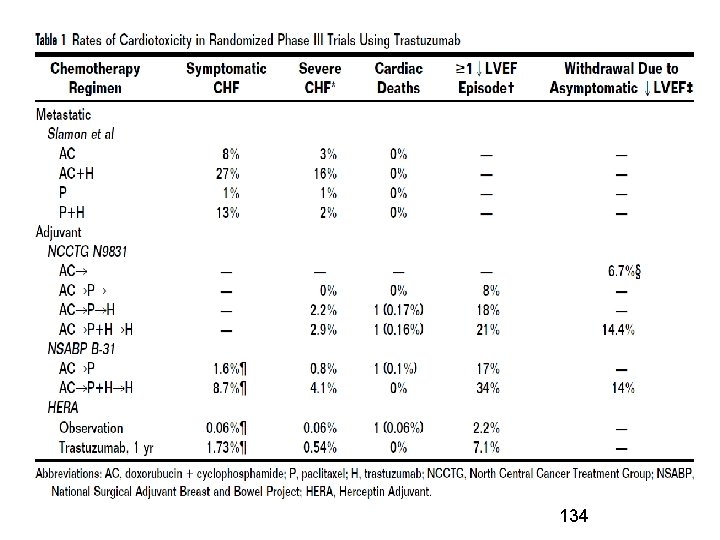
134

Tossicità urinaria • Manifestazioni cliniche: Cistite, cistite emorragica, danno renale con insufficienza renale fino all’anuria • Cause: tossicità dei farmaci antitumorali: cisplatino, (carboplatino), ciclofosfamide, ifosfamide, streptozocina, methotrexate, mitomicina-C, ecc. • Concause: farmaci concomitanti, disidratazione, dosi dei farmaci antitumorali. • Prevenzione: controllo funzione renale, idratazione adeguata, protezione con MESNA con ifosfamide e ciclofosfamide alte dosi, uso di diuretici osmotici (mannitolo) per cisplatino. • Terapia: idratazione, diuretici, dopamina 135

Stravaso: classificazione dei farmaci Vescicanti Mecloretamina Daunorubicina Doxorubicina Epirubicina Idarubicina Dactinomicina Mitomicina-C Vinblastine Vincristine Vindesine Vinorelbine Irritanti Carmustina Ciclophosfamide Dacarbazina Etoposide Fluorouracile Ifosfamide Mephalan Mitoxantrone Streptozocina Possible irritanti Carboplatin Cisplatin Docetaxel Irinotecan Oxaliplatin Paclitaxel Topotecan Non-vesicanti Asparaginase Bleomycin Bortezumib Cladribine Cytarabine Etoposide phosphate Gemcitabine Interferons Interleukin-2 Methotrexate Monoclonal antibodies Pemetrexed Raltitrexed Thiothepa 136

Diarrea • Effetto irritativo o tossico diretto sulla parete intestinale con disepitelizzazione indotto da chemio e/o radioterapia; può aggiungersi a problematiche interstinali correlate a interventi o malattia; sovrapposizione infettiva; enterocolite da antibiotici. • Soprattutto con – Fluorouracile (maggiore con l’infusione continua), capecitabina, irinotecan, nuovi farmaci (Lapatinib) – Fattori di rischio: dosi, dieta, antibiotici, precedente patologia intestinale • Dolori addominali crampiformi (possono mancare), alvo frequente, con feci acquose o semisolide. • Impatto importante in caso di diarrea protratta o abbondante con disidratazione, alterazioni elettrolitiche, soprattutto se concomita vomito. 137

Diarrea: nursing. Valutare • Anamnesi: considerare anche altre cause. Allergie, intolleranze, infezioni. • Numero di scariche nelle 24 ore • Entità, colore e consistenza delle feci • Diuresi e stato di idratazione • Perdita di peso • Addome e regione perianale 138

Diarrea: terapia • Astringenti: loperamide: 4 mg subito poi 2 mg dopo ogni scarica; octreotide in casi refrattari. • Fermenti lattici (utilità dubbia) • Idratazione adeguata e apporto di Sali minerali – Per via orale – Per via endovenosa nei casi più severi • Igiene regione perianale dopo l’evacuazione e protezione della cute con creme all’ossido di alluminio • Considerare l’ospedalizzazione in caso di presenza di febbre in fase di neutropenia, dolori addominali, sanguinamento, disidratazione con restrizione diuresi, incapacità di assumere liquidi, stato soporoso, alterazioni obiettività addominale, durata > 24 ore. 139

Diarrea: nursing – Adeguata assunzione di liquidi e sali minerali. • Dieta adeguata – Inizialmente dieta liquida, idratazione-nutrizione parenterale in caso di diarrea importante – Poi introduzione dieta basso contenuto di fibre: banane, riso, mousse di mela. – Aggiungere in seguito: parmigiano, patate bollite, pollo bollito, uova bollite o in camicia – Evitare derivati del latte e derivati, grassi, frutta fresca, fritti, fibre, caffè, alcool, cibi piccanti e che producono gas. – Pasti piccoli e frequenti 140

Aspetti pratici per i pazienti • Bevi una sufficiente quantità di liquidi: bevande sportive, gelatina, brodo sono migliori dell’ascqua perché contengono sali e zuccheri. • I succhi di frutta preferiti sono albicocca, pesca, nettare di pera e mirtillo – Il succo di mela può indurre diarrea; – Il succo di pomodoro, arancio e ananas sono troppo acidi. – Il succo di pompelmo interagisce con moti farmaci

Informazioni per il paziente: chiama il medico o l’infermiere se… • Il trattamento che hai ricevuto dal medico come profilassi non arresta la diarrea • La diarrea peggiora con aumento del numero delle scariche giornaliere • Non puoi bere e trattenere i liquidi ingeriti: dovresti assumere almeno 1, 5 l di fluidi al giorno • Vedi sangue nelle feci • Compaiono ulcere nella regione anale • Hai dolore gastrico severo o febbre • Ti senti molto debole e hai vertigini • La quantità di urine emesse giornalmente si riduce ed il colore si fa scuro • Perdi peso

Mucosite o stomatite • I termini mucosite e stomatite vengono utilizzati in maniera interscambiabile per indicare le alterazioni del cavo orale. • Si riferisce ad un processo infiammatorio che interessa soprattutto il cavo orale, ma che può coinvolgere anche la mucosa del tratto gastrointestinale • Quadro di severità variabile da eritema con lieve dolore locale, edema, fino alla comparsa di lesioni ulcerative multiple, confluenti e sanguinanti delle mucose • Incidenza: 40% in caso di terapie convenzionali > 70% in caso di terapie ad alte dosi. Talora tossicità dose-limitante. 143

Mucosite o stomatite • Il paziente lamenta spesso irritazione, dolore, difficoltà e dolore nella deglutizione, secchezza delle fauci, talora ulcere dolenti e sanguinanti, alterazioni del gusto. • La mucosite interferisce con la qualità di vita, la nutrizione, la comunicazione verbale e non verbale (sorriso, bacio) e in generale con il benessere individuale, contribuendo al carico dei sintomi • L’integrità della mucosa orale (similmente alla cute) rappresenta la prima linea di difesa contro le infezioni • Può portare a riduzione di dosaggio dei farmaci chemioterapici e ad un trattamento subottimale della malattia. 144

Mucosite o stomatite • Farmaci: antracicline, fluorouracile, methotrexate, taxani, alchilanti, etoposide. – Dose farmaci, radioterapia concomitante, fattori individuali – Sovra-infezioni: batterica, virale, micotica – Neutropenia indotta • Fattori di rischio: deficit enzimatici (Fluorouracile) e polimorfismi genetici (Methotrexate), scarsa igiene orale, fumo e alcool, stato nutrizionale, parodontopatia, età (< 20 e > 65), corticosteroidi, terapie ad alte dosi, trapianto di midollo, a trattamenti per emopatie (leucemie acute), neoplasie del testa e collo dopo chemio-radioterapia 145
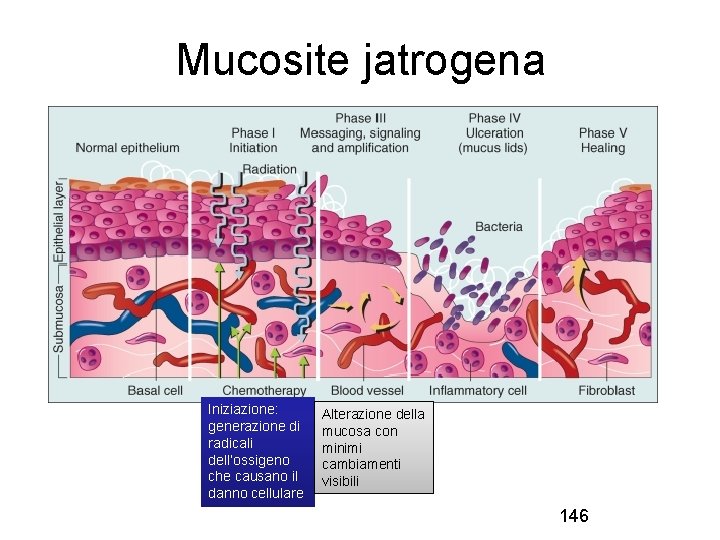
Mucosite jatrogena Iniziazione: generazione di radicali dell’ossigeno che causano il danno cellulare Alterazione della mucosa con minimi cambiamenti visibili 146
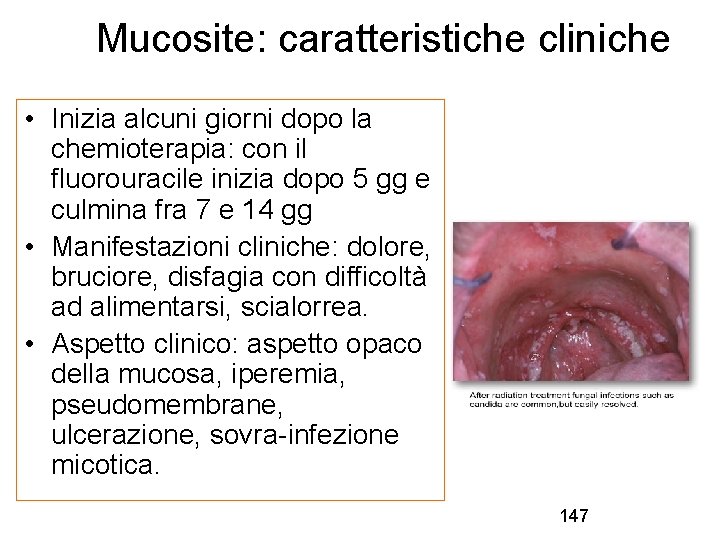
Mucosite: caratteristiche cliniche • Inizia alcuni giorni dopo la chemioterapia: con il fluorouracile inizia dopo 5 gg e culmina fra 7 e 14 gg • Manifestazioni cliniche: dolore, bruciore, disfagia con difficoltà ad alimentarsi, scialorrea. • Aspetto clinico: aspetto opaco della mucosa, iperemia, pseudomembrane, ulcerazione, sovra-infezione micotica. 147

Mucosite: prevenzione • I pazienti possono ritardare e ridurre la normale igiene orale a causa della mancanza di tempo o energie per queste attività. Questa trascuratezza può contribuire all’insorgenza della mucosite • Il mantenimento di una igiene orale ottimale è importante e richiede l’uso routinario dello spazzolino e filo interdentale, ed altri interventi profilattici. • Crioterapia orale con ghiaccio e sciacqui con allopurinolo per il fluorouracile, sciacqui al cavo orale con bicarbonato (controindicate soluzioni alcooliche), soluzioni a antifungini. • Idratazione e nutrizione adeguate 148

Mucosite: Trattamento • Collutori, soluzioni di xilocaina viscosa, soluzioni a base di sucralfato; evitare assunzione di cibi caldi, irritanti ecc. Antiherpetici ed antifungini in caso di sovrapposizioni infettive. Anestetici locali o analgesici, sino alla morfina nelle gravi mucositi da trapianto • Fattore di crescita keratinocitario (recente introduzione) 149
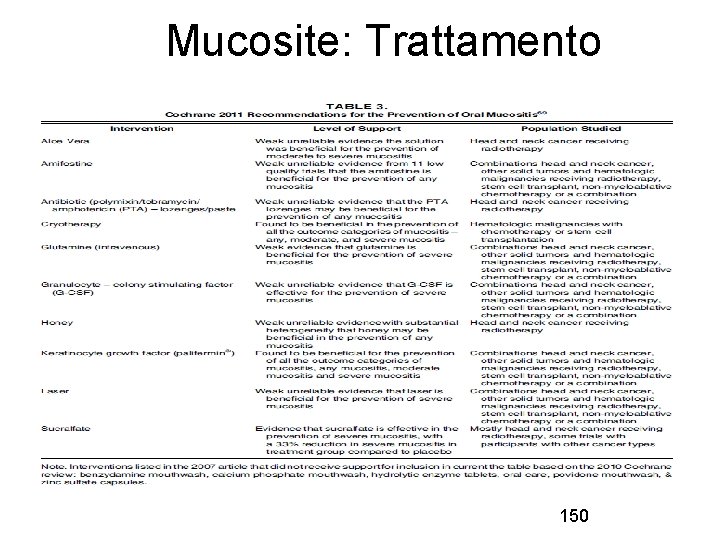
Mucosite: Trattamento 150

Cancer Related Fatigue (CRF) • Dal 2000 la fatigue è a tutti gli effetti riconosciuta come • una malattia correlata al cancro e non più considerata semplicemente come un insieme di sintomi che affliggono l’esistenza e fiaccano la volontà del malato di tumore (International Classification of Disease del Center for Disease Control and prevention - CDC).

Definizione e entità del fenomeno • Nel 2000, il NCCN (National Comprehensive Cancer Network) ha sviluppato la seguente definizione per indicare la fatigue correlata al cancro (CRF): “Una sensazione soggettiva e persistente di stanchezza correlata al cancro o ai trattamenti per il cancro, che interferisce con le attività quotidiane“. • Occorre nel 14% - 96% delle persone con cancro, particolarmente in quelle che ricevono un trattamento antitumorale

CRF: incidenza • • In corso di chemioterapia In corso di radioterapia A due anni dal trattamento In fase terminale 80% 70% 80 -90% • 70 -80 % pazienti oncologici ne è affetto (Portenoy R. K. et al. Cancer-related fatigue: guidelines for evaluation and management. The Oncologist, 1999, 4, 1 -10).

CRF: aspetto multidimensionale • LA CRF può essere descritta come una condizione che provoca distress e ridotta capacità di svolgere le normali attività come conseguenza di mancanza di energia. L’impatto è multidimensionale: fisico, psicosociale ed emozionale: �Sensazioni fisiche: difficoltà a svolgere le quotidiane attività. �Sensazioni di tipo emozionale: diminuite motivazioni e cambiamenti nel tono dell’umore. �Sensazioni di tipo cognitivo: difficoltà a concentrarsi o a formulare pensieri compiutamente.

I sintomi della CRF • • Sono quelli tipici dell’astenia cronica (esaurimento di energia, estrema stanchezza, debolezza e spossatezza, ma aggravati dalla patologia tumorale) conseguenze rilevanti come la forte difficoltà a compiere normali attività quali cucinare, pulire, fare una doccia, rifare il letto. Non solo: i disturbi interessano anche la sfera intellettuale, affettiva e psicologica. I criteri internazionali per la definizione di ‘fatigue correlata a cancro’ si basano sulla seguente classificazione: 1. Sintomi presenti tutti i giorni o quasi per almeno due settimane nell’ultimo mese: · spossatezza significativa · diminuzione dell’energia · accresciuto bisogno di riposo, in maniera non proporzionale all’attività sostenuta 2. Inoltre devono essere presenti cinque (o più) dei sintomi seguenti: · debolezza generalizzata e pesantezza degli arti · diminuzione della concentrazione o dell’attenzione · diminuzione della motivazione o dell’interesse nelle normali attività · insonnia o ipersonnia · sensazione di non aver riposato durante il sonno · sensazione di dover compiere sforzi per superare l’inattività · marcata reazione emotiva (tristezza, frustrazione o irritabilità) alla sensazione di fatigue · difficoltà a portare a termine le attività quotidiane

Impatto sulla vita del paziente �LA CRF è definita spesso dal paziente come uno dei sintomi più stressanti associati al cancro e ai suoi trattamenti. �Nonostante questo è spesso trascurato e non riportato nella pratica clinica quotidiana. �La CRF può avere un impatto importante sulla qualità di vita del paziente e della famiglia con coinvolgimento della sfera fisica, psicosociale, lavorativa ed economica (fenomeno cd multidimensionale)
Percezione del paziente SVOGLIATO LENTO ESAUSTO CONFUSO ESAURITO PROSTRATO SCORAGGIATO TRASCURATO PIGRO DEBOLE APATICO FIACCO A TERRA STANCO INDIFFERENTE ABBATTUTO

Fattori contribuenti alla fatigue �Terapia antineoplastica, chemioterapia, agenti modificatori della risposta biologica (BRM), nuovi farmaci target, terapie ormonali (es agenti antiandrogeni o antiestrogeni) e radioterapia. Particolare prevalenza in caso di trattamenti multimodali o con protocolli ad alte dosi per la malattia avanzata. �Problematiche metaboliche, nutrizionali, ormonali come anemia, malnutrizione, ipotiroidismo, menopausa, disidratazione. �Problematiche d’organo: scompenso cardiaco, fibrosi polmonare, miopatie. �Altre cause come dolore e suo trattamento, (particolarmente analgesici oppioidi), distress emozionale, disturbi del sonno.

CRF: necessità di misurare il fenomeno • • • EORTC QLQc-30 European organisation for research of treatment of cancer (J. N. C. Inst. 1990) Rotterdam Symptom Checklist (Br. J. Cancer 1990) Brief Fatigue Inventory (Cancer 1999) FACT – F (G) Functional assessment of cancer therapy fatigue FACT-An (Anemia)(J. Pain Symptom Manage 1997) Fatigue Symptom Inventory (Qual. Life Res. 1998) Piper Fatigue Scale (Onc. Nurs. 1998) Cancer Fatigue Scale (Pain Symptom Manage 2001)

Nella pratica quotidiana può essere utile una valutazione con VAS o Common terminology criteria CTAE � VAS Per monitorare la fatigue e il suo trend nel tempo può essere utile l’utilizzo di scale o di analoghi visivi (ad es. assenza, lieve, moderata, grave o la numerazione da 0 a 10 dove 0 corrisponde all’assenza di fatigue e 10 alla peggiore fatica immaginabile). � Diario personale L’uso di un diario personale può aiutare a comprendere l’andamento della fatigue o a identificare attività specifiche sono associate con l’esacerbazione della sintomatologia. � Domande da porre Nella pratica quotidiana l’uso di tre domande può aiutare a definirne la gravità e il suo andamento: - Provi un senso di affaticamento? - Se si quanto è stato grave, da 0 a 10, nel corso dell’ultima settimana? - Come ha influito sulla tua capacità di svolgere le attività quotidiane?

Obiettivi nel trattamento della CRF • Differenti a seconda se il paziente è in trattamento attivo o in fase avanzata di malattia • Variano notevolmente a seconda delle informazioni date al paziente • Incidono a seconda della fase in cui si trova il paziente: negazione, collera, patteggiamento depressione accettazione
Trattamento della CRF Counseling… terapia occupazionale… Carnitina… Supporto psicologico… Fidioterapia… Psicostimolanti … trasfusioni Eritropoietina…

Terapia • Farmaci psicostimolanti ed antidepressivi • Trattamento dell’anemia: trasfusioni, eritropoietina, ferro, vitamine emoattive • Esercizio fisico • Terapia cognitiva e comportamentale • Attività e riposo • Educazione del paziente

Esercizio fisico • Alcuni piccoli studi clinici. • Buon intervento soprattutto a scopo preventivo • Riduzione della fatica, miglioramento della qualità del sonno, riduzione dello stress emotivo, miglioramento delle capacità fisiche e della qualità della vita. • Aumento della sensazione di autocontrollo e di autostima.

Interventi possibili • Informare il paziente sul problema della fatigue • Collaborare con i medici per il trattamento farmacologico dell’anemia (eritropoietina, emoderivati e controllo effetti collaterali e reazioni) • Collaborare con i medici per il trattamento farmacologico delle cause fisiche della fatigue • Potenziare i fattori che facilitano il recupero dell’energia • Mantenere un idoneo ed equilibrato apporto energetico • consigliare di aggiornare “il diario della fatigue” • consigliare di diluire le faccende domestiche nell’arco della settimana • Far eseguire quotidianamente esercizi fisici leggeri • Programmare le attività domestiche inserendo anche dei piccoli esercizi fisici • Insegnare affinchè il paziente sia in grado di ascoltare il proprio corpo • Stimolare l’assunzione di liquidi prima, durante e dopo l’attività fisica

Interventi �Consigliare di alimentarsi ogni volta che si ha appetito senza necessariamente rispettare gli orari �Consigliare di assaggiare altri gusti �Stimolare una corretta igiene del cavo orale �Garantire adeguati periodi di riposo durante il giorno �Consigliare di non dormire mai più del necessario �Aiutare ad avere sempre lo stesso ritmo sonno-veglia �Evitare il consumo di sostanze eccitanti �Svolgere attività mentali �Assecondare attività che recano benessere (lettura, musica, film, bricolage) �Insegnare e far svolgere esercizi di rilassamento (training autogeno, massaggio dolce, biodanza, ecc) �Programmare e attuare interventi a carattere psicologico �Facilitare le relazioni familiari e sociali del paziente �Educare i care givers al controllo della fatigue

Reazioni infusionali e da ipersensibilità • L’utilizzo dei farmaci antitumorali può essere seguito da reazioni allergiche/da ipersensibilità o meglio definite come infusionali. • Diversi meccanismi patogenetici • Eventi di varia gravità, fino allo shock anafilattico e potenzialmente letali • Le reazioni di grado severo sono rare (≤ 5%), mentre quelle lievimoderate sono spesso sottostimate. • Le reazioni da ipersensibilità severe sono definite come risposte immunologiche una sostanza o antigene estraneo. • I farmaci antitumorali come gli altri farmaci possono essere riconosciuti dal sistema immunologico come “non self”. • Questo può scatenare una reazione di tipo I caratterizzata dal rilascio di istamina ed altri mediatori dell’infiammazione che inducono i sintomi della reazione da ipersensibilità. 167

Definizione di anafilassi • Una definizione precisa non è importante per il trattamento in emergenza di una reazione anafilattica…. • Non c’è una definizione universalmente riconosciuta • La European Academy of Allergology and Clinical Immunology Nomenclature Committee ha proposto la seguente definizione: • L’anafilassi è una reazione da ipersensibilità generalizzata o sistemica, severa e pericolosa per la vita. • E’ caratterizzata dallo sviluppo rapido di problemi che mettono in pericolo la vita, a carico delle vie aeree o della respirazione, o della circolazione usualmente con associate alterazioni della cute e delle mucose. 168

Classificazione delle affezioni da ipersensibilità (Gell e Coombs) • Affezioni di tipo I (anafilattico): mediate da anticorpi Ig. E. Vengono liberate sostanze vasoattive e spasmogene che agiscono sui vasi e sulla muscolatura liscia alterandone le funzioni; • Affezioni di tipo II (reazioni citotossiche anticorpo-mediate): Gli anticorpi interagiscono con gli antigeni presenti sulla superficie cellulare, cioè vanno a danneggiare direttamente le cellule rendendole suscettibili alla fagocitosi: es anemia emolitica, trombocitopenia immune, reazioni trasfusionali • Affezioni di tipo III (mediata da immunocomplessi): Il legame antigene-anticorpo forma un complesso che attiva il sistema del complemento: es malattia da siero e vasculiti. • Affezioni di tipo IV (cellulo-mediata): Il danno tissutale è prodotto dall'attivazione di cellule del sistema immunitario (linfociti T): es dermatiti da contatto, psoriasi, esantema maculopapulare, eritema multiforme, necrolisi epidermica

Fisiopatologia � Le reazioni da ipersensibilità a farmaci antitumorali sono in genere reazioni di tipo I che hanno tre fasi � Sensibilizzazione: esposizione all’antigene con formazione di anticorpi specifici (generalmente di classe Ig. E) che si legano ai recettori di mastociti ed basofili � Fase di attivazione: alla successiva introduzione dell’antigene questo si lega alle IGE legate sulle cellule determinandone la degranulazione e la liberazione di mediatori chimici (istamina ed altre) � Fase di azione dei mediatori con espressione clinica � Reazioni anafilattoidi, clinicamente indistinguibili dall’anafilassi, ma mediate direttamente dal farmaco senza intervento di anticorpi Ig. E.

Fisiopatologia • Reazioni allergiche da ipersensibilità • Reazioni anafilattoidi • Reazioni infusionali 171

Fattori di rischio • Età, sesso, fattori genetici, stato nutrizionale, livello di stress, fattori ormonali ed ambientali, precedente esposizione al farmaco, storia di atopia • Modalità di somministrazione: – Ev, orale, topica, im. – Durata di somministrazione: bolo ev vs infusione lenta – Caratteristiche immunologiche del farmaco • • Molecole proteiche (asparaginasi) Metalli pesanti (Platino e Carboplatino) Farmaci che necessitano diluenti (taxani e podofillotossine) Formulazioni liposomiali dei farmaci 172
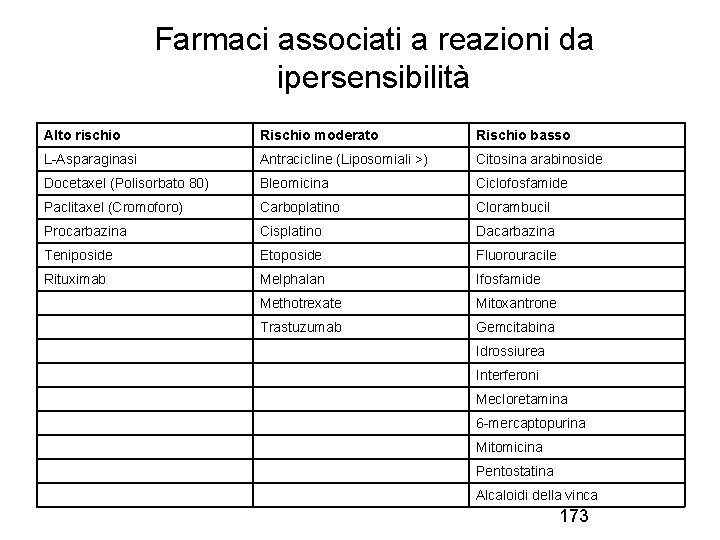
Farmaci associati a reazioni da ipersensibilità Alto rischio Rischio moderato Rischio basso L-Asparaginasi Antracicline (Liposomiali >) Citosina arabinoside Docetaxel (Polisorbato 80) Bleomicina Ciclofosfamide Paclitaxel (Cromoforo) Carboplatino Clorambucil Procarbazina Cisplatino Dacarbazina Teniposide Etoposide Fluorouracile Rituximab Melphalan Ifosfamide Methotrexate Mitoxantrone Trastuzumab Gemcitabina Idrossiurea Interferoni Mecloretamina 6 -mercaptopurina Mitomicina Pentostatina Alcaloidi della vinca 173

Fisiopatologia: reazioni anafilattoidi e infusionali • Reazioni anafilattoidi, clinicamente indistinguibili dall’anafilassi, senza intervento di anticorpi Ig. E, ma per legame del farmaco direttamente ai mastociti in pazienti anche non precedentemente esposti al farmaco. Esempi: – Reazione al taxolo (al cremoforo contenente diluenti di disverso tipo) – Reazione al Md. C per TAC • Reazioni infusionali causate dal rilascio di citochine spesso alla prima infusione (caratteristico dei nuovi farmaci biologici proteici) 174

L-asparaginasi • Associata con il più alto rischio di ipersensibilità – Rischio documentato fino al 35% (5 -8% per dose e fino al 33% dopo la 4° dose) – Reazioni più frequenti nelle somministrazioni settimanali o mensili rispetto a quelle giornaliere – La via im può comportare rischio minore, come pure concomitante somministrazione di cortisone e vincristina – Le reazioni possono essere ritardate (ore dopo) • La L-asparaginasi è un polipeptide di origine batterica; molecole più recenti con minor rischio sono l’Erwinase e la pergaspargase (molecola pegilata meno immunogena) 175

Derivati del platino • Cisplatino: è associato con una maggiore incidenza in caso uso prolungato (dopo 6 o più dosi) – L’incidenza oggi appare meno pronunciata con l’utilizzo di premedicazioni corticosteroidee standard – Maggiore tasso di incidenza riportato 10 -25% dopo somministrazioni multiple intravescicali • Carboplatino: soprattutto in caso di trattamenti ripetuti (fino al 12%) • Oxaliplatino: fino al 10 -12% soprattutto in caso di dosi ripetute 176

Taxani • Paclitaxel: reazioni spesso di tipo anafilattoide (cremoforo) – Alta incidenza nei primi trials clinici (fino a 41%) – Riduzione a 1 -3% dopo introduzione di adeguate premedicazioni (Ex desametazone 20 mg 12 ore prima dell’infusione, antistaminici e ranitidina) – Nuove formulazioni senza cremoforo (es. Abraxane: formulazione con nanotecnologia): premedicazione non necessaria, reazioni < 1% • Docetaxel: reazione a polisorbato 80 (Tween 80: conservante): premedicazione corticosteroidea prima e dopo l’infusione (2 giorni) anche per ridurre la ritenzione idrica da Taxotere 177

Reazioni da altri farmaci. • Bleomicina: reazioni anche gravi causate dal massivo rilascio di pirogeni leucocitari • Agenti biologici: non sono comunemente associati a reazioni da ipersensibilità – Più spesso gli anticorpi monoclonali provocano reazioni per rilascio di citochine che si verificano in genere al primo ciclo con brivido, febbre, astenia, broncospasmo ed ipotensione, minimizzati dalla premedicazione con paracetamolo, antistaminici, cortisonici • Procarbazina e methotrexate provocano polmoniti interstiziali e vasculiti. 178

Reazioni da ipersensibilità: clinica • Esordio acuto – Da pochi minuti a 15 -30 minuti dopo l’inizio della somministrazione ev. – Anche 2 ore dopo somministrazione orale • Esordio talora ritardato anche di parecchie ore, anche in rapporto al metabolismo del farmaco • Possibilità di recidiva dei sintomi dopo l’iniziale risposta ai trattamenti per l’allergia fino a 8 -24 ore dopo • Possibilità di decesso, generalmente per asfissia da edema e spasmo laringeo, collasso cardiocircolatorio e shock 179

Reazioni da ipersensibilità: clinica • Più comuni – – – – – Agitazione Orticaria e rash cutaneo Angioedema Dispnea (Broncospasmo) Prurito Brividi Arrossamento o cianosi Vertigini Ipotensione • Meno comuni – Nausea/Vomito – Diarrea – Dolori e movimenti addominali – Ostruzione nasale – Tosse – Dolore retrosternale o alla schiena – Convulsioni – Starnuti – Bruciore genitale – Sapore metallico 180
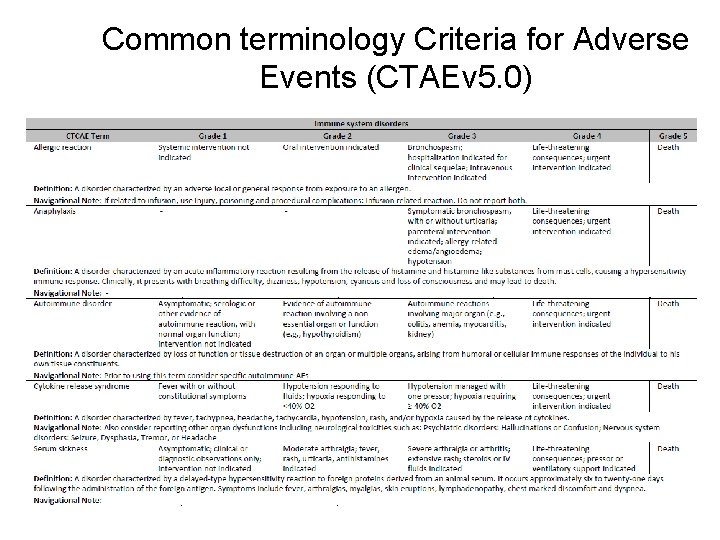
Common terminology Criteria for Adverse Events (CTAEv 5. 0)

Criteri diagnostici per l’anafilassi
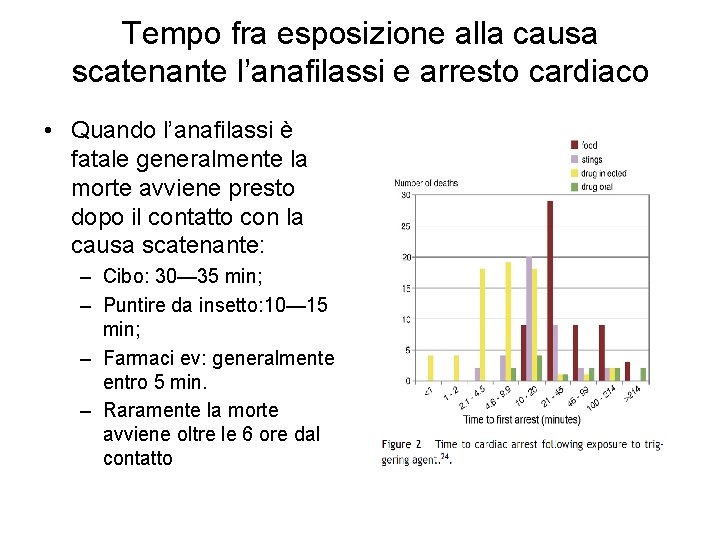
Tempo fra esposizione alla causa scatenante l’anafilassi e arresto cardiaco • Quando l’anafilassi è fatale generalmente la morte avviene presto dopo il contatto con la causa scatenante: – Cibo: 30— 35 min; – Puntire da insetto: 10— 15 min; – Farmaci ev: generalmente entro 5 min. – Raramente la morte avviene oltre le 6 ore dal contatto

Reazioni da ipersensibilità: diagnosi • Diagnosi generalmente clinica – Rapporto temporale con la somministrazione del farmaco • Possibilità di misurare i mediatori allergici – Triptasi enzima secreto dai mastociti (vn: 10 -12 ng/ml) aumenta nelle reazioni allergiche severe (es. lo shock anafilattico), ritornando alla norma dopo qualche giorno. • Test cutanei o RAST • Anamnesi accurata per i dentificare i pz ad alto rischio di allergia: precedente esposizione al farmaco, altre precedenti reazioni da ipersensibilità a farmaci, storia di allergia o atopia. 184

Prevenzione dell’allergia e anafilassi • Anamnesi allergologica, conoscenza dei farmaci antitumorali per individuare i pazienti a rischio • Familiarità con le principali premedicazioni utilizzate come prevenzione delle reazioni da farmaci. – Somministrazione di premedicazioni e verifica della loro assunzione domiciliare da parte del pz. • Corticosteroidi: Desametazone 10 -20 mg ev immediatamente prima o anche il giorno precedente • Antistaminici (Anti-H 1): Clorfeniramina (Trimeton) 10 -20 mg • Antistaminici (Anti-H 2): Cimetidina (Ranidil) 300 mg ev o Ranitidina 150 mg / ev • Istruire il paziente a segnalare eventuali disturbi iniziali • Monitorare i parametri vitali e Sat 02 prima e durante la terapia in particolare per farmaci e pz a rischio 185

Management dell’allergia e anafilassi • Sospendere immediatamente l’infusione e mantenere la linea venosa con isotonica salina. • Chiamare aiuto e stare con il paziente. • Mantenere la pervietà delle vie aeree • Monitorare i parametri vitali, saturazione O 2 , e anticipare il bisogno di rianimazione cardiorespiratoria • Rapida disponibilità carrello di emergenza con: – Farmaci (adrenalina, steroidi, antistaminici, aminofillina, dopamina) – Dispositivi medici: per ossigenoterapia con maschera (mantenere Sat. O 2 > 92%), cateteri per reperire validi accessi venosi, monitor cardiaco, defibrillatore e dispositivi per la rianimazione cardiorespiratoria. • Conoscere i farmaci assunti dal pz cronicamente che potrebbero ostacolare la gestione dell’evento (beta bloccanti, ace inibitori, antidepressivi) 186

Management dell’allergia e anafilassi • Adrenalina: 0, 3 -0, 5 mg (soluzione 1: 1000) sottocute ripetibile dopo 5 -20 minuti o – 0, 1 mg/Kg (soluzione 1: 10. 000) ev sotto controllo del rianimatore / medico dell’emergenza urgenza, con monitoraggio ecg, in caso di broncospasmo con stridore o shock (in almeno 3 -5 minuti) • Antistaminici: Difenidramina 50 mg o clorfeniramina (Trimeton) – H 2 antagonisti (ranitidina ) come farmaci ancillari • • • Cortisone: Idrocortisone (Flebocortid 500 mg o 6 metilprednisolone Solumedrol 125 mg / ev) Aminofillina e/o Beta stimolanti in aerosol (Salbuterolo, ecc) Dopamina Soluzioni isotoniche ev: fisiologica o Ringer-lattato per mantenere PA valida A paziente stabilizzato: monitorare – Ogni 15’ per 4 volte, poi ogni ora per 4 volte, poi ogni 4 ore • Documentare l’evento sulla cartella infermieristica e medica 187

Linee guida ESMO: management reazioni infusionali Rosellò S, et al. Ann Oncol 2017; 28(suppl 4): iv 100

Linee guida ESMO: management reazioni infusionali Rosellò S, et al. Ann Oncol 2017; 28(suppl 4): iv 100

Algoritmo per l’anafilassi Working Group of the Resuscitation Council (UK)

Documentare l’evento

Rechallenge dopo reazioni da ipersensibilità • Considerare l’entità della reazione e le alternative terapeutiche. • Spesso le reazioni al Paclitaxel si risolvono con l’immediata sospensione del farmaco e le infusioni possono essere proseguite con successo dopo 30 -60 minuti – Razionale: la reazione avvenuta può esaurire i mediatori della reazione e prevenirne ulteriori. • L’intensificazione della premedicazione può essere utile • Regimi di de-sensibilizzazione possono essere condotti in accordo con l’allergologo 192
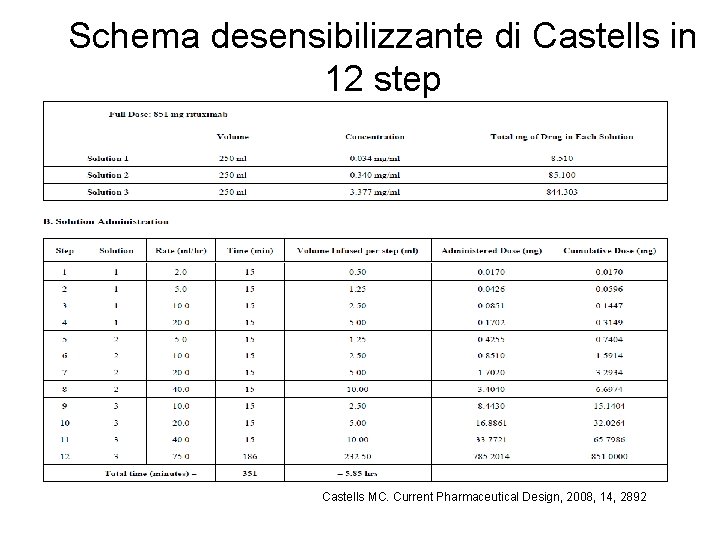
Schema desensibilizzante di Castells in 12 step Castells MC. Current Pharmaceutical Design, 2008, 14, 2892

Conclusioni • Oggi molte opzioni terapeutiche disponibili • Terapie innovative di tipo target e immunoterapiche in grande espanzione • Effetti avversi talora importanti e doselimitanti • Necessità di esperienza del medico e dell’infermiere nella selezione dei pazienti e nell’applicazione del programma di terapia • Corretto utilizzo dei trattamenti di supporto fondamentale. 194
- Slides: 194