Universidade Federal do Acre Engenharia Agronmica Programa de






















![Exercício [CO 2]2 Kc = [CO]2. [O 2] 0. 42 = 0, 62 x Exercício [CO 2]2 Kc = [CO]2. [O 2] 0. 42 = 0, 62 x](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-26.jpg)


![Exercício H 2 + I 2 V = k. [H 2]. [I 2] [H Exercício H 2 + I 2 V = k. [H 2]. [I 2] [H](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-32.jpg)
![Exercício Início Vi = k. x. y Duplicamos [H 2] = 2 x Final Exercício Início Vi = k. x. y Duplicamos [H 2] = 2 x Final](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-33.jpg)







- Slides: 42

Universidade Federal do Acre Engenharia Agronômica Programa de Educação Tutorial - PET Tutor: Dr. Ribamar Silva Petianas: Sonaira Souza e Maria Izabel

Cinética Química Conceito - A velocidade das reações químicas e os fatores que nelas interferem; As reações podem ser: - Rápidas → combustão da pólvora; - Lentas → ferrugem;

Cinética Química Velocidade de uma reação Velocidade média → Consumo de reagentes ou formação de produtos no decorrer da reação; Valor é sempre positivo; Valor = quociente entre o módulo da variação do número de mols (∆n) e o intervalo de tempo em que ocorreu essa variação (∆t) vezes o coeficiente estequiométrico; V = I∆n. I ∆t x CE

Cinética Química Ex. : Analise a reação C 2 H 2 + 2 H 2 C 2 H 6: C 2 H 6(mol/L) 0 12 15 20 23 Tempo (min) 0 4 6 10 13 - Qual a Vm de C 2 H 6 no intervalo 0 a 4 min: ∆n = 12 – 0 = 12 mols ∆t = 4 – 0 = 4 min ∆n 12 mols Vm = ∆t = 4 min Vm = 3 mols/min

Cinética Química Ex. : Analise a reação C 2 H 2 + 2 H 2 C 2 H 6: H 2 (mol/L) 23 20 15 12 0 Tempo (min) 0 4 6 10 13 - Qual a Vm de H 2 no intervalo 4 a 10 min: ∆n = 12 – 20 = - 8 mols ∆t = 10 – 4 = 6 min ∆n - 8 mols Vm = ∆t = 6 min x 2 Vm = 0, 7 mol/min

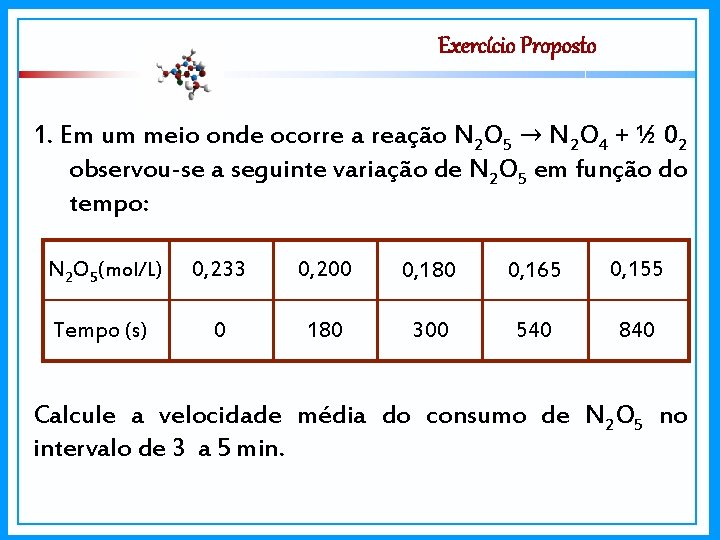
Exercício Proposto 1. Em um meio onde ocorre a reação N 2 O 5 → N 2 O 4 + ½ 02 observou-se a seguinte variação de N 2 O 5 em função do tempo: N 2 O 5(mol/L) 0, 233 0, 200 0, 180 0, 165 0, 155 Tempo (s) 0 180 300 540 840 Calcule a velocidade média do consumo de N 2 O 5 no intervalo de 3 a 5 min.

Cinética Química Resolução: Tempo 3 min =180 s 0, 200 mol/L 5 min = 300 s 0, 180 mol/L. Aplicando a fórmula: V m= Vm = I∆n. I ∆t I 0, 180 – 0, 200=I 5 -3 Vm = 0, 010 mol/min I- 0, 020 I 2

Cinética Química Como ocorre uma reação química? Ligações dos reagentes → Rompidas; Novas ligações → Produtos; Etapas intermediárias → Complexo ativado;

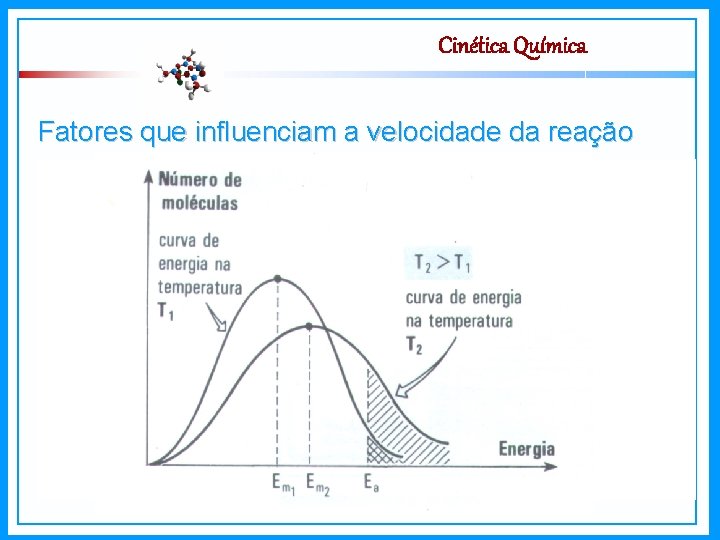
Cinética Química Fatores que influenciam a velocidade da reação Temperatura - Temperatura → freqüência e energia dos choques entre partículas; - Temperatura → velocidade da reação;

Cinética Química Catalizadores - São substâncias que interferem na velocidade das reações químicas sem serem consumidas no processo; Ex. : Água oxigenada e alguns metais (Cu, Fe, Ni) - Catalisadores alteram a velocidade da reação atuando sobre o complexo ativado;

Cinética Química Concentração dos reagentes - Partículas presentes num mesmo volume nº de choques possíveis entre elas; - Água oxigenada como agente clareador;

Cinética Química Superfície de contato - Superfície de contato entre os reagentes mais rápida é a reação; Fe(s) + 2 H+ Fe 2+ + H 2(g) Reação lenta Fe(s) + 2 H+ Fe 2+ + H 2(g) Reação rápida

Cinética Química Outros fatores - Luz e eletricidade afetam a velocidade de algumas reações; Ex. : Fotossíntese e Eletrólise. - Transferência de energia para os reagentes formarem o complexo ativado; - Sistema gasoso pressão - pressão volume concentração

Exercício Proposto 1. Com respeito aos fatores que influem na velocidade de uma reação, assinale as alternativas verdadeiras: ( F) Quanto menor a energia de ativação, mais facilmente se forma o complexo ativado e, portanto, menos rápida é a reação; (V) Quanto maior a temperatura, maior energia possuem as moléculas e, portanto, mais rápida é a reação;

Exercício Proposto (V) Quanto maior a pressão em uma reação onde os reagentes e produtos são gasosos, mais rápida é a reação; (V) Catalisadores, quando misturados com os reagentes, possuem a propriedade de aumentar a velocidade da reação; (F) Quanto maior a concentração, maior é o número de moléculas colidindo num determinado espaço, e portanto, menos rápido é a reação;

Cinética Química Lei da ação das massas (Guldberg – Waage) A velocidade de uma reação é diretamente proporcional (k) ao produto das concentrações molares dos reagentes, estando cada concentração elevada a um expoente igual ao respectivo coeficiente na equação química. a. A + b. B i d c. C + d. D Vd = Kd [A]a x [B]b Vi = Ki [C]c x [D]d

Cinética Química Ex. : 2 A + 3 B i d C 2 + 3 D Vd = Kd [A]2 x [B]3 Vi = Ki [C 2] x [D]3

Exercício Escreva a equação de velocidade da reação direta nos seguintes casos: a) H 2(g) + I 2(g) 2 HI(g) Vd = Kd. [H 2]. [I 2] b) 2 SO 2(g) + O 2(g) Vd = Kd. [SO 2]2. [O 2] 2 SO 3(g)

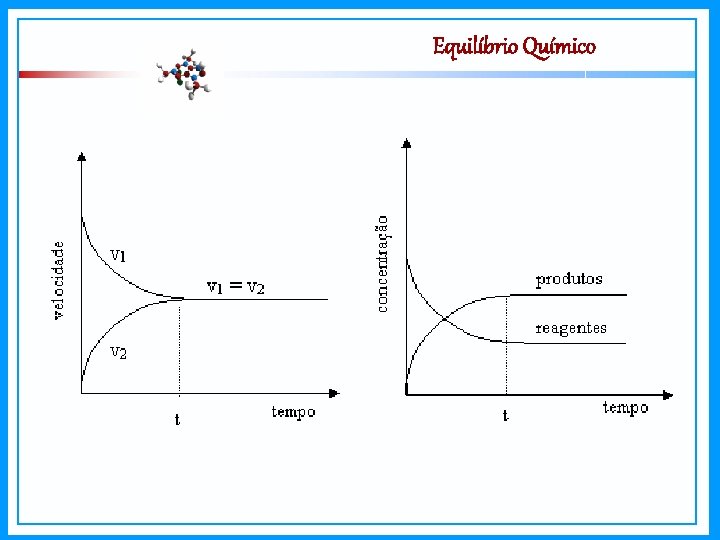
Equilíbrio Químico Quando uma reação atinge o equilíbrio químico? Quando Vd = Vi ≠ 0 [reagentes] e [produtos] constantes A + B v 1 v 2 ? - No início da reação [A] e [B] são máximos V 1 = max - No início da reação [C] e [D] = zero V 2 = zero

Equilíbrio Químico - No decorrer da reação A + B v 2 v 1 - [A] e [B] V 1 = - [C] e [D] V 2 = C+D

Equilíbrio Químico - Equilíbrio químico V 1 = V 2 ≠ 0 As reações não cessam - V 1 ƒ ([A] e [B]) - V 2 f ([C] e [D]) cte cte

Equilíbrio Químico

Equilíbrio Químico Constante de Equilíbrio Kc V 1 = V 2

Equilíbrio Químico Ex. : Indique a expressão da constante de equilíbrio para as reações a seguir: a) 2 A 2(g) + B 3(g) [C 2(g)]. [D 3(g)]2 Kc = [A(g)]2. [B 3(g)] b) 3 A 2(s) + 2 B(g) [C(g)]2 Kc = [B(g)]2 C 2(g) + 2 D 3(g) = (mol/L)3 2 C(g) + 2 D(s)

Exercício Num recipiente de 5 L, a uma dada temperatura, misturamse O 2 e CO. Atingido o equilíbrio, constata-se a existência de 3 mols CO, 1 mol O 2 e 2 mols CO 2. Calcule o valor da constante de equilíbrio em termos das concentrações. n 1 = 3 = 0. 6 mol/L V 5 [O 2] = n 1 = 0, 2 mol/L V 5 n 1 = 2 = 0. 4 mol/L [CO 2] = V 5 [CO] =
![Exercício CO 22 Kc CO2 O 2 0 42 0 62 x Exercício [CO 2]2 Kc = [CO]2. [O 2] 0. 42 = 0, 62 x](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-26.jpg)
Exercício [CO 2]2 Kc = [CO]2. [O 2] 0. 42 = 0, 62 x 0, 2 = 2, 2 (mol/L) -1

Deslocamento de Equilíbrio Fotores que afetam o equilíbrio químico Concentração A+B C + D

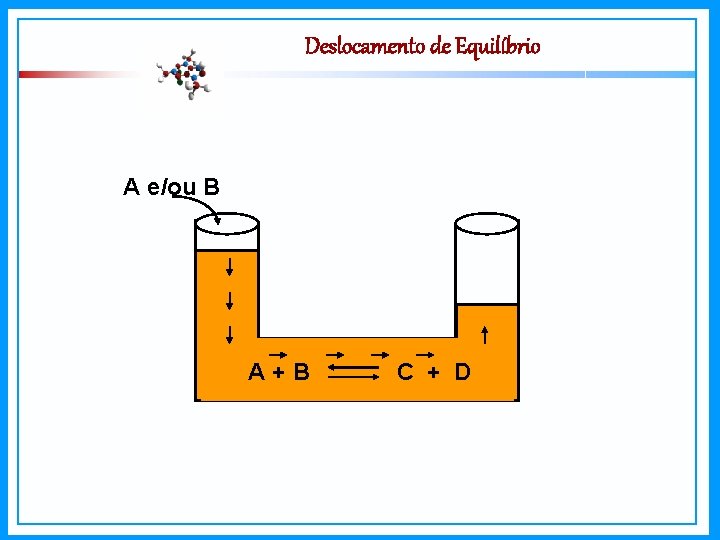
Deslocamento de Equilíbrio A e/ou B A+B C + D

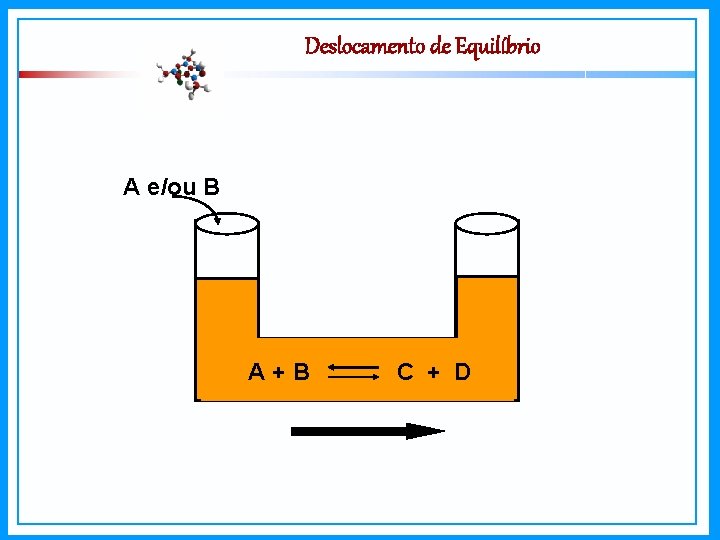
Deslocamento de Equilíbrio A e/ou B A+B C + D

Deslocamento de Equilíbrio Lei de Guldberg-Waage: - Quantidade de um participante favorece a reação que transforma esse participante em outro(s) - Quantidade de um participante favorece a reação que form esse participante.

Exercício Na reação H 2 + I 2 velocidade da reação: ( ) Aumenta 4 vezes ( ) Aumenta 2 vezes ( ) Diminui 2 vezes 2 HI, se duplicarmos a [H 2] a
![Exercício H 2 I 2 V k H 2 I 2 H Exercício H 2 + I 2 V = k. [H 2]. [I 2] [H](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-32.jpg)
Exercício H 2 + I 2 V = k. [H 2]. [I 2] [H 2] = x [I 2] = y Início Vi = ki. x. y 2 HI
![Exercício Início Vi k x y Duplicamos H 2 2 x Final Exercício Início Vi = k. x. y Duplicamos [H 2] = 2 x Final](https://slidetodoc.com/presentation_image_h2/86b16aff258091e03c6ab32ffcbfc1a4/image-33.jpg)
Exercício Início Vi = k. x. y Duplicamos [H 2] = 2 x Final Vf = k. 2 x. Y Vi = k. x. y Vf k. 2 x. y Vi = 1 Vf 2 Vf = 2. V i Velocidade aumentou 2 vezes

Deslocamento de Equilíbrio Temperatura - Reação endotérmica A + B + calor C + D Temperatura - Reação exotérmica A + B C + D + calor Temperatura

Deslocamento de Equilíbrio Lei de Van´t Hoff: - Temperatura provoca o deslocamento do equilíbrio → reação absorve calor (Endotermica) - Temperatura provoca o deslocamento do equilíbrio → reação libera calor (Exotérmica) Endotérmica → ∆H > 0 Exotérmica → ∆H < 0

Deslocamento de Equilíbrio Ex. : M + P - 20 kcal M + P ∆H= -20 kcal X + Y + 20 kcal Se Temperatura Calor Deslocamento para a esquerda [M] e [P] [X] e [Y] e Kc = [X]. [Y] [M]. [P]

Deslocamento de Equilíbrio Pressão Lei de Robin: - Pressão provoca o deslocamento do equilíbrio → reação contração de volume - Pressão provoca o deslocamento do equilíbrio → reação expansão de volume Obs. : Sistemas em equilíbrio com participantes gasosos

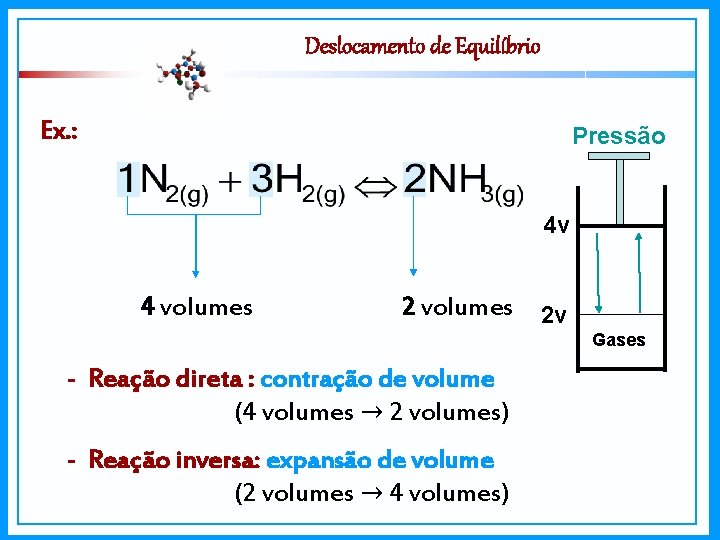
Deslocamento de Equilíbrio Ex. : Pressão 4 v 4 volumes 2 v Gases - Reação direta : contração de volume (4 volumes → 2 volumes) - Reação inversa: expansão de volume (2 volumes → 4 volumes)

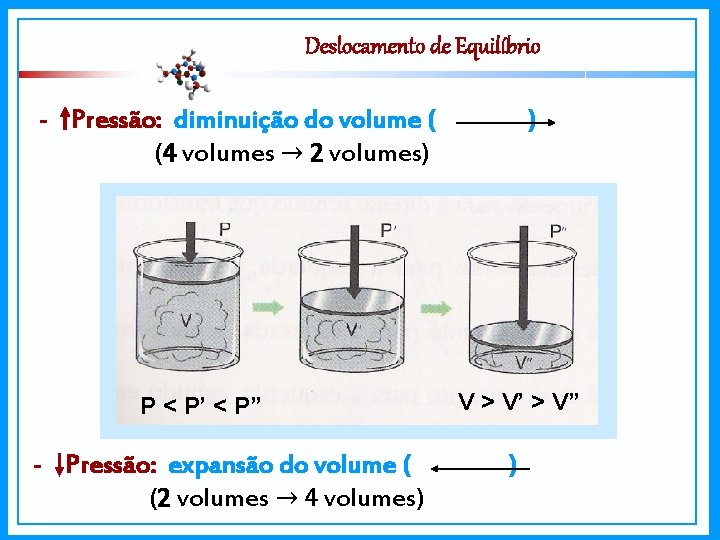
Deslocamento de Equilíbrio - Pressão: diminuição do volume ( (4 volumes → 2 volumes) P < P’ < P” - Pressão: expansão do volume ( (2 volumes → 4 volumes) ) V > V’ > V” )

Equilíbrio Químico de Gases Constante de Equilíbrio Pressões parciais , onde:

Considerações Finais Cinética Química; Equilíbrio Químico; Fatores que afetam o Equilíbrio Químico; Equilíbrio Químico de Gases.
