Universidade Federal da Paraba Centro de Cincias Exatas

Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Prof. Dr. Ary da Silva Maia O BLOCO p (GRUPOS 16 a 18)

Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Prof. Dr. Ary da Silva Maia O Grupo 16

O GRUPO 16 (Grupo do Oxigênio): Os elementos (O, S, Se, Te, Po): 3 ametais, 1 semi-metal e 1 metal. Todos os elementos são sólidos, exceto o oxigênio. Todos apresentam várias formas alotrópicas. Maior quantidade de estados alotrópicos : S. Comportamento diferenciado do O: Menor raio atômico. Ausência de orbitais d. Eletronegatividade muito alta. Prof. Dr. Ary Maia Junho 2010 3
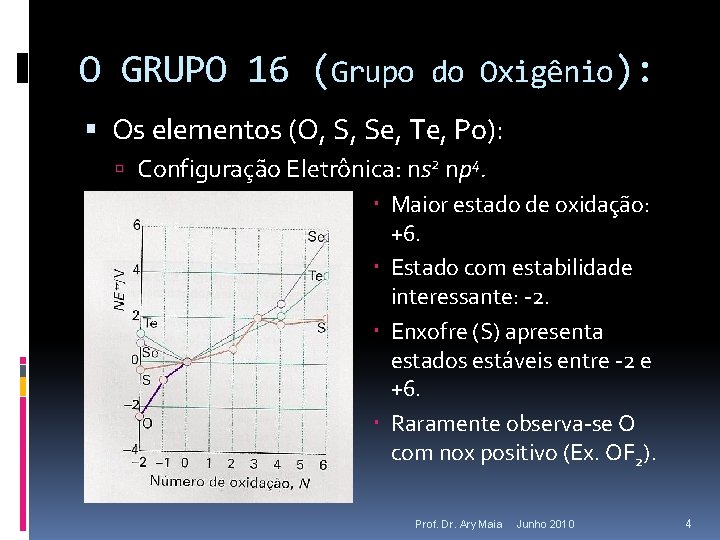
O GRUPO 16 (Grupo do Oxigênio): Os elementos (O, S, Se, Te, Po): Configuração Eletrônica: ns 2 np 4. Maior estado de oxidação: +6. Estado com estabilidade interessante: -2. Enxofre (S) apresenta estados estáveis entre -2 e +6. Raramente observa-se O com nox positivo (Ex. OF 2). Prof. Dr. Ary Maia Junho 2010 4

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Oxigênio: Apresenta-se na forma de 2 alótropos (O 2 e O 3). 21% em massa da atmosfera, 3º elemento mais abundante no Sol, Elemento mais abundante na superfície da Lua (46%), Elemento mais abundante na crosta terrestre (46%). Gás incolor, inodoro e reativo. Solúvel em água (25 o. C e 1 atm) 3, 08 cm 3/100 cm 3 água doce, < 2, 0 cm 3/100 cm 3 água salgada. 10 x mais solúvel em solventes orgânicos. Prof. Dr. Ary Maia Junho 2010 5

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Oxigênio (cont. ): Obtido facilmente a partir da atmosfera. Principal utilidade industrial é a fabricação de aço. Diversos processos de oxidação. A molécula de O 2 é paramagnética. Esta configuração eletrônica, através da TOM pode prever três estados diferentes para a molécula de oxigênio: Dois estados excitados (singletos) Um estado fundamental (tripleto). Prof. Dr. Ary Maia Junho 2010 6
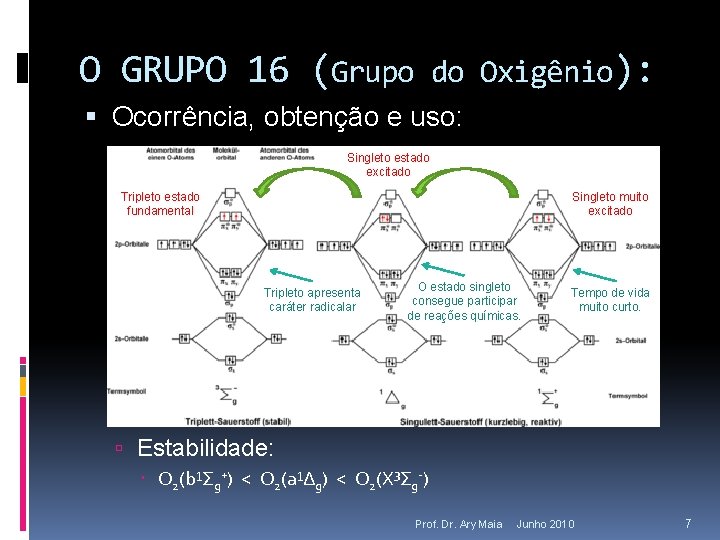
O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Singleto estado excitado Tripleto estado fundamental Singleto muito excitado Tripleto apresenta caráter radicalar O estado singleto consegue participar de reações químicas. Tempo de vida muito curto. Estabilidade: O 2(b¹Σg+) < O 2(a¹Δg) < O 2(X³Σg-) Prof. Dr. Ary Maia Junho 2010 7

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ozônio: Molécula angular (117º), diamagnética. Gás azul (Líquido azul escuro e sólido violeta). Cheiro pungente (ozein (grego): que tem cheiro). Produzido por descarga elétrica ou radiação ultravioleta sobre o O 2. Só é menos oxidante que F 2, O atômico, radical OH e o íon perxenato (Xe. O 6)4 Absorve fortemente na região de 220 a 290 nm (impede penetração de raios UV na atmosfera terrestre). Prof. Dr. Ary Maia Junho 2010 8

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ozônio (cont. ): Mecanismo de Chapman (1964). A formação do Ozônio ocorre na Estratosfera a uma altitude média de 30 km onde os radiação solar ultravioleta tem tamanho de onda menor que 242 nm O 2 + h O + O (1) O átomo de O reage rapidamente com O 2 na presença de uma terceira molécula M (O 2 ou N 2), para formar o Ozônio O + O 2 + M O 3 + M (2) Na presença de radiação na faixa de 240 a 320 nm temos O 3 + h O 2 + O (3) E também podemos ter a seguinte reação O 3 + O O 2 + O 2 (4) Prof. Dr. Ary Maia Junho 2010 9
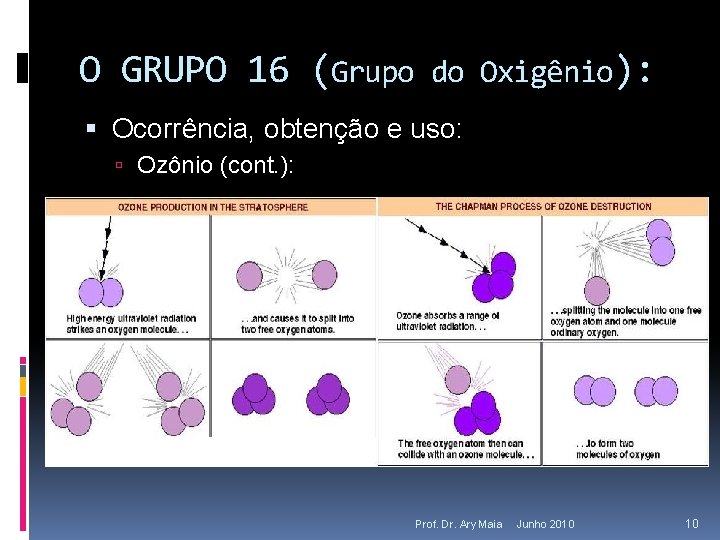
O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ozônio (cont. ): Prof. Dr. Ary Maia Junho 2010 10

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ozônio (cont. ): A destruição de Ozônio no ciclo de Chapman é dado por X + O 3 XO + O 2 XO + O X + O 2 O 3 + O O 2 + O 2 onde X pode ser H, OH, NO, Cl ou Br, dando origem a diferentes ciclos reacionais: Ciclo do HOx – onde HOx são radicais contendo H (H, OH, HO 2). Ciclo do NOx – onde NOx é principalmente o NO. Ciclo do Cl. Ox – onde Cl. Ox são principalmente os CFCs. Prof. Dr. Ary Maia Junho 2010 11

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ciclo do HOx – onde HOx são radicais contendo H (H, OH, HO 2). H + O 3 OH + O 2 OH + O 3 HO 2 + O 2 OH + O 2 HO 2 + O OH + O 2 O 3 + O O 2 + O 2 OH + O 2 OH + O 3 HO 2 + O 2 H + O 2 + M HO 2 + M HO 2 + O 3 OH + O 2 HO 2 + O OH + O 2 O 3 + O 3 O 2 + O 2 O + M O 2 + M Prof. Dr. Ary Maia Junho 2010 12

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ciclo do NOx – onde NOx é principalmente o NO. NO + O 3 NO 2 + O 2 NO 2 + O NO + O 2 O 3 + O O 2 + O 2 NO + O 3 NO 2 + O 2 NO 2 + O 3 NO 3 + O 2 NO 3 + hν NO + O 2 2 O 3 3 O 2 Prof. Dr. Ary Maia Junho 2010 13

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Ciclo do Cl. Ox – onde Cl. Ox são principalmente os CFCs. Formação do radical Cl CFCl 3 + hν CFCl 2 + Cl CF 2 Cl 2 + hν CF 2 Cl + Cl Cl + O 3 Cl. O + O 2 Reação com o O 3 Cl. O + O Cl + O 2 O 3 + O O 2 + O 2 Prof. Dr. Ary Maia Junho 2010 14

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Enxofre: Ocorre principalmente na forma de: Elemento nativo. Nos meteoritos. Nos vulcões. H 2 S e compostos organossulfurados do petróleo. Alguns minérios como galena (Pb. S) e barita (Ba. SO 4). Obtido por dois processos: Processo Frasch: Depósitos subterrâneos são forçados para a superfície usando-se água superaquecida, vapor e ar comprimido (em desuso). Processo Claus: 2 H 2 S + 3 O 2 2 SO 2 + 2 H 2 O 2 H 2 S + SO 2 3 S + 2 H 2 O Prof. Dr. Ary Maia Junho 2010 15
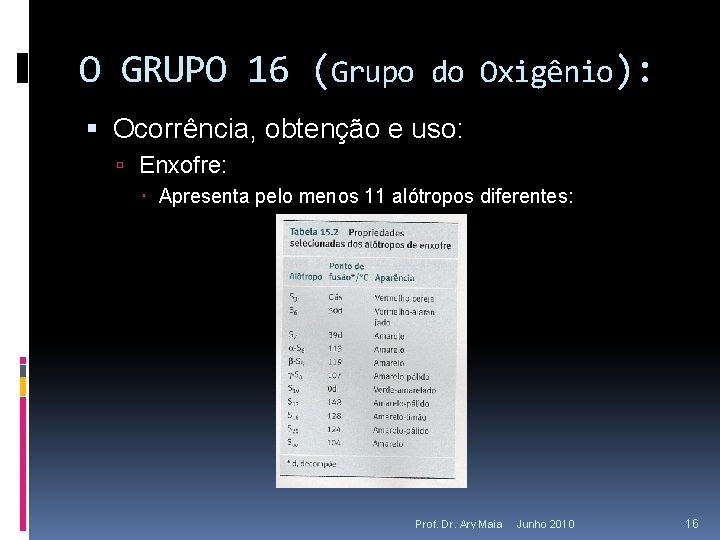
O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Enxofre: Apresenta pelo menos 11 alótropos diferentes: Prof. Dr. Ary Maia Junho 2010 16

O GRUPO 16 (Grupo do Oxigênio): Ocorrência, obtenção e uso: Enxofre (cont. ): É reativo reagindo com diversos elementos à temperatura ambiente. Maior parte do S produzido é usado na fabricação de ácido sulfúrico. Selênio, Telúrio e Polônio: Se e Te ocorrem na forma de sulfetos presentes na lama eletrolítica do refino de cobre. Selênio, semelhante ao enxofre apresenta várias formas alotrópicas. Telúrio e Polônio são altamente tóxicos. (Po também é radioativo). Prof. Dr. Ary Maia Junho 2010 17
- Slides: 17