Universidade Federal da Paraba Centro de Cincias Exatas

Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Prof. Dr. Ary da Silva Maia PRINCÍPIOS DE QUÍMICA INORG NICA NOMENCLATURA

COMPOSTOS DE COORDENAÇÃO: • Natureza elétrica das espécies coordenadas: – ADUTOS: • Espécie coordenada apresenta carga elétrica nula: – Ex: [Co(NH 3)3 Cl 3], [Cl 3 BNH 3], [Fe(CO)5] – SAIS COMPLEXOS OU ÍONS COMPLEXOS: • Espécie coordenada apresenta carga negativa ou positiva: – Ex: [Co(NH 3)6]Cl 3 , K 2[Pt. Cl 6], [Cr(NH 3)6][Cu. Cl 5], [Cr(H 2 O)6]3+ , [Pt(CN)4]2 - Março/2010 Prof. Dr. Ary Maia 2

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 1. O ânion é designado em primeiro lugar (apesar de ser escrito à direita do cátion), depois o cátion precedido da preposição de. 2. Ao se escrever a fórmula do complexo, os ligantes são escritos na ordem: aniônicos, neutros (moleculares) e catiônicos. Se houver mais de um ligante de mesma natureza, esses são colocados em ordem alfabética. Março/2010 Prof. Dr. Ary Maia 3

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 3. Ao se denominar os complexos, os ligantes são citados em primeiro lugar em ordem alfabética, seguidos do átomo central com o NOX em algarismo romano entre parênteses. 4. Se houverem ligantes de mesma natureza, usam-se os prefixos numéricos di, tri, tetra, etc. para indicar o número desses ligantes. Se o ligante tiver em sua estrutura prefixos numéricos (ligantes orgânicos) usam-se, para se evitar ambigüidades, os prefixos bis, tris, tetrakis, pentakis, etc. e o nome dos ligantes entre parênteses. Março/2010 Prof. Dr. Ary Maia 4

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 5. Os ligantes terminados em eto, ito ou ido mudarão a terminação para o e os terminados em ato não sofrerão alteração. Íon Ligante Cl- cloreto Cloro O 2 - óxido Oxo OH- hidróxido Hidroxo SO 42 - sulfato Sulfato NO 3 - nitrato Nitrato Exceção: Hidreto (H-) não sofre alteração. Também se usa hidro. Março/2010 Prof. Dr. Ary Maia 5

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 6. Os ligantes moleculares mantém os seus respectivos nomes. Exceções: Água (aquo), Amônia (amin), Monóxido de carbono (carbonil). 7. Em complexos polinucleares quando o ligante atuar entre dois centros de coordenação, ele é precedido da letra (mu) separada por hífens repetida antes do nome de cada ligante diferente atuando como ponte. Quando a simetria do complexo permitir pode-se usar um nome simplificado indicando o nome do ligante atuando como ponte precedida de seguido do número de ligantes e de átomos ou íons centrais com os seus respectivos prefixos numéricos. Março/2010 Prof. Dr. Ary Maia 6
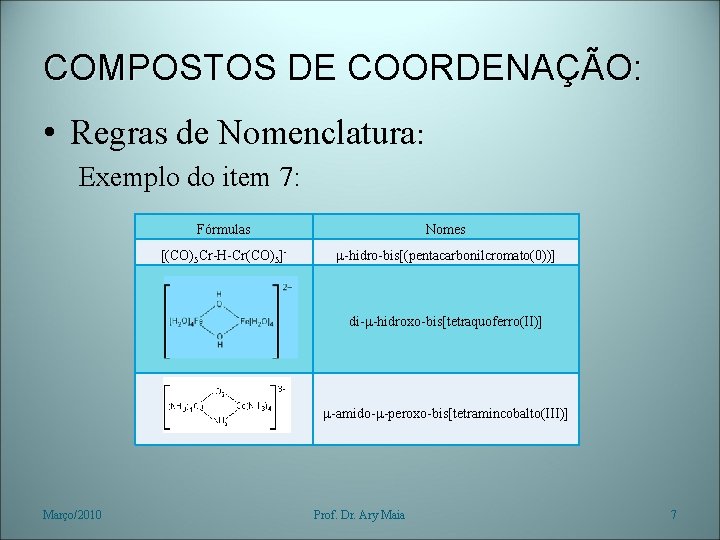
COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: Exemplo do item 7: Fórmulas Nomes [(CO)5 Cr-H-Cr(CO)5]- -hidro-bis[(pentacarbonilcromato(0))] di- -hidroxo-bis[tetraquoferro(II)] -amido- -peroxo-bis[tetramincobalto(III)] Março/2010 Prof. Dr. Ary Maia 7

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 8. Se o complexo for aniônico, a terminação é ato seguida do NOX do átomo central em algarismo romano e entre parênteses. Nesse caso, o termo íon antes do nome do complexo é desnecessário, já que o sufixo ato indica que o mesmo é um ânion. 9. No caso do ligante ambidentado, indica-se qual o átomo por meio do qual ocorre a ligação, se houver necessidade usa-se também a nomenclatura alternativa abaixo: Março/2010 M NO 2 nitro M SCN tiocianato M ONO nitrito M NCS isotiocianato Prof. Dr. Ary Maia 8

COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: 10. O oxigênio (O 2) atuando como ligante chama-se dioxigênio, já o nitrogênio atuando como ligante chama-se dinitrogênio. • Nomenclatura dos principais ligantes: 1. nions terminados em eto: Março/2010 Espécies Nome do íon Nome do ligante F- Fluoreto Fluoro Cl- Cloreto Cloro Br- Brometo Bromo I- Iodeto Iodo CN- Cianeto Ciano NH 2 - Amideto Amido Prof. Dr. Ary Maia 9

COMPOSTOS DE COORDENAÇÃO: 2. nions terminados em ido: Espécies Nome do íon Nome do ligante OH- Hidróxido Hidroxo O 2 - Óxido Oxo O 22 - Peróxido Peroxo 3. nions terminados em ato: Março/2010 Espécies Nome do íon Nome do ligante CO 32 - Carbonato NO 3 - Nitrato SO 42 - Sulfato C 2 O 42 - Oxalato CH 3 COO- Acetato CH 3 COCH-3 Acetilacetonato (ACAC) Prof. Dr. Ary Maia 10

COMPOSTOS DE COORDENAÇÃO: 4. Radicais derivados de hidrocarbonetos: • Manutenção do nome do radical. Espécies Nome do radical Nome do ligante CH 3 Metil (Me) C 2 H 5 Etil (Et) C 6 H 5 Fenil (Ph ou ) C 5 H 5 Ciclopentadienil (Cp) 5. Ligantes moleculares terminados em a: • Março/2010 Substituição do a por o: Espécies Nome da molécula Nome do ligante C 5 H 5 N Piridina Piridino (Py) C 10 H 8 N 2 Dipiridina Dipiridino (Dipy) C 2 H 8 N 2 Etilenodiamina Etilenodiamino (En) P(C 6 H 5)3 Trifenilfosfina Trifenilfosfino (PPh 3 ou P 3) Prof. Dr. Ary Maia 11

COMPOSTOS DE COORDENAÇÃO: 6. Ligantes com nomes específicos: Espécies Nome da espécie Nome do ligante H 2 O Água Áqua NH 3 Amônia Amino ou Amin CO Monóxido de carbono Carbonil NO Monóxido de nitrogênio Nitrosil O 2 (*) Oxigênio (molecular) Dioxigênio N 2 (*) Nitrogênio (molecular) Dinitrogênio H- Hidreto Hidro ou Hidreto * Nas formulas, esses ligantes devem ser escritos entre parênteses. Março/2010 Prof. Dr. Ary Maia 12
![COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: – EXEMPLOS: [Ag(NH 3)2]+ Diaminprata(I) [Mn(CO)5]- Pentacarbonilmanganato(-I) COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: – EXEMPLOS: [Ag(NH 3)2]+ Diaminprata(I) [Mn(CO)5]- Pentacarbonilmanganato(-I)](http://slidetodoc.com/presentation_image_h/9c232ccfc2929b0accf6099442bad988/image-13.jpg)
COMPOSTOS DE COORDENAÇÃO: • Regras de Nomenclatura: – EXEMPLOS: [Ag(NH 3)2]+ Diaminprata(I) [Mn(CO)5]- Pentacarbonilmanganato(-I) [Co(NH 3)6]3+ Hexamincobalto(III) [Fe(SCN)6]3 - Hexatiocianatoferrato(III) [Mn(CO)6]+ Hexacarbonilmanganês(I) cis-[Pt(NH 3)2 Cl 2]+2 cis-diaminadicloroplatina(II) [Ni(CO)4] Tetracarbonilniquel(0) [Co(NH 3)6]Cl 3 Cloreto de hexaminocobalto [Co(NH 3)6][Co. F 6] Hexafluorocobaltato(III) de hexamincobalto(III) K 2[Pt. Cl 6] Hexacloroplatinato(IV) de potássio Março/2010 Prof. Dr. Ary Maia 13

Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Prof. Dr. Ary da Silva Maia PRINCÍPIOS DE QUÍMICA INORG NICA NOMENCLATURA Para maiores detalhes consulte http: //www. quimica. ufpb. br/arymaia ou mande e-mail para arymaia@quimica. ufpb. br
- Slides: 14