UNIVERSIDAD PRIVADA JUAN MEJA BACA ENLACE QUMICO TEORIA

UNIVERSIDAD PRIVADA JUAN MEJÍA BACA ENLACE QUÍMICO TEORIA DE LEWIS Profesor: Ing. Alberto Carrasco Tineo

TEORIA DE LEWIS DEL ENLACE COVALENTE Se basa en las siguientes hipótesis: • Los átomos para conseguir 8 e– en su última capa comparten tantos electrones como le falten para completar su capa (regla del octeto). • Cada pareja de e– compartidos forma un enlace. • Se pueden formar enlaces sencillos, dobles y triples con el mismo átomo. 2
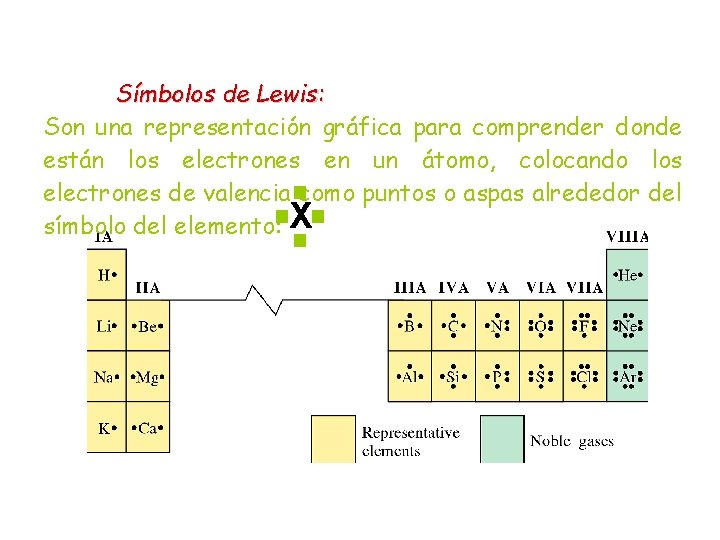
Símbolos de Lewis: Son una representación gráfica para comprender donde están los electrones en un átomo, colocando los electrones de valencia como puntos o aspas alrededor del v símbolo del elemento: X v


REGLA DEL OCTETO En general los elementos representativos configuraciones electrónicas de gases nobles. adquieren Los átomos se unen compartiendo electrones hasta conseguir completar la última capa con 8 e- (4 pares de e-) es decir conseguir la configuración de gas noble: s 2 p 6

Tipos de pares de electrones: 1 - Pares de e- compartidos entre dos átomos (representado con una línea entre los at. unidos) · enlaces sencillos · enlaces dobles · enlaces triples 2 - Pares de e- no compartidos (ó par solitario)
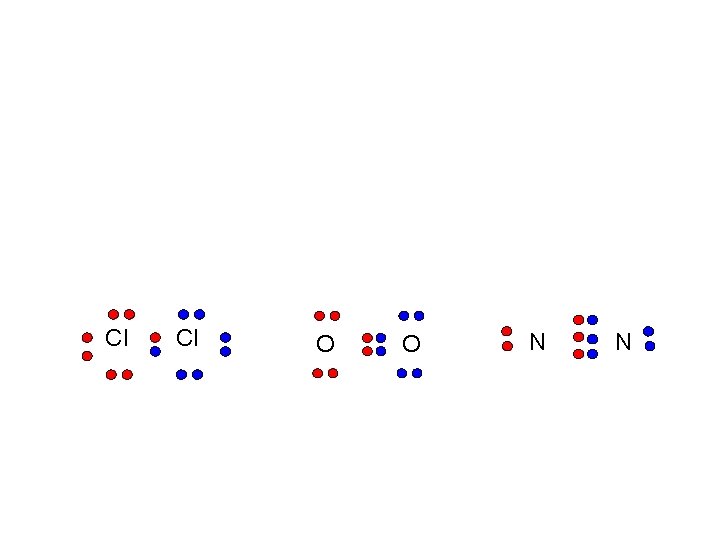
Cl Cl O O N N

Estructura de Lewis: Es una representación simplificada de los enlaces de una molécula, utilizando un punto por cada electrón que forman el enlace de la molécula.

COMO DIBUJAR ESTRUCTURAS DE LEWIS

Escriba la fórmula puntual de Lewis para las siguientes moleculas. 1 - Se suman los e- de valencia de los átomos presentes en la molécula. Para un anión poliatómico se le añade un e- más por cada carga negativa y para un catión se restan tantos electrones como cargas positivas. 2 - Se dibuja una estructura básica lo mas simétrica posible, en general el átomo menos electronegativo ocupa la posición central. 3 - Se calcula el nº de e- de valencia quedan disponibles. 4 - Se distribuyen los e- de forma que se complete un octeto para cada átomo. Ejemplo 1: CH 4 1) C: 1 s 22 s 2 p 2 4 e. H: 1 s 1 1 e- x 4= 4 e 2) 8 e- Ejemplo 2: H 2 CO 1) C: 1 s 22 s 2 p 2 4 e. H: 1 s 1 1 e- x 2= 2 e. O: 1 s 22 s 2 p 4 6 e- 12 e- 2) 3) e- de v. libres: 12 -6= 6 4)
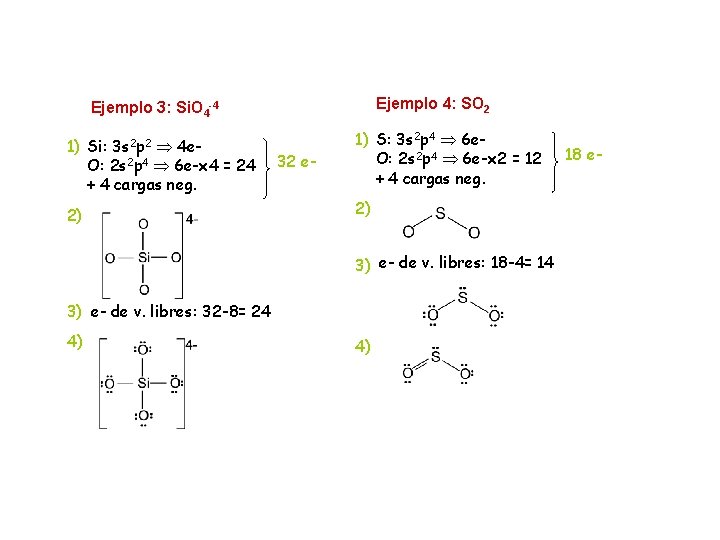
Ejemplo 4: SO 2 Ejemplo 3: Si. O 4 -4 1) Si: 3 s 2 p 2 4 e. O: 2 s 2 p 4 6 e-x 4 = 24 + 4 cargas neg. 2) 32 e- 1) S: 3 s 2 p 4 6 e. O: 2 s 2 p 4 6 e-x 2 = 12 + 4 cargas neg. 2) 3) e- de v. libres: 18 -4= 14 3) e- de v. libres: 32 -8= 24 4) 4) 18 e-

RESONANCIA • No siempre existe una única estructura de Lewis que pueda explicar las propiedades de una molécula o ion. • Existen moléculas que pueden tener varias estructuras equivalentes sin que se pueda dar preferencia a una sobre las demás
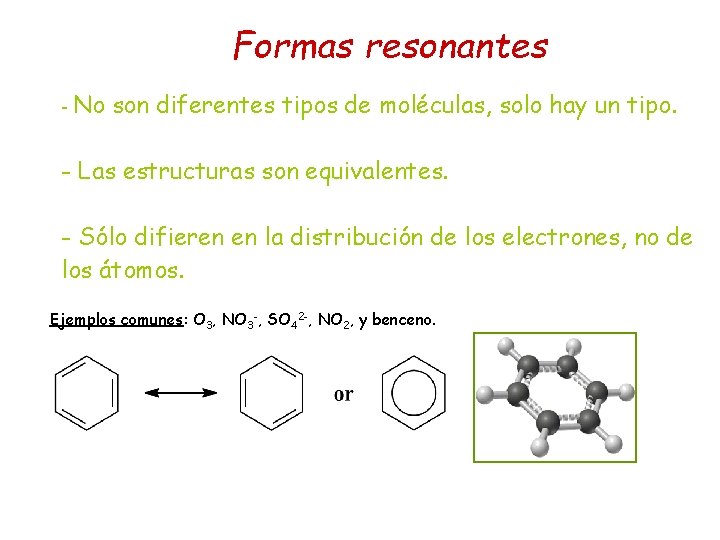
Formas resonantes - No son diferentes tipos de moléculas, solo hay un tipo. - Las estructuras son equivalentes. - Sólo difieren en la distribución de los electrones, no de los átomos. Ejemplos comunes: O 3, NO 3 -, SO 42 -, NO 2, y benceno.
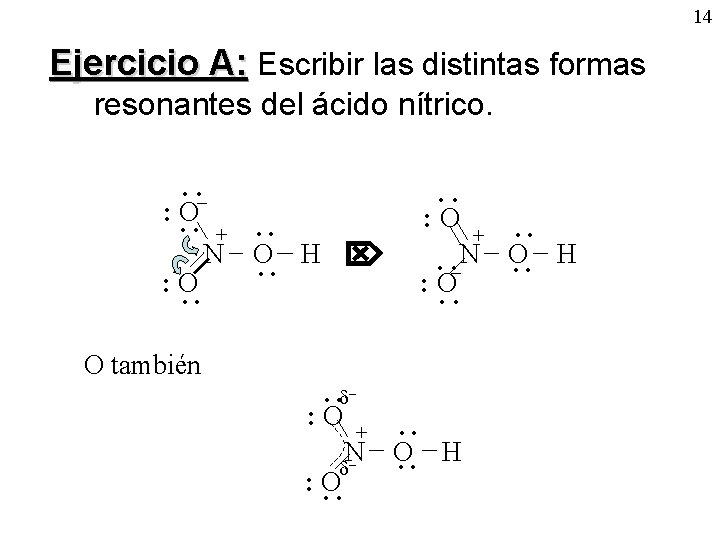
14 Ejercicio A: Escribir las distintas formas resonantes del ácido nítrico. · ·– : O ·· + ·· N O H ·· : O ·· ·· : O + N · ·– : O ·· O también · · – : O + ·· N O H – ·· : O ·· ·· O H ··

Carga Formal ØEs un medio para contabilizar los electrones de valencia. La carga formal es la diferencia entre el nº de e- de valencia y el nº de easignado en la estructura de Lewis (los e- no compartidos y la mitad de los e - compartidos). X= nº de e- de valencia Cf = X – (Y + Z/2) Y= nº de e- no compartidos Z= nº de e- compartidos En ocasiones es posible escribir más de una estructura de Lewis para una misma molécula: I II Utilizando el concepto de carga formal podemos determinar cual es la estructura de Lewis más probable: El valor de Cf sea mas proximo a 0 La Cf negativa debe estar localizada sobre el átomo + electronegativo
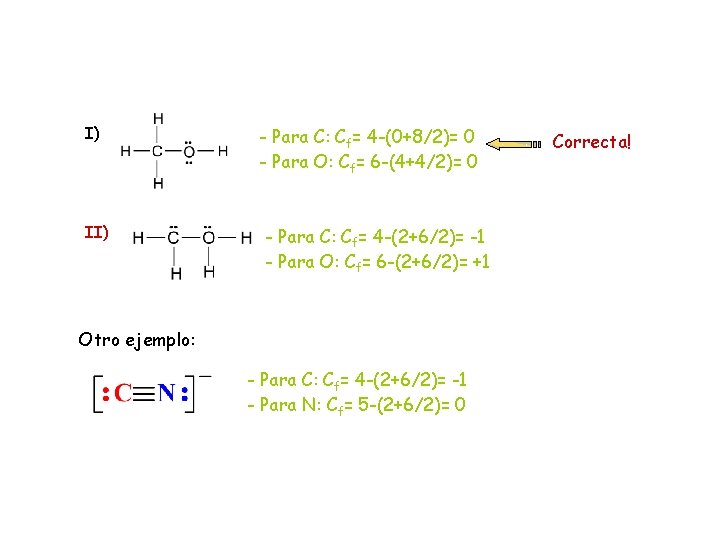
I) II) - Para C: Cf= 4 -(0+8/2)= 0 - Para O: Cf= 6 -(4+4/2)= 0 - Para C: Cf= 4 -(2+6/2)= -1 - Para O: Cf= 6 -(2+6/2)= +1 Otro ejemplo: - Para C: Cf= 4 -(2+6/2)= -1 - Para N: Cf= 5 -(2+6/2)= 0 Correcta!
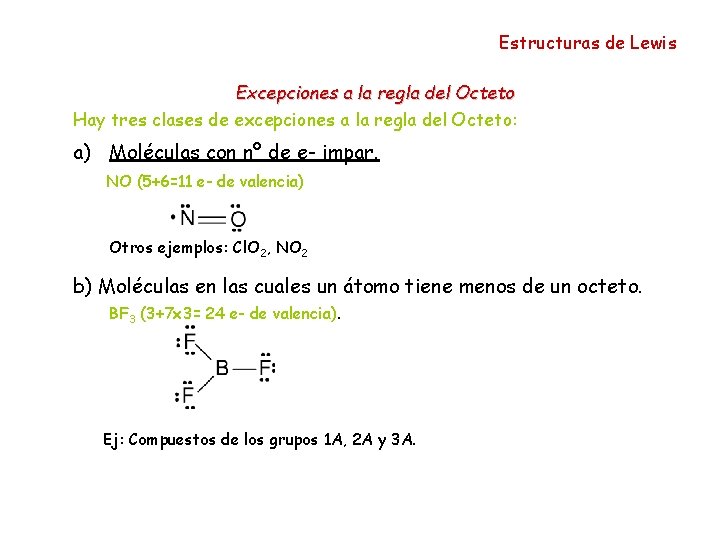
Estructuras de Lewis Excepciones a la regla del Octeto Hay tres clases de excepciones a la regla del Octeto: a) Moléculas con nº de e- impar. NO (5+6=11 e- de valencia) Otros ejemplos: Cl. O 2, NO 2 b) Moléculas en las cuales un átomo tiene menos de un octeto. BF 3 (3+7 x 3= 24 e- de valencia). Ej: Compuestos de los grupos 1 A, 2 A y 3 A.
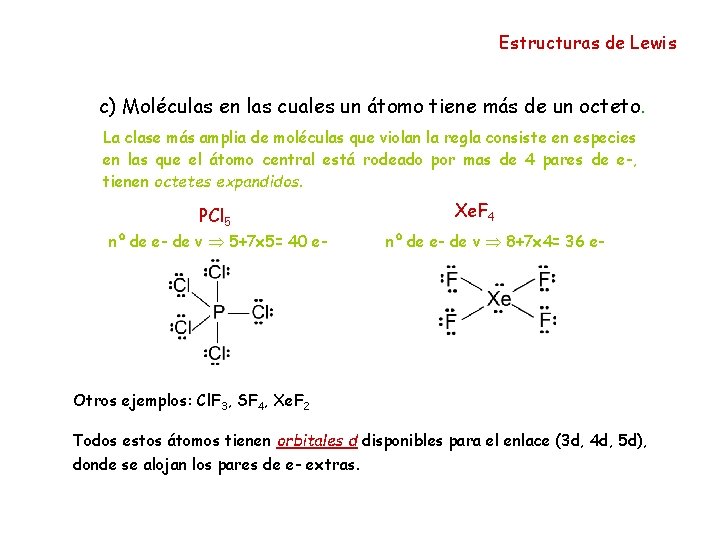
Estructuras de Lewis c) Moléculas en las cuales un átomo tiene más de un octeto. La clase más amplia de moléculas que violan la regla consiste en especies en las que el átomo central está rodeado por mas de 4 pares de e-, tienen octetes expandidos. PCl 5 nº de e- de v 5+7 x 5= 40 e- Xe. F 4 nº de e- de v 8+7 x 4= 36 e- Otros ejemplos: Cl. F 3, SF 4, Xe. F 2 Todos estos átomos tienen orbitales d disponibles para el enlace (3 d, 4 d, 5 d), donde se alojan los pares de e- extras.

Excepciones a la teoría de Lewis • Moléculas tipo NO y NO 2 que tienen un número impar de electrones. • Moléculas tipo Be. Cl 2 o BF 3 con marcado carácter covalente en las cuales el átomo de Be o de B no llegan a tener 8 electrones. • Moléculas tipo PCl 5 o SF 6 en las que el átomo central tiene 5 o 6 enlaces (10 o 12 e– ). 19

OCTETO INCOMPLETO • El boro el berilio y otros elementos forman compuestos sin que se cumpla la regla del octeto. • El boro tiene 6 electrones en su última capa en lugar de 8 cuando forma enlaces covalentes.
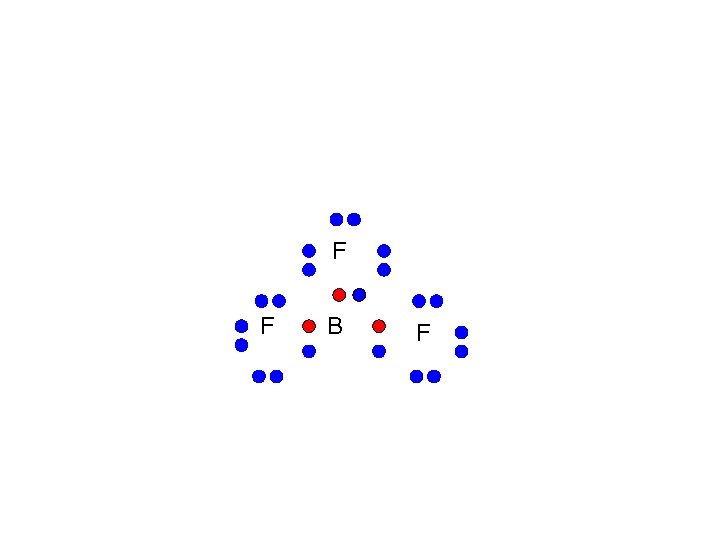
F F B F

OCTETO AMPLIADO • La regla del octeto se basa en que el último nivel es s 2 p 6 pero a partir del tercer nivel existen otros orbitales d , f al que pueden promocionar electrones. • Se obtiene estructuras que aunque no tienen configuración de gas noble, también son estables
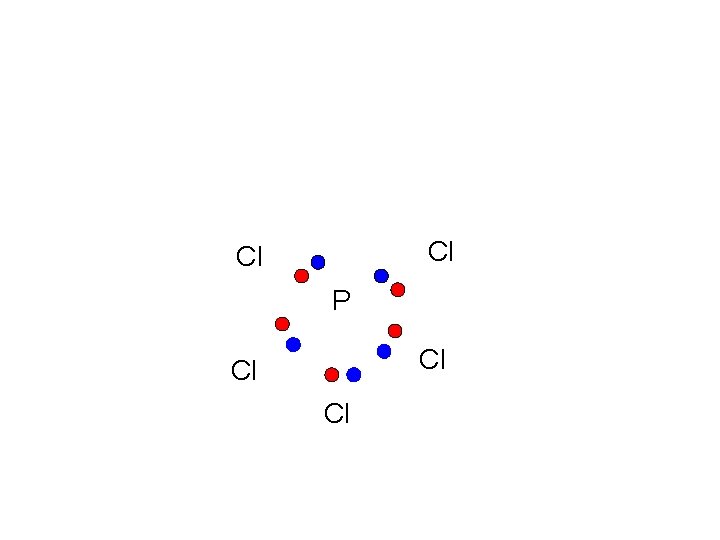
Cl Cl P Cl Cl Cl

REGLA DEL DUETO • Así como los elementos electronegativos, cumplen la regla del octeto, para alcanzar la configuración de un gas noble. El Hidrogeno, cumple la regla del dueto. • La regla del dueto consiste en que el H 2, al combinarse con otro elemento, ya sea en un enlace iónico o un enlace covalente, lo hace para completar su orbital con 2 electrones.
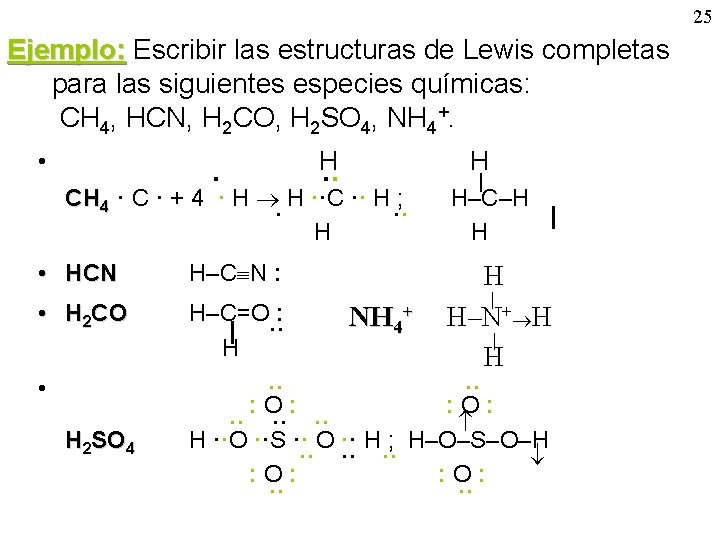
25 Ejemplo: Escribir las estructuras de Lewis completas para las siguientes especies químicas: CH 4, HCN, H 2 CO, H 2 SO 4, NH 4+. • · H ·· H CH 4 · C · + 4 · H H ··C ·· H ; · ·· H | H–C–H | H • HCN H–C N : • H 2 CO H–C=O : | ·· H • ·· ·· : O: ·· ·· ·· H ··O ··S ·· O ·· H ; H–O–S–O–H ·· ·· ·· : O: ·· ·· H 2 SO 4 NH 4+ H | H–N+ H | H

26 Ejemplo: a) Ordene según la polaridad creciente, basándote en los valores de electronegatividades de la tabla adjunta, los enlaces siguiente: H–F, H–O, H–N, H–C, C–O y C–Cl Elemento F O Cl N C S H Electronegat. 4, 0 3, 5 3, 0 2, 5 2, 1 b) la polaridad de la molécula de CH 4 ¿será igual o distinta de la de CCl 4? • a) H–C < C–Cl < H–N < C–O < H–F • b) El CH 4 es globalmente apolar ( = 0) pues la suma vectorial de los dipolos de cada enlace (dirigidos hacia el centro) se anula debido a sus geometría tetraédrica. El CCl 4 es igualmente apolar por la misma razón; sin embargo los dipolos de los enlaces están en esta ocasión dirigidos hacia fuera.

Ejercicio : 27 Explique: a) Si las estructuras de Lewis justifican la forma geométrica de las moléculas o si ésta se debe determinar experimentalmente para poder proponer la representación correcta. b) Si cada molécula se representa en todos los casos por una única formula estructural. c) Representar las estructuras de Lewis de las siguientes especies: H 2 O y NO 3 – d) ¿Justifican las representaciones de las moléculas anteriores la estabilidad de las mismas? a) Las estructuras de Lewis, indican el nº de enlaces que deberán formarse, pero no entra para nada en la dirección que tomarán éstos y, por tanto, en la geometría molecular. Por tanto, la geometría debe obtenerse experimentalmente, o acudir al modelo de repulsión de pares electrónicos o a la teoría de la hibridación. b) En principio sí, pero cuando existen formas resonantes hay más de una fórmula estructural para la misma molécula.
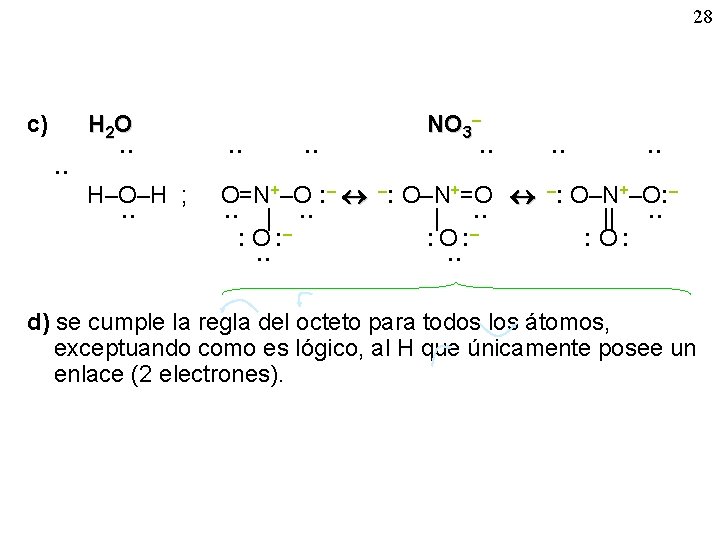
28 c) ·· H 2 O ·· H–O–H ; ·· ·· ·· NO 3– ·· ·· ·· O=N+–O : – –: O–N+=O –: O–N+–O: – ·· || ·· – – : O: ·· ·· d) se cumple la regla del octeto para todos los átomos, exceptuando como es lógico, al H que únicamente posee un enlace (2 electrones).

29 Ejercicio : Cuatro elementos diferentes A, B, C, D tienen número atómico 6, 9, 13 y 19 respectivamente. Se desea saber: a) El número de electrones de valencia de cada uno de ellos. b) Su clasificación en metales y no metales. c) La fórmula de los compuestos que B puede formar con los demás ordenándolos del más iónico al más covalente. a) A B C D Z=6 Z=9 Z = 13 Z = 19 2 -4 2 -7 2 -8 -3 2 -8 -8 -1 c) DB (más iónico) CB 3 b) No metal Metal AB 4 (más covalente)

Problemas 5. Escriba las estructuras de Lewis para las siguientes moléculas: a) b) c) d) HF CCl 4 CO CO 2

Problemas 6. Escriba las estructuras de Lewis para las siguientes moléculas: a) b) c) d) e) f) NH 4+ C 2 H 6 C 2 H 4 C 2 H 2 HCl HCN
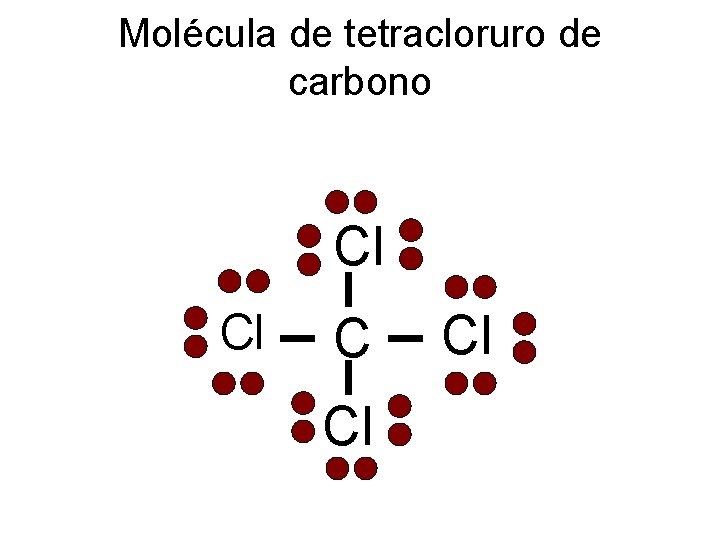
Molécula de tetracloruro de carbono Cl Cl Cl
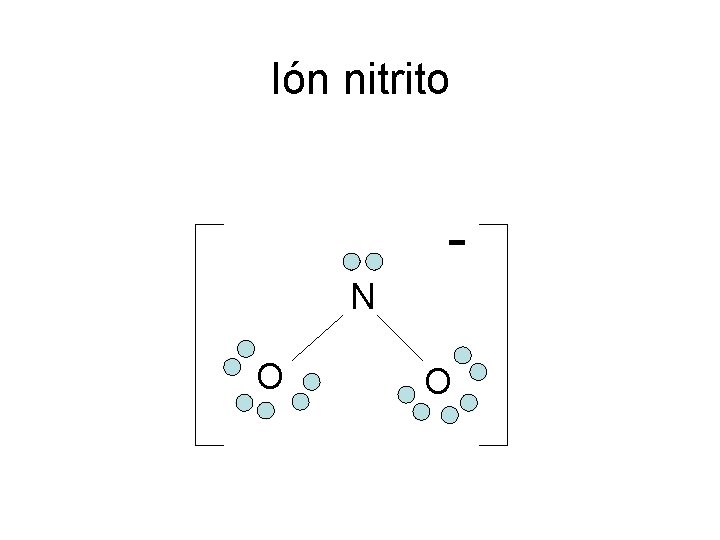
Ión nitrito N O O
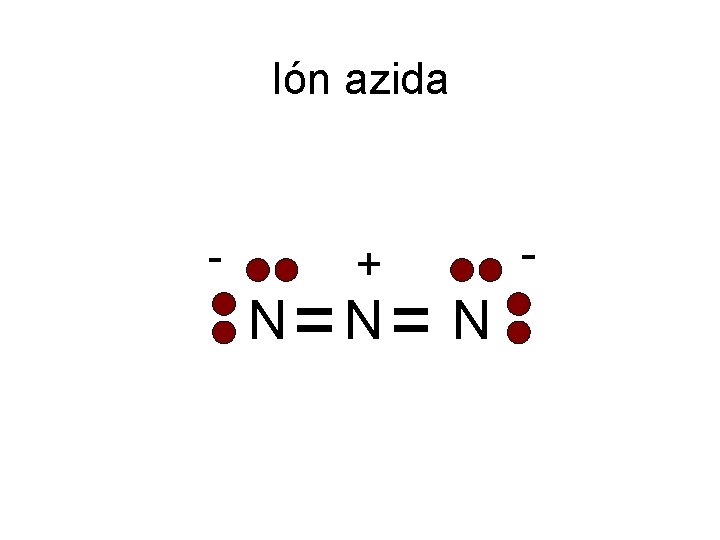
Ión azida - N + N - N
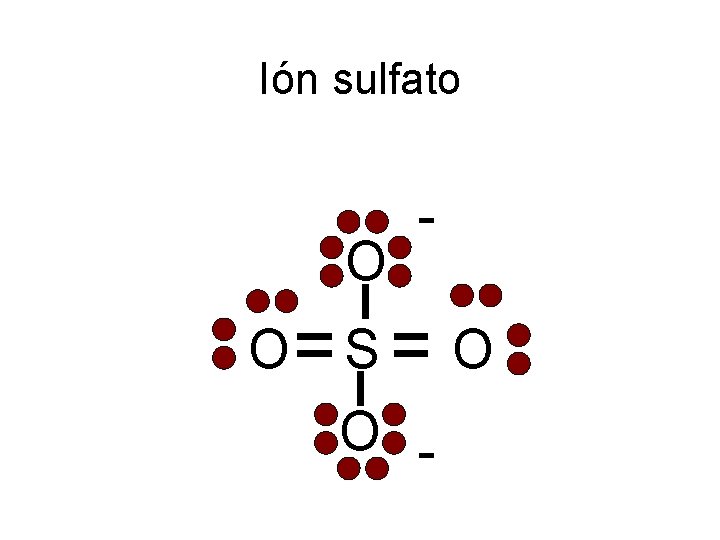
Ión sulfato O O - S O - O
Moléculas de lewis • Enlace simple F 2 Cl 2 HF H Cl HI H 2 O SH 2 NH 3 CH 4 • Enlace covalente dativo H 3 O + NH 4 + • Enlaces múltiples O 2 N 2 CO 2 CNH • CH 2=C H 2 • Octetos incompletos B Cl 3 BF 3 Al Cl 3 • Octetos ampliados H 2 SO 4 F 6 S P Cl 5 • Resonancia SO 3 NO 3 - C 6 H 6 O 3

Ejemplo: La configuración electrónica de un elemento: 37 a) ¿Permite conocer cuál es su situación en el sistema periódico? b) ¿Indica qué clase de enlaces puede formar con otros elementos? c) ¿Es suficiente información para saber si el elemento es sólido, líquido o gas? d) ¿Sirve para conocer si el elemento es o no molecular? Justifique las respuestas. a) Sí. b) Sí. c) No. d) Sí. Si acaba en “s” o d” se tratará de un elemento metálico y el compuesto no será molecular. Igualmente, los gases nobles (p 6) se encuentran como átomo aislados. Son moleculares los elementos no metálicos (p 2 - p 5).
- Slides: 37