Universidad Nacional Autnoma de Mxico Facultada de Estudios



























- Slides: 38

Universidad Nacional Autónoma de México Facultada de Estudios Superiores Cuautitlán C-1 Bioquímica Diagnostica Grupo: 1151 Química I Numero de Equipo 8 Lázaro Rivas Salvador Raymundo Izquierdo Orozco Carlos Eduardo Hernández Sánchez Daniel de Jesús Importancia Química y Biológica de: Hierro Osmio e Iridio Rutenio

HIERRO

HISTORIA Y CARACTERÍSTICAS Era utilizado por el hombre prehistórico. “Edad del hierro” Sirve al desarrollo industrial-tecnológico. Segundo elemento en abundancia en la corteza terrestre. Encontrado en Grupo VIII de transicion, con Co y Ni Es blanco plateado (puro). Tenaz, ductil, conductor de calor y atraíble por imanes

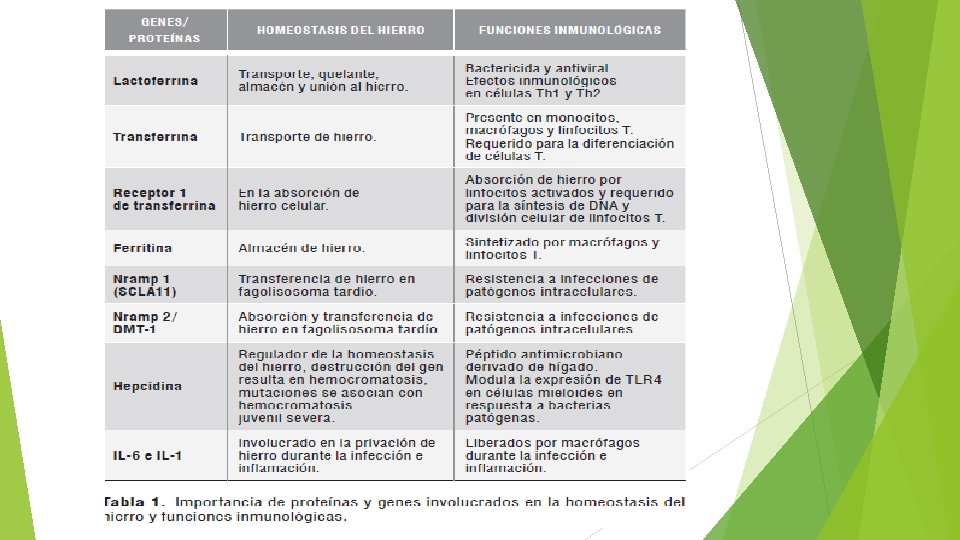
IMPORTANCIA QUÍMICA El hierro tiene dos estados de oxidación conocidos Fe (II) Fe (III). Forma iones bromuros, cloruros, óxidos, carbonatos, hidróxidos, nitratos, fosfatos, sulfato, dicromáticos. IMPORTANCIA BIOLÓGICA Desarrollo celular y elaboración de la sangre. Constituye el núcleo de la hemoglobina de la sangre. Modulación de la respuesta inmune del hospedero contra patógenos. Cofactor de enzimas Organismo 35 -48 mg/kg de peso. Acción catalítica en la producción de la clorofila.


Datos de consumo: Absorción del hierro incrementa cuando bajan los niveles en el organismo y viceversa (intestino). La necesidad de consumo es baja y solo 10 % es absorbida por el organismo. Dentro del hierro dietario hay dos tipos: • Heme: Se encuentra en carne, pescado, pollo. • No heme: 90% de la dieta encontrada en cereales, leguminosas, vegetales y huevos.



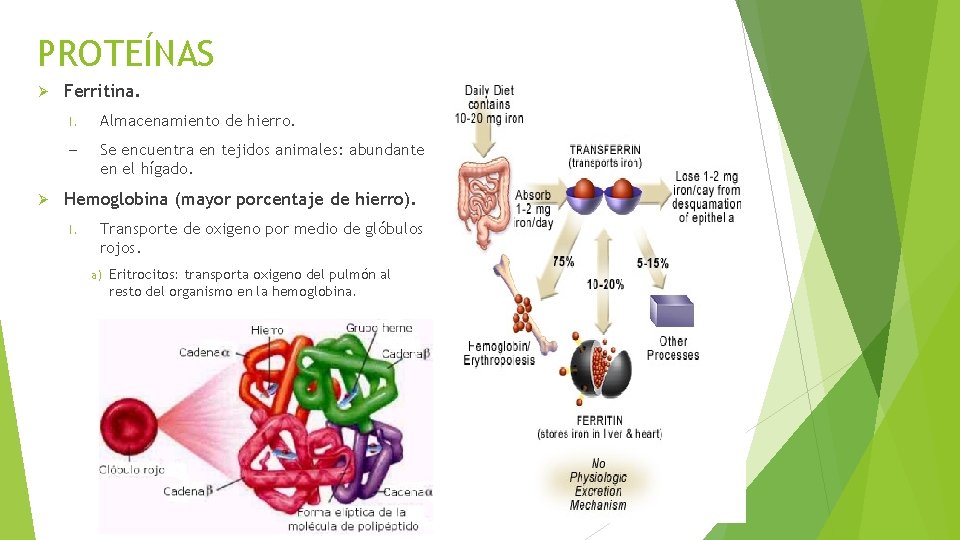
PROTEÍNAS Ferritina. I. Almacenamiento de hierro. – Se encuentra en tejidos animales: abundante en el hígado. Hemoglobina (mayor porcentaje de hierro). I. Transporte de oxigeno por medio de glóbulos rojos. a) Eritrocitos: transporta oxigeno del pulmón al resto del organismo en la hemoglobina.

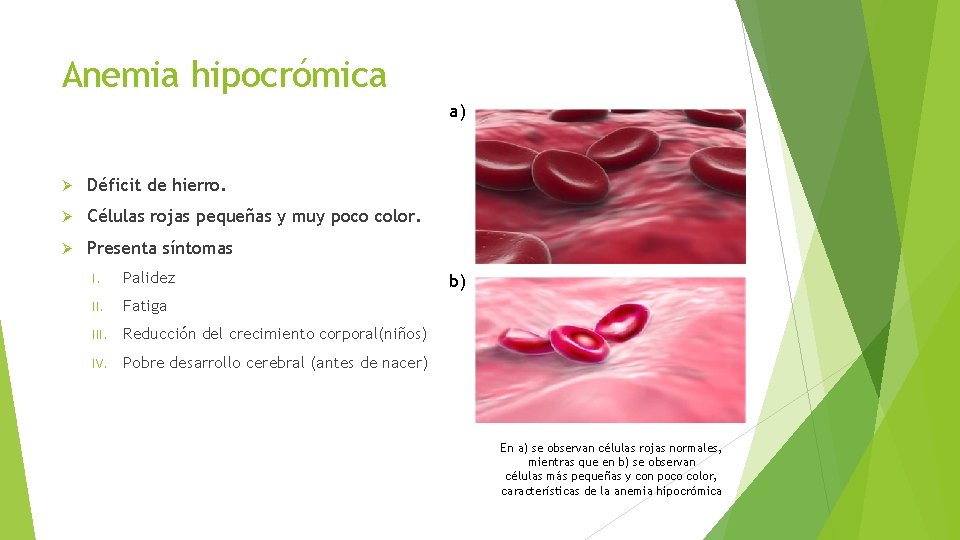
Anemia hipocrómica a) Déficit de hierro. Células rojas pequeñas y muy poco color. Presenta síntomas I. Palidez II. Fatiga III. Reducción del crecimiento corporal(niños) IV. Pobre desarrollo cerebral (antes de nacer) b) En a) se observan células rojas normales, mientras que en b) se observan células más pequeñas y con poco color, características de la anemia hipocrómica

Anemia ferropénica Disminución de electrolitos por perdida de sangre en hemorragias o déficit nutricional. Depósitos de hierro agotados (ferritina) transporte de hierro reducido concentración de hemoglobina baja. Síntomas: • Fatiga muscular • Cansancio • Debilidad • Fragilidad y perdida del cabello • Encanecimiento precoz • Uñas frágiles • Dolor de cabeza • Insomnio • Irritabilidad • Falta de concentración y disminución de la memoria

Diagnostico: • Valores de ferritina Población vulnerable: • Lactantes • Niños • Adolescentes • Mujeres en edad fértil (embarazadas)

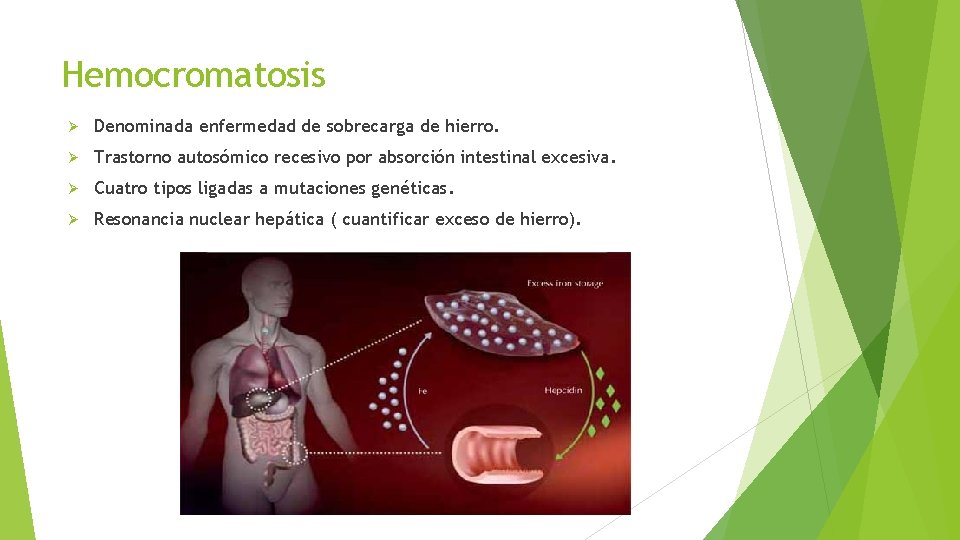
Hemocromatosis Denominada enfermedad de sobrecarga de hierro. Trastorno autosómico recesivo por absorción intestinal excesiva. Cuatro tipos ligadas a mutaciones genéticas. Resonancia nuclear hepática ( cuantificar exceso de hierro).

Síndrome de las piernas inquietas Trastorno neurológico en la vejez. Déficit de hierro, ferritina y dopamina.


Historia Su nombre es Iridio. Este es un metal de transición (los que se encuentran al centroabajo en la tabla periódica) de color blanco plateado y uno de los elementos mas densos y resistentes a la corrosión que se conocen. Sus sales son bastantes coloridas razón por lo cual en la Antigüedad se le acuñó en honor a la diosa Iris su nombre actual, por lo que deriva de “arco iris”. Se encuentra en mayor parte en meteoritos que caen a al tierra.

Usos y Aplicaciones Son metales estratégicos, debido a sus aplicaciones especializadas en los sectores del automóvil, agricultura, productos químicos, petróleo, industrias eléctricas, electrónicas, dental, médico y aeroespacial. También tienen usos importantes en el medio ambiente relacionados con las tecnologías, como los convertidores catalíticos y celdas de combustible.

Importancia Química Dentro de sus propiedades es posible destacar que es casi inmune al ataque de casi cualquier ácido conocido. Como es un metal de transición, dispone de varios electrones para poder unirse a otros elementos, creando así compuestos llamados de coordinación, que poseen geometrías bien definidas y variadas. Uno de los compuestos que forma el Iridio es conocido como Complejo de Vaska de formula (Ir. Cl(CO)[P(C 6 H 5)3]2) y tiene la rara capacidad de unirse al oxigeno que respiramos de manera reversible, así como la hemoglobina de la sangre.

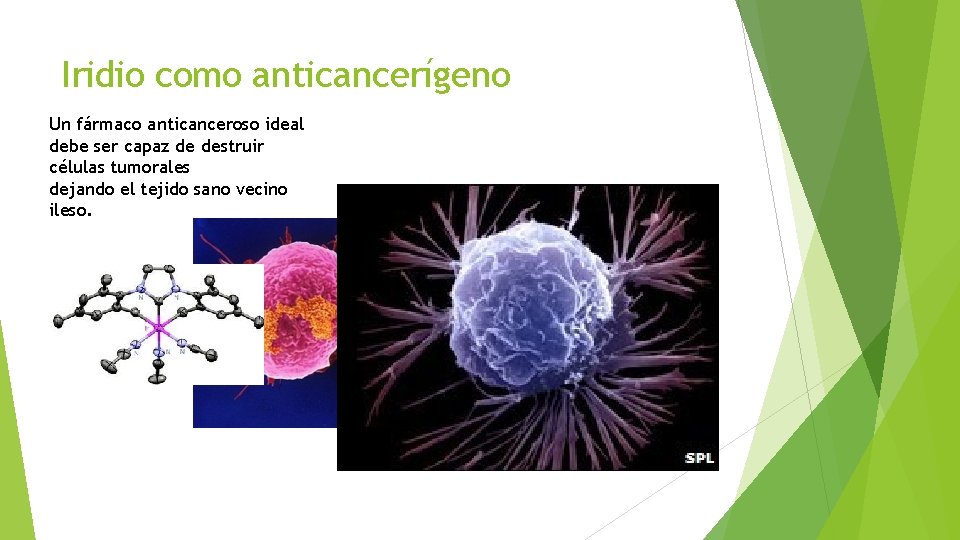
Iridio como anticancerígeno Un fármaco anticanceroso ideal debe ser capaz de destruir células tumorales dejando el tejido sano vecino ileso.

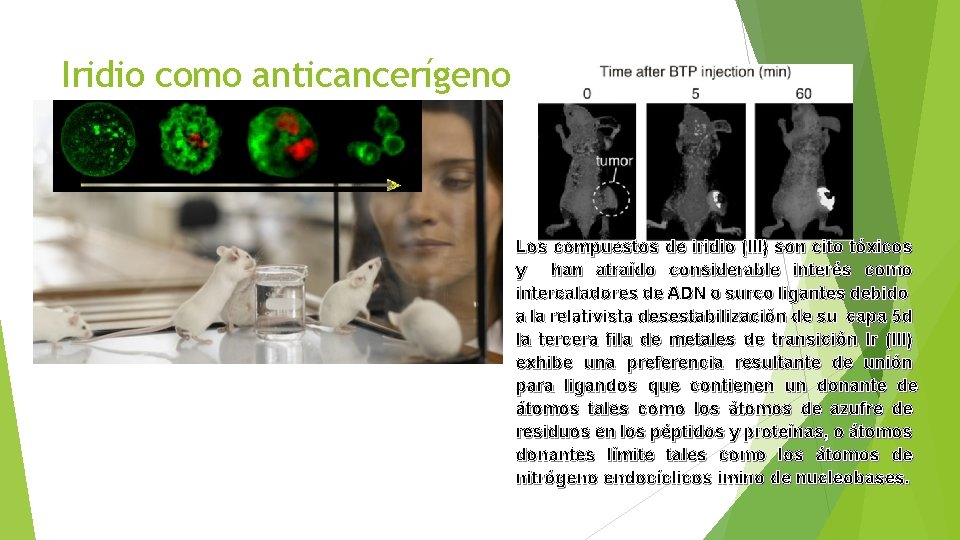
Iridio como anticancerígeno Los compuestos de iridio (III) son cito tóxicos y han atraído considerable interés como intercaladores de ADN o surco ligantes debido a la relativista desestabilización de su capa 5 d la tercera fila de metales de transición Ir (III) exhibe una preferencia resultante de unión para ligandos que contienen un donante de átomos tales como los átomos de azufre de residuos en los péptidos y proteínas, o átomos donantes límite tales como los átomos de nitrógeno endocíclicos imino de nucleobases.

Iridio Como fármaco No sólo debido a sus propiedades de unión a ADN potenciales, sino también a su posible influencia en las propiedades redox e hidrofobicidad de los compuestos resultantes. La Fragmentación del ADN (hipodiploidía) se considera que es un indicador de la muerte celular apoptótica y se detectó en altos niveles en células BJAB siguientes 72 h exposiciones a los rayos IR (III) complejos. Las especies reactivas de oxígeno (ROS) son subproductos de las reacciones aeróbicas del metabolismo que tiene lugar principalmente en la mitocondria. Altos niveles de ROS pueden tener un efecto destructivo sobre el ADN y las proteínas de muchos y puede desencadenar la apoptosis a través del estrés oxidativo resultante.

Conclusión § El iridio es un metal escaso cuyo origen extraterrestre lo hacen un elemento único y con cualidades aun desconocidas. § Es un metal cuyas características de transición y la poca reactividad hacia tejidos del cuerpo lo hacen un candidato para el desarrollo de estructuras que serán base para la producción de nuevos fármacos § Dado su alto costo y carencia de estudios respecto a su uso a largo plazo, sigue estando presente en etapa de investigación Las aplicaciones que se le puedan dar como anticancerígeno.

11/11/12

Características Principales 1. Es un metal blanco duro y frágil; presenta cuatro formas cristalinas diferentes. 2. Los estados de oxidación más comunes son +2, +3 y +4 3. 4. Número atómico 44 Se encuentra normalmente en minas de platino y se emplea como catalizador en algunas aleaciones de platino. 11/11/12

Historia El rutenio fue descubierto por Karl Ernst Claus en 1844. Jöns Berzelius y Gottfried Osann casi lo descubrieron en 1827. Es posible que el químico polaco Jedrzej Sniadecki aislara este elemento en 1807. 11/11/12

Obtención del Rutenio Para su producción el metal se aísla comercialmente por un proceso químico complejo, la fase final es la reducción del cloruro de amonio formando el rutenio en polvo. El polvo se consolida mediante técnicas de metalurgia o procesos de soldadura. 11/11/12

Efectos sobre la salud Los compuestos del rutenio se encuentran muy raramente. Los compuestos del rutenio manchan mucho la piel. Parece que el rutenio ingerido es retenido fuertemente en los huesos. El óxido de rutenio, Ru. O 4, es altamente tóxico y volátil, y debe ser evitado El rutenio no desempeña ningún papel biológico, pero puede ser carcinógeno y se puede acumular en los huesos. 11/11/12

Rutenio empleado en la industria Los fabricantes farmacéuticos y de procesos de química fina que emplean catalizadores conteniendo metales preciosos, están siendo retados por los incrementos en los costos de energía, laboral, materias primas y otros gastos de producción y gastos generales fijos. La mayoría de los fabricantes de farmacéuticos usan catalizadores conteniendo metales preciosos que incorporan platino, paladio, rutenio, rodio, o alguna combinación. 11/11/12

Aplicaciones El dióxido de rutenio junto con el sulfuro de cadmio se emplean para descomponer sulfuro de hidrógeno. Esto se utiliza para eliminar este producto contaminante y tóxico en el refinado del petróleo y en otros procesos químicos Forma aleaciones con el paladio y platino para otorgarles una mayor dureza y ser utilizados en la fabricación de contactos eléctricos que requieran una resistencia muy grande o diversos objetos para darles un acabado de lujo. 11/11/12

Osmio

Historia Su nombre es Osmio. Este es un metal de transición De la palabra griega "osme" que significa "olor", debido a que un compuesto de este elemento presentaba un olor muy desagradable. En su forma metálica es el material más denso de la naturaleza, es azul grisáceo, frágil, duro, poco dúctil y brillante, incluso a altas temperaturas, aunque es difícil encontrarlo en esta forma.

Importancia química Es muy común en su forma a de compuesto : El tetróxido de osmio se encuentra en forma de cristales amarillentos que son volátiles. En química esto se dice que sublima, o sea pasa de estado sólido a gas sin pasar por el estado liquido. Dada la cantidad de electrones externos que el osmio posee (disponibles para enlazar) se sabe que genera compuestos espacialmente tetraédricos. Es sintetizado a partir de polvo de osmio puro puesto en presencia de oxígeno

Usos Primero que todo, es ampliamente usado en síntesis orgánica se usa como agente para oxidar algunos compuestos específicos de carbono (alquenos) que poseen dobles enlaces. Es usado en técnicas de microscopia electrónica como método de tinción de muestras. El tetróxido de osmio es un agente de contraste, . El tetróxido de osmio tiene especial preferencia por teñir a los compuestos lipídicos como las membranas biológicas que forman las células También se usa en a fabricación de marca pasos por su resistencia. Es sumamente venenoso. La inhalación de una mínima cantidad de esta sal puede generar edemas pulmonares y posterior muerte. Además, este compuesto puede teñir la cornea lo que pudiese inducir ceguera. En el laboratorio, lo mejor es guardarlo en frascos de vidrio porque atraviesa el plástico.

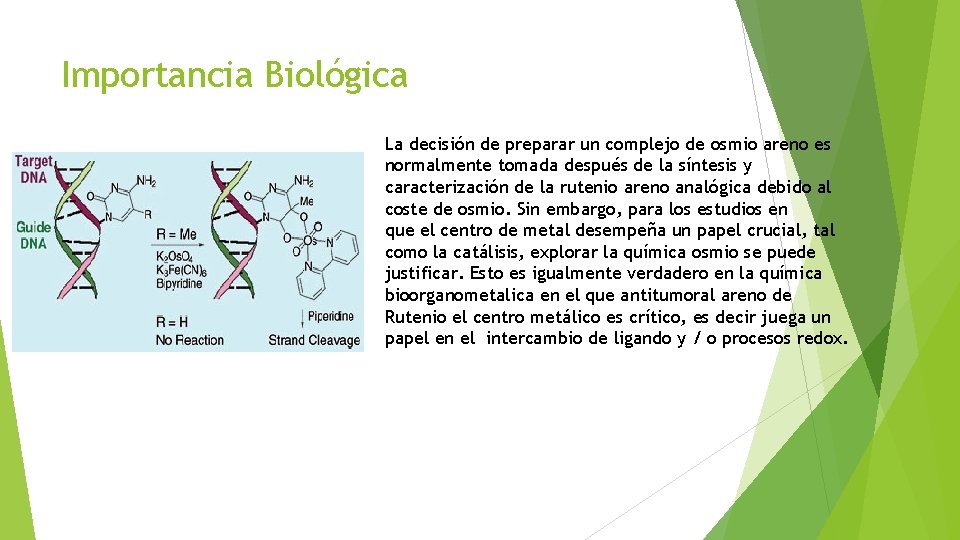
Importancia Biológica La decisión de preparar un complejo de osmio areno es normalmente tomada después de la síntesis y caracterización de la rutenio areno analógica debido al coste de osmio. Sin embargo, para los estudios en que el centro de metal desempeña un papel crucial, tal como la catálisis, explorar la química osmio se puede justificar. Esto es igualmente verdadero en la química bioorganometalica en el que antitumoral areno de Rutenio el centro metálico es crítico, es decir juega un papel en el intercambio de ligando y / o procesos redox.

Osmio como base par anticancerígenos El osmio en un estudio se utilizo como estrucutura base para el desarrollo de una anticancerígeno, como se viene haciendo desde antes con el Rutenio y se encontraron diferentes niveles de citotoxicidad y un grado diferente de reducción de Síntesis de ADN. En el caso de areno de Ru y Os complejos coordinados para fosfito ligandos de carbohidratos, los complejos son ligeramente más citotóxicos que sus homólogos el osmio y el rutenio pueden inhibir una proteína quinasa a un ritmo similar, lo que sugiere que para estos complejos, el centro metálico no participa y solo juegan un papel estructural

Conclusión: El osmio es el metal mas denso dada su constitución atómica y juega un papel importante en el desarrollo de materiales y estructuras. Su importancia Biológica esta en el papel que juega en tinción de tejidos al microscopio y recientemente su uso como estructura base para la creación de anticancerígenos esta abriendo nuevas puertas al tratamiento d eesta enfermedad. Aun su uso esta en fase de prueba Aunque los resultados suenan prometedores dado su costo y obtención tiene que tomarse en cuenta el uso del osmio frente a una Panacea como lo es el cáncer.

Bibliografías Nicolas P. E. Barry et al(2012) …. Encapsulation of inorganic guest molecules into an organometallic hexacationic arene osmium metalla-prism: Synthesis Charcaterisation and anticancer Activity, Journal of Organometallic Chemistry, , 705, 6 P. El sevier Yvonne Geldmacher, Melanie Oleszak, William S. Sheldrick(2012), Rhodium(III) and iridium(III) complexes as anticancer agents, Inorganica. Chimica Acta , El sevier, 19. P Estrin Dario, etal…(2006), Construyendo con átomos y moléculas, Universitaria de Buenos Aires, Buneos Aires, Colección Ciencia Joven, 17, 119 P. El metabolismo del hierro y la anemia ferropénica. MONTSERRAT VILAPLANA. Farmacéutica comunitaria. Máster en Nutrición y Ciencias de los Alimentos. Abril 2001. (En línea) << http: //apps. elsevier. es/watermark/ctl_servlet? _f=10&pident_articulo=12004009&pident_usuario=0 &pident_revista=4&fichero=4 v 20 n 04 a 12004009 pdf 001. pdf&ty=151&accion=L&origen=doymafarma& web=www. doymafarma. com&lan=es>> Consulta 05 noviembre 2012. Chantes Guerra A. et al. El hierro, elemento metálico importante en la vida y en los procesos infecciosos. Elementos 85 (2012) 41 -48 Centro de Investigaciones en Ciencias Microbiológicas, Instituto de Ciencias, BUAP y Facultad de Estudios Superiores Iztacala, Universidad Nacional Autónoma de México. (En línea) <<http: //www. elementos. buap. mx/num 85/pdf/41. pdf>> Consulta: 31 octubre 2012

o Original Research Article. SEMERGEN - Medicina de Familia, Volume 34, Issue 2, February 2008, Pages 80 -86. M. Martínez García. (En línea) <<http: //www. sciencedirect. com/science/article/pii/S 1138359308718549>> Consulta: 31 octubre 2012 Una revisión del síndrome de piernas inquietas o Importancia de la ferropenia en el niño pequeño: repercusiones y prevención Original Research Article. Anales de Pediatría, Volume 74, Issue 6, June 2011, Pages 415. e 1 -415. e 10 A. Moráis López, J. Dalmau Serra, Comité de Nutrición de la AEP. (En línea) <<http: //www. sciencedirect. com/science/article/pii/S 1695403311000907>> Consulta: 31 octubre 2012 o BURRIEL MARTÍ, Fernando (2008), Química analítica cualitativa. Ed. Thomson. Madrid, España. 18 ed. 1052 pag. Se encuentra en FESC-C 1: QD 81 B 87 o Fenotipo, genotipo e historia de las enfermedades de sobrecarga de hierro. Med Clin (Barc). 2006; 126(17): 676 -9. Artículo 153. 312. (En línea) <<www. scienciedirect. com>> Consulta: 15 octubre 2012. o Anemia por deficiencia de hierro. Dra. Nelly Baiocchi Ureta. Médico pediátra. Hospital Nacional Cayetano Heredia. Septiembre-Diciembre 2006. (En línea) <<http: //sisbib. unmsm. edu. pe/bvrevistas/rpp/v 59 n 3/pdf/a 04. pdf>> Consulta: 31 octubre 2012.