Universidad de San Carlos de Guatemala Facultad de



























- Slides: 53

Universidad de San Carlos de Guatemala Facultad de Ciencias Médicas Química SEMANA # 16 HIDROCARBUROS SATURADOS Lic. Sofía Tobías V.

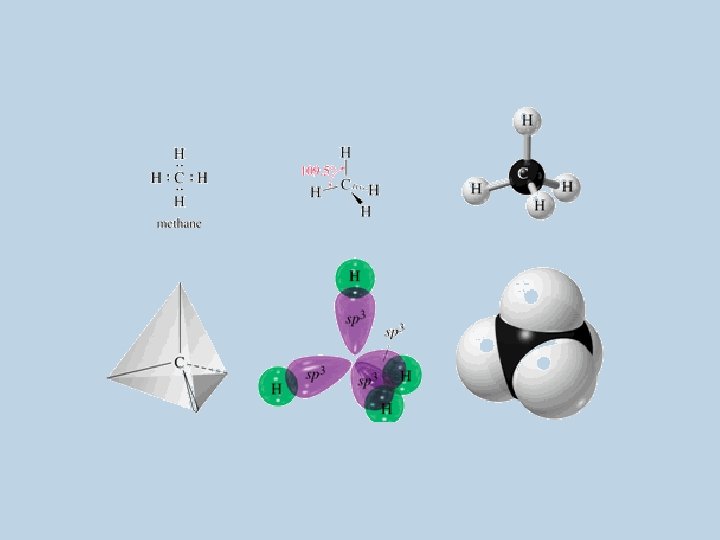
I. HIDROCARBUROS • Están compuestos por átomos de dos elementos: carbono e hidrógeno. • Los enlaces entre los átomos de carbono pueden ser simples, dobles ó triples.

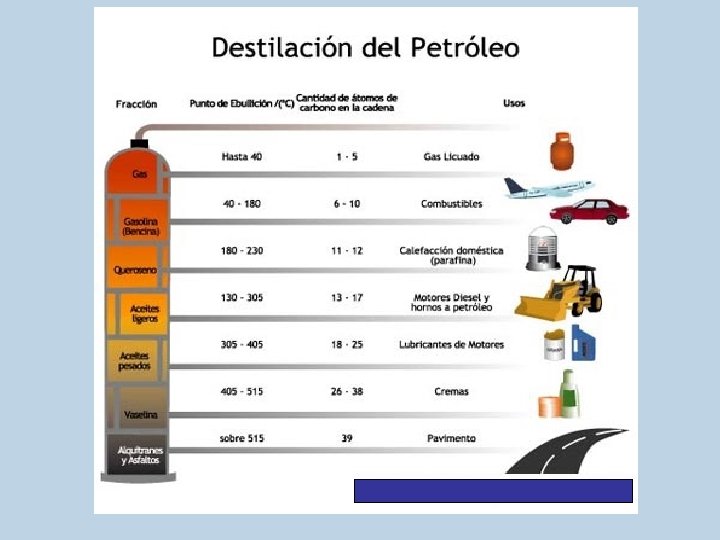
• El petróleo y el gas natural se componen de una mezcla compleja de hidrocarburos. • Los esqueletos de carbono pueden formar cadenas o anillos. • Todo lo anterior permite establecer la clasificación de los mismos.



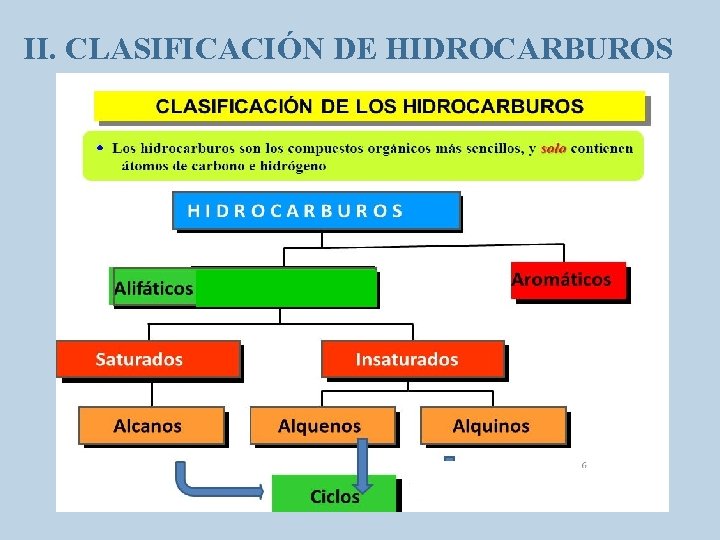
II. CLASIFICACIÓN DE HIDROCARBUROS

III. HIDROCARBUROS SATURADOS • Son los compuestos básicos de la química orgánica. • Saturado describe el tipo de enlaces de la molécula hidro carbonada.

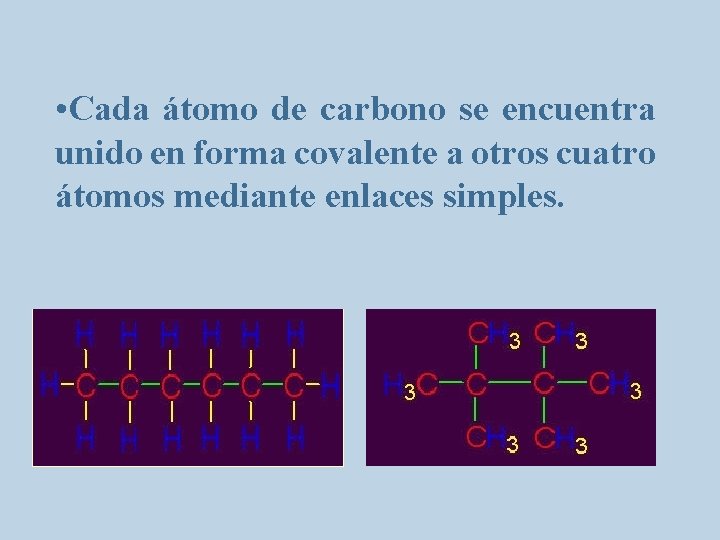
• Cada átomo de carbono se encuentra unido en forma covalente a otros cuatro átomos mediante enlaces simples.

• Pertenecen a la serie Alifática. • Se conocen como Alcanos o Parafínicos. • Comprenden todos los hidrocarburos saturados de cadena abierta y cíclicos. A. Alcanos Su fórmula general es: Cn H 2 n+2

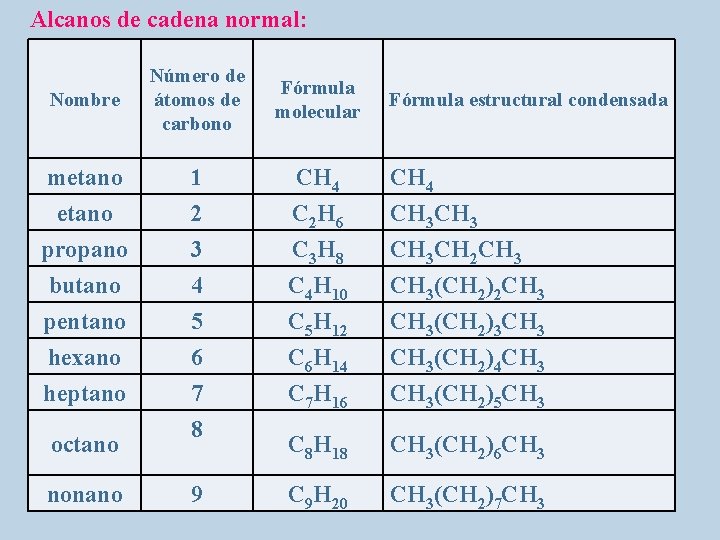
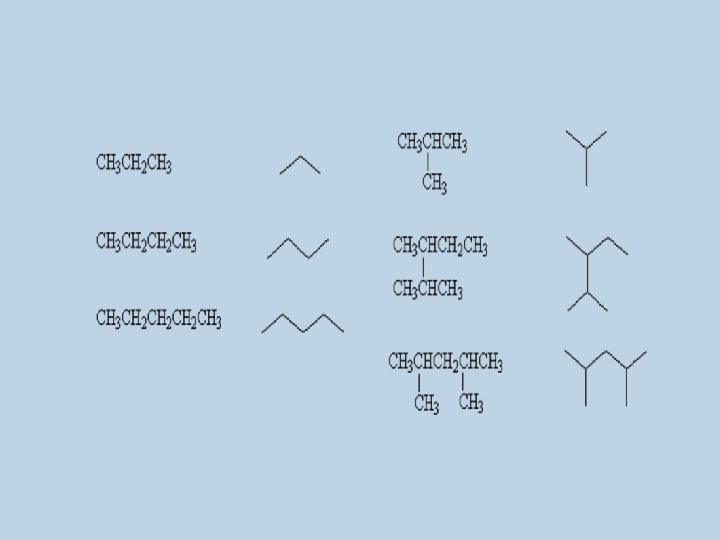
Alcanos de cadena normal: Nombre Número de átomos de carbono Fórmula molecular metano 1 CH 4 etano 2 C 2 H 6 CH 3 propano 3 C 3 H 8 CH 3 CH 2 CH 3 butano 4 C 4 H 10 CH 3(CH 2)2 CH 3 pentano 5 C 5 H 12 CH 3(CH 2)3 CH 3 hexano 6 C 6 H 14 CH 3(CH 2)4 CH 3 heptano 7 C 7 H 16 CH 3(CH 2)5 CH 3 C 8 H 18 CH 3(CH 2)6 CH 3 C 9 H 20 CH 3(CH 2)7 CH 3 octano nonano 8 9 Fórmula estructural condensada

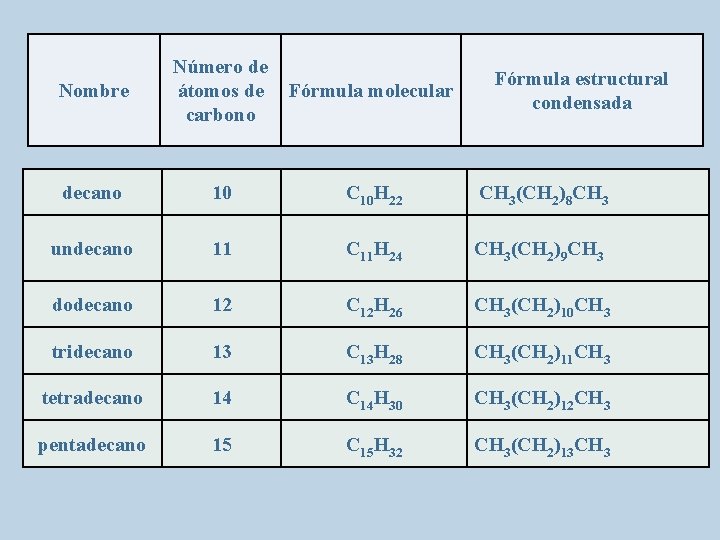
Nombre Número de átomos de carbono Fórmula molecular decano 10 C 10 H 22 CH 3(CH 2)8 CH 3 undecano 11 C 11 H 24 CH 3(CH 2)9 CH 3 dodecano 12 C 12 H 26 CH 3(CH 2)10 CH 3 tridecano 13 C 13 H 28 CH 3(CH 2)11 CH 3 tetradecano 14 C 14 H 30 CH 3(CH 2)12 CH 3 pentadecano 15 C 15 H 32 CH 3(CH 2)13 CH 3 Fórmula estructural condensada

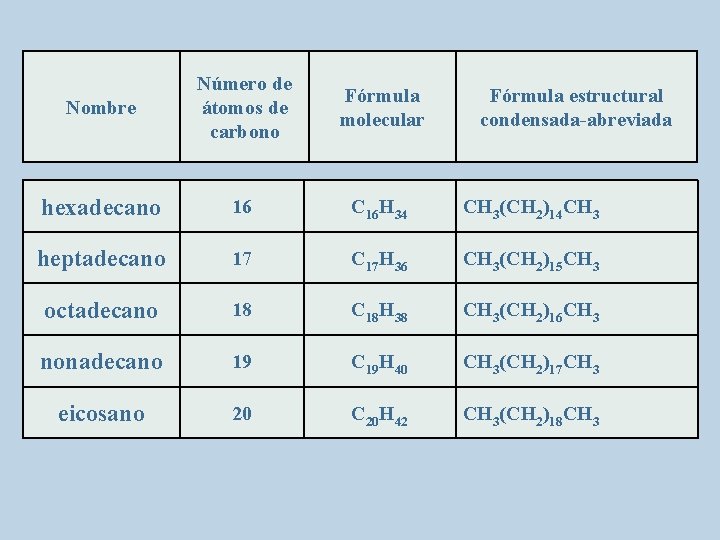
Nombre Número de átomos de carbono Fórmula molecular hexadecano 16 C 16 H 34 CH 3(CH 2)14 CH 3 heptadecano 17 C 17 H 36 CH 3(CH 2)15 CH 3 octadecano 18 C 18 H 38 CH 3(CH 2)16 CH 3 nonadecano 19 C 19 H 40 CH 3(CH 2)17 CH 3 eicosano 20 C 20 H 42 CH 3(CH 2)18 CH 3 Fórmula estructural condensada-abreviada

HIDROCARBUROS SATURADOS Alcanos cont… Nomenclatura común • Para dar nombre al hidrocarburo de cadena continua se antepone la letra n(normal) al nombre del compuesto.

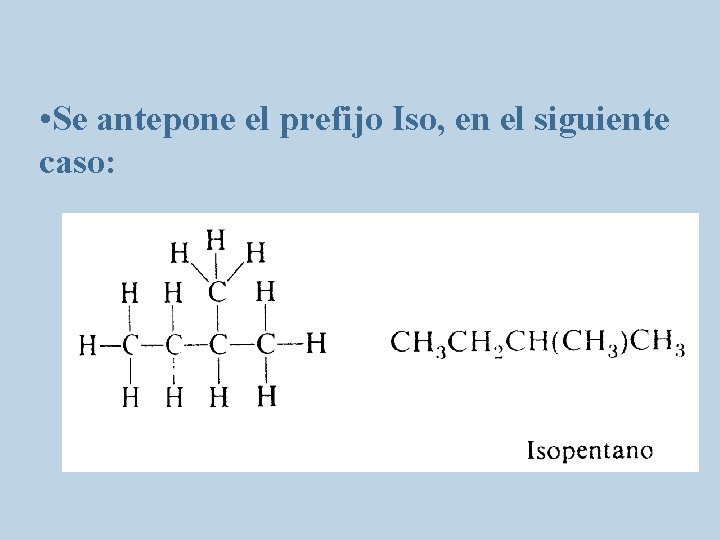
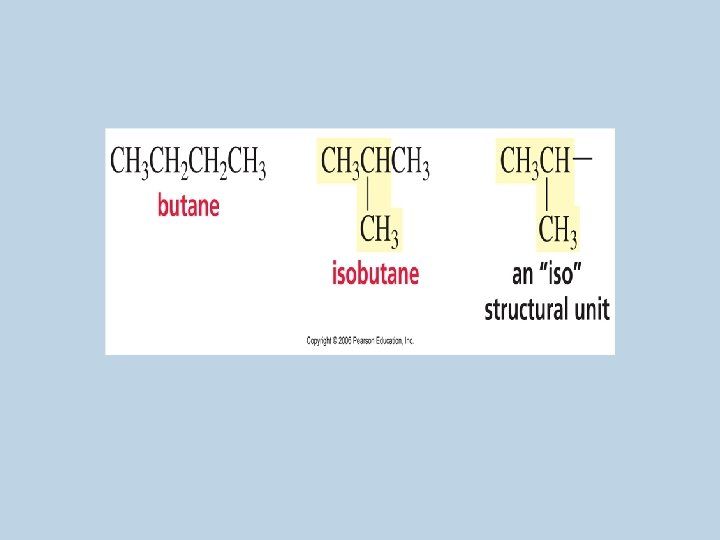
• Se antepone el prefijo Iso, en el siguiente caso:

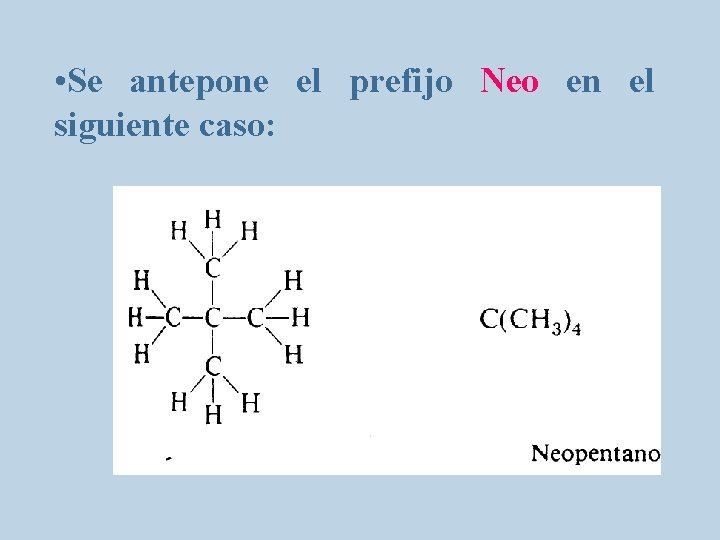
• Se antepone el prefijo Neo en el siguiente caso:

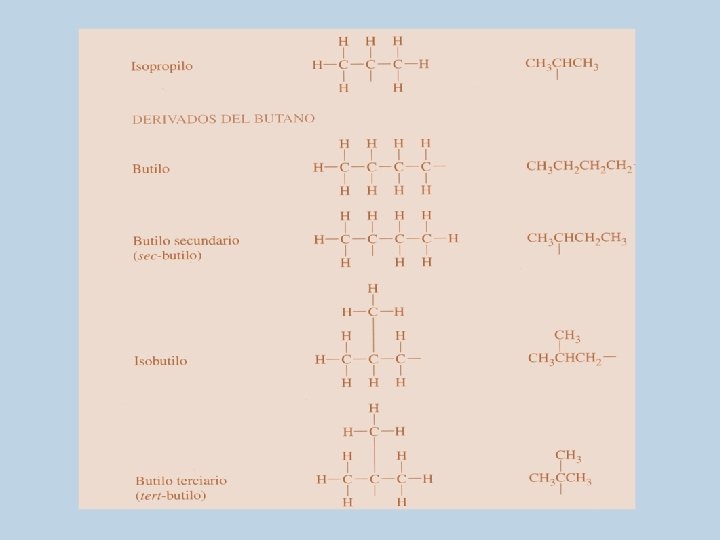
Nomenclatura UIQPA Grupos alquilo: grupo de átomos que permanecen después de eliminar un átomo de hidrógeno de un alcano. • El metano (CH 4) pierde un H (hidrogeno) y se transforma en metilo (CH 3 -). • Para nombrar los grupos alquilo, ANO se reemplaza por ILO. CH 4 Met. ANO CH 3 Met. ILO el sufijo



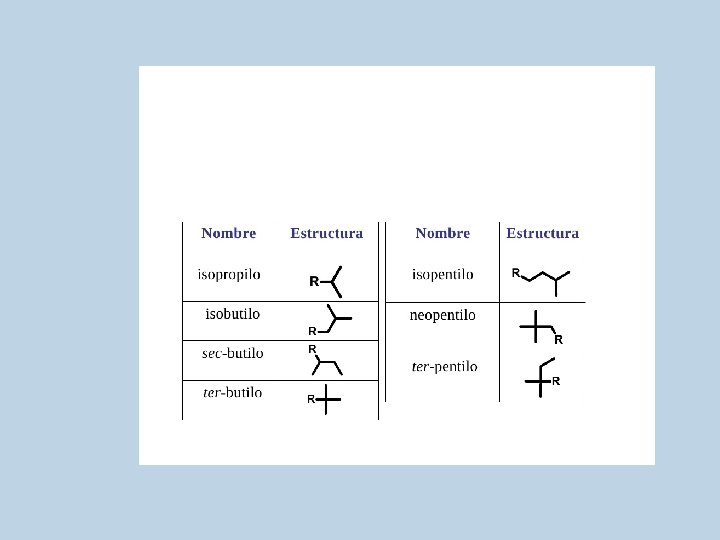
RADICAL NOMBRE Isopentilo Sec-pentilo Ter-pentilo Neopentilo


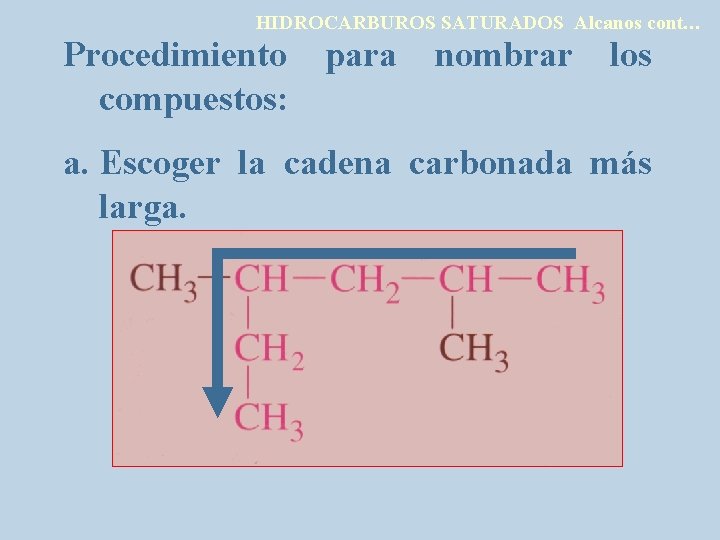
HIDROCARBUROS SATURADOS Alcanos cont… Procedimiento para compuestos: nombrar los a. Escoger la cadena carbonada más larga.

b. Numerar la cadena de tal forma que le toquen los números más pequeños a los carbonos con ramificaciones o radicales. 4 5 6 3 2 1

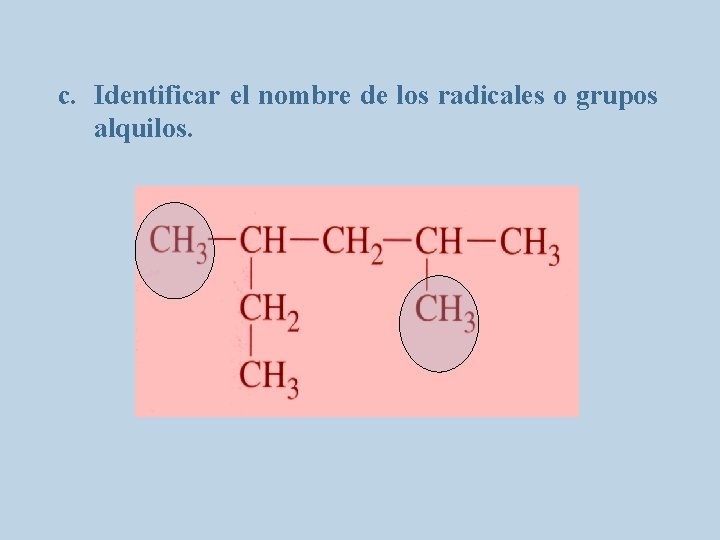
c. Identificar el nombre de los radicales o grupos alquilos.


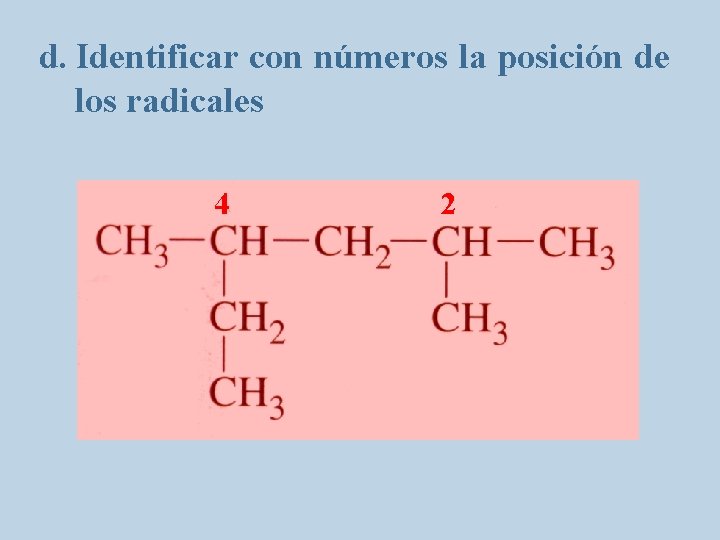
d. Identificar con números la posición de los radicales 4 2

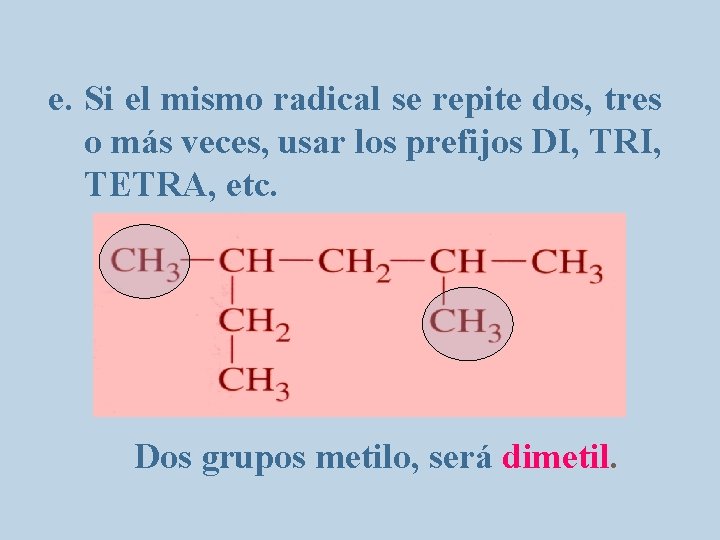
e. Si el mismo radical se repite dos, tres o más veces, usar los prefijos DI, TRI, TETRA, etc. Dos grupos metilo, será dimetil.

f. Nombrar los radicales en orden alfabético. Ejemplo: Butilo-etilo-metilo Entre número y número se debe escribir una coma y entre número y nombre un guión. Ejemplo: 2, 4 – Dimetil

g. El final del nombre depende del número de átomos de carbono que posee la cadena principal. 6 carbonos = 4 hexano 3 2 1 5 6 2, 4 – Dimetilhexano.


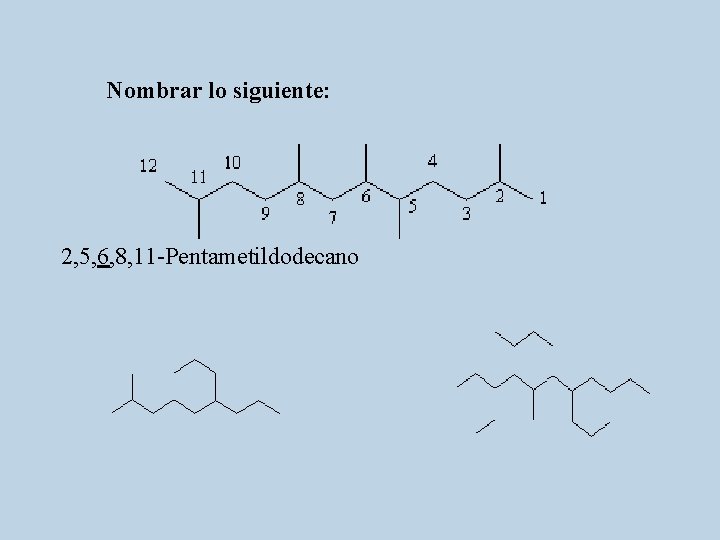
Nombrar lo siguiente: 2, 5, 6, 8, 11 -Pentametildodecano

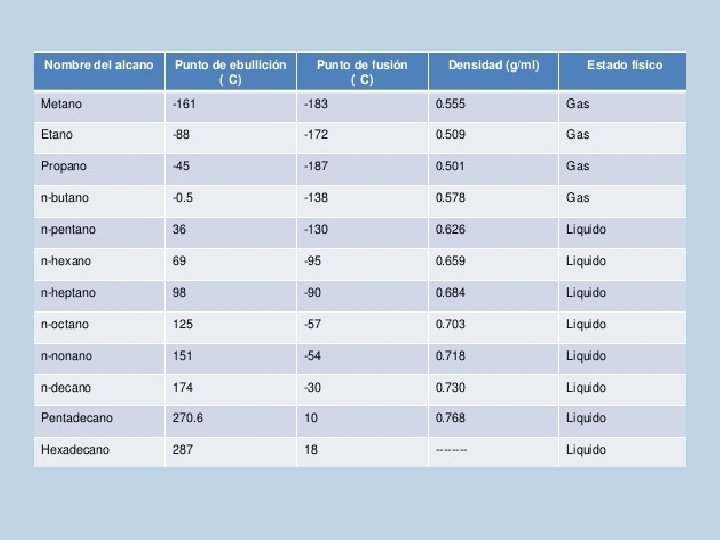
IV. Propiedades físicas de los Alcanos: • Apolares • Insolubles en agua pero si en solventes orgánicos. • Menos densos que el agua.


• A temperatura ambiente pueden encontrarse como gases, líquidos ó sólidos: De metano a butano son gaseosos. De pentano a hexadecano son líquidos De heptadecano en adelante son sólidos. • Incoloros, inodoros e insípidos.

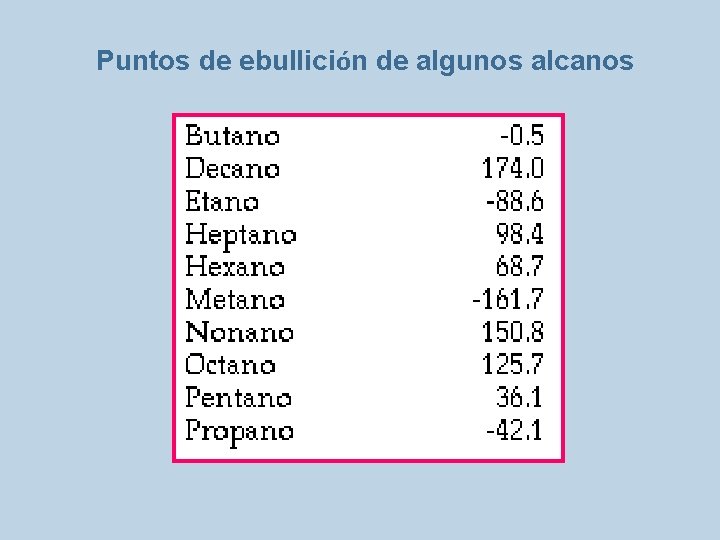
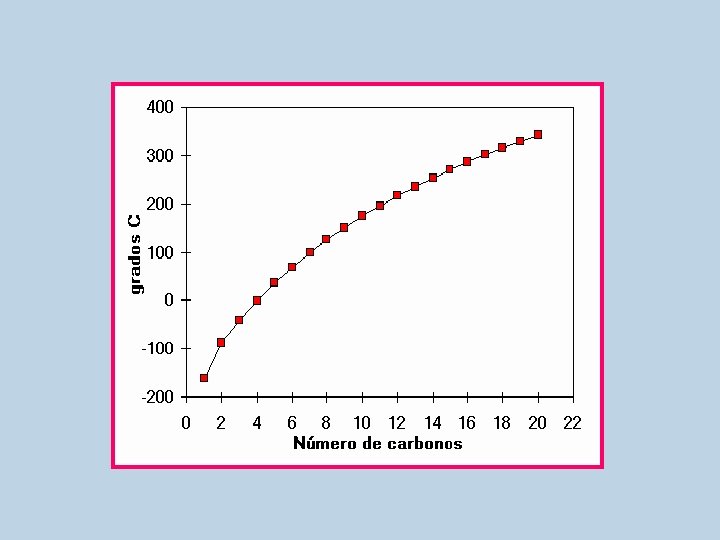
• Puntos de ebullición: los alcanos de cadena continua aumentan su punto de ebullición conforme aumenta su masa molar. • Los isómeros de cadena continua tienen puntos de ebullición mayores a los ramificados.

Puntos de ebullición de algunos alcanos


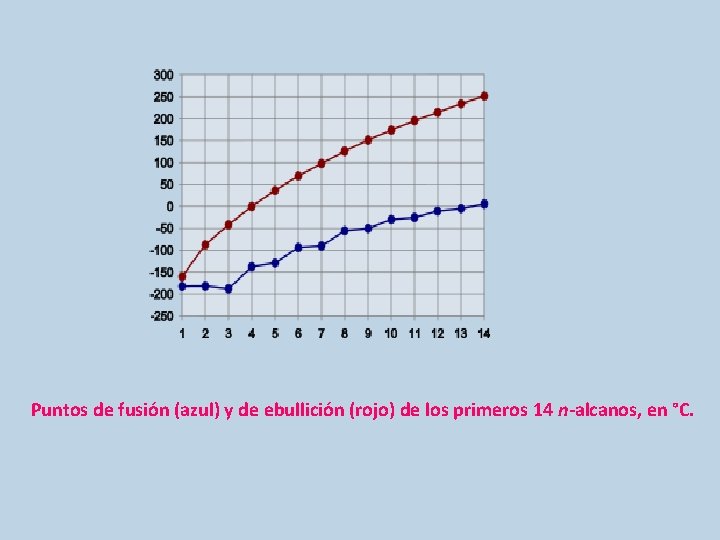
• Puntos de fusión: no hay una tendencia que permita predecirlos. • Los isómeros más simétricos tienden a tener valores más elevados que los poco simétricos.

Puntos de fusión (azul) y de ebullición (rojo) de los primeros 14 n-alcanos, en °C.

V. Propiedades Químicas de los alcanos: • Son los menos reactivos de todos los compuestos orgánicos. • No reaccionan con: H 2 SO 4 concentrado. Na. OH. KMn. O 4.

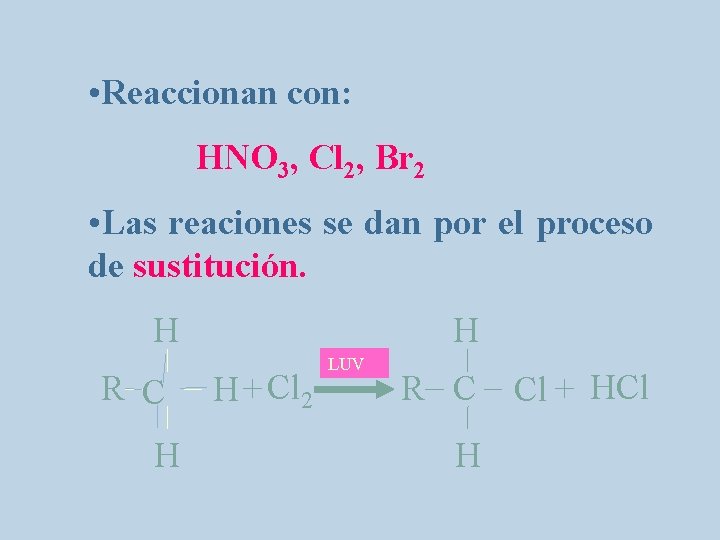
• Reaccionan con: HNO 3, Cl 2, Br 2 • Las reaciones se dan por el proceso de sustitución. H R C H H H + Cl 2 LUV R C H Cl + HCl

• Reaccionan con el oxígeno (combustión). Combustión: oxidación acompañada de liberación de energía. Los productos dependen de la cantidad de oxígeno presente.

• Combustión Completa C 8 H 18 +12. 5 O 2 8 CO 2 +9 H 2 O • Combustión Incompleta 2 C 8 H 18 +17 O 2 2 C 8 H 18 +9 O 2 16 CO +18 H 2 O 16 C +18 H 2 O

VI. Serie Homóloga: Es una familia de compuestos semejantes que presentan las siguientes características:

1. Tienen los mismos elementos y fórmula general muy simple. CH 3 CH 2 CH 3 Fórmula gral. Cn H 2 n+2

2. La fórmula molecular de cada homólogo difiere de la anterior y posterior por un CH 2. CH 4 CH 3

3. Conforme aumenta la masa molecular hay una variación gradual en las propiedades físicas. 4. Todos los homólogos tienen propiedades químicas semejantes.

VII. Grupo funcional: Es toda distribución de átomos en particular que confiere propiedades características a una molécula orgánica. R-OH RNH 2 R-O-R

B. Cicloalcanos • Poseen enlaces simples C-C. • Se encuentran en una estructura cerrada (anillos o estructuras ciclicas). • Su fórmula general es : Cn. H 2 n

Nomenclatura a. Se antepone la palabra ciclo. b. A continuación se da el nombre del alcano del cuál se deriva, dependiendo del número de carbonos del anillo.

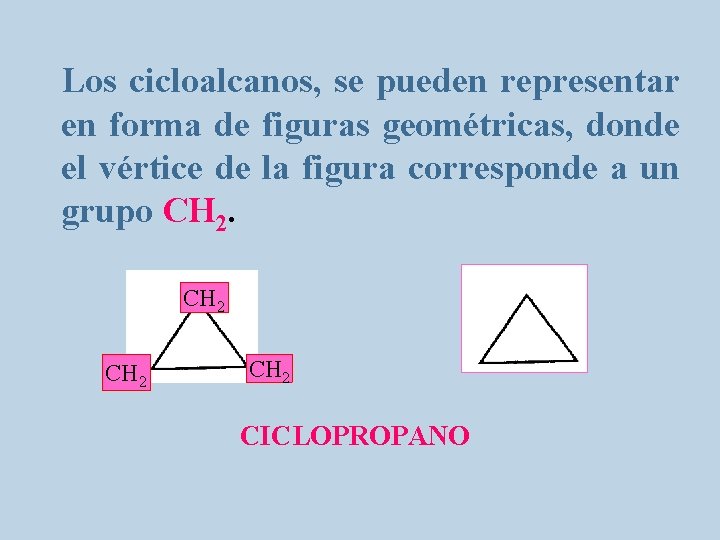
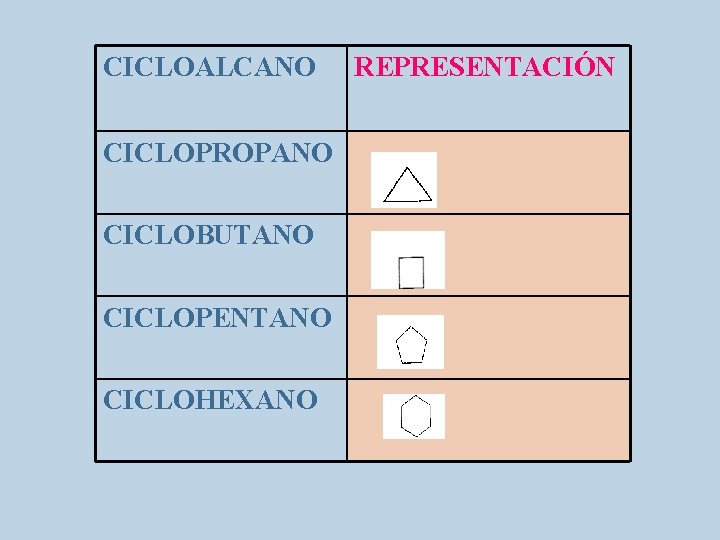
Los cicloalcanos, se pueden representar en forma de figuras geométricas, donde el vértice de la figura corresponde a un grupo CH 2 CICLOPROPANO

CICLOALCANO CICLOPROPANO CICLOBUTANO CICLOPENTANO CICLOHEXANO REPRESENTACIÓN

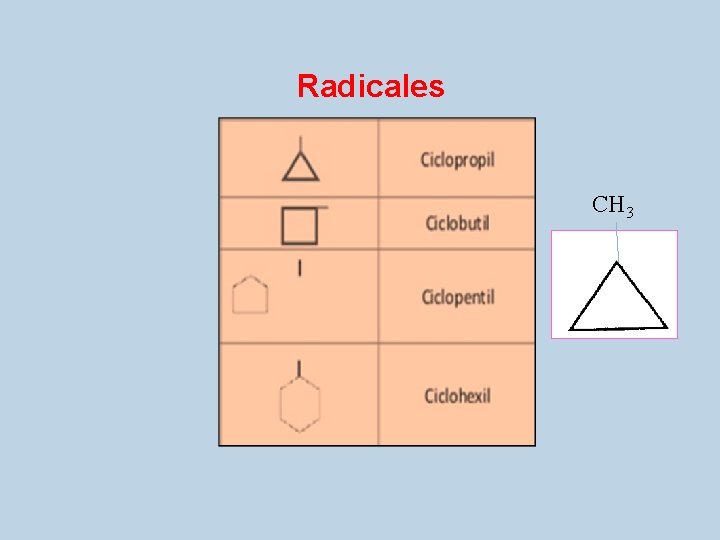
Radicales CH 3

CH 3