UNIT 1 LUNION CHIMIQUE Faites par Myra Karim








- Slides: 11

UNITÉ 1: L’UNION CHIMIQUE Faites par: Myra Karim Massoud Classe: 1 ere préparatoire B Numéro: 28

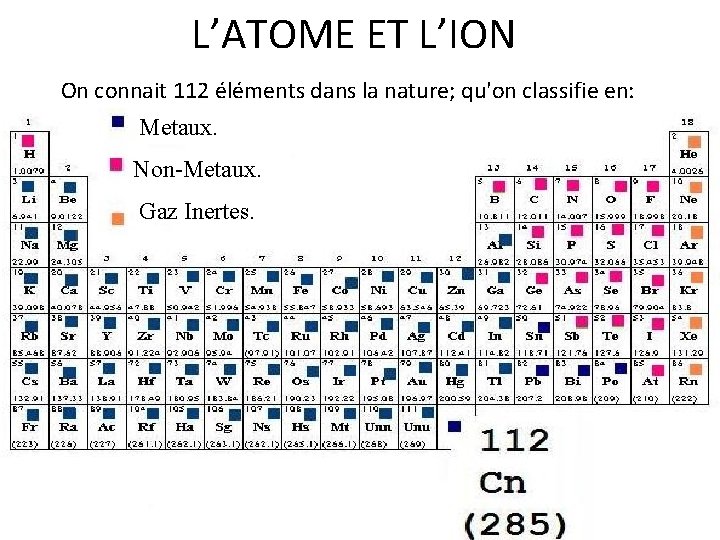
L’ATOME ET L’ION On connait 112 éléments dans la nature; qu'on classifie en: Metaux. Non-Metaux. Gaz Inertes.

1 -Les Métaux: Les éléments Sont solides(sauf le mercure). v Ont un éclat métallique. v Bons conducteurs de la chaleur et d’électricité. v Peuvent être martelés et étirés. v Niveaux d’énergie externe peut contenir 1, 2 ou 3 électrons. v Forme une ion positive (+) Ex: 11 Na. K 2 L 8 M 1 Na+K 2 L 8 v 2 -Les Non-métaux: Sont solides, liquides et gaz. v N’ont pas un éclat métallique. v Mauvais conducteurs de la chaleur et d’électricité. v Ne peuvent pas être ni martelés ni étirés. v Niveaux d'énergie externe peut contenir 5, 6 ou 7 électrons. v Forme une ion négative (-) Ex: 8 OK 2 L 6 O- -K 2 L 8 v sodium o 2

3 - Les Eléments inertes: q. Ils sont des éléments dont le niveau externe de l'atome est fffsaturée. q Ils n'entrent pas en union chimique avec d'autres atomes et ffffleur structure moléculaire est formée d'un seul atome. q Ils ne forment ni ion positive ni négative dans le conditions ffffnormales.

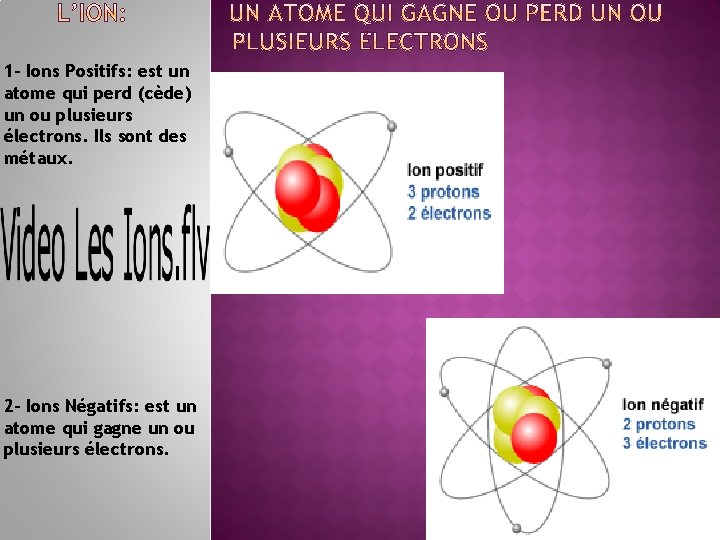
1 - Ions Positifs: est un atome qui perd (cède) un ou plusieurs électrons. Ils sont des métaux. 2 - Ions Négatifs: est un atome qui gagne un ou plusieurs électrons.

Liaison ionique Métal + Non-métal Perd / Gagne Ion positif / Ion négatif -Durant une réaction chimique l'atome métallique cède les électrons du niveau externe a l'atome non métallique et une force électrostatique est crée entre l’ion positif du métal et l’ion négatif du non métal; du aux chargés contraires, formant des molécules d'un composé ionique.

-Conclusion: la liaison ionique c'est une liaison qui résulte de l'attraction entre lion (+) du métal et l’ion (-) du non métal. -Exemple: 11 Na. K 2 L 8 M 1 + 17 Cl. K 2 L 8 M 7 = Na+K 2 L 8 Cl-K 2 L 8 M 8 (métal perd+non métal gagne) + =

-C’est La liaison entre 2 non-métaux: dans ce cas les 2 atomes ne perdent ni gagnent d'électrons mais ils les partage. Chaque atome partage un nombre d'électrons égal au nombre nécessaires pour saturer la couche externe des atomes -Conclusion: C'est une liaison entre les non métaux partage d'électrons pour saturer le niveau d'énergie externe de chacun d’eux.

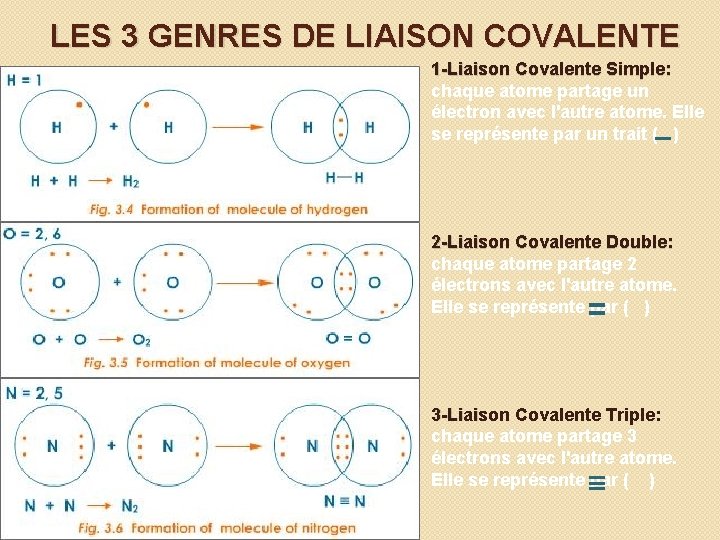
LES 3 GENRES DE LIAISON COVALENTE 1 -Liaison Covalente Simple: chaque atome partage un électron avec l'autre atome. Elle se représente par un trait ( ) 2 -Liaison Covalente Double: chaque atome partage 2 électrons avec l'autre atome. Elle se représente par ( ) 3 -Liaison Covalente Triple: chaque atome partage 3 électrons avec l'autre atome. Elle se représente par ( )

