Unidad II SubUnidad 2 2 ISOMERA Y REACCIONES
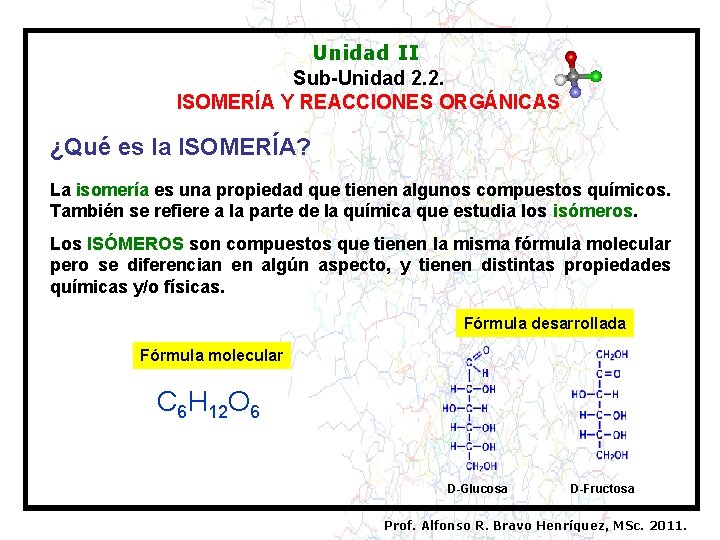
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ¿Qué es la ISOMERÍA? La isomería es una propiedad que tienen algunos compuestos químicos. También se refiere a la parte de la química que estudia los isómeros. Los ISÓMEROS son compuestos que tienen la misma fórmula molecular pero se diferencian en algún aspecto, y tienen distintas propiedades químicas y/o físicas. Fórmula desarrollada Fórmula molecular C 6 H 12 O 6 D-Glucosa D-Fructosa Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
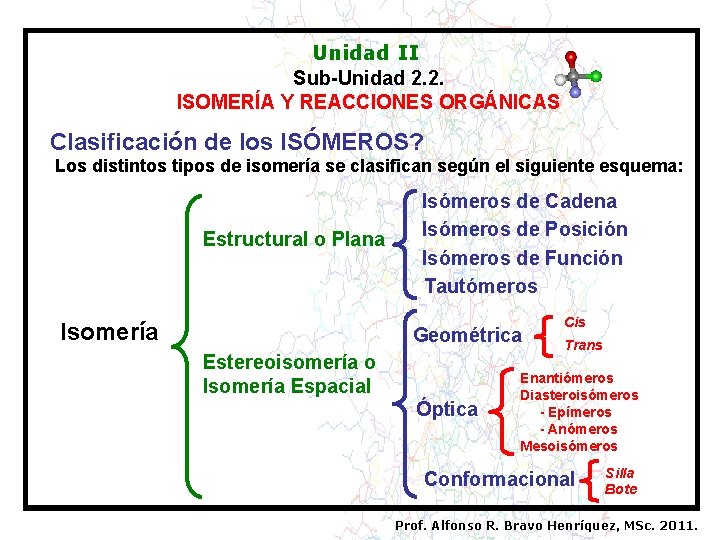
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Clasificación de los ISÓMEROS? Los distintos tipos de isomería se clasifican según el siguiente esquema: Estructural o Plana Isomería Isómeros de Cadena Isómeros de Posición Isómeros de Función Tautómeros Geométrica Estereoisomería o Isomería Espacial Óptica Cis Trans Enantiómeros Diasteroisómeros - Epímeros - Anómeros Mesoisómeros Conformacional Silla Bote Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL o PLANA: La isomería estructural o plana se debe a diferencias de estructura y puede explicarse mediante fórmulas planas. Los Isómeros Estructurales se subdividen en: Isómeros de Cadena o Esqueleto Isómeros de Posición Isómeros de Función Tautómeros Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
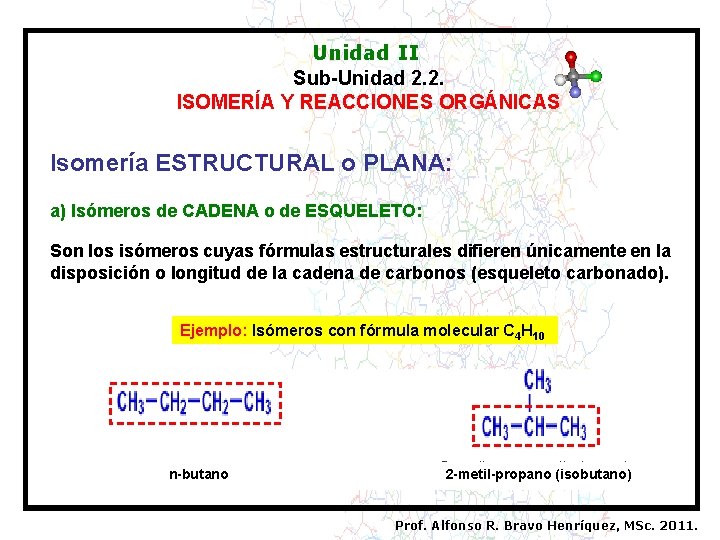
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL o PLANA: a) Isómeros de CADENA o de ESQUELETO: Son los isómeros cuyas fórmulas estructurales difieren únicamente en la disposición o longitud de la cadena de carbonos (esqueleto carbonado). Ejemplo: Isómeros con fórmula molecular C 4 H 10 n-butano 2 -metil-propano (isobutano) Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
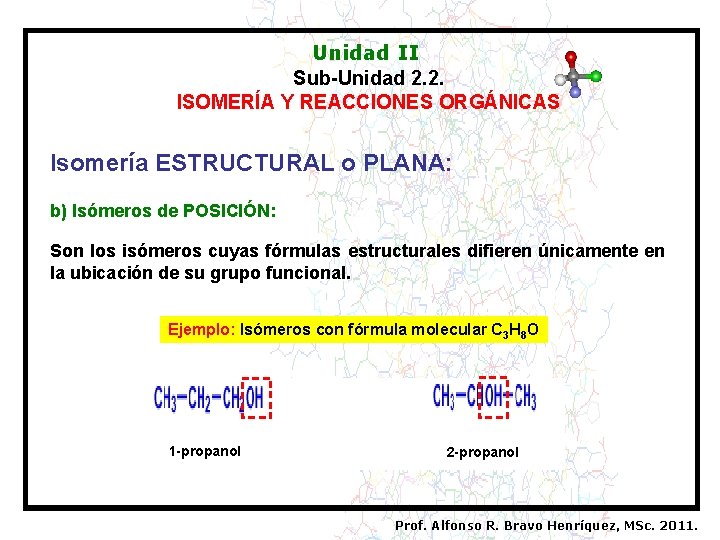
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL o PLANA: b) Isómeros de POSICIÓN: Son los isómeros cuyas fórmulas estructurales difieren únicamente en la ubicación de su grupo funcional. Ejemplo: Isómeros con fórmula molecular C 3 H 8 O 1 -propanol 2 -propanol Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
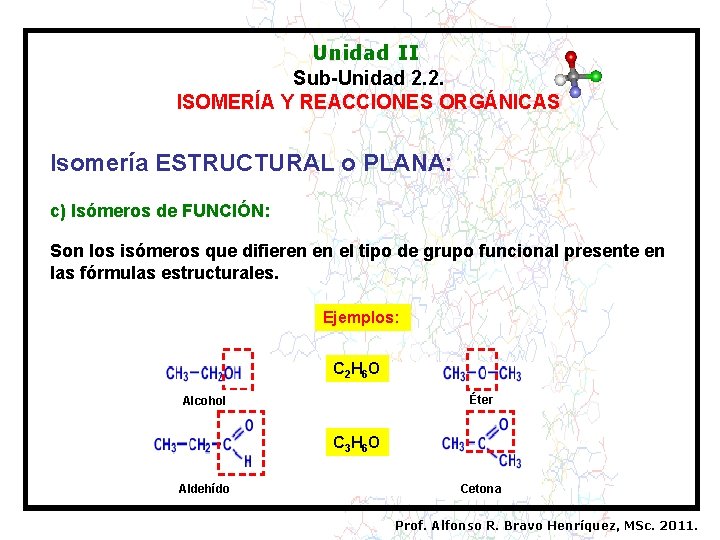
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL o PLANA: c) Isómeros de FUNCIÓN: Son los isómeros que difieren en el tipo de grupo funcional presente en las fórmulas estructurales. Ejemplos: C 2 H 6 O Éter Alcohol C 3 H 6 O Aldehído Cetona Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
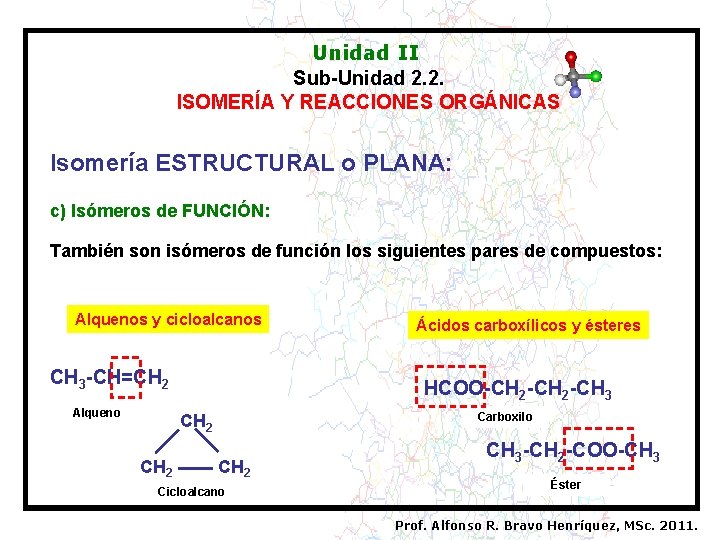
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL o PLANA: c) Isómeros de FUNCIÓN: También son isómeros de función los siguientes pares de compuestos: Alquenos y cicloalcanos CH 3 -CH=CH 2 Alqueno HCOO-CH 2 -CH 3 Carboxilo CH 2 Ácidos carboxílicos y ésteres CH 2 Cicloalcano CH 3 -CH 2 -COO-CH 3 Éster Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
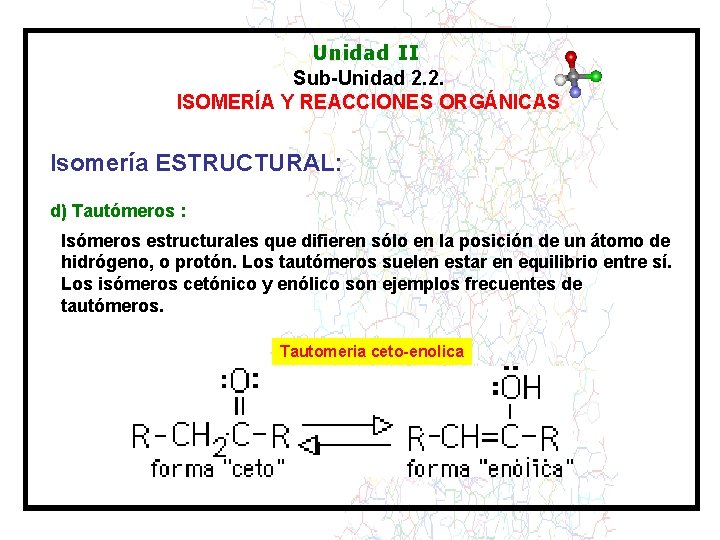
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS Isomería ESTRUCTURAL: d) Tautómeros : Isómeros estructurales que difieren sólo en la posición de un átomo de hidrógeno, o protón. Los tautómeros suelen estar en equilibrio entre sí. Los isómeros cetónico y enólico son ejemplos frecuentes de tautómeros. Tautomeria ceto-enolica
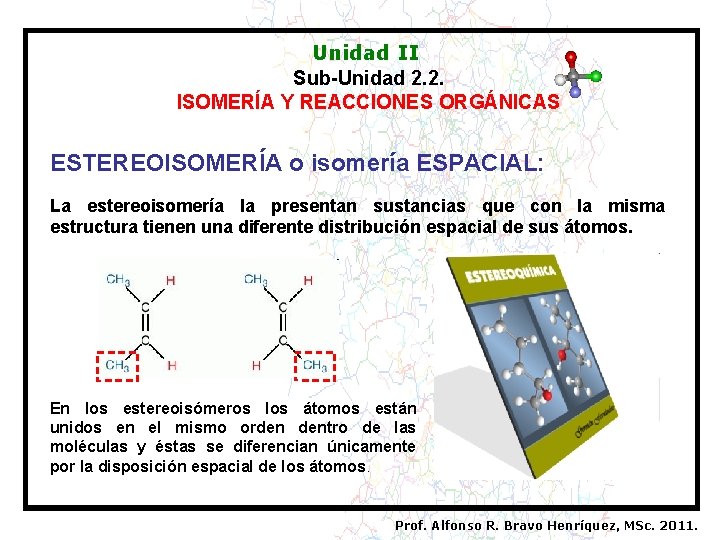
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: La estereoisomería la presentan sustancias que con la misma estructura tienen una diferente distribución espacial de sus átomos. En los estereoisómeros los átomos están unidos en el mismo orden dentro de las moléculas y éstas se diferencian únicamente por la disposición espacial de los átomos. Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
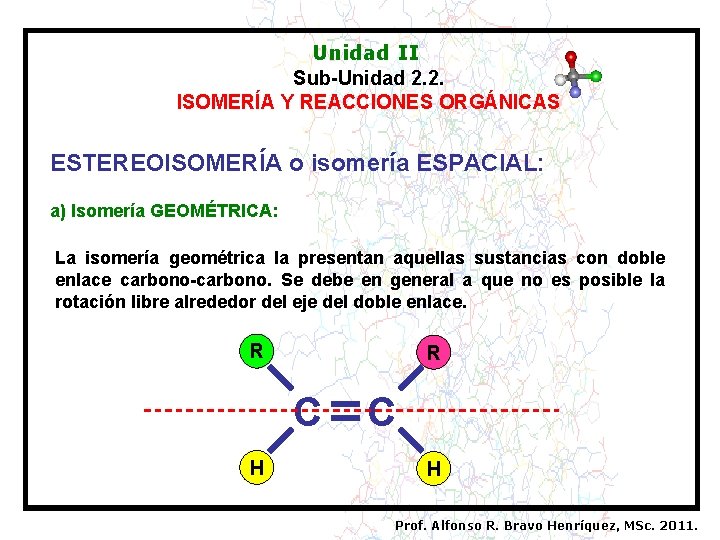
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: a) Isomería GEOMÉTRICA: La isomería geométrica la presentan aquellas sustancias con doble enlace carbono-carbono. Se debe en general a que no es posible la rotación libre alrededor del eje del doble enlace. R R C H Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
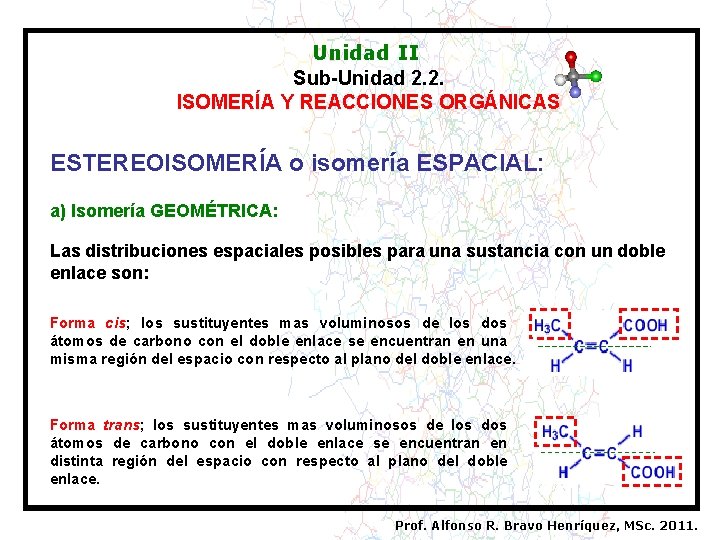
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: a) Isomería GEOMÉTRICA: Las distribuciones espaciales posibles para una sustancia con un doble enlace son: Forma cis; los sustituyentes mas voluminosos de los dos átomos de carbono con el doble enlace se encuentran en una misma región del espacio con respecto al plano del doble enlace. Forma trans; los sustituyentes mas voluminosos de los dos átomos de carbono con el doble enlace se encuentran en distinta región del espacio con respecto al plano del doble enlace. Prof. Alfonso R. Bravo Henríquez, MSc. 2011.

Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: La isomería óptica la presentan aquellas sustancias que al ser atravesadas por luz polarizada plana producen un giro del plano de vibración de la luz. Se dice que estas sustancias tienen actividad óptica. La luz que vibra en un solo plano se llama luz polarizada. Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
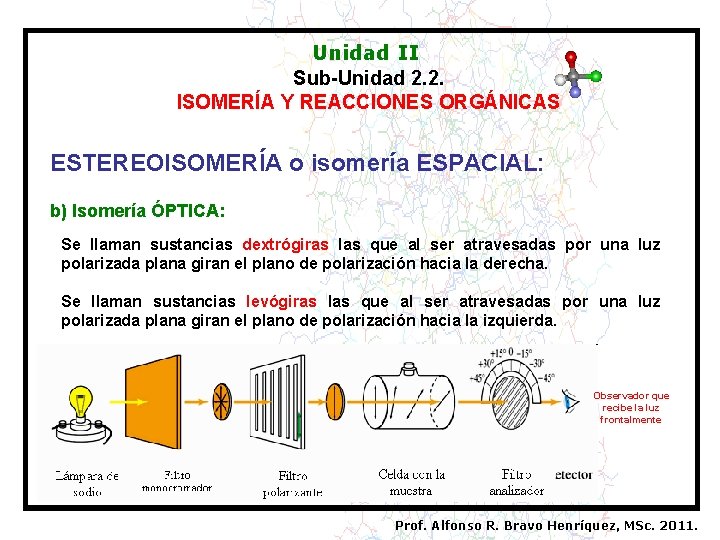
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: Se llaman sustancias dextrógiras las que al ser atravesadas por una luz polarizada plana giran el plano de polarización hacia la derecha. Se llaman sustancias levógiras las que al ser atravesadas por una luz polarizada plana giran el plano de polarización hacia la izquierda. Observador que recibe la luz frontalmente Prof. Alfonso R. Bravo Henríquez, MSc. 2011.

Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: ¿ Por qué un compuesto tiene ACTIVIDAD ÓPTICA? La causa de la actividad óptica es la asimetría molecular, por la presencia en la molécula de al menos un átomo de carbono asimétrico o quiral. Como consecuencia, desvía el plano de la luz polarizada hacia la derecha (isómero dextrógiro) o la izquierda (isómero levógiro). El átomo de carbono asimétrico o quiral (*) se caracteriza por estar unido a cuatro sustituyentes diferentes. * C * Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
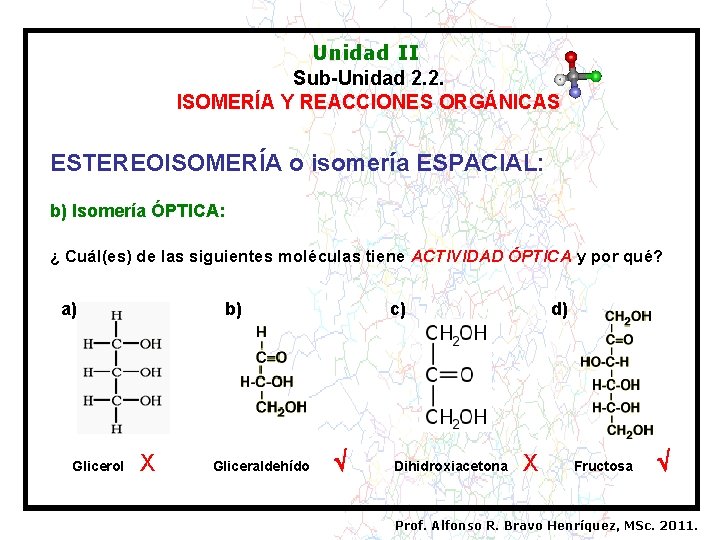
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: ¿ Cuál(es) de las siguientes moléculas tiene ACTIVIDAD ÓPTICA y por qué? a) Glicerol b) X Gliceraldehído c) Dihidroxiacetona d) X Fructosa Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
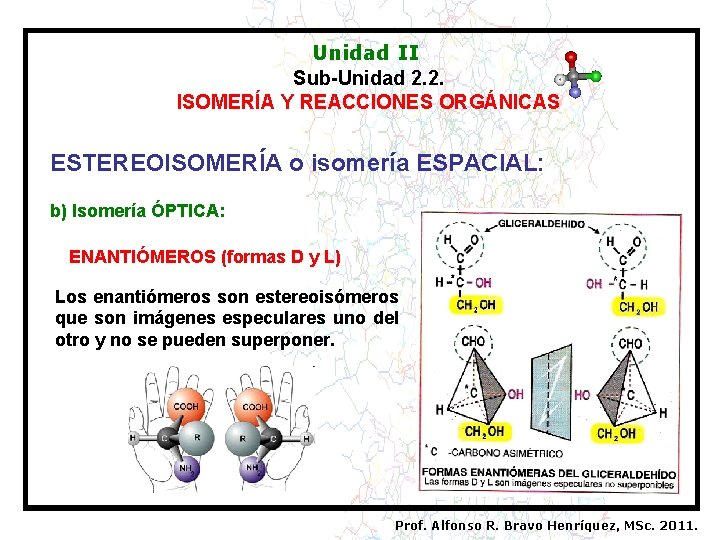
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: ENANTIÓMEROS (formas D y L) Los enantiómeros son estereoisómeros que son imágenes especulares uno del otro y no se pueden superponer. Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
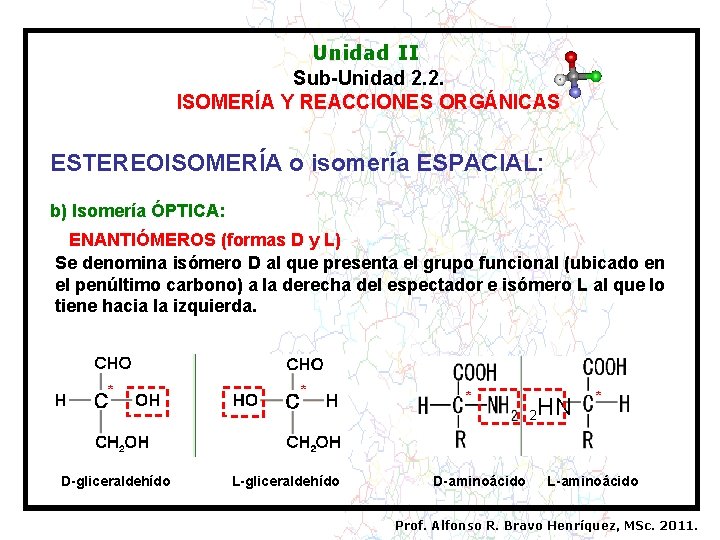
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: ENANTIÓMEROS (formas D y L) Se denomina isómero D al que presenta el grupo funcional (ubicado en el penúltimo carbono) a la derecha del espectador e isómero L al que lo tiene hacia la izquierda. * D-gliceraldehído * L-gliceraldehído * D-aminoácido 2 HN * L-aminoácido Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
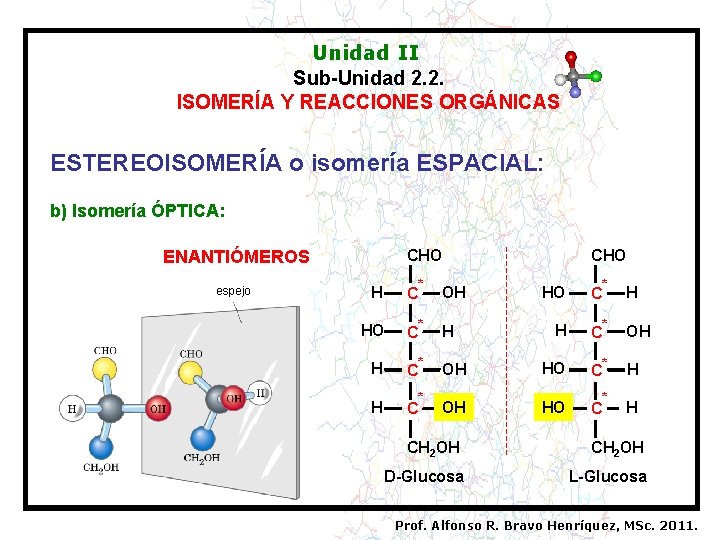
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: CHO ENANTIÓMEROS espejo * HO * C H H C* OH OH HO C* H OH HO * C H H C HO C* H H C* H C * CHO OH CH 2 OH D-Glucosa L-Glucosa Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
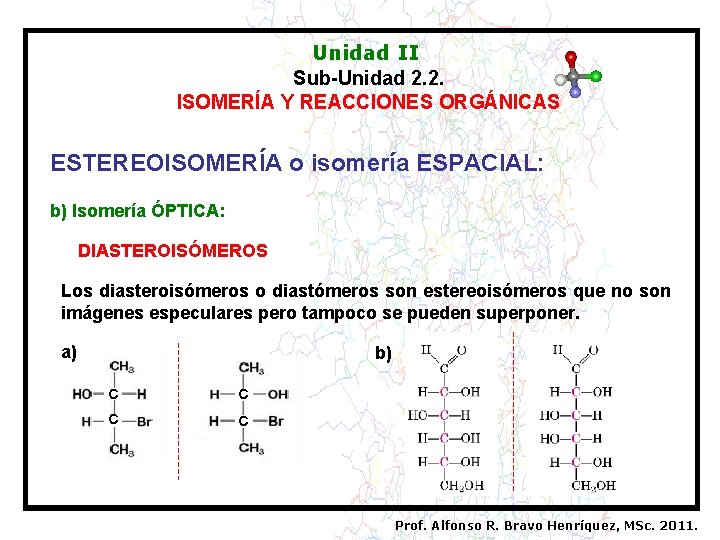
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: DIASTEROISÓMEROS Los diasteroisómeros o diastómeros son estereoisómeros que no son imágenes especulares pero tampoco se pueden superponer. a) b) C C Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
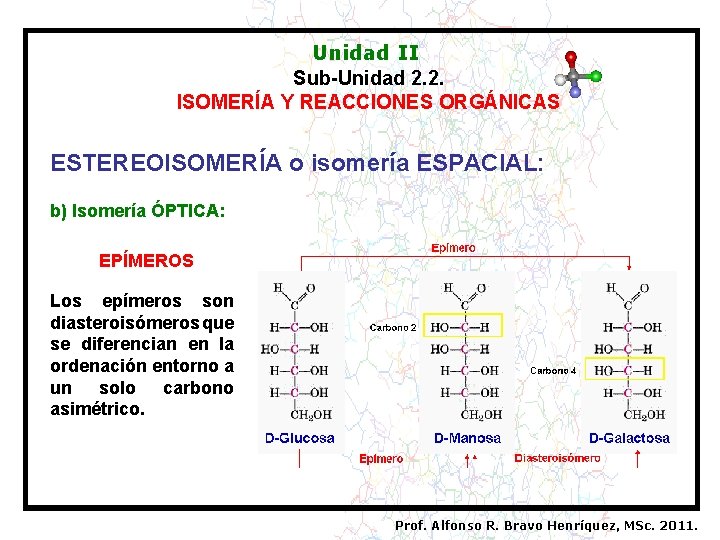
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: EPÍMEROS Los epímeros son diasteroisómeros que se diferencian en la ordenación entorno a un solo carbono asimétrico. Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
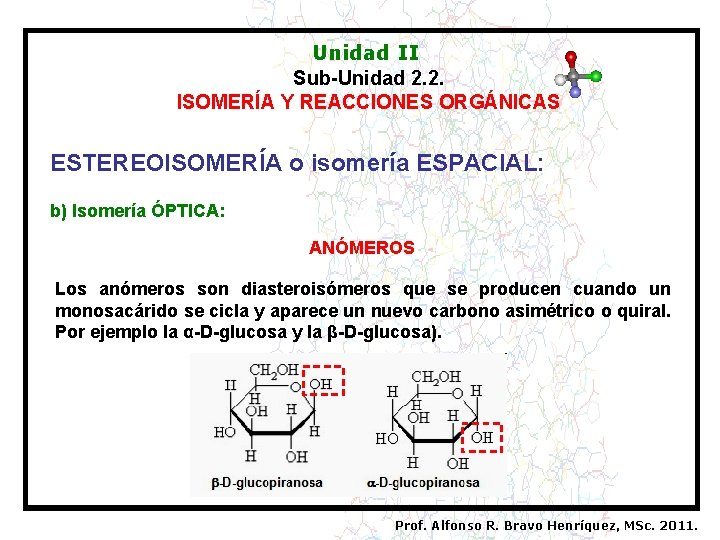
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: ANÓMEROS Los anómeros son diasteroisómeros que se producen cuando un monosacárido se cicla y aparece un nuevo carbono asimétrico o quiral. Por ejemplo la α-D-glucosa y la β-D-glucosa). Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
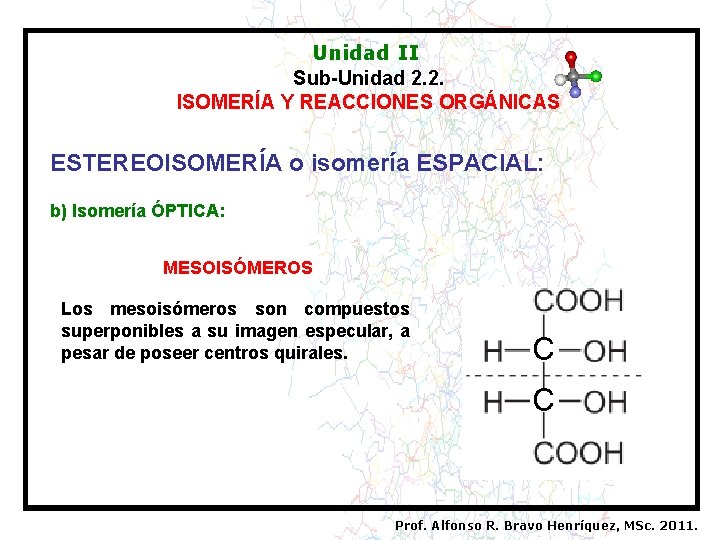
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: b) Isomería ÓPTICA: MESOISÓMEROS Los mesoisómeros son compuestos superponibles a su imagen especular, a pesar de poseer centros quirales. C C Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
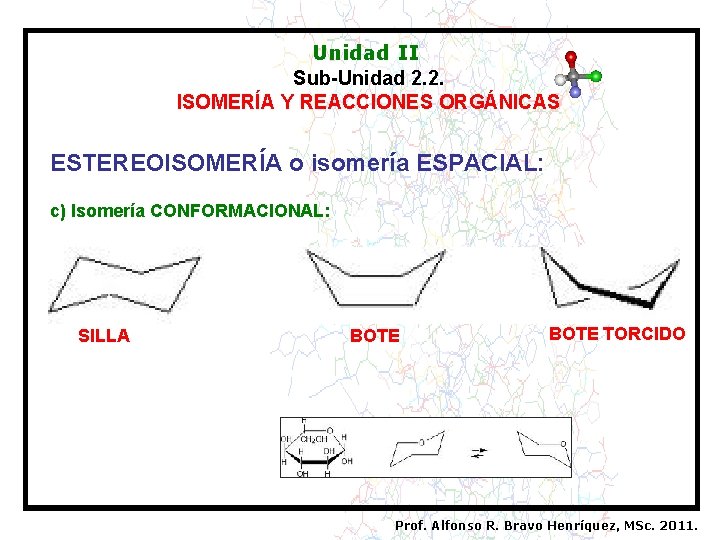
Unidad II Sub-Unidad 2. 2. ISOMERÍA Y REACCIONES ORGÁNICAS ESTEREOISOMERÍA o isomería ESPACIAL: c) Isomería CONFORMACIONAL: SILLA BOTE TORCIDO Prof. Alfonso R. Bravo Henríquez, MSc. 2011.
- Slides: 23