UNIDAD II PROPIEDADES COLIGATIVAS Objetivo comprender la relacin

UNIDAD II: PROPIEDADES COLIGATIVAS Objetivo: comprender la relación entre la concentración de soluto y las propiedades de las soluciones.

Propiedades coligativas Son aquellas propiedades físicas de las soluciones que dependen más bien de la cantidad de soluto que de su naturaleza.

Cuatro son las propiedades coligativas: 1) Disminución de la presión de vapor 2) Disminución del punto de congelación 3) Aumento del punto de ebullición 4) Presión osmótica
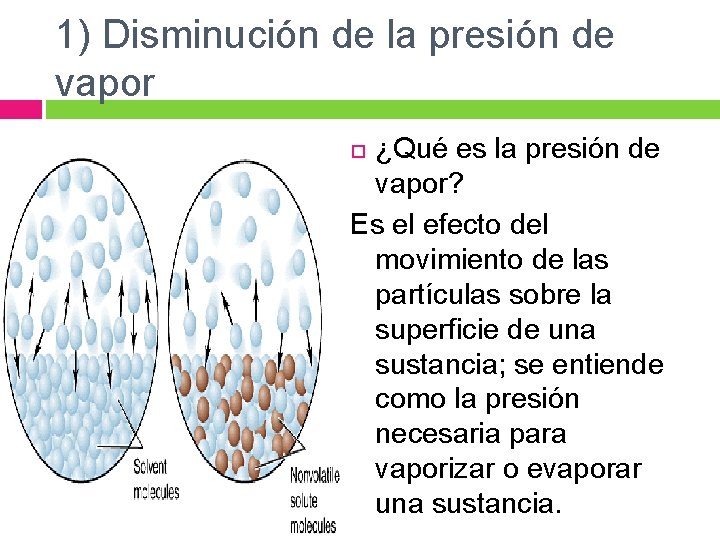
1) Disminución de la presión de vapor ¿Qué es la presión de vapor? Es el efecto del movimiento de las partículas sobre la superficie de una sustancia; se entiende como la presión necesaria para vaporizar o evaporar una sustancia.
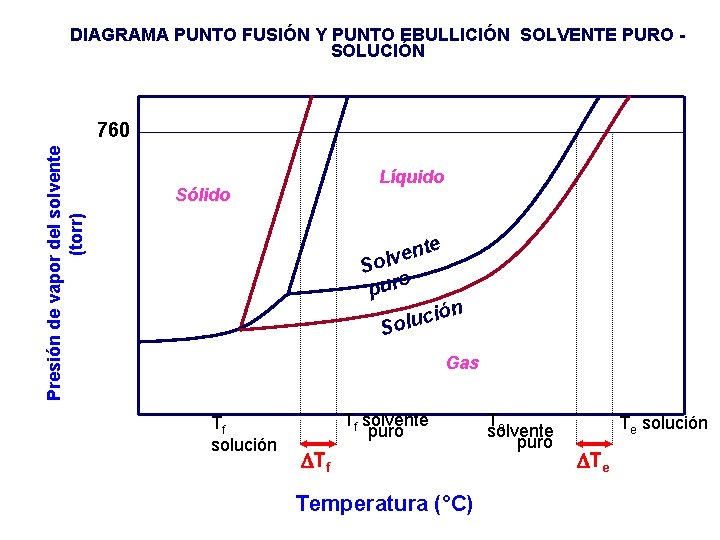
DIAGRAMA PUNTO FUSIÓN Y PUNTO EBULLICIÓN SOLVENTE PURO SOLUCIÓN Presión de vapor del solvente (torr) 760 Líquido Sólido nte e v l So puro n ó i c u Sol Gas Tf solución Tf solvente puro Tf Temperatura (°C) Te solvente puro Te solución Te

Interpretación del gráfico En un solvente puro (es decir, sin soluto) existen menos moléculas y por tanto una mayor presión o movimiento de estas moléculas sobre la superficie de la sustancia (presión de vapor). En cambio, cuando el solvente se mezcla con un soluto (solución), existe una menor presión de vapor (menor movimiento de las moléculas). Por tanto, la presión de vapor disminuye cuando se tiene una solución.

2) Descenso Crioscópico Cuando se tiene una solución y la presión de vapor disminuye, significa que se requiere de menor temperatura para lograr la congelación. Esto se conoce como descenso crioscópico. Esta propiedad de las soluciones tiene un uso masivo en países donde nieva con frecuencia, ya que al agregar sal al hielo, éste se derrite con mayor facilidad.

Explicación… El hielo es uno de los 3 estados naturales del agua, no es otra cosa que agua sólida cristalizada, congelada. El agua pura a la altitud del nivel del mar se congela a 0 ºC y la densidad del hielo a esta temperatura es de 0, 9169 gr/cm 3. Mientras que la mayoría de las sustancias se contraen al congelarse, el agua es una de las pocas sustancias que al congelarse aumenta de volumen, o lo que es igual disminuye su densidad. Pero este equilibrio dinámico también se rompe al añadir sal. Cuando añadimos sal al hielo lo que se funde no es el hielo sino una mezcla de hielo y sal. Cuando la sal Na. Cl (Na+, Cl–) entra en contacto con el hielo, los iones se combinan con las moléculas altamente polares del agua. Esta mezcla tiene un punto de congelación inferior a 0º C y es la base de la aplicación de hielo en las carreteras. El descenso crioscópico es la reducción del punto de fusión de un disolvente puro que se consigue por la presencia de solutos. ¿Cualquier sustancia extraña nos permitiría rebajar el punto de congelación? . Pues si, por cada mol de partículas extrañas disueltas en un kilo de agua, el punto de congelación baja en aproximadamente 1, 7 -1, 9 ° C. Podríamos añadir azúcar, alcohol, u otras sales que también bajaríamos el punto de congelación y derretiríamos el hielo. El descenso crioscópico es directamente proporcional a la molalidad o cantidad de soluto por kilo de disolvente.

¿Por qué sal en las carreteras? La sal se utiliza en las carreteras y caminos, simplemente porque es barata y fácilmente disponible. Sin entrar a valorar la eficacia de la sal frente a otros productos que en cualquier caso también dependerá de la granulometría, de los métodos de reparto, del tipo de asfalto de la carretera, etc. existe un debate importante en cuanto a la repercusión ecológica del uso masivo de este producto en nuestras carreteras. La sal se diluye en agua y ésta corre por ríos, acuíferos y demás, y además se cuestiona que repercursiones tendrá su uso a largo plazo
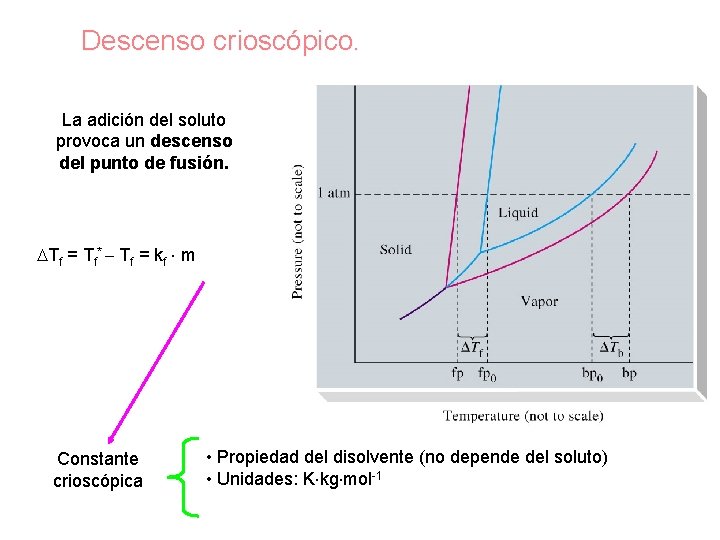
Descenso crioscópico. La adición del soluto provoca un descenso del punto de fusión. Tf = Tf* - Tf = kf × m Constante crioscópica • Propiedad del disolvente (no depende del soluto) • Unidades: K×kg×mol-1

Tf = Kf • m Donde: Tf = Disminución del punto de congelación Kf = Constante molal de descenso del punto de congelación m = molalidad de la solución (Moles / kg solvente) Tf = Tf solvente - Tf solución

Ejemplo ¿Cuál es el punto de congelación de una disolución que contiene 9, 75 gr de nitrobenceno C 6 H 5 NO 2 en 175 gr de benceno? (Kf = 5, 12) (MM: 123 g/mol) Datos: Gramos soluto: 9, 75 Gramos solvente: 175 g Kf : 5, 12 __________ Molalidad: gramos soluto / masa molar x kg solvente Molalidad : 9, 75 / (123 x 0, 175) = 0, 453 Tf = Kf • m x = 5, 12 x 0, 453 X = 2, 319. Si el benceno congela a los 5, 48 º C y la variación de temperatura es 2, 319 º C, entonces la solución congelará a los 5, 48 – 2, 319 = 3, 161 º C

3) Ascenso ebulloscópico En una solución, el punto de ebullición aumenta respecto al solvente puro; debido a que se tienen más partículas a las cuales llevar hasta el estado gaseoso.
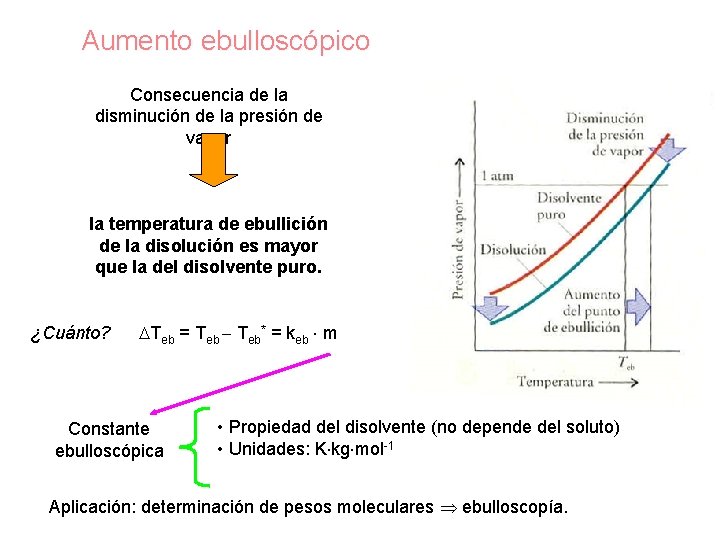
Aumento ebulloscópico Consecuencia de la disminución de la presión de vapor la temperatura de ebullición de la disolución es mayor que la del disolvente puro. ¿Cuánto? Teb = Teb - Teb* = keb × m Constante ebulloscópica • Propiedad del disolvente (no depende del soluto) • Unidades: K×kg×mol-1 Aplicación: determinación de pesos moleculares Þ ebulloscopía.
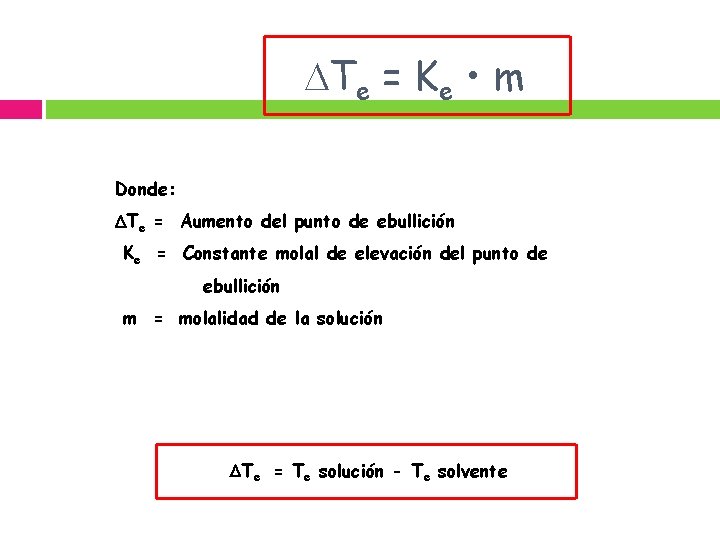
Te = Ke • m Donde: Te = Aumento del punto de ebullición Ke = Constante molal de elevación del punto de ebullición m = molalidad de la solución Te = Te solución - Te solvente
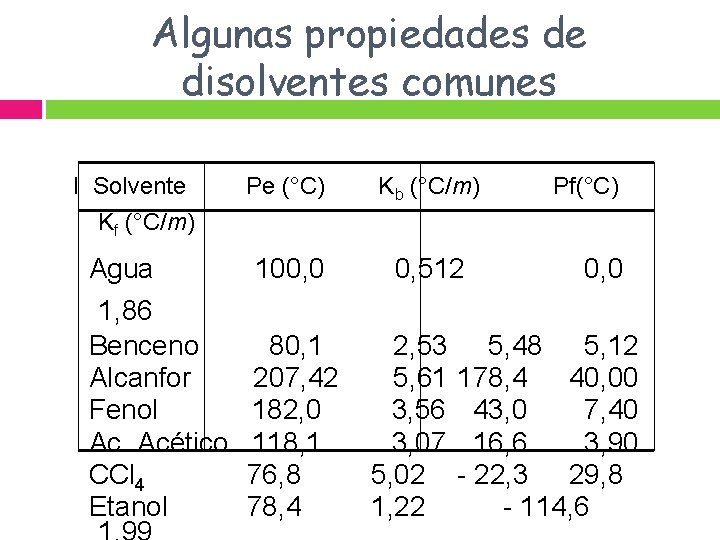
Algunas propiedades de disolventes comunes I Solvente Pe (°C) Kb (°C/m) Kf (°C/m) Pf(°C) Agua 100, 0 0, 512 0, 0 1, 86 Benceno 80, 1 2, 53 5, 48 5, 12 Alcanfor 207, 42 5, 61 178, 4 40, 00 Fenol 182, 0 3, 56 43, 0 7, 40 Ac. Acético 118, 1 3, 07 16, 6 3, 90 CCl 4 76, 8 5, 02 - 22, 3 29, 8 Etanol 78, 4 1, 22 - 114, 6

Ejemplo Calcule el punto de ebullición de una solución que se prepara disolviendo 24, 6 gr de glucosa C 6 H 12 O 6 de masa molar=180 gr en 250 gr de agua. Datos: Gramos soluto : 24, 6 Gramos solvente: 250 g Kb = 0, 512 _______________________ Molalidad: gramos soluto / masa molar x kg solvente Molalidad : 24, 6 / 180 x 0, 250 = 0, 546 Tf = Kb • m x = 0, 512 x 0, 546 X = 0, 279 Si el agua ebulle a 100 ºC, entonces la solución lo hará a (100 + 0, 279) = 100, 279 º C

4) Presión osmótica Se define como la presión que debe aplicarse para detener de manera completa la osmosis. Fórmula: π = M x R x T Donde: π: presión osmótica M: molaridad (mol / litro) R: constante de los gases T: temperatura
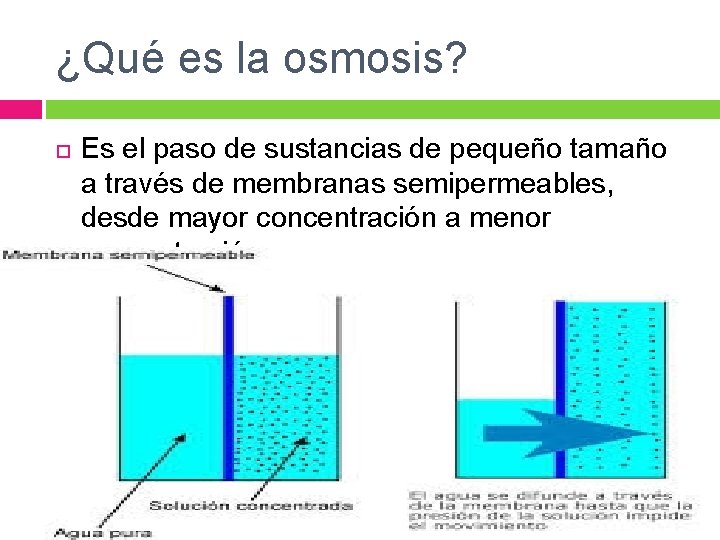
¿Qué es la osmosis? Es el paso de sustancias de pequeño tamaño a través de membranas semipermeables, desde mayor concentración a menor concentración.

En las membranas biológicas, el agua se transporta mediante osmosis para regular las concentraciones de sustancias en el medio intracelular. Este mecanismo funciona transportando agua desde la zona con menor concentración de soluto (es decir, mayor cantidad de agua) hacia la zona con mayor cantidad de soluto (o menor cantidad de agua). Una vez que se ha alcanzado el nivel deseado, la presión de las sustancias a ambos lados de la membrana, es suficiente para detener el proceso de transporte.
- Slides: 20