Unidad 6 Equilibrio qumico 0 Sistemas en equilibrio

Unidad 6 Equilibrio químico
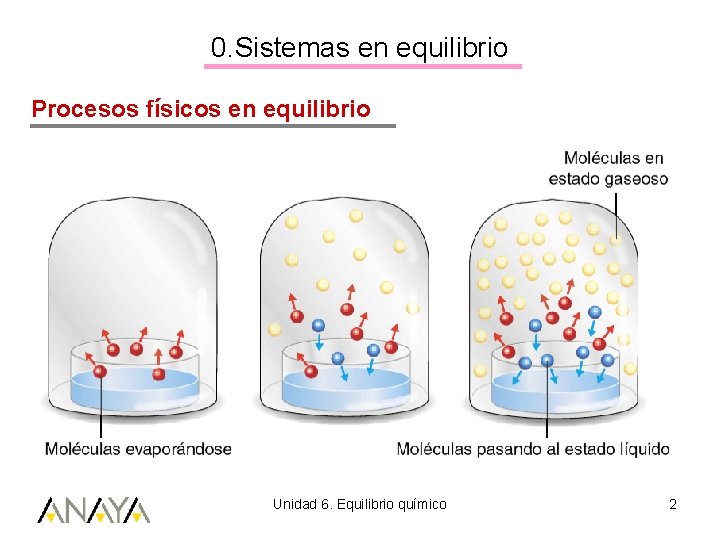
0. Sistemas en equilibrio Procesos físicos en equilibrio Unidad 6. Equilibrio químico 2
0. Sistemas en equilibrio • Reacciones químicas en equilibrio Unidad 6. Equilibrio químico 3

0. Sistemas en equilibrio Equilibrio químico o físico, es un estado del sistema en el que no se observan cambios a nivel macroscópico a medida que transcurre el tiempo • Equilibrio dinámico • Coexisten reactivos y productos • Se da en recipientes cerrados • La velocidad directa e inversa es igual. Con velocidad simultánea en ambos sentidos • La concentración de productos y reactivos son constantes Unidad 6. Equilibrio químico 4
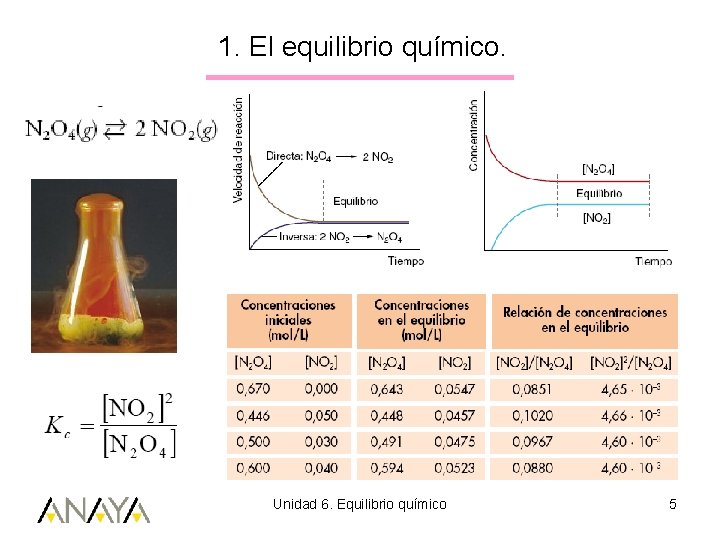
1. El equilibrio químico. Unidad 6. Equilibrio químico 5
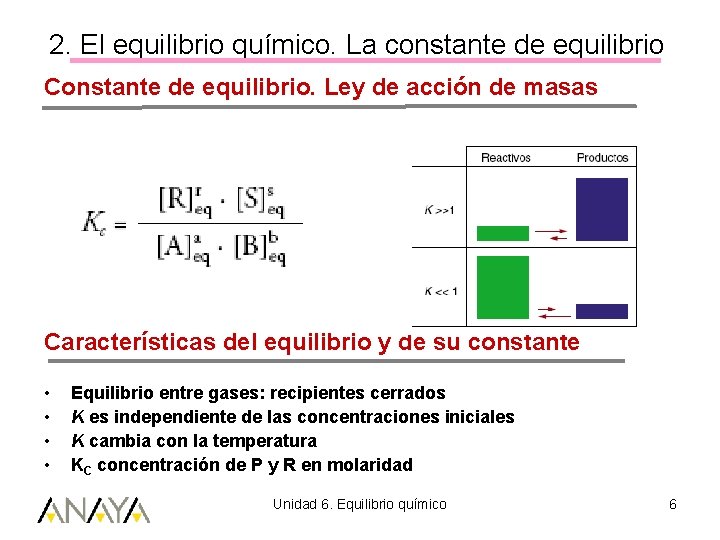
2. El equilibrio químico. La constante de equilibrio Constante de equilibrio. Ley de acción de masas Características del equilibrio y de su constante • • Equilibrio entre gases: recipientes cerrados K es independiente de las concentraciones iniciales K cambia con la temperatura KC concentración de P y R en molaridad Unidad 6. Equilibrio químico 6

2. El equilibrio químico. La constante de equilibrio Relación entre G y K La constante de equilibrio está relacionada con el cambio que experimenta la energía estándar libre de Gibbs DGº= - RT·Ln. Kp • Cuanto más espontáneo sea un proceso en condiciones estándar, mayor será el valor de la constante de equilibrio y viceversa. • • DGº<0, K>1 la reacción se desplaza hacia los productos DGº>0, K<1 la reacción se desplaza hacia los reactivos Unidad 6. Equilibrio químico 7
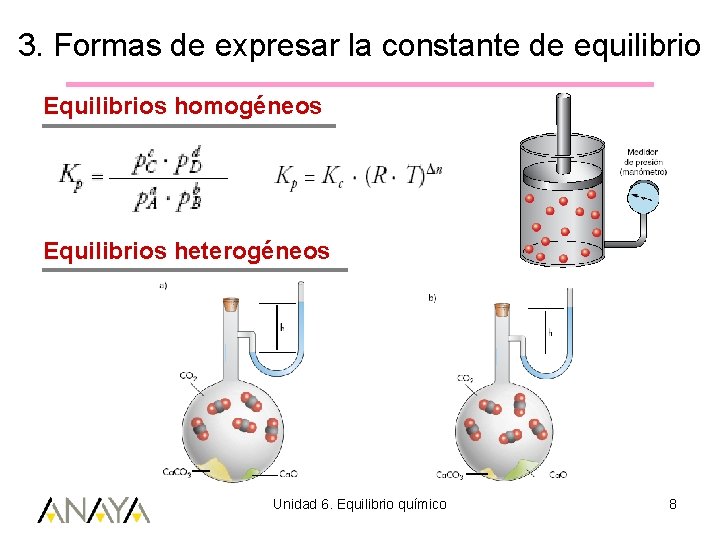
3. Formas de expresar la constante de equilibrio Equilibrios homogéneos Equilibrios heterogéneos Unidad 6. Equilibrio químico 8
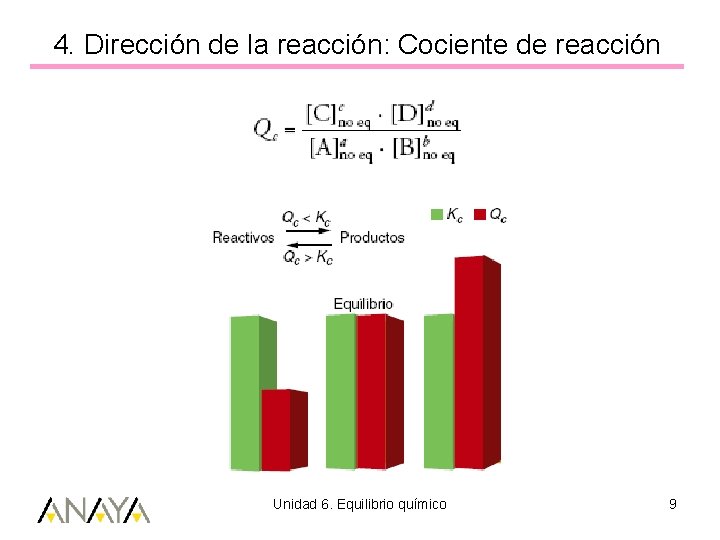
4. Dirección de la reacción: Cociente de reacción Unidad 6. Equilibrio químico 9

5. Grado de disociación a: fracción de mol que se disocia. Tanto por uno de reactivo disociado en el equilibrio Unidad 6. Equilibrio químico 10

6. Factores que modifican el equilibrio Principio de Le Châtelier Un sistema en equilibrio responderá a una perturbación desplazando el equilibrio en sentido opuesto al efecto de la perturbación. Cambios en la concentración El aumento de concentración de una sustancia lleva al equilibrio en sentido opuesto donde se encuentre, y viceversa Unidad 6. Equilibrio químico 11
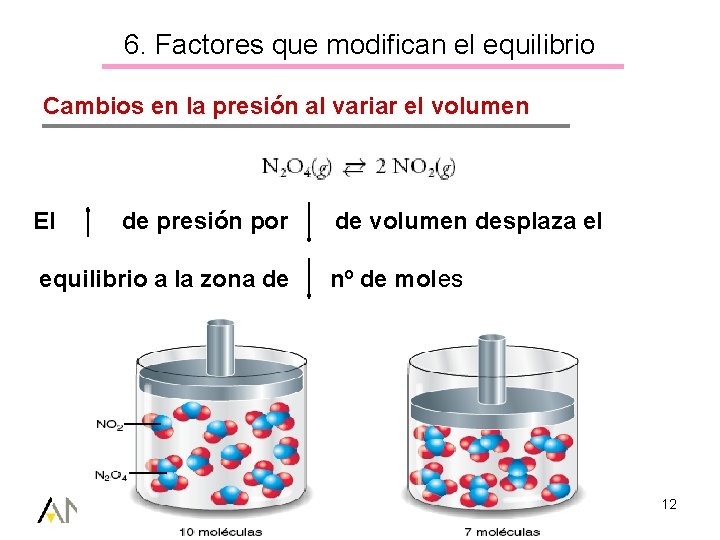
6. Factores que modifican el equilibrio Cambios en la presión al variar el volumen El de presión por equilibrio a la zona de de volumen desplaza el nº de moles Unidad 6. Equilibrio químico 12

6. Factores que modifican el equilibrio Adición de un gas inerte • P = cte • V = cte volumen varia la concentración y se reajusta el equilibrio presión total pero no la concentración NO VARÍA Cambios en la temperatura • Reacción endotérmica: Si T aumenta, el equilibrio se desplaza hacia la derecha: K aumenta. • Reacción exotérmica: Si T aumenta, el equilibrio se desplaza hacia la izquierda: K disminuye. Efecto de un catalizador • No cambia K Unidad 6. Equilibrio químico 13

7. Solubilidad y precipitación Producto de solubilidad Solubilidad Unidad 6. Equilibrio químico 14

7. Solubilidad y precipitación Condiciones para la formación de un precipitado Q= producto iónico (cociente de reacción) Q<Ks, no se formará precipitado Q>Ks, sí se formará precipitado Q= Ks, el sistema se encuentra en equilibrio Unidad 6. Equilibrio químico 15

7. Solubilidad y precipitación Relación entre solubilidad y producto de solubilidad Equilibrio Aa. Bb(s) Conc inicial Co Conc equilibrio a An+ (aq) Co -S + b. B m- (aq) 0 0 a· S b·S Según la Ks anteriormente establecida Ks= (a. S)a·(b. S)b Despejamos S= a+b √( Ks/(aa·bb) Unidad 6. Equilibrio químico 16

7. Solubilidad y precipitación Precipitación fraccionada En disolución tengo Cl- y Cr. O 4 -2 Unidad 6. Equilibrio químico 17
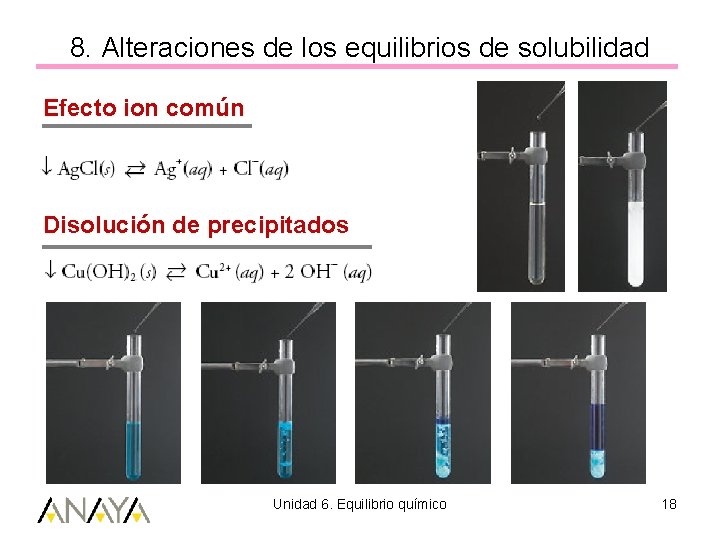
8. Alteraciones de los equilibrios de solubilidad Efecto ion común Disolución de precipitados Unidad 6. Equilibrio químico 18
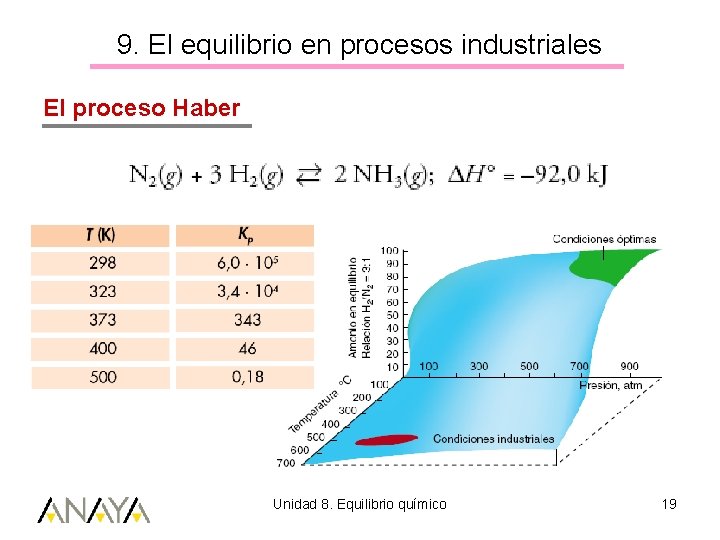
9. El equilibrio en procesos industriales El proceso Haber Unidad 8. Equilibrio químico 19
- Slides: 19