Unidad 1 Generalidades Lic Biologa Maestra Oropesa Bruno

Unidad 1. Generalidades Lic. Biología Maestra: Oropesa Bruno Erika Primer semestre

1. 1. Química, Ciencia y Medio Ambiente QUÍMICA � ciencia que estudia tanto la composición, estructura y propiedades de la materia como los cambios que ésta experimenta durante las reacciones químicas y su relación con la energía.

Las disciplinas de la química se han agrupado según la clase de materia bajo estudio o el tipo de estudio realizado. Entre éstas se tienen la química inorgánica, que estudia la materia inorgánica; la química orgánica, que trata con la materia orgánica; la bioquímica, el estudio de substancias en organismos biológicos; la físico-química, que comprende los aspectos energéticos de sistemas químicos a escalas macroscópicas, moleculares y atómicas; la química analítica, que analiza muestras de materia y trata de entender su composición y estructura

El medio ambiente es el conjunto de todas las cosas vivas que nos rodean. De éste obtenemos agua, comida, combustibles y materias primas que sirven para fabricar las cosas que utilizamos diariamente.

Al abusar o hacer mal uso de los recursos naturales que se obtienen del medio ambiente, lo ponemos en peligro y lo agotamos. El aire y el agua están contaminándose, los bosques están desapareciendo, debido a los incendios y a la explotación excesiva y los animales se van extinguiendo por el exceso de la caza y de la pesca.

BIBLIOGRAFÍA Anonimo. 2013. Química. 2013. www. es. wikipedia. org/wiki/Quimica Anonimo. 2000. medio ambiente. 2013. www. cino. org. mx/ninos/html/onu-n 5. htp

a l e d n o i c a l e R 1. 2. s a r t o n o c a c i m í qu s a i c cien

1. 2 Relación de la Química con las demás ciencias La Química como una ciencia involucrada en el campo del saber y de la investigación, siendo su área primordial el estudio de las propiedades, composición y estructura de la materia, Necesita de las demás ciencias al igual que ella necesitan de la química, para de esta manera, dar el mayor soporte a la objetividad de manera total al conocimiento.

Se incluye esta ciencia en la química, debido a que la misma necesita el empleo de formulas, símbolos y números para llevar a cabo, un sin numero de operaciones aritméticas que facilitan la veracidad y objetividad de un estudio o simplemente, obtener resultados confiable de hasta la mas mínima operación cuantitativa que se lleven a cabo en esta ciencia

Relación con la Biología Como la biología es la ciencia de la vida, necesita de la química para de esta forma estudiar en el área anatómica y morfológica la estructura y composición de las células, tejidos y de los organismo vivos en si.

RELACIÓN CON LA FÍSICA Cuando se lleva a cabo una reacción química, es de suma importancia tomar en cuanta el equilibrio de la misma y su termodinámica, encontrando la química una basta explicación en la física, la cual expone este comportamiento de manera detallada.

Relación con Geología Esta ciencia, se encarga del estudio de la trasformaciones y cambios de forma interior de la corteza terrestre. La química se vincula en ella, ayudándole en su investigación a descubrir, la composición química de los terrenos y los tipos de minerales que se encuentran en ellas.

Bibliografía Anónimo. 2009. Relación de la quimica con otras ciencias. 2013. http: //zafaquimica. blogspot. mx/2009/06/relacion-de-laquimica-con-las-demas. html


Bioquímica Es una cienciaque estudia la composición química de los seres vivos, especialmente las proteínas, carbohidratos, lípidos y ácidos nucleico, además de otras pequeñas moléculas presentes en las células y las reacciones químicas que sufren estos compuestos (metabolismo) que les permiten obtenergía (catabolismo) y generar biomoléculas propias (anabolismo)

Neuroquímica es el estudio de las moléculas orgánicas que participan en la actividad neuronal. Este término es empleado con frecuencia para referir a los neurotransmisores y otras moléculas como las drogas neuro-activas que influencian la función neuronal.

Xenobioquímica Es la disciplina que estudia el comportamiento metabólico de los compuestos cuya estructura química no es propia en el metabolismo regular de un organismo determinado. Pueden ser metabolitos secundarios de otros organismos (P. ejemplo las micotoxinas, los venenos de serpientes y los fitoquímicos cuando ingresan al organismo humano) o compuestos poco frecuentes o inexistentes en la naturaleza.

Bibliografía Anónimo. 2013. Bioquímica. 2013. http: //es. wikipedia. org/wiki/Bioqu%C 3%ADmica

1. 4 Definiciones Básicas Neto

Química. - Es la ciencia que estudia todo lo relacionado con los procesos en los que se forman unas sustancias a partir de otras Materia. - Es todo aquello que tiene masa y ocupa un lugar en el espacio. Este término engloba todos los cuerpos, objetos y seres que existen en la naturaleza. Materiales. - De lo que están hechos los objetos, los seres y los cuerpos. Son sistemas de materia de aspecto homogéneo. Un determinado material puede estar formado por uno o varios constituyentes Neto

Mezclas homogéneas. Son sistemas de materia en los que no se distingue a simple vista que esté formado por dos o más constituyentes. Hay dos grandes tipos de mezclas homogéneas: las disoluciones y los coloides. Núcleos. - Son la parte positiva de las partículas químicas. Concentran la mayor parte de la masa de las partículas que constituyen. Están formados por protones (con carga positiva) y neutrones (sin carga). Sustancias. - Sistemas de materia de aspecto homogéneo de un solo constituyente. Cada sustancia posee un conjunto de propiedades específicas que la distinguen de las demás Electrones. - Son la parte negativa de las partículas químicas. No se puede saber ni su forma, ni su tamaño, ni su localización precisa, ni cómo se mueven.

Número atómico. Es el número de protones que hay en un núcleo. Se representa con la letra z. Número de masa. Es el número de protones y neutrones en un núcleo. Se representa con la letra A. Sustancias elementales. Son aquellas cuyas partículas sólo contienen fragmentos del mismo tipo, es decir, están formadas por un solo elemento(un solo fragmento o el mismo repetido varias veces). Sustancias compuestas. Son aquellas que en su estructura contienen fragmentos de distinto tipo, es decir, que contienen distintos elementos.

Mezclas heterogéneas. Son sistemas de materia en los que se distinguen a simple vista dos o más materiales (de ahí su aspecto heterogéneo). Por ejemplo: madera y petróleo, madera y oro, agua y petróleo, etcétera.

Anónimo. 2013. Definiciones básicas. 2013. http: //plinios. tripod. com/definiciones. htm

1. 5 Composición y propiedades De la materia: átomo, molécula, elemento Compuesto, mezcla, solución, fase

Átomo Los átomos son la unidad básica de toda la materia, la estructura que define a todos los elementos y tiene propiedades químicas bien definidas. Todos los elementos químicos están compuestos por átomos con exactamente la misma estructura y a su vez, éstos se componen de tres tipos de partículas, como los protones, los neutrones y los electrones. Propiedades atómicas • Masa: La mayor parte de la masa del átomo viene de los nucleones, los protones y neutrones del núcleo. • Tamaño: Los átomos no están delimitados por una frontera clara, por lo que su tamaño se equipara con el de su nube electrónica. Sin embargo, tampoco puede establecerse una medida de esta, debido a las propiedades ondulatorias de los electrones. • Niveles de energía: un electrón ligado en el átomo posee una energía potencial inversamente proporcional a su distancia al núcleo y de signo negativo, lo que quiere decir que esta aumenta con la distancia.
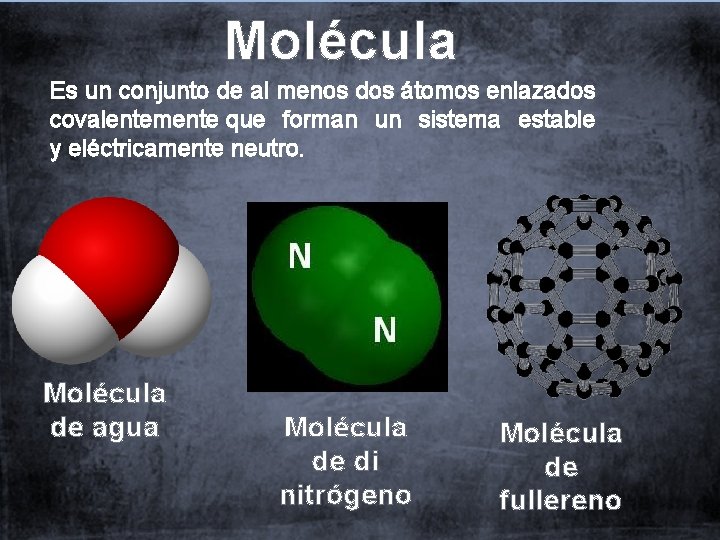
Molécula Es un conjunto de al menos dos átomos enlazados covalentemente que forman un sistema estable y eléctricamente neutro. Molécula de agua Molécula de di nitrógeno Molécula de fullereno

Elemento Es una sustancia pura formada por átomos que tienen el mismo número atómico, es decir, el mismo número de protones. Cada elemento se distingue de los demás por sus propiedades características. Se denomina número atómico al número de protones que tiene el núcleo de un átomo. Este número es igual al número de electrones que el átomo neutro posee alrededor del núcleo

Compuesto es una sustancia formada por la unión de dos o más elementos de la tabla periódica. Una característica esencial es que tiene una fórmula química.

Mezcla es un sistema material formado por dos o más sustancias puras mezcladas pero no combinadas químicamente. En una mezcla no ocurre una reacción química y cada uno de sus componentes mantiene su identidad y propiedades químicas

Una solución (o disolución) es una mezcla de dos o más componentes, perfectamente homogénea ya que cada componente se mezcla íntimamente con el otro, de modo tal que pierden sus características individuales. Esto último significa que los constituyentes son indistinguibles y el conjunto se presenta en una sola fase (sólida, líquida o gas) bien definida. Fase fase (del latín phase: partes o fase) a cada una de las partes macroscópicas de una composición química y propiedades físicas homogéneas que forman un sistema. Los sistemas monofásicos se denominan homogéneos, y los que están formados por varias fases se denominan mezclas o sistemas heterogéneos.

Bibliografía 1. Anonimo. 2013. átomo. 2013. http: //www. ojocientifico. com/4442/que-es-un-atomo 2. Anonimo. 2013. compuesto. 2013. http: //es. wikipedia. org/wiki/Compuesto_qu%C 3%ADmico 3. Anonimo. 2013. Mezcla. 2013. http: //es. wikipedia. org/wiki/Mezcla 4. Anonimo. 2013. Elemento. 2013. http: //es. wikipedia. org/wiki/Elemento_qu%C 3%ADmico 5. Anónimo. 2013. molécula. 2013. http: //es. wikipedia. org/wiki/Mol%C 3%A 9 cula 4. Anonimo. 2006. Disolución. 2013. http: //www. profesorenlinea. cl/Quimica/Disoluciones_quimicas. html

1. 6. Estructura del Átomo
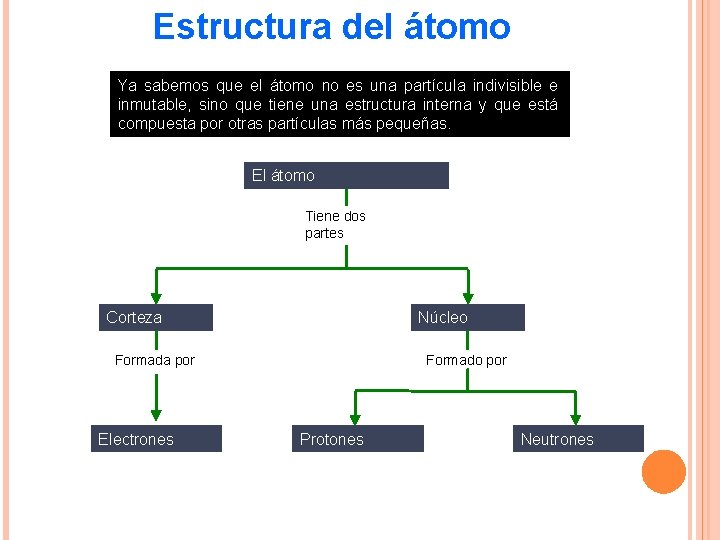
Estructura del átomo Ya sabemos que el átomo no es una partícula indivisible e inmutable, sino que tiene una estructura interna y que está compuesta por otras partículas más pequeñas. El átomo Tiene dos partes Corteza Núcleo Formada por Electrones Formado por Protones Neutrones
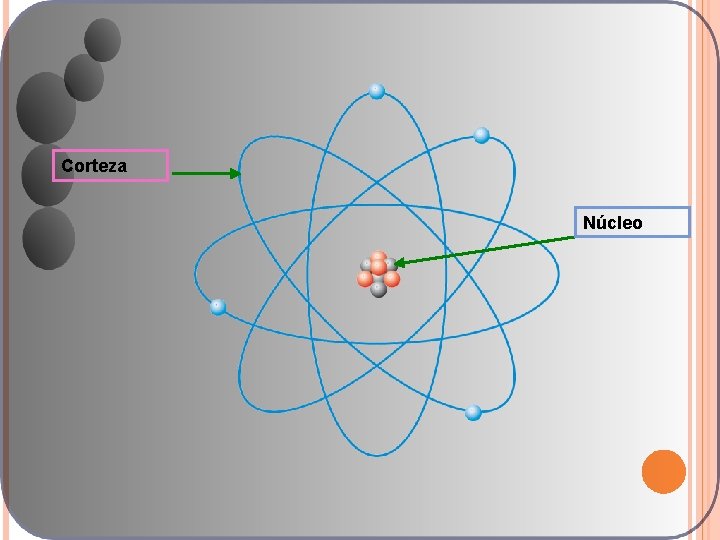
Corteza Núcleo

Corteza Es la zona externa del átomo, de diámetro unas 100000 veces mayor que el radio del núcleo. En ella se mueven los electrones, que son partículas con carga negativa. Un átomo neutro tiene el mismo número de electrones que de protones. Si el átomo cede o gana uno o más electrones, da lugar a un ion. Como el volumen de la corteza es mucho mayor que el del núcleo, este puede considerarse hueco, ya que entre los electrones solo hay vacío. Electrón
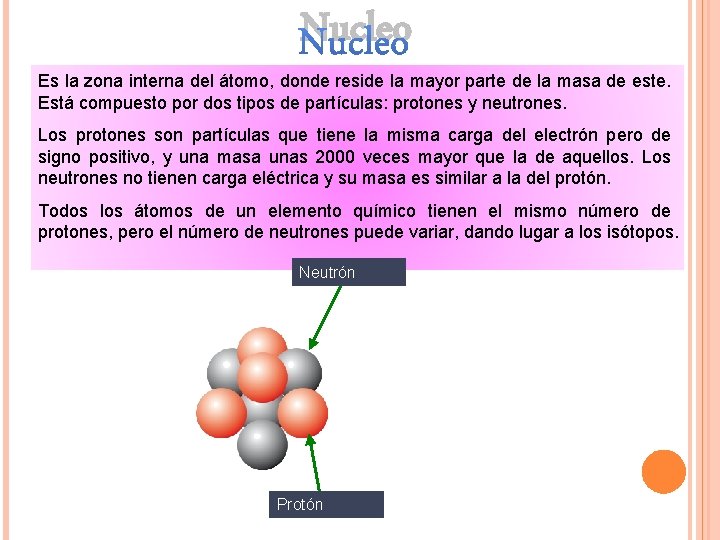
Nucleo Es la zona interna del átomo, donde reside la mayor parte de la masa de este. Está compuesto por dos tipos de partículas: protones y neutrones. Los protones son partículas que tiene la misma carga del electrón pero de signo positivo, y una masa unas 2000 veces mayor que la de aquellos. Los neutrones no tienen carga eléctrica y su masa es similar a la del protón. Todos los átomos de un elemento químico tienen el mismo número de protones, pero el número de neutrones puede variar, dando lugar a los isótopos. Neutrón Protón

Bibliografía Anónimo. 2013. Estructura del átomo. 2013. http: //www. quimicaweb. net/grupo_trabajo_fyq 3/tema 4/in dex 4. htm

1. 7. Introducción a tipos de enlace
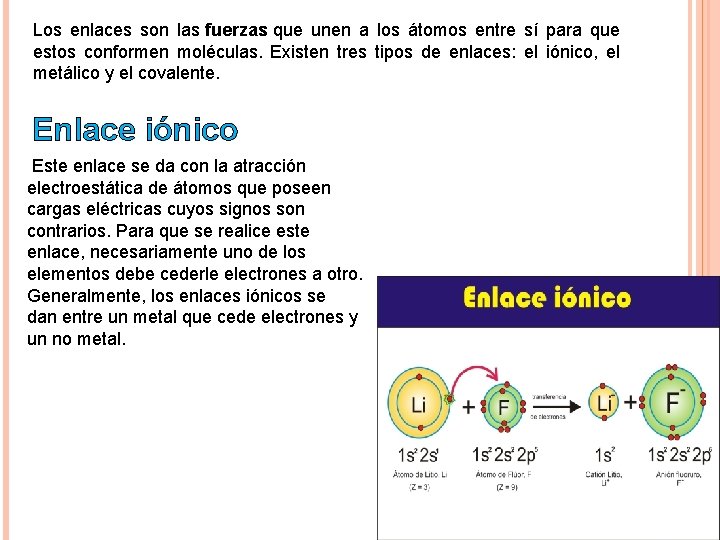
Los enlaces son las fuerzas que unen a los átomos entre sí para que estos conformen moléculas. Existen tres tipos de enlaces: el iónico, el metálico y el covalente. Enlace iónico Este enlace se da con la atracción electroestática de átomos que poseen cargas eléctricas cuyos signos son contrarios. Para que se realice este enlace, necesariamente uno de los elementos debe cederle electrones a otro. Generalmente, los enlaces iónicos se dan entre un metal que cede electrones y un no metal.

Enlace covalente A diferencia de los enlaces iónicos, los covalentes se establece a partir del compartimiento, entre dos o varios átomos, de electrones y no de su transferencia. De esta manera, los átomos se unen por medio de los electrones ubicados en las últimas órbitas. Suele establecerse entre elementos gaseosos no metales.

Enlace metálico Es el que mantiene unidos a los átomos de los metales entre sí y sólo se da entre sustancias que se encuentren en estado sólido. Los átomos metálicos conforman estructuras muy compactas al agruparse muy próximos entre sí. Los electrones de valencia tienen la capacidad de moverse con libertad en el compuesto metálico a causa de la baja electronegatividad que tienen los metales. Esto hace que el compuesto posea conductividad térmica y eléctrica. Estos enlaces se caracterizan por encontrarse en estado sólido, poseer brillo metálico, son maleables y dúctiles y emiten electrones al recibir calor.

Bibliografía Anonimo. 2013. tipos de enlace. 2013. http: //www. tiposde. org/ciencias-naturales/480 -tipos-de-enlaces/

1. 8. Tabla Periódica

La tabla periódica de los elementos es la organización que, atendiendo a diversos criterios, distribuye los distintos elementos químicos conforme a ciertas características. Historia La historia de la tabla periódica está íntimamente relacionada con varias cosas, clave para el desarrollo de la química y la física: el descubrimiento de los elementos de la tabla periódica el estudio de las propiedades comunes y la clasificación de los elementos la noción de masa atómica (inicialmente denominada "peso atómico") y, posteriormente, ya en el siglo XX, de número atómico y las relaciones entre la masa atómica (y, más adelante, el número atómico) y las propiedades periódicas de los elementos.
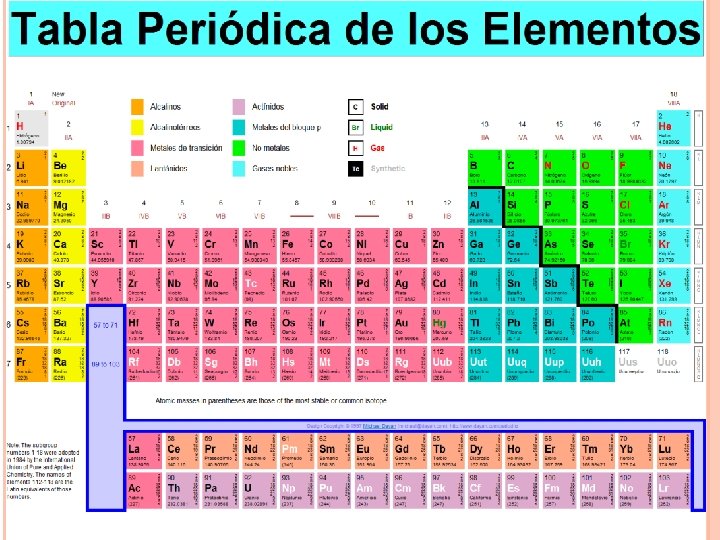

“Grupos” A las columnas verticales de la Tabla Periódica se les conoce como grupos. Todos los elementos que pertenecen a un grupo tienen la misma valencia, y por ello, tienen características o propiedades similares entre si. Por ejemplo los elementos en el grupo IA tienen valencia de 1 (un electrón en su último nivel de energía) y todos tienden a perder ese electrón al enlazarse como iones positivos de +1. Los elementos en el último grupo de la derecha son los Gases Nobles, los cuales tienen su último nivel de energía lleno (regla del octeto) y por ello son todos extremadamente no-reactivos

Periodos Las filas horizontales de la Tabla Periódica son llamadas Períodos. Contrario a como ocurre en el caso de los grupos de la tabla periódica, los elementos que componen una misma fila tienen propiedades diferentes pero masas similares: todos los elementos de un período tienen el mismo número de orbitales. Siguiendo esa norma, cada elemento se coloca de acuerdo a su configuración electrónica.
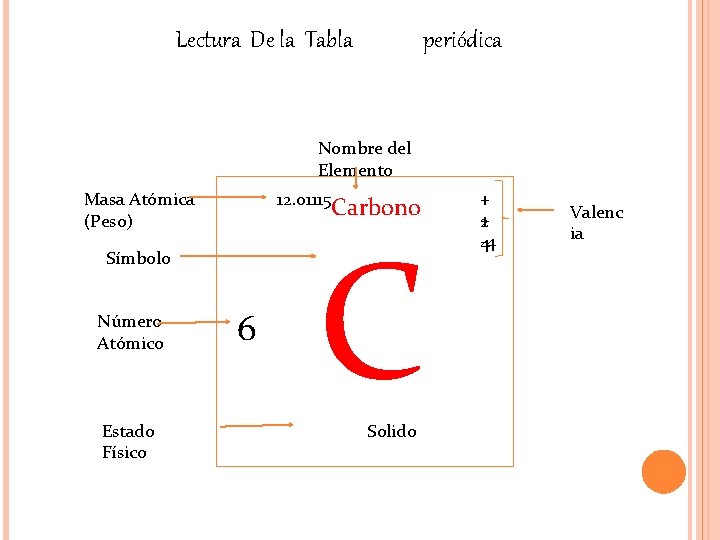
Lectura De la Tabla periódica Nombre del Elemento Masa Atómica (Peso) 12. 01115 Símbolo Número Atómico Estado Físico 6 Carbono C Solido + 2+ -4 4 Valenc ia

Bibliografía Anónimo. 2013. características de la tabla periódica. 2013. http: //www. educared. org/global/anavegar 3/premiados/ganadores/b/1046/c aracteristicastablaperiodica. htm Martínez P. 2013. tabla periódica. 2013. http: //platea. pntic. mec. es/pmarti 1/educacion/3_eso_materiales/b_iii/ conceptos/conceptos_bloque_3_3. htm Anónimo. 2013. Propiedades periódicas. 2013. http: //teleformacion. edu. aytolacoruna. es/EQUIMICA/document/pro pper/propper. htm


Los isótopos son variaciones de los elementos químicos que contienen diferentes número de neutrones. Debido a que los isótopos son reconocibles, proporcionan una manera eficaz de seguimiento de los procesos biológicos durante la experimentación. Existen muchos usos potenciales para los isótopos en la experimentación, pero varias aplicaciones son más prevalentes.

Isótopos diferenciados Cada elemento químico tiene un único número de protones, un hecho que dio lugar a la tabla periódica. De manera similar, un isótopo de un elemento dado tiene su propio número único de neutrones; la designación de un isótopo está determinada por la suma de protones y de neutrones en el núcleo (referidos como el número de masa).

Isótopos inusuales pueden ser utilizados como marcadores en las reacciones químicas. Esto puede ser útil, especialmente en el campo de la biología celular, donde los laboratorios de investigación como el Pandey Lab de la Johns Hopkins University están encontrando nuevas maneras de estudiar el cáncer y otras enfermedades que amenazan la vida. Por ejemplo, el etiquetado de isótopos estables con aminoácidos (SILAC) en el cultivo celular es un proceso por el cual poblaciones de células hermanas se diferencian in vitro utilizando diversas formas de aminoácidos.

Aplicación: datación radiactiva Los isótopos radiactivos se utilizan a menudo para medir la edad de materiales que contienen carbono. Un método popular de datación radiactiva se llama datación por carbono (la datación de materiales orgánicos). Debido a que la vida de un radioisótopo no está afectada por ninguna influencia fuera del núcleo, su tasa predecible de decadencia actúa como un reloj. El estudio de los radioisótopos en los alrededores de fósiles de animales, por ejemplo, ofrece una manera de estimar la edad de los fósiles.
Bibliogra fía 1. De La Torre C. 2013. Isotopos usados en biología. 2013. http: //www. ehowenespanol. com/isotopos-usados-biologiainfo_231016/

FIN
- Slides: 57