Unemorragia cerebrale su base genetica MASTER II LIVELLO

Un’emorragia cerebrale su base genetica MASTER II LIVELLO IN TERAPIA INTENSIVA PEDIATRICA(0 -18 ANNI) Direttore: Prof. ssa P. Papoff Candidato: dott. ssa M. C. Cardellini (UOC di Pediatria e Neonatologia-Ospedale San Giovanni Battista di Foligno)

Caso clinico Marco , lattante di due mesi e mezzo, arriva in Clinica Pediatrica a Perugia per comparsa nelle 24 ore precedenti di sonnolenza, iporeattività e scarsa alimentazione. Veniva riferita febbricola dalla sera precedente, negati traumi. Anamnesi perinatale: nato a termine da TC; Indice di Apgar 1’ 9, 5’ 10; peso 3030 gr EO all’ ingresso: intenso pallore muco-cutaneo, FB normotesa, pianto valido, poco reattivo. MV normotrasmesso su tutti campi, attività cardiaca ritmica, addome piano, trattabile, peristalsi valida. Faringe roseo, otoscopia nella norma. TC 36, 4°C. Sat. O 2 100% in aa, FC 170 bpm, FR 43 atti/min, PA 89/60 mm. Hg, Refill capillare 2”. 1°Sospetto clinico: sepsi. Si posiziona accesso venoso, si prelevano esami ematici con QE e si effettua Ceftriaxone ev

Esami ematici Esami ematici: GB 26. 780(L 31, 3%, M 8, 4%, N 60, 2%) GR 2. 140. 000, Hb 5, 6 mg/dl, Ht 16, 8%, PTL 428. 000, PT 20, 5 sec(v. n. 9, 8 -14, 3) INR 1, 83 (0, 8 -1, 20), PTT 1, 37 sec(0, 8 -1, 20) Fibrinogeno 413 mg/d. L (150 -400), D-Dimero 1255 ng/ml(0 -500) Azotemia 16 mg/dl, Creatinina 0, 32 mg/dl, GOT 37 UI/L, GPT 19 UI/L, elettroliti nella norma, PCR 3 mg/dl. Richiediamo alla mamma se ci sono stati traumi…. . A questo punto ci dice che in anamnesi familiare c’e’ un deficit del fattore II della coagulazione che presentano entrambi i fratellini di Marco Contattiamo immediatamente il Collega della Medicina Vascolare e somministriamo CPP(fattore II, IX e X) a 30 U/kg e richiediamo GRC Ecografia cerebrale: …. . deviazione della linea mediana verso sinistra. Nello spazio extracerebrale a destra si apprezza immagine iperecogena disomogenea in sede frontale e temporale, e immagine transonica in sede occipitale. Si richiede consulenza NCH e approfondimento diagnostico con TC encefalo. Ecoaddome: negativo
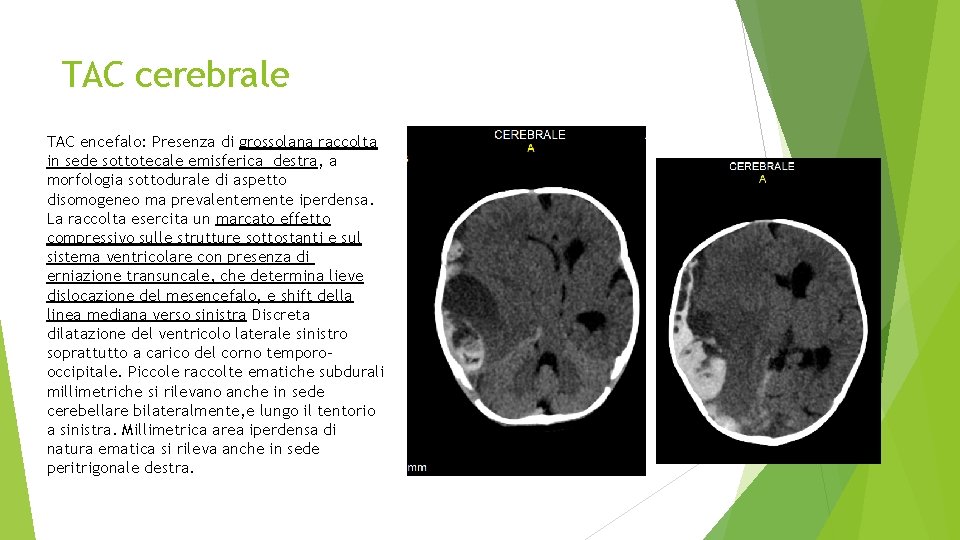
TAC cerebrale TAC encefalo: Presenza di grossolana raccolta in sede sottotecale emisferica destra, a morfologia sottodurale di aspetto disomogeneo ma prevalentemente iperdensa. La raccolta esercita un marcato effetto compressivo sulle strutture sottostanti e sul sistema ventricolare con presenza di erniazione transuncale, che determina lieve dislocazione del mesencefalo, e shift della linea mediana verso sinistra Discreta dilatazione del ventricolo laterale sinistro soprattutto a carico del corno temporooccipitale. Piccole raccolte ematiche subdurali millimetriche si rilevano anche in sede cerebellare bilateralmente, e lungo il tentorio a sinistra. Millimetrica area iperdensa di natura ematica si rileva anche in sede peritrigonale destra.
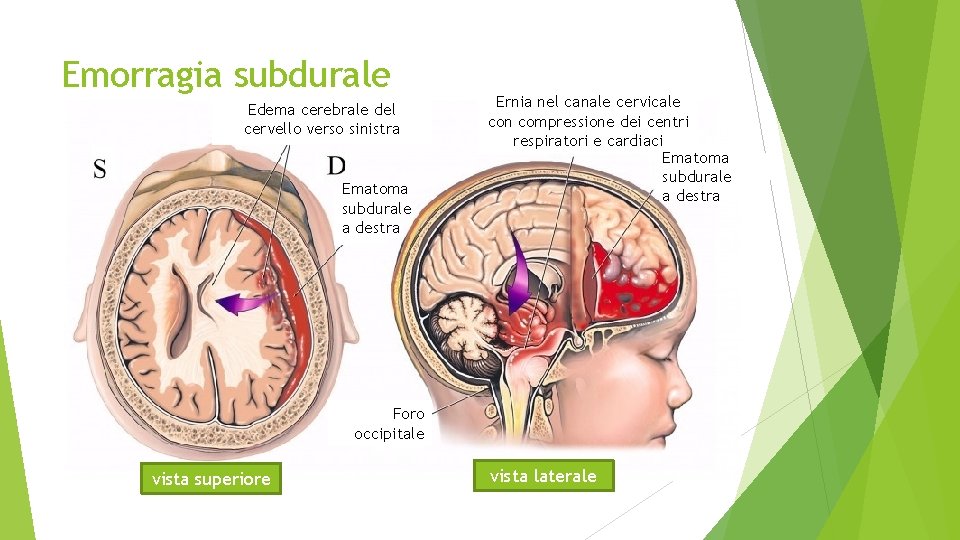
Emorragia subdurale Edema cerebrale del cervello verso sinistra Ematoma subdurale a destra Ernia nel canale cervicale con compressione dei centri respiratori e cardiaci Ematoma subdurale a destra Foro occipitale vista superiore vista laterale

Cause di emorragia subdurale CAUSE DI ESD COMMENTI Trauma non accidentale: Shaken Baby Syndrome Rappresenta la causa più frequente di ESD. Di solito associata ad altre lesioni e ad emorragie retiniche. Sia la ESD che le emorragie retiniche possono essere isolate. Trauma accidentale Minime cadute domestiche raramente causano ESD è descritta come conseguenza di cadute maggiori e in traumi da colpo di frusta. Le emorragie retiniche sono associate solo a danni severi. Perinatali ESD dopo parto traumatico può essere associato ad emorragie retiniche, generalmente si riassorbe entro 4 settimane senza particolari esiti. Malformazioni vascolari (aneurismi, malformazioni artero-venose) Sanguinamenti spontanei da malformazioni vascolari. Rari in età pediatrica. Infezioni cerebrali Meninfoencefalite Traumi minori possono causare ESD quadro è presente una cisti aracnoidea. Rare le emorragie retiniche associate. Disordini coagulativi ed ematologici -Leucemia - Anemia falciforme -CID - Emofilia -Malattia di Von Wilebrand -Porpora trombocitopenica idiopatica -Malattia di Menkes Possono essere associate ad emorragie retiniche. Per la diagnosi sono necessari puntura lombare ed esami di laboratorio. Malattie metaboliche -Glutarico-aciduria -Galattosemia -Malattia di Menkes Si associano ad ampliamento degli spazi subdurali che può esitare in ESD per stretching e rottura dei vasi subdurali. Descritta l’associazione con emorragie retiniche nelle prime due condizioni. Generalmente si associano ad altri segni e sintomi caratteristici. Disordini biochimici (ipernatremia) ESD descritta in associazione a disidratazione ipernatriemica. L’ipernatriemia potrebbe anche essere la complicanza di un trauma cranico. Complicazioni neurochirurgiche ESD è comunemente riportata come complicanza post-operatoria neurochirurgica. Area Ped. 2016; 17 (3): 122 -125

All’ ingresso in TIN Inviato in sala operatoria per Intervento neurochirurgico di evacuazione della raccolta ematica e quindi trasferito presso TIN All’ ingresso : pallido, reattivo agli stimoli dolorosi, tono e postura normali per l’ età (sedato in SO con oppiodi a basse dosi) Pupille isocoriche, reagenti alla luce, crisi cloniche all’ arto superiore sinistro e alla lingua. PV: sat. O 2 99% in ventilazione meccanica convenzionale, FC 160 bpm, PA 110/70. Posizionato accesso intraosseo tibiale dx sostituito con CVC. Terapia antibiotica con Ceftriaxone e Vancomicina Sedazione/analgesia con Sufentanil e Midazolam Carico di Fenobarbital Proseguita Trasfusione di GRC Infusione di Na. Cl 0, 9% con target >145 m. Eq/L Fluidi
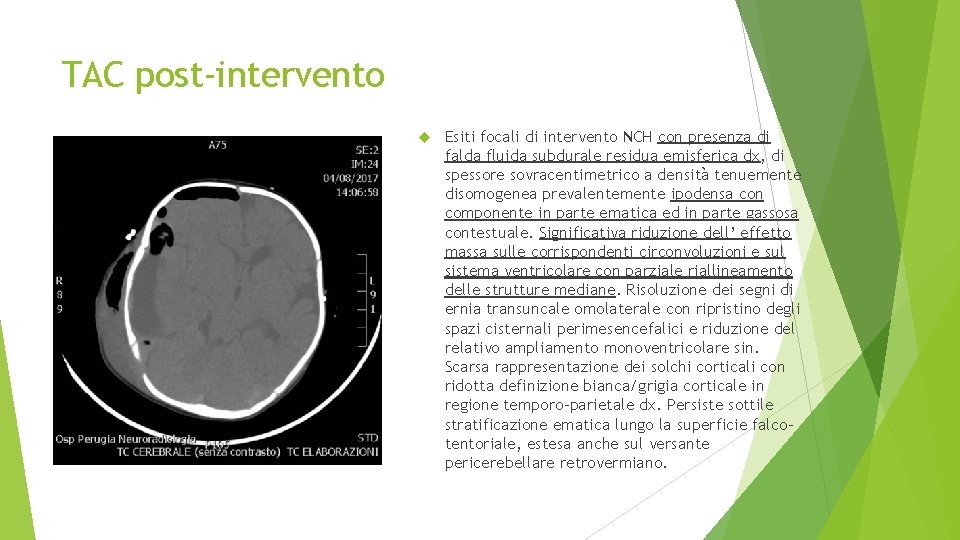
TAC post-intervento Esiti focali di intervento NCH con presenza di falda fluida subdurale residua emisferica dx, di spessore sovracentimetrico a densità tenuemente disomogenea prevalentemente ipodensa con componente in parte ematica ed in parte gassosa contestuale. Significativa riduzione dell’ effetto massa sulle corrispondenti circonvoluzioni e sul sistema ventricolare con parziale riallineamento delle strutture mediane. Risoluzione dei segni di ernia transuncale omolaterale con ripristino degli spazi cisternali perimesencefalici e riduzione del relativo ampliamento monoventricolare sin. Scarsa rappresentazione dei solchi corticali con ridotta definizione bianca/grigia corticale in regione temporo-parietale dx. Persiste sottile stratificazione ematica lungo la superficie falcotentoriale, estesa anche sul versante pericerebellare retrovermiano.

Decorso clinico Ecocuore: nella norma Babygramma: nella norma FOO: papille ottiche a margini netti, retina normovascolarizzata, non si apprezzano lesioni emorragiche. Dato il buon drive respiratorio il piccolo è stato estubato dopo 2 giorni con successiva necessità di supporto con nasocannule per poche ore. Per la comparsa di crisi cloniche all’ arto superiore di sinistra e buccali (confermate all’ EEG) è stata intrapresa tp con Fenobarbitale associato dopo 24 ore a Midazolam e Fenitoina, sospesi questi ultimi a seguito di monitoraggio e normalizzazione dell’EEG con assenza di crisi elettriche. Dal 05 all’ 08/08: NPT, associata dal 07/08 a nutrizione enterale dapprima per gavage e successivamente al biberon Somministrati colloidi e Furosemide Somministrazione di vit k ev e PCC

Decorso clinico La RMN-encefalo 11/08 : riduzione dell’effetto massa con riallineamento parziale delle strutture mediane. 25/08: presenza di nuovo piccolo ematoma subdurale prevalentemente frontale a sx per cui veniva incrementata la dose di PCC ed effettuato nuovo controllo neuroradiologico a distanza di una settimana, che evidenziava un quadro encefalografico in lieve miglioramento. Data la persistenza all’esame obiettivo neurologico di ipertono agli arti superiori con scarso controllo della motilità dell’arto superiore dx è stato intrapreso un percorso di neuroriabilitazione. In considerazione dello studio farmacocinetico veniva dimesso dopo circa 1 mese con schema terapeutico di somministrazione del Complesso Protrombinico ogni 4 giorni tramite CVC tunnellizzato.
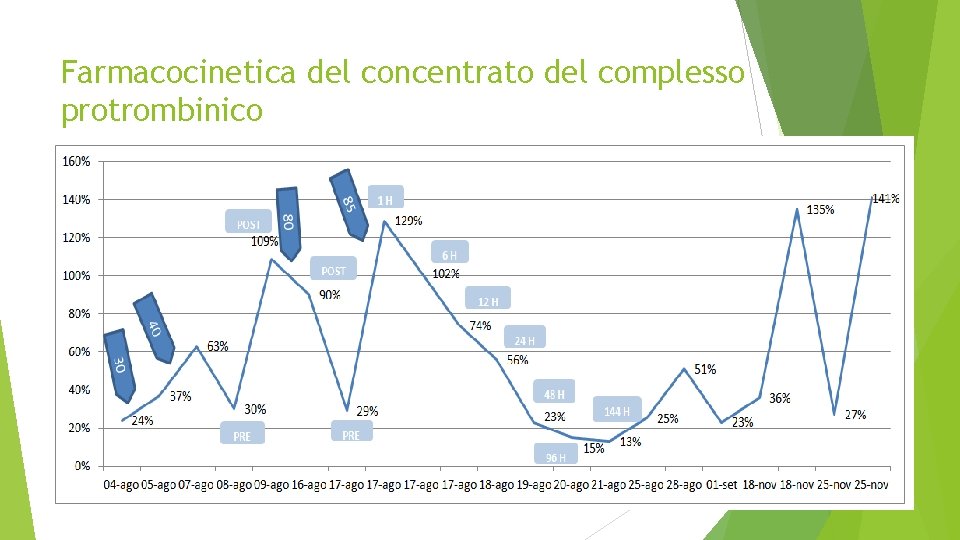
Farmacocinetica del concentrato del complesso protrombinico

Anamnesi familiare Due fratelli maggiori di 6 e 2 anni Il più grande ha presentato una macroematuria all’ età di 4 anni e ½. Diagnosi di forma lieve paucisintomatica di deficit del Fattore II (8 -9%) della coagulazione effettuata in seguito ad intervento chirurgico per ernia inguinale con successiva formazione di ematoma del testicolo. Il secondo ha presentato un’ emorragia cerebrale parietale bilaterale posttraumatica. Affetto da deficit lieve/moderato di Fattore II della coagulazione con attività residua del 5%. Tale alterazione coagulativa è stata riscontrata nel corso di studio familiare attività residua: Madre FII 48%, Padre FII 60%. Genitori non consanguinei. La famiglia è presa in carico e seguita dal Centro di Riferimento Regionale per l’ Emofilia ed i difetti della coagulazione

Studio genetico familiare Madre: eterozigote per la mutazione c. 1016 G>A(Arg 339 Glu), antigene 70%, attività 48% Padre. Eterozigote per la mutazione c. 119 G>A(Arg 40 Glu), antigene 88%, attività 60% Figlio 1: eterozigote composto per le mutazioni c. 119 G>A e c. 1016 G<A, antigene 26%, attività 8% Figlio 2: eterozigote composto per le mutazioni c. 119 G>A e c. 1016 G<A Antigene 16%, attività 5%

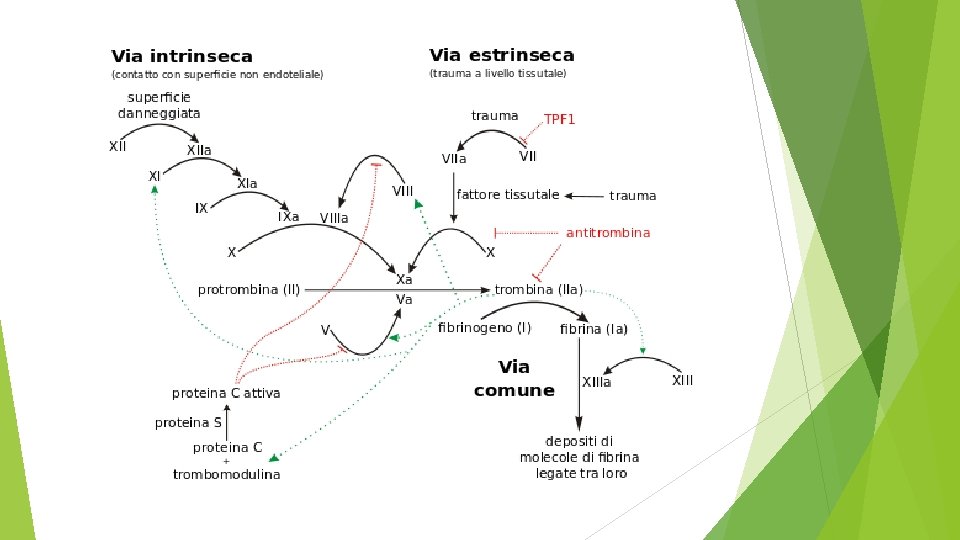
Alterazioni nella cascata coagulativa
Emostasi ALTERAZIONE DI TALE EQUILIBRIO EMORRAGIA TROMBOSI L’emostasi è un meccanismo molto complesso che richiede l’ integrazione ed il corretto funzionamento di una serie di fattori rappresentati da glicoproteine plasmatiche, piastrine circolanti e cellule dell’ endotelio vascolare. Questo fenomeno e’ finalizzato all’ arresto dell’ emorragia e deriva da una delicato equilibrio tra processi procoagulativi e processi anticoagulanti.
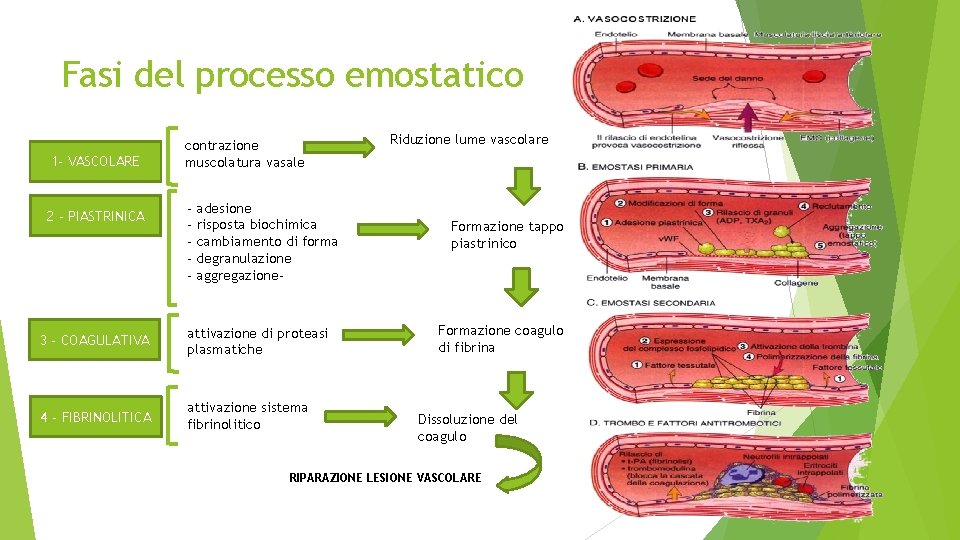
Fasi del processo emostatico 1 - VASCOLARE 2 - PIASTRINICA contrazione muscolatura vasale - adesione - risposta biochimica - cambiamento di forma - degranulazione - aggregazione- 3 - COAGULATIVA attivazione di proteasi plasmatiche 4 - FIBRINOLITICA attivazione sistema fibrinolitico Riduzione lume vascolare Formazione tappo piastrinico Formazione coagulo di fibrina Dissoluzione del coagulo RIPARAZIONE LESIONE VASCOLARE
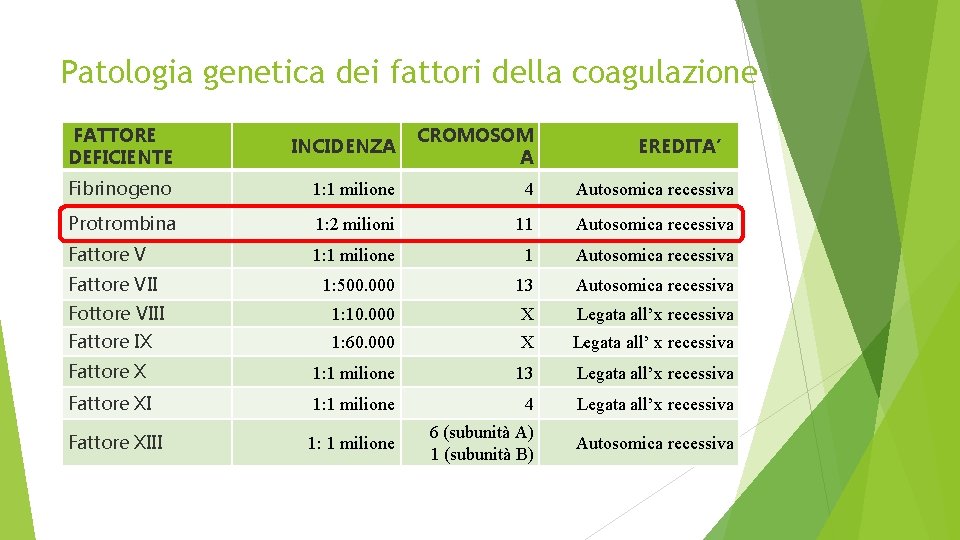
Patologia genetica dei fattori della coagulazione FATTORE DEFICIENTE INCIDENZA CROMOSOM A EREDITA’ Fibrinogeno 1: 1 milione 4 Autosomica recessiva Protrombina 1: 2 milioni 11 Autosomica recessiva Fattore V 1: 1 milione 1 Autosomica recessiva Fattore VII 1: 500. 000 13 Autosomica recessiva Fottore VIII 1: 10. 000 X Legata all’x recessiva Fattore IX 1: 60. 000 X Legata all’ x recessiva Fattore X 1: 1 milione 13 Legata all’x recessiva Fattore XI 1: 1 milione 4 Legata all’x recessiva Fattore XIII 1: 1 milione 6 (subunità A) 1 (subunità B) Autosomica recessiva

Fattore II della coagulazione La protrombina(fattore II) è uno zimogeno vit K dipendente sintetizzata primariamente nel fegato e composta da 579 amminoacidi. La molecola del Fattore II contiene un dominio acido ϒ carbossiglutammico, due domini di kringle( o a dito di zinco) e un dominio catalitico serin proteasi E’ codificata dal gene del fattore II localizzato 11 p 11 -q 12, ed include: 14 esoni e 13 introni. La trombina contiene 308 amminoacidi ed è generata dalla protrombina attraverso l’ attivazione del Fxa. Il principale ruolo della protrombina è convertire il fibrinogeno in fibrina sotto la catalisi del complesso protrombinico (Fxa, Fva, Ca++-PL) Inoltre partecipa al processo anticoagulante attivando il sistema della proteina C Gioca un ruolo nell’ infiammazione, nella proliferazione cellulare e nella riparazione tissutale. Phenotypic and genetic analysis of dysprothrombinemia due to a novel homozygous mutation Hematology 2017

Fattore II della coagulazione Sono state identificate circa 50 mutazioni del gene del Fattore II Le manifestazioni tipiche del deficit del fattore II sono: sanguinamento ombelicale, emartri e sanguinamenti del tratto GI L’ emorragia cerebrale severa è rara come manifestazione clinica del deficit del fattore II e viene riportata solo nell’ 8 -12% dei pz. L’ attività del FII<1 IU/dl può essere un fattore di rischio per ICH L’ emivita della protrombina è nota essere di circa 60 h La concentrazione nel plasma della protrombina ha valori normali dal 60140% Prophylactic Administration of Prothrombin Comlex Concentrates for Congenital Prothrombin Deficiency with a Novel Frameshift Mutation – Pediatr Bood Cancer 2013

Deficit del Fattore II La carenza congenita del Fattore II è un raro, ereditario disordine della caoagulazione. Nel 1947 Quick per primo descrisse il deficit del fattore II Nel 1969 Shapiro e colleghi furoni i primi a riportare anomalie strutturali della protrombina Il deficit ereditario del fattore II è un disordine autosomico recessivo che si puo manifestare come IPOPROTROMBINEMIA: riduzione complessiva della sintesi di protrombina o come DISPROTROMBINEMIA: la sintesi di una protrombina disfunzionale. Negli individui omozigoti le emorragie possono essere di vario tipo, mentre gli individui eterozigoti spesso rimangono clinicamente asintomatici Congenital Factor II deficiency: Maroccan cases Internationatl Journal of Laboratory Hematology 2012

Severità del deficit Deficit severo: Fattore II<1% Deficit moderato: Fattore II con un livello tra 1% e il 5% Deficit minore: Fattore II >5% Defict del Fattore II è un rarissimo disordine ereditario con una prevalenza di 1: 2 milioni nella popolazione generale Come molti disordini autosomici recessivi il deficit del Fattore II è più elevato nei gruppi etnici e nelle regioni dove è più frequente la consangiuneità. Congenital Factor II deficiency: Moroccan cases Int. Lab. Hem 2013

E la vit K? La Vit. K è un fattore antiemorragico liposolubile disponibile in tre forme differenti: K 1: origine vegetale K 2: sintetizzata da batteri nell’ intestino umano K 3: di origine sintetica La vit K è un cofattore enzimatico essenziale per l’ attività biologica dei fattori della coagulazione vit-K dipendenti Il deficit di vit. K nel periodo neonatale e nel II-III mese di vita è associato a rischio emorragico responsabile del quadro definito “emorragia da deficit di vit K”(VKDB) che può manifestarsi come forma precoce, classica o tardiva

Vitamina K Alla nascita i livelli di vit K nel plasma del neonato sono bassi, tale vit ha un passaggio molto scarso attraverso la placenta; inoltre l’ intestino del neonato è sterile e la sintesi della vit K endogena inizia con la comparsa della flora batterica intestinale L’ assorbimento della vit K è strettamente dipendente dalla disponibilità intestinale di bile che puo’ essere carente in presenza di una colestasi anche misconosciuta. Il maggior fattore di rischio per VKDB è l’ allattamento esclusivo al seno. Il latte materno presenta un bassissimo contenuto di vit. K(1 -4 µg/l contro 800 -900 µg/l del cavolo) per un apporto giornaliero raccomandato di circa 1 µg/kg. Nei neonati e nei lattanti per mantenere un’ adeguata funzione del sistema emostatico è necessario un apporto di vit K di 10 -15µg/die.

VKDB si classifica per eziologia in IDIOPATICA che prevede come unico fattore di rischio l’ allattamento esclusivo al seno e SECONDARIA associata all’ uso di farmaci materni, malattia epatobiliare o malassorbimento ereditario, deficit di fattori di coagulazione vit K dipendenti autosomico-recessivi Per il timing di esordio si identificano tre forme di VKDB La FORMA PRECOCE: si manifesta entro le prime 24 ore di vita, quasi esclusivamente nei neonati figli di madre che assumono farmaci che inibiscono la vit. K quali anticonvulsivanti (carbamazepina, fenitoina, barbiturici), antitubercolinici (isoniazide e rifarmpicina), antiobiotici (cefalosporine) e antagonisti della vit. K (coumadin e warfarin). Si manifesta con cefaloematoma ed emorragie intracraniche ed addominali

VKDB La FORMA CLASSICA si manifesta entro 24 ore-7 gg di vita ed è associata a ritardata o inadeguata alimentazione. Piu’ lieve contempla ematomi, maggior sangiunamento dai punti di prelievo, o a livello ombelicale o GI. La FORMA TARDIVA è stata descritta solo negli allattati al seno esclusivo. Si manifesta tra seconda-dodicesima settimana di vita. E’ in genere gravissima con mortalità del 20% ed emorragia intracranica nel 50% dei casi. L’ incidenza negli allattati al seno non supplementati è del 4, 4 -7, 2/100. 000 nati vivi( 1 caso ogni 15: 000 -20: 000 nati). I neonati con colestasi ne sono particolarmente a rischio

La profilassi con vit K Dal 1961 la profilassi neonatale con vit. K è riconosciuta come un adeguato approccio per la prevenzione del VKDB precoce e classica alla dose di 0, 5 -1 mg Im alla nascita Dal 2003 l’ American Accademy of Pediatrics raccomanda la profilassi IM con 0, 5 -1 mg Im di vit K in una sola dose e lo riconferma nel 2009. Una consensus conference della SIP nel 2004 indica il trattamento profilattico con vit k alla dose di 0, 5 mg alla nascita e 25 ug/die per os dal 15°giorno alla 14° settimana di vita SIN: 0, 5 -1 mg im se PN>2000 gr; in caso di somministrazione orale la dose raccomandata è 2 mg. Dopo la 2° sett di vita ed in caso di allattamento esclusivo al seno 25 -50ϒ/die dal 15° giorno fino al termine della 14° sett. ; se è stata effettuata la somministrazione di vit K per os l’ inizio della profilassi va anticipata all’ 8° giorno di vita. ESPGHAN 2016: 1 mg im alla nascita (Accademia Americana di Pediatria) 2 mg alla nascita per os seguiti da 1 mg a settimana x 3 mesi (protocollo danese) 2 mg alla nascita per os, seguiti da 2 mg a 4 -6 gg e a 4 -6 sett di vita(protocollo tedesco)

La terapia con PCC Per quanto riguarda l’efficacia del complesso protrombinico concentrato(PCC) uno studio ha rilevato che la somministrazione di PCC non è piu’ efficace della somministrazione di plasma fresco congelato. Al momento non ci sono evidenze sufficienti per raccomandare uso PCC nei neonati e nei lattanti. PCC è un complesso protrombinico concentrato che contiene fattori vit K dipendenti: II, VII, IX, e X e dei fattori anticoagulanti vit. K come prot C e S. La primaria indicazione al trattamento con PCC è il trattamento e la profilassi perioperatoria dei sanguinamenti nei deficit acquisiti dei fattori della coagulazione protrombinici E’ in incremento l’uso off-label per il trattamento delle emorragie severe nei neonati. Sebbene l’ efficacia nei neonati e nei lattanti sia ancora incerta. Effectiveness of prothrombin complex concentrate(PCC) in neonates and infants with bleeding or risk of bleeding: a sistematic review and meta-analysis Eur J Pediatr 2017

Conclusioni Probabilmente le mutazioni riscontrate non spiegano da sole la sintomatologia presentata Le manifestazioni emorragiche si sono avute in tutti e tre i fratelli precocemente, quindi sicuramente sono mutazioni di rilievo , ma con diversa espressività fenotipica, il che ci fa pensare che altri fattori e/o altri geni, influiscano o abbiano influito nel determinare l’ emorragia cerebrale. Lo studio genetico familiare è ancora in corso(sequenziamento del gene) Probabilmente il deficit di vit K puo’ aver giocato un ruolo non secondario. . . Marco aveva ricevuto alla nascita 1 mg Im di vit K e proseguito la somministrazione per via orale Forse si poteva mettere in atto un diverso schema terapeutico di profilassi ? Lo studio del gene speriamo ci chiarirà meglio le cose…. . Dato il basso numero di pz con deficit del FII è essenziale il continuo sforzo di collaborazione con i registri internazionali per aumentare le conoscenze di questo e di altri difetti coagulativi
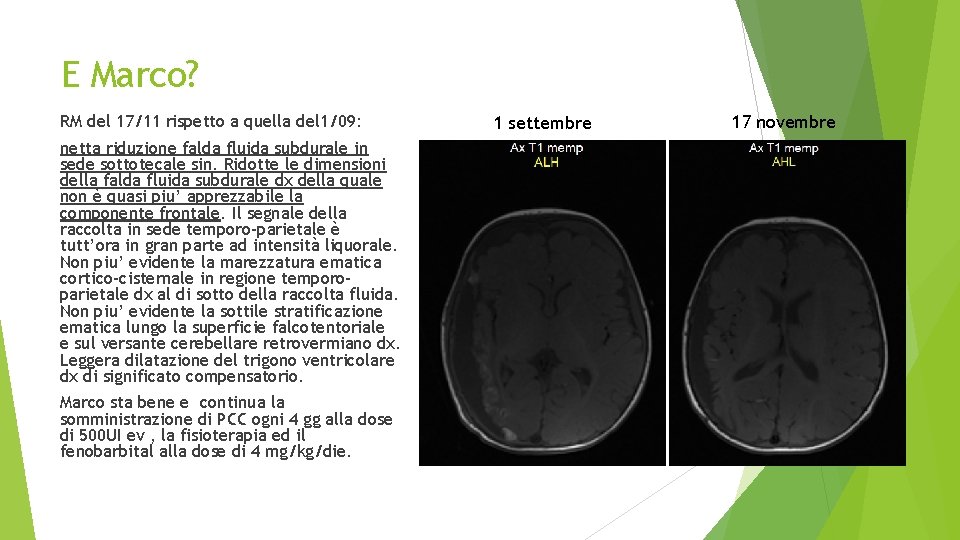
E Marco? RM del 17/11 rispetto a quella del 1/09: netta riduzione falda fluida subdurale in sede sottotecale sin. Ridotte le dimensioni della falda fluida subdurale dx della quale non è quasi piu’ apprezzabile la componente frontale. Il segnale della raccolta in sede temporo-parietale è tutt’ora in gran parte ad intensità liquorale. Non piu’ evidente la marezzatura ematica cortico-cisternale in regione temporoparietale dx al di sotto della raccolta fluida. Non piu’ evidente la sottile stratificazione ematica lungo la superficie falcotentoriale e sul versante cerebellare retrovermiano dx. Leggera dilatazione del trigono ventricolare dx di significato compensatorio. Marco sta bene e continua la somministrazione di PCC ogni 4 gg alla dose di 500 UI ev , la fisioterapia ed il fenobarbital alla dose di 4 mg/kg/die. 1 settembre 17 novembre
Grazie per l’ attenzione!
- Slides: 31