Un dossier CRM pour une demande de remboursement

Un dossier CRM pour une demande de remboursement Point de vue

Pierre Chevalier ex expert interne INAMI pour la Commission de Remboursement des Médicaments

Pierre Chevalier EX • Médecin généraliste 35 ans de pratique • Président du Groupe de Recherche et d’Actions pour la Santé – GRAS ASBL • Rédacteur en chef de la revue Minerva FR revue EBM belge • Chargé de cours à l’Université Catholique de Louvain enseignement Evidence-Based Medicine en Masters • Expert INAMI pour la Commission de remboursement des Médicaments Liens d’intérêts

Pierre Chevalier actuellement • Rédacteur pour la revue Minerva • Rédacteur pour le Formulaire de Soins aux Personnes Agées - Farmaka • Consultant pour les Consensus de l’INAMI • Relecteur revue Prescrire, Folia Pharmacotherapeutica Liens d’intérêts

Un dossier CRM Suivant la classe du médicament • Classe 1 : spécialités ayant une plus-value thérapeutique démontrée par rapport aux alternatives thérapeutiques existantes = revendication de la firme • Classe 2 : spécialités n’ayant pas une plusvalue thérapeutique démontrée par rapport aux alternatives thérapeutiques existantes • Classe 3 : génériques et copies

Un dossier CRM Suivant la classe du médicament • Classe 1 : spécialités ayant une plus-value thérapeutique démontrée par rapport aux alternatives thérapeutiques existantes • Classe 2 : spécialités n’ayant pas une plusvalue thérapeutique démontrée par rapport aux alternatives thérapeutiques existantes • Classe 3 : génériques et copies


Dossier classe 1 - AR 1° identification de la spécialité 2° caractéristiques de la spécialité au niveau du Service public fédéral Economie, PME, Classes moyennes et Energie, ainsi que, le cas échéant, les prix pratiqués dans les autres Etats Membres de l’Union européenne 3° caractéristiques de la spécialité en ce qui concerne l’autorisation et la mention de la procédure d’enregistrement appliquée, référant à la législation belge et/ou européenne en vigueur en la matière

Dossier classe 1 - AR 4° proposition relative au remboursement 5° justification de la proposition relative au remboursement, accompagnée d’études cliniques, épidémiologiques et économicosanitaires publiées et non publiées, ainsi que de motivations scientifiques

Structure du dossier CRM • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

Présentation de la pathologie Sources pouvant être utilisées : toutes… 1. Dossier réalisé par la firme : - présentation soignée, beaux graphiques, belles illustrations - souvent, tableau clinique noirci pour le pronostic, les complications - pour aboutir à une démonstration de la nécessité d’un alternative thérapeutique

Présentation de la pathologie Sources pouvant être utilisées: toutes… 2. Propres sources - littérature EBM - Guides de Pratique Clinique validés (guidelines) - Synthèses publiées

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

Données épidémiologiques Confrontation des sources - OMS - Données de la firme - Généralement données internationales - Rareté de données belges - Exception : médecine générale Intego (KUL) - Données Pharmanet

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux • Dossier de la firme : essai de démonstration de la nécessité du nouveau médicament si nécessaire, renforcé plus tard lors d’un hearing en séance de la CRM demandé par la firme qui sera accompagnée par d’éminents experts



modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux Autres sources • Consensus INAMI • GPC belge SSMG – Domus Medica – Société scientifique • GPC internationaux • Problèmes majeurs : place de ces nouveaux médicaments ; validité des GPC

Validité des GPC ? Exemple des Nouveaux Anticoagulants Oraux
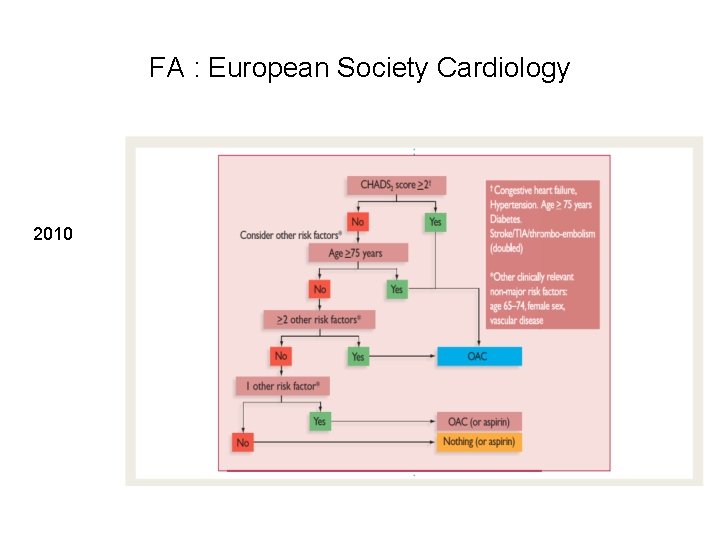
FA : European Society Cardiology 2010

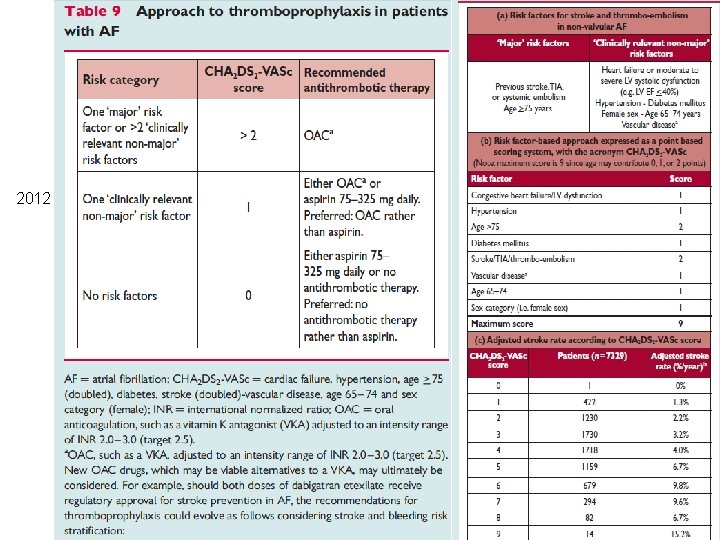
2012
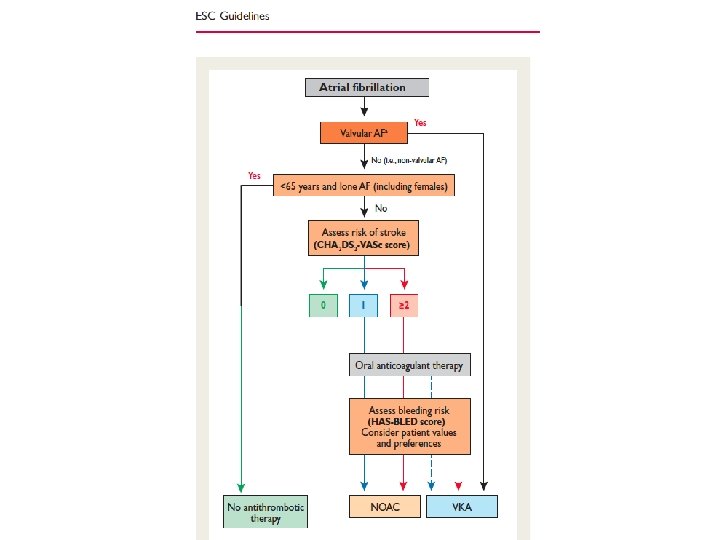


NHG-Standaard Atriumfibrilleren (2013) Antitrombotische behandeling • Adviseer orale anticoagulantia aan alle vrouwen > 65 jaar en alle mannen > 75 jaar. • Bespreek met mannen van 65 tot 75 jaar zonder cardiovasculaire comorbiditeit (zeldzaam) dat het voordeel van antitrombotische medicatie niet opweegt tegen het nadeel • Adviseer acetylsalicylzuur (80 mg per dag) bij een contra-indicatie voor orale anticoagulantia. • * Geef uitleg over bijwerkingen van orale anticoagulantia en schrijf zo nodig maagbescherming voor. Orale anticoagulantia • Schrijf bij voorkeur een cumarinederivaat voor (fenprocoumon of acenocoumarol; INR 2 -3). Overweeg zelfcontrole van INR bij patiënten die controle door trombosedienst belastend vinden.

Des preuves aux décisions Grading of Recommendations Assessment, Development and Evaluation

Et. D

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

propriétés pharmaco-thérapeutiques Mécanisme d’action • Dossier de la firme • RCP et dossier EPAR (European public assessment reports – EMA pour chaque médicament obtenant une autorisation de mise sur le marché) Place dans le groupe pharmaco-thérapeutique • Dossier de la firme • CBIP • FDA Posologie proposée • Dossier de la firme • RCP et dossier EPAR Mode d’administration • Dossier de la firme • RCP et dossier EPAR

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

évaluation de la valeur thérapeutique et de l’intérêt de la spécialité • • • efficacité effets indésirables applicabilité confort d’utilisation degré de preuve

Evaluation de l’efficacité • Phase I : volontaire (sain) : toxicité, pharmacocinétique • Phase II : population limitée de patients : posologie (efficacité, tolérance), interactions • Phase III : nombre important de patients « représentatifs » pour la pathologie à traiter, versus placebo ou traitement de référence • Phase IV : après commercialisation : utilité, tolérance à grande échelle

Evaluation de l’efficacité • Phase I : volontaire (sain) : toxicité, pharmacocinétique • Phase II : population limitée de patients : posologie (efficacité, tolérance), interactions • Phase III : nombre important de patients « représentatifs » pour la pathologie à traiter, versus placebo ou traitement de référence • Phase IV : après commercialisation : utilité, tolérance à grande échelle

Evaluation de l’efficacité • Sources à disposition programme de développement clinique du médicament (firme)
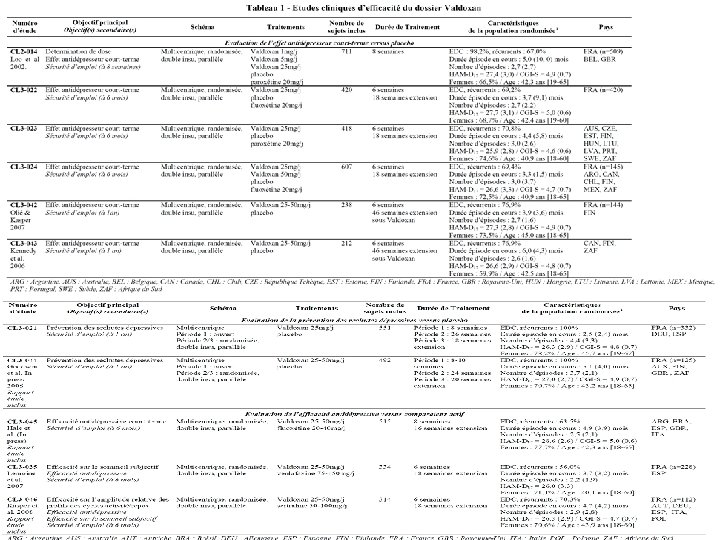
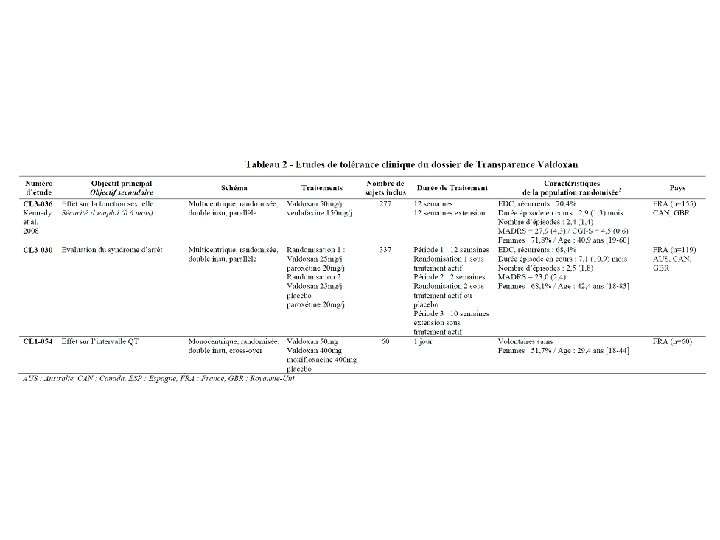
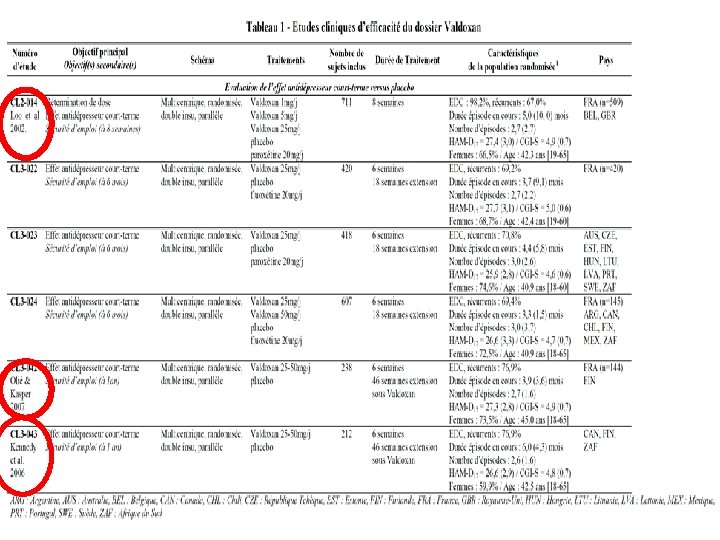

Avantage des experts CRM • Disposition, pour les études non publiées, des CSR complets (> 1. 000 pages souvent synopsis)

Analyse des études • Caractéristiques de l’étude • Résultats • Commentaires de la CRM

Caractéristiques de l’étude • Type d’étude : RCT en double aveugle, de non infériorité • Population incluse • Critères d’exclusion • Traitement évalué (dose, titration) • Critères de jugement • Durée d’étude • Qualité méthodologique: marge de non infériorité

Résultats de l’étude • • En chiffres : valeurs relatives ET absolues Pas les graphiques Avec IC à 95 % Analyse en sous-groupes - validité du p - suivant stratification initiale ?

Commentaires de la CRM • Critères de jugement : fort (événement clinique), intermédiaire • Pertinence clinique versus signification statistique • Pertinence clinique : différence minimale cliniquement pertinente • Validité méthodologique

Evaluation de l’efficacité Intérêt de consulter d’autres sources : exemple FDA • Sur base des analyses en sous-groupes fournies par les auteurs de cette étude, la FDA a fait mentionner dans la notice de ce médicament (NACO) qu’en cas de FA, il est moins efficace (en termes de prévention de l’AVC) que les AVK chez les patients avec une fonction rénale « normale » (clairance de créatinine > 95 ml/min). FDA approves anti-clotting drug Savaysa. Page last updated: 01/08/2015.

Evaluation de l’efficacité Intérêt de consulter d’autres sources : exemple IQWIG (Allemagne) • In its dossier, the company presented no data for the assessment of the added benefit of evolocumab in patients with Ho. FH in whom drug and dietary lipid-lowering options have been exhausted. Hence there was no hint of an added benefit of evolocumab in comparison with the ACT; an added benefit is therefore not proven.

Evaluation de l’efficacité Intérêt de consulter d’autres sources : exemple NICE (GB) - 2009 : memantine continue to be recommended only for people with moderate Alzheimer’s disease - 2010 : memantine is not recommended as a treatment option for patients with moderately severe to severe Alzheimer’s disease except as part of well-designed clinical studies

Evaluation des effets indésirables • Dans les études pour l’enregistrement + études de phase III • limites : - statistiques : population incluse - pertinence clinique : population (hyper) sélectionnée

Applicabilité Données sur l’utilisation dans des populations plus particulières • personnes âgées • insuffisance rénale • insuffisance hépatique • différences versus autres traitements

Confort d’utilisation • Mode de préparation/administration/conservation • Conditionnement Commentaires : • analyse théorique • pas accès à un échantillon domaine réservé à l’AFMPS Source : revue Prescrire


Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

preuves issues de la pratique quotidienne

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmacoéconomiques - incidence budgétaire • Références • Résumé

analyse méthodologique des données pharmaco-économiques • Modèle pharmacoéconomique • Canevas déterminé par le KCE

analyse méthodologique des données pharmaco-économiques • Données de base souvent discutables (hypothèses mal vérifiées, non confirmées, difficilement vérifiables) • Modèle = hypothèse • Incremental cost-effectiveness ratio par Quality adjusted life years ICER/QALY : combien ça coute en plus par année de vie (de qualité) en plus

analyse méthodologique des données pharmaco-économiques Intérêt ? ? Plafond acceptable d’ICER/QALY ? ? Combien la société est-elle prête à payer ? Fiabilité du modèle même si « techniquement parfait » ? Dépend des hypothèses de départ… • Voir KCE ? • •

analyse méthodologique des données pharmaco-économiques Vaccin antipneumococcique: PPV 23 non conjugué, PPV 13 conjugué

analyse méthodologique des données pharmaco-économiques

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

Incidence budgétaire • Modèle (hypothèses) • Dans les 2 à 3 années suivantes - Coût de ce nouveau traitement pour l’INAMI - Impact sur le coût des médicaments pour ce type de traitement - Impact sur le budget de l’INAMI pour soigner cette pathologie (hospitalisations, complications, . . )

Incidence budgétaire Point de vue CRM Difficultés pour l’estimation : - nombre de patients qui seront traités avec ce médicament - pénétration du marché du nouveau médicament - pas de difficulté pour comparer les prix des traitements médicamenteux - coût/gain par rapport à d’autres traitements - impact sur les complications, hospitalisations…

Nombre de patients/pénétration du marché • Firme : - minimiser le nombre de patients qui seront traités avec le nouveau traitement (plus cher…) - réduire la prise de part de marché • CRM : - tenter d’évaluer ce nombre (données Pharmanet, …. ) - évolution de la progression de produits similaires dans leur part de marché

comparer les prix des traitements médicamenteux Coût annuel d’un traitement • Un NACO : 923, 45 euro • Un AVK (warfarine): 83, 95 euro • Aspirine (160 mg) 32, 85 euro

coût/gain par rapport à d’autres traitements • En termes de suivi nécessaire (monitoring) - firme : pas (peu, moindre) suivi nécessaire - CRM : incertitudes, suivi nécessaire • En termes d’autres traitements nécessaires - firme: autres traitements médicamenteux nécessaires - CRM : hypothèses à vérifier

impact sur les complications, hospitalisations… • Firme : diminution des complications, diminution des hospitalisations pour la pathologie • CRM : hypothèses à vérifier

Structure du dossier • Partie administrative • EVALUATION - présentation de la pathologie - données épidémiologiques - modalités thérapeutiques actuelles et besoins thérapeutiques et sociaux - propriétés pharmaco-thérapeutiques - évaluation de la valeur thérapeutique et de l’intérêt de la spécialité: efficacité, effets indésirables, applicabilité, confort d’utilisation, degré de preuve - preuves issues de la pratique quotidienne - analyse méthodologique des données pharmaco-économiques - incidence budgétaire • Références • Résumé

Résumé classe 1 • Différentes rubriques permettant de juger de la plus-value thérapeutique

Plus-value thérapeutique • CRM peut conclure à une plus-value thérapeutique pour une (sous) population précise • Bases solides pour ce choix limité ?
- Slides: 70