Uloga medicinske sestre u klinikim ispitivanjima Csaba Dohoczky

Uloga medicinske sestre u kliničkim ispitivanjima Csaba Dohoczky dr. med. Ministarstvo zdravstva Opatija, Svibanj 2003.

ØKratka priča o razvoju lijekova ØPravila igre ØProces kliničkog ispitivanja ØUloga

Lijek mora biti: 1. Siguran 2. Učinkovit 3

Razvoj lijeka je: ØDugotrajan proces ØRizičan / neizvjestan proces ØVrlo skup proces 4
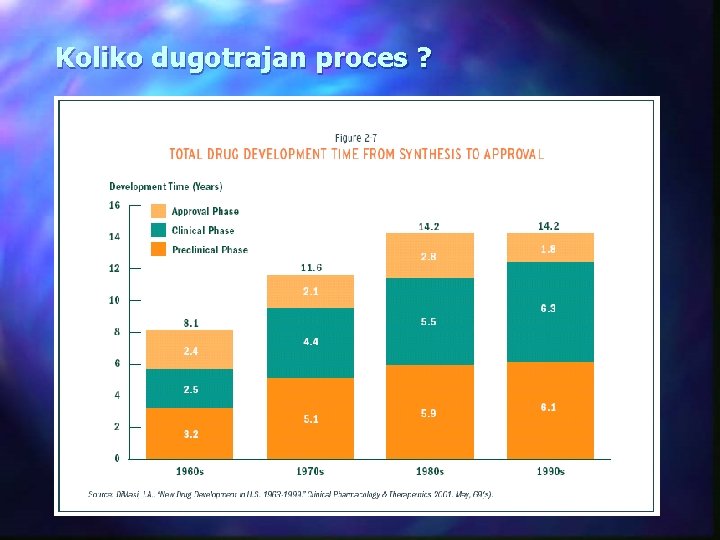
Koliko dugotrajan proces ?
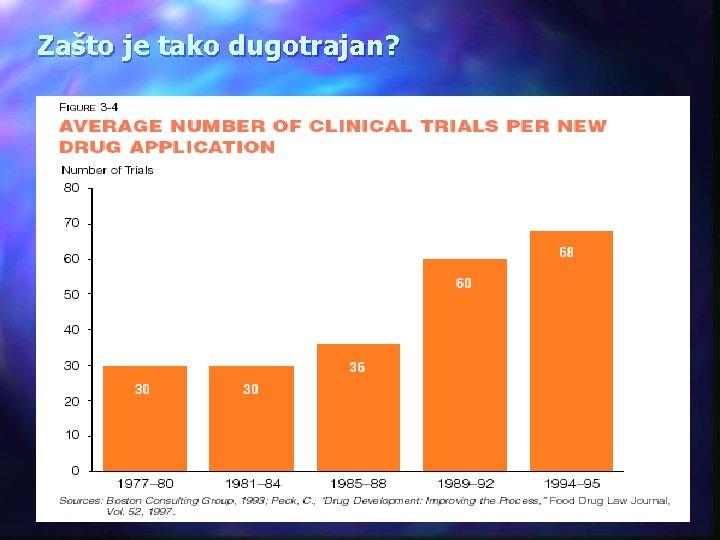
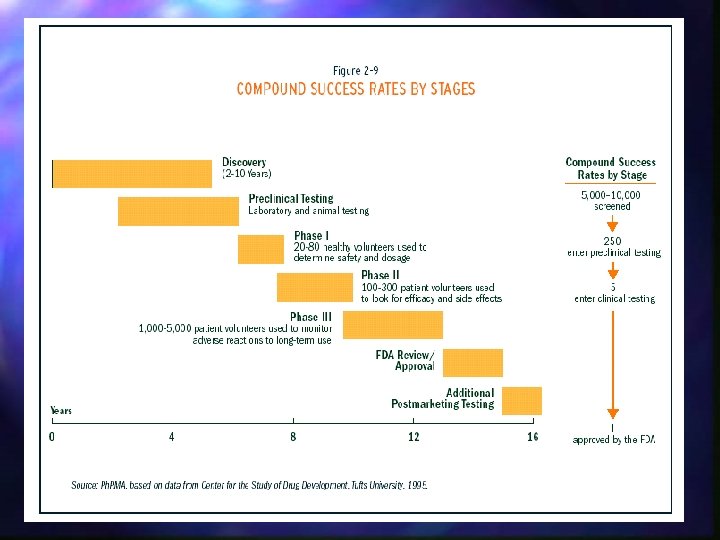
Zašto je tako dugotrajan?
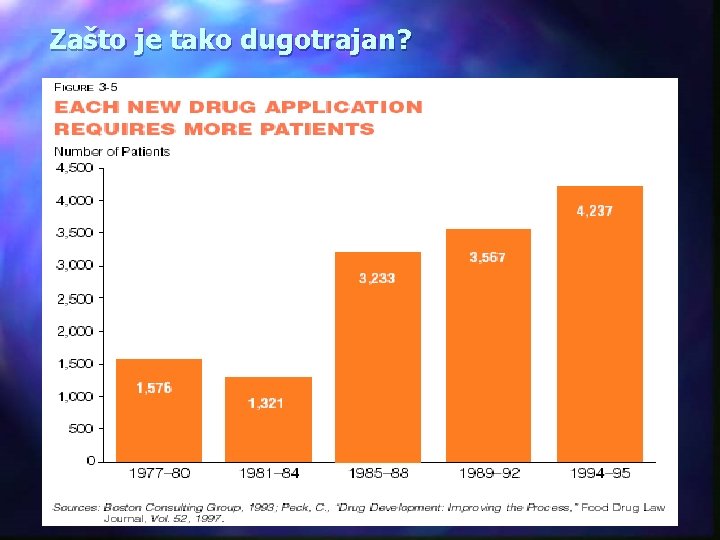
Zašto je tako dugotrajan?
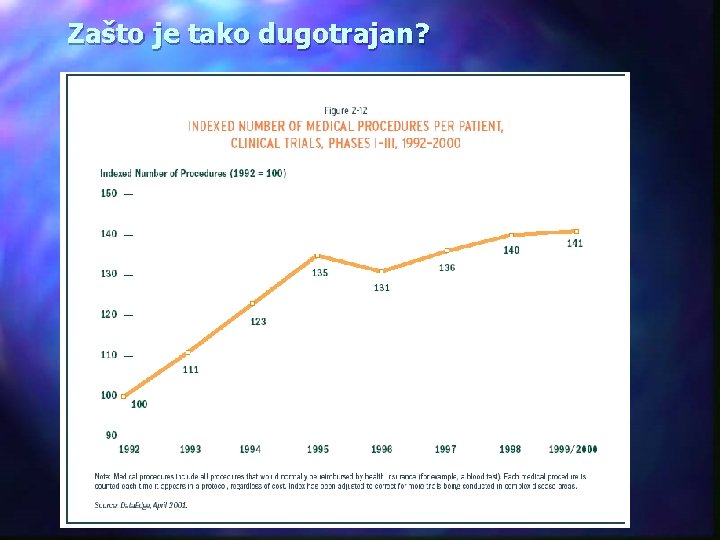
Zašto je tako dugotrajan?

Razvoj lijeka je: ØDugotrajan proces ØRizičan/neizvjestan proces ØVrlo skup proces 9

Otkriven 1859. U 1897: “Bez vrijednosti” Od 1899. "Aspirin“na tržištu 11

U 1899. , Bayer je proizvodio oko tonu of heroina godišnje, a izvozio ga je u 23 zemlje.

Rizik / neizvjesnost TALIDOMID Sinteza 1954. , Ispitivan kao lijek protiv alergije, Od 1957. na tržištu kao hipnotik. Povučen 1960. 5, 000 do 10, 000 djece rođeno s teškim oštećenjima ekstremiteta. Od 1998. talidomid je ponovno u upotrebi (lepra, Chronova bolest) 13

FDA Safety-Based Drug Withdrawals 2001 Baycol (cerivastatin) Cholesterol drug. Risk of rhabdomyolysis, severe damage to muscle that is sometimes fatal, especially when used at a high dose or with another drug called gemfibrozil Approved 1997, Bayer Raplon (rapacuronium bromide) Injectable anesthesia drug administered as a muscle relaxant for breathing tube placement and surgery. Risk of bronchospasm, an inability to breathe normally that can lead to permanent injury or death Approved 1999 Organon 2000 Lotronex (alosetron) Treatment for irritable bowel syndrome in women. Risk of intestinal damage resulting from reduced blood flow to the intestine (ischemic colitis) and severely obstructed or ruptured bowels (complications of severe constipation) Approved 2000, Glaxo. Smith. Kline Propulsid (cisapride) Treatment for nighttime heartburn. Risk of fatal heart rhythm abnormalities Approved 1993 Janssen Pharmaceutica Phenylpropanolamine Decongestant used in many prescription and over-the-counter cough and cold medications Risk of hemorrhagic stroke (bleeding in the brain) On market prior 1962.

Razvoj lijeka je: ØDugotrajan proces ØRizičan / neizvjestan proces ØVrlo skup proces 15
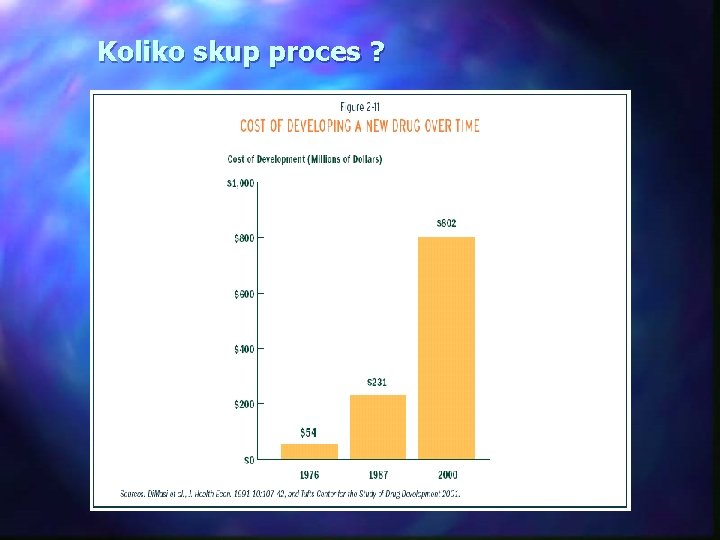
Koliko skup proces ?

Razvoj lijeka je: ØDugotrajan proces 14, 2 godine ØRizičan / neizvjestan proces 1 od 10. 000 ØVrlo skup proces 6. 000 kn 17

ØKratka priča o razvoju lijekova ØPravila igre ØProces kliničkog ispitivanja ØUloga

EMEA International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use

Zakoni, pravilnici Zakon o lijekovima i medicinskim proizvodima (NN 124/1997. ) Pravilnik o dobroj kliničkoj praksi (NN 143/1998. ) Pravilnik o prometu lijekovima i medicinskim proizvodima (NN 143/1998. ) http: //www. nn. hr

Međunarodne deklaracije i smjernice “Helsinška deklaracija” : Preporuke za liječnike koji provode biomedicinska istraživanja na ljudima http: //www. wma. net/ “ICH Guidelines” http: //www. ich. org

International Conference on Harmonisation Good clinical practice GCP Dobra klinička parksa DKP

Dobra klinička praksa je: standard za kliničke pokuse koji uključuje plan, provedbu, završetak, kontrolu, analize, načine izvješća i dokumentaciju istraživanja na čovjeku kojim se osigurava da su pokusi znanstveno i etički utemeljeni te da su kliničke značajke lijeka i medicinskog proizvoda koji se ispituje za dijagnostiku, liječenje ili prevenciju na odgovarajući način dokumentirani.

ØKratka priča o razvoju lijekova ØPravila igre ØProces kliničkog ispitivanja ØUloga

Proces kliničkog ispitivanja 1. dio Sponzor (naručitelj) = Industrija Dokumentacija: Protokol (plan pokusa) Case Report Form - CRF (Test lista) Informed consent – IC (Informirani pristanak) Investigators Brochure – IB (Upute za istraživača)

Proces kliničkog … 2. dio Principal Investigator (Glavni istraživač) Bolničko povjerenstvo za lijekove Ethics Committee (Etičko povjerenstvo ustanove)

Proces …. 3. dio Regulatory approval (Odobrenje Ministarstva Zdravstva RH) Prestudy meeting (naručitelj + izvršioci) Study initiation (uključivanje ispitanika uz prethodno potpisani Informirani pristanak)

Proces …. 4. dio Recruitment (uključivanje) Standardne operativne procedure (SOP) Working documents (upute) CRF, Data log, Work sheet, Forms DATUM I POTPIS !!!

Proces …. 5. dio Monitor (motritelj), Audit (nadzor), Inspekcija Što gledaju: Ethics (informirani pristanak) Compliance (pridržavanje protokola) Source document (nalazi, pov. bolesti) Raw data (originalni zapis/podatak) CRF (zapisano, datum, potpis) Accountability (“inventura” lijekova)

Proces …. 6. dio Zatvaranje kliničkog dijela studije Kompletiranje CRFa, Data management (obrada podataka) Data qery (razjašnjavanje nejasnoća u zapisanim podacima) Statistička obrada Study report (završno izvješće)

ØKratka priča o razvoju lijekova ØPravila igre ØProces kliničkog ispitivanja ØUloga

Preduvjet : Edukacija ! - struka - engleski jezik

Edukacija: Good clinical practice GCP Dobra klinička parksa DKP

Proces kliničkog ispitivanja 1. dio Sponzor (naručitelj) = Industrija Dokumentacija: Protokol (plan pokusa) Case Report Form - CRF (Test lista) Informed consent – IC (Informirani pristanak) Investigators Brochure - IB(Upute za istraživača)

Proces kliničkog … 2. dio Principal Investigator (Glavni istraživač) Bolničko povjerenstvo za lijekove Ethics Committee (Etičko povjerenstvo ustanove)

Proces …. 3. dio Regulatory approval (Odobrenje Ministarstva Zdravstva RH) Prestudy meeting DA ! Study initiation (uključivanje ispitanika uz prethodno potpisani Informirani pristanak) ?

The Informed Consent Process Informed consent is more than just a signature on a form, it is a process of information exchange that may include, in addition to reading and signing the informed consent document, subject recruitment materials, verbal instructions, question/answer sessions and measures of subject understanding. Thus, rather than an endpoint, the consent document should be the basis for a meaningful exchange between the investigator and the subject.

GCP kaže: Informed Consent must inform patient about: • the purpose of the study • the use of drug(s) • tests and any inconveniences • confidentiality will be maintained • is free to withdraw at any time • invite the patient to participate

Informirani pristanak je dokument potpisan i datiran rukom ispitanika na odobrenom obrascu.

GCP kaže: The investigator remains ultimately responsible, even when delegating the task of obtaining informed consent to another individual knowledgeable about the research.

Proces …. 4. dio Recruitment (uključivanje) Standardne operativne procedure (SOP) Working documents (upute) DA ! CRF, Data log, Work sheet, Forms DATUM I POTPIS !!! DA !

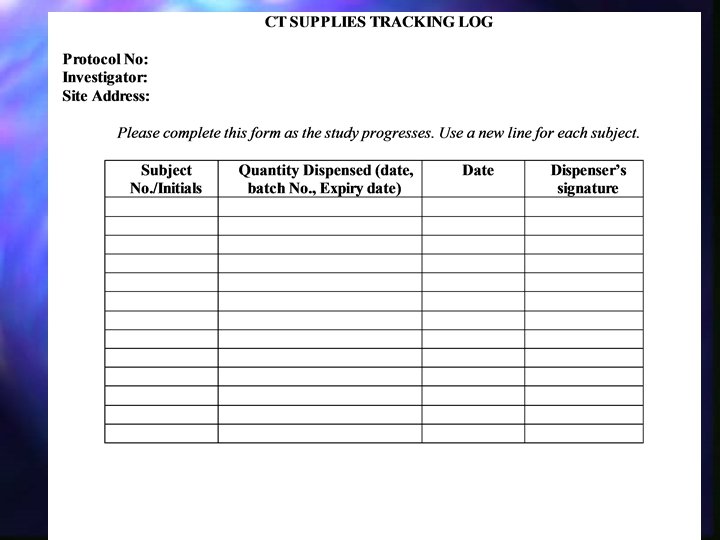

Proces …. 5. dio DA ! Monitor (motritelj), Audit (nadzor), Inspekcija Što gledaju: Ethics (informirani pristanak) Compliance (pridržavanje protokola) Source document (nalazi, pov. bolesti) Raw data (originalni zapis/podatak) CRF (zapisano, datum, potpis) Accountability (“inventura” lijekova)

Patient visit = dolasci bolesnika Dogovaranje: - pregleda - pretraga (EKG, Rtg, CT, MR, EMG. . . ) - laboratorijskih pretraga Kontakt s ispitanikom !

Proces …. 6. dio Zatvaranje kliničkog dijela studije Kompletiranje CRFa, Data management (obrada podataka) Data qery (razjašnjavanje nejasnoća u zapisanim podacima) Statistička obrada Study report (završno izvješće)

Hvala na pažnji Ministarstvo zdravstva RH Uprava za stručno medicinske poslove csaba. dohoczky@miz. hr Tel 4607 540 Fax 4677 105
- Slides: 47