Ukady dyspersyjne roztwory Roztwory koloidalne Roztwory waciwe Sposoby

Układy dyspersyjne - roztwory -Roztwory koloidalne -Roztwory właściwe -Sposoby wyrażania stężeń roztworów -Przeliczanie stężeń -Reguła mieszania roztworów

Układ • Układ – wyodrębniony obszar materii oddzielony od otoczenia wyraźnymi graniami (np. roztwór soli w probówce) • Otoczenie – wszystko to, co znajduje się poza układem (np. ścianki probówki i wszystko to, co znajduje się w jej otoczeniu) • Faza układu – jednorodna pod względem fizycznym część układu oddzielona od reszty układu wyraźną powierzchnią rozdziału (np. woda w stanie ciekłym, woda stanie stałym – lód, woda w stanie gazowym – para wodna) • Składnik układu – substancja o określonych właściwościach fizykochemicznych (np. woda w różnych stanach skupienia) • Układ dyspersyjny – układ składający się z fazy zdyspergowanej (rozproszonej - np. sacharoza) – fz oraz fazy dyspersyjnej (rozpraszającej, np. woda) – fd

Układ dyspersyjny Podział układów dyspersyjnych ze względu na stan skupienia fz i f d Stan skup. fz f. rozpraszana Stan skup. fd f. rozpraszająca Gaz Ciecz Ciało stałe Gaz Aerozol, mgła Roztwory właściwe, emulsje Dym, kurz Ciecz Roztwory gazowe Piana Ciało stałe Piana stała Mokra gąbka Stopy metali Roztwory właściwe, koloidy
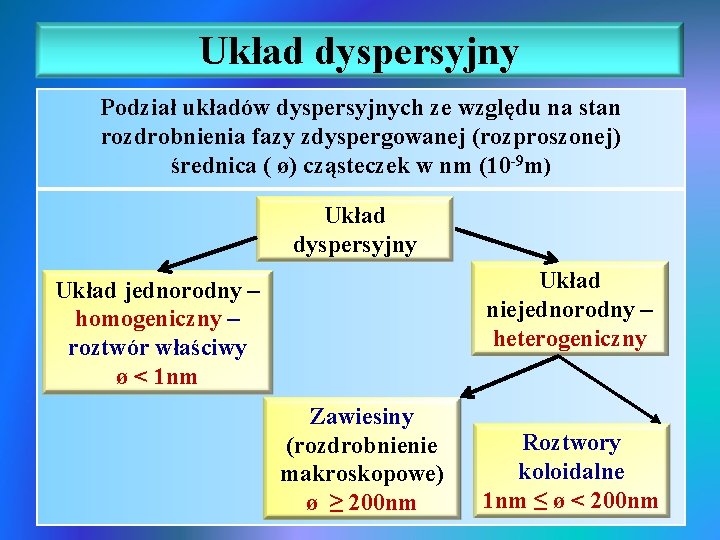
Układ dyspersyjny Podział układów dyspersyjnych ze względu na stan rozdrobnienia fazy zdyspergowanej (rozproszonej) średnica ( ø) cząsteczek w nm (10 -9 m) Układ dyspersyjny Układ niejednorodny – heterogeniczny Układ jednorodny – homogeniczny – roztwór właściwy ø < 1 nm Zawiesiny (rozdrobnienie makroskopowe) ø ≥ 200 nm Roztwory koloidalne 1 nm ≤ ø < 200 nm

Roztwory koloidalne v Roztwór koloidalny – układ dyspersyjny, w którym śr. cz. fazy rozp. zawarte są w granicach 1 nm ≤ ø < 200 nm Podział układów koloidalnych ze względu na : Rodzaj fazy Powinowactwo do Budowę fazy rozpraszającej rozpuszczalnika rozproszonej Ø hydrozole (woda) Ø alkozole (alkohol) Ø aerozole (powietrze) Ø liofilowe - duże powinowactwo do rozpuszczalnika, (łatwo ulegają solwatacji), Ø liofobowe - małe powinowactwo do rozpuszczalnika, | (nie ulegają Ø cząsteczkowe (pojedyncze makrocząsteczki) Ø fazowe (bardzo małe kryształy) Ø micelarne (micela)
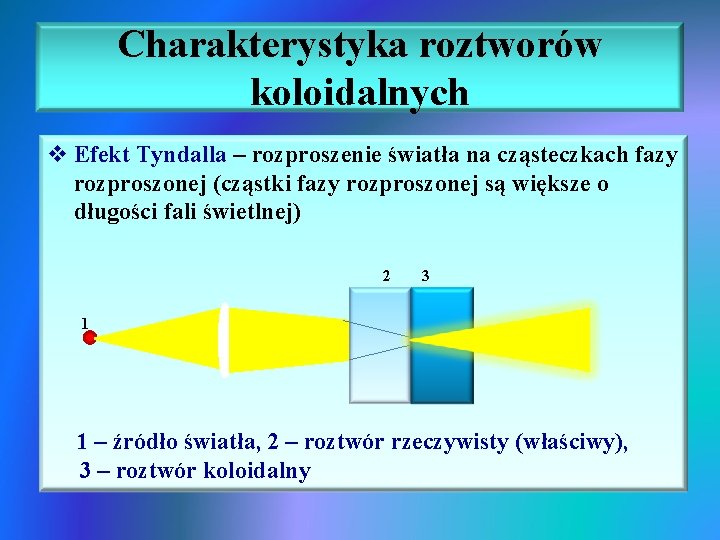
Charakterystyka roztworów koloidalnych v Efekt Tyndalla – rozproszenie światła na cząsteczkach fazy rozproszonej (cząstki fazy rozproszonej są większe o długości fali świetlnej) 2 3 1 1 – źródło światła, 2 – roztwór rzeczywisty (właściwy), 3 – roztwór koloidalny
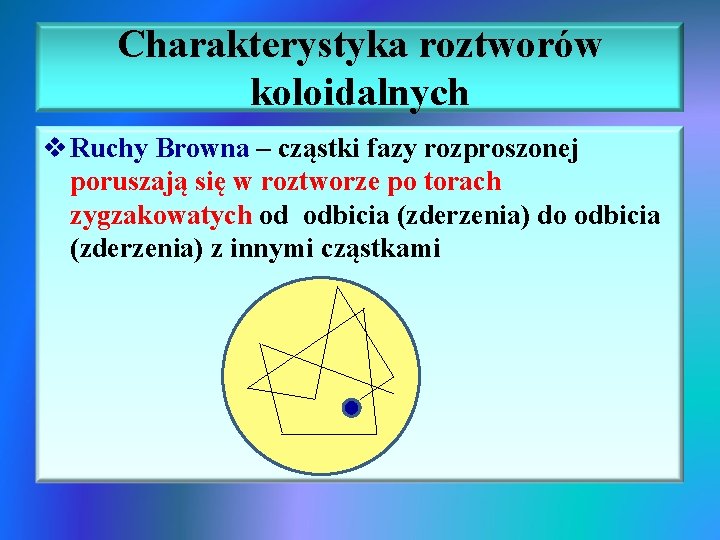
Charakterystyka roztworów koloidalnych v Ruchy Browna – cząstki fazy rozproszonej poruszają się w roztworze po torach zygzakowatych od odbicia (zderzenia) do odbicia (zderzenia) z innymi cząstkami

Charakterystyka roztworów koloidalnych v. Koagulacja – zjawisko łączenia się cząstek fazy rozproszonej koloidu w większe zespoły tworzące nieregularną sieć – koagulat. v. Peptyzacja – zjawisko odwrotne do koagulacji. KOAGULACJA (koloid) ZOL ŻEL (koagulat) PEPTYZACJA v. Denaturacja – nieodwracalny proces przechodzenia zolu w żel.

Charakterystyka roztworów koloidalnych Czynniki powodujące proces koagulacji i denaturacji koloidu Koagulacja koloidu Ø dodanie niektórych elektrolitów, Ø dodanie nieelektrolitów, Ø zmiana temperatury (obniżenie / podwyższenie) Ø działanie czynnikami mechanicznymi, Ø przepływ prądu elektrycznego, Ø działanie świtała, Ø inne. Denaturacja koloidu Ø dodanie: ü stężonych roztworów kwasów lub zasad, ü roztworów soli metali ciężkich, ü niektórych związków organicznych (alkoholu, aldehydu), Ø wysokie zmiany temperatury, Ø promieniowanie uv.
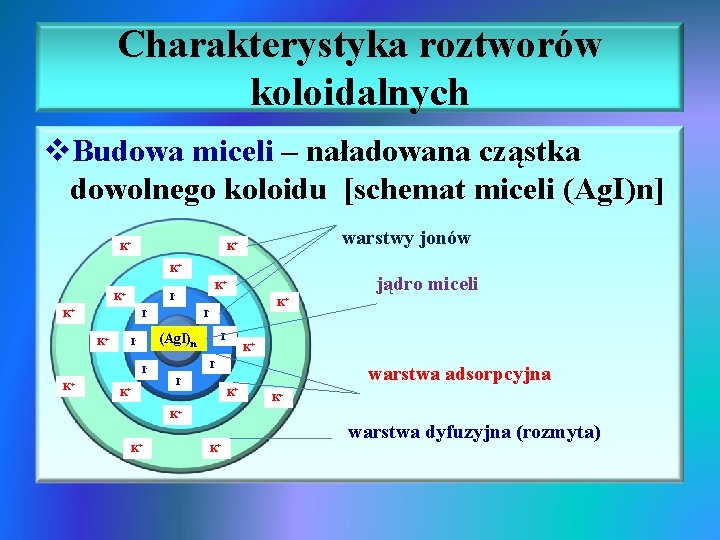
Charakterystyka roztworów koloidalnych v. Budowa miceli – naładowana cząstka dowolnego koloidu [schemat miceli (Ag. I)n] K warstwy jonów K+ K+ K+ IK+ K+ K+ II- (Ag. I)n I- K+ II- warstwa adsorpcyjna K+ K+ K+ jądro miceli K+ I- K+ K+ warstwa dyfuzyjna (rozmyta)

Roztwory właściwe v Roztwór właściwy – jednorodna (homogeniczna) mieszanina dwóch lub więcej składników, składnik występujący w nadmiarze nazywa się rozpuszczalnikiem a pozostałe składniki substancjami rozpuszczonymi (w zależności od stanu skupienia wyróżnia się roztwory: gazowe, ciekłe, stałe). v Mieszanina – układ złożony z co najmniej dwóch substancji w dowolnym stosunku. v Rozpuszczanie – proces mieszania prowadzący do powstania roztworu. v Rozpuszczalność – maksymalna liczba gramów substancji, która rozpuszcza się w określonych warunkach temp. i ciśnienia w 100 g rozpuszczalnika dając roztwór nasycony
Roztwory właściwe v Podział roztworów ze względu na zawartość substancji rozpuszczonej: Roztwory Roztwór nienasycony c < cmax Roztwór przesycony c > cmax Roztwór nasycony c = cmax Ø c – stężenie roztworu. Ø cmax – stężenie roztworu wynikające z rozpuszczalności.

Efekty towarzyszące procesom rozpuszczania v Solwatacja – proces otaczania jonów lub cząsteczek przez cząsteczki rozpuszczalnika (jeżeli rozpuszczalnikiem jest woda – uwodnienie – hydratacja). v Efekty energetyczne – proces endoenergetyczny z pobieraniem energii cieplnej z otoczenia, proces egzoenergetyczny z oddaniem energii cieplnej do otoczenia. v Efekt ebulioskopowy – temp. wrzenia roztworu jest wyższa niż temp. wrzenia rozpuszczalnika. v Efekt krioskopowy – temp. krzepnięcia roztworu jest niższa niż temp. krzepnięcia rozpuszczalnika

Efekty towarzyszące procesom rozpuszczania /cd. v Kontrakcja – zmniejszenie objętości układu po połączeniu dwóch różnych cieczy (np. woda + etanol): Ø zmniejszenie objętości mieszanych cieczy o ok. 3%, wynikająca z zrywania wodorowych woda – woda i wiązań wodorowych alkohol – alkohol, Ø z powstawania nowych wiązań wodorowych woda – alkohol, które są krótsze niż wiązanie alkohol – alkohol, ale dłuższe niż woda – woda, Ø wiązania wodorowe mają długość pośrednią, v Dyfuzja – proces prowadzący do wyrównania stężenia w całej objętości roztworu v Dysocjacja – rozpad cząsteczek substancji rozpuszczaj na jony pod wpływem polarnego rozpuszczalnika
![Sposoby wyrażania stężeń roztworów v. Stężenie procentowe [%]: Cp (C%) - procent masowy (wagowy) Sposoby wyrażania stężeń roztworów v. Stężenie procentowe [%]: Cp (C%) - procent masowy (wagowy)](http://slidetodoc.com/presentation_image_h2/c9e2957962252d90e6c67bb10a503403/image-15.jpg)
Sposoby wyrażania stężeń roztworów v. Stężenie procentowe [%]: Cp (C%) - procent masowy (wagowy) substancji rozpuszczonej w roztworze (w 100 g roztworu) Ø ms – masa substancji rozpuszczonej [g] Ø mr – masa roztworu [g], Ø mrozp – masa rozpuszczalnika [g] Ø mr = ms + mrozp
![Sposoby wyrażania stężeń roztworów v Stężenie molowe [mol/dm 3] = [mol. dm-3] : Cm Sposoby wyrażania stężeń roztworów v Stężenie molowe [mol/dm 3] = [mol. dm-3] : Cm](http://slidetodoc.com/presentation_image_h2/c9e2957962252d90e6c67bb10a503403/image-16.jpg)
Sposoby wyrażania stężeń roztworów v Stężenie molowe [mol/dm 3] = [mol. dm-3] : Cm – liczba moli substancji rozpuszczonej (zawartej) w 1 dm 3 roztworu: Ø ü ü ü n - liczba moli substancji rozpuszczonej, Vr – objętość roztworu w dm 3, ms - masa sub. rozp. mr - masa roztw. m – masa molowa sub. rozp. dr – gęstość roztw.

Przeliczanie stężeń roztworów Przeliczenie z Cp na Cm Ø Ø Ø ü Przeliczenie z Cm na Cp Cm – stężenie molowe roztworu [mol/dm 3], Cp – stężenie procentowe roztworu [%], dr – gęstość roztworu w g/dm 3: gęstość należy przeliczyć z g/cm 3 mnożąc ją przez 1000, np. d = 1, 2 g/cm 3= 1200 g/dm 3) Ø M – masa molowa [mol/dm 3]

Reguła mieszania roztworów – metoda krzyżowa v Uwagi: Ø rozcieńczając roztwór wodą, należy przyjąć, że jest to roztwór 0%, Ø zatężając roztwór solą bezwodną, należy przyjąć, że jest to roztwór 100%, Ø zatężając roztwór hydratem (solą uwodnioną), należy przyjąć, że jest to roztwór wodny o określonym stężeniu: np. Cu. SO 4. 5 H 2 O: ü mr = M = 64 g/mol + 32 g/mol + 4. 16 g/mol + 5. 18 g/mol = 160 g/mol + 90 g/mol = 250 g/mol ü ms = 160 g

Reguła mieszania roztworów – metoda krzyżowa (Cp) v Obliczanie stężenia procentowego po wymieszaniu roztworu o masie mr 1 i stężeniu Cp 1 z roztworem o masie mr 2 i stężeniu Cp 2 (Cp 1 > Cpx> Cp 2) mr 1 Cp 1 – Cpx mr 2 Cpx – Cp 2 mr 1 Cpx mr 2 Ø z proporcji: (Cp 1 – Cpx). mr 1 = (Cpx – Cp 2). mr 2

Reguła mieszania roztworów – metoda krzyżowa (Cm) v Obliczanie stężenia molowego po wymieszaniu roztworu o objętości Vr 1 i stężeniu Cm 1 z roztworem o objętości Vr 2 i stężeniu Cm 2 (Cm 1 > Cmx> Cm 2) Vr 1 Cm 1 – Cmx mr 2 Cmx – Cm 2 mr 1 Cpx Vr 2 Ø z proporcji: (Cm 1 – Cmx). Vr 1 = (Cmx – Cm 2). Vr 2
- Slides: 20