Uhlovodky jsou organick sloueniny obsahujc pouze atomy uhlku

Uhlovodíky jsou organické sloučeniny obsahující pouze atomy uhlíku a vodíku.

Rozdělení uhlovodíků q Hlavní kritérium dělení: ü tvar uhlíkového řetězce, ü druhy vazeb mezi atomy uhlíku.

Podle tvaru řetězce q Alifatické uhlovodíky jsou tvořeny řetězci uhlíkových atomů, které nejsou uzavřeny do kruhu (uhlovodíky s otevřeným řetězcem nebo acyklické uhlovodíky ). q Alicyklické uhlovodíky aspoň část uhlíkového řetězce je uspořádána do jednoho nebo několika kruhů, které nejsou aromatické. q Aromatické uhlovodíky obsahují konjugovaný systém dvojných vazeb.

Podle přítomnosti jednoduchých a násobných vazeb q Nasycené uhlovodíky mají jen jednoduché ( σ ) vazby q Nenasycené uhlovodíky mají násobné ( dvojné nebo trojné ) vazby ( vazby δ a π )

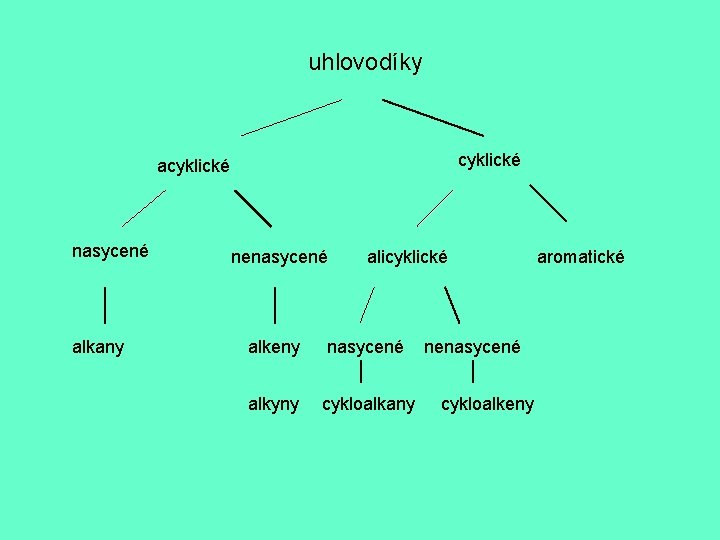
uhlovodíky cyklické acyklické nasycené alkany nenasycené alicyklické alkeny nasycené alkyny cykloalkany nenasycené cykloalkeny aromatické

Alkany a cykloalkany q Alkany a cykloalkany jsou organické sloučeniny, uhlovodíky, které obsahují jenom jednoduché vazby C - C a C - H.

Struktura alkanů a cykloalkanů q Mezi atomy uhlíku i mezi atomy uhlíku a vodíku jsou vazby. q. Atomy uhlíku jsou v hybridním stavu sp 3, všechny jeho vazby směřují z těžiště do vrcholů pravidelného čtyřstěnu :

q Každý následující alkan se od předcházejícího liší o jeden atom uhlíku a dva atomy vodíku, o tzv. homologický přírůstek ( homologický rozdíl ) -CH 2 -. q Takové řady, kde následující člen se liší od předcházejícího o skupinu -CH 2 - , se nazývají řady homologické. q Obecný vzorec alkanů je Cn. H 2 n+2.
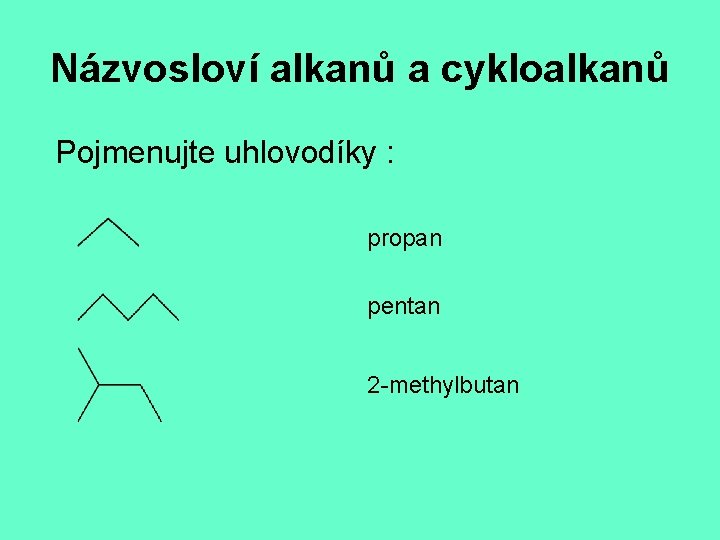
Názvosloví alkanů a cykloalkanů Pojmenujte uhlovodíky : propan pentan 2 -methylbutan
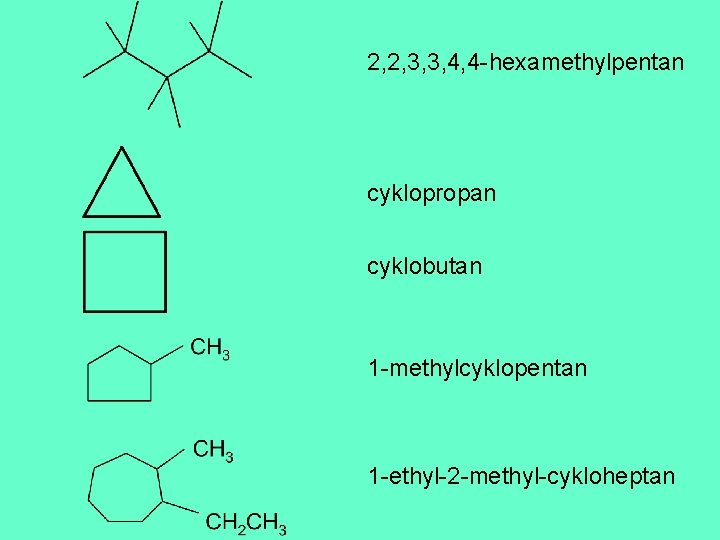
2, 2, 3, 3, 4, 4 -hexamethylpentan cyklopropan cyklobutan 1 -methylcyklopentan 1 -ethyl-2 -methyl-cykloheptan
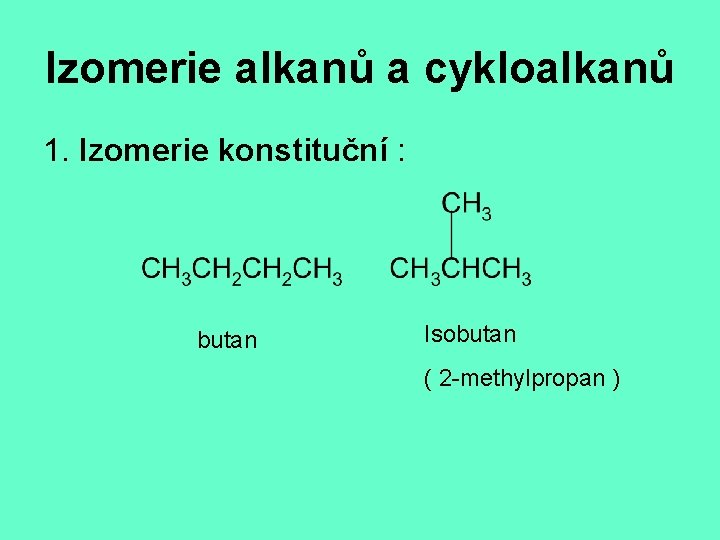
Izomerie alkanů a cykloalkanů 1. Izomerie konstituční : butan Isobutan ( 2 -methylpropan )
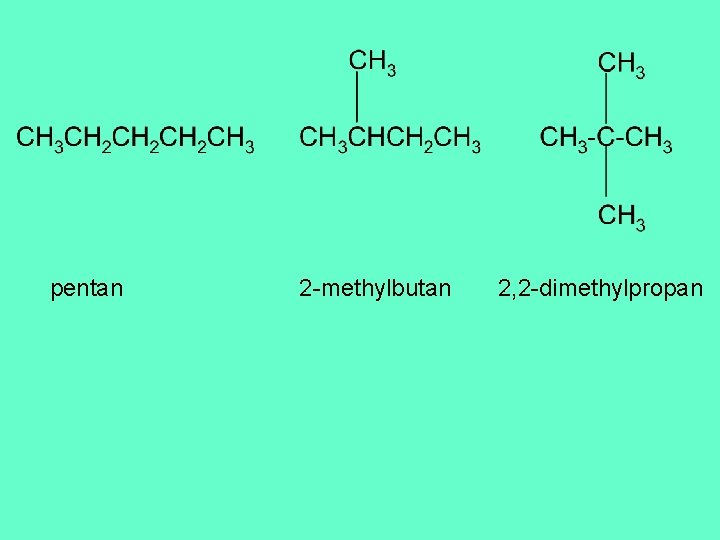
pentan 2 -methylbutan 2, 2 -dimethylpropan
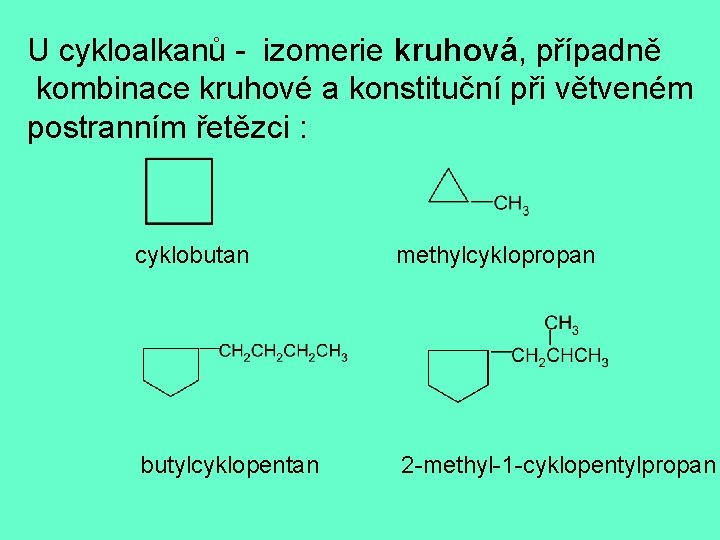
U cykloalkanů - izomerie kruhová, případně kombinace kruhové a konstituční při větveném postranním řetězci : cyklobutan methylcyklopropan butylcyklopentan 2 -methyl-1 -cyklopentylpropan

2. Stereoizomerie : q V důsledku rotace atomů uhlíku kolem vazby vznikají u alkanů a cykloalkanů různá prostorová uspořádání nazývaná konformace. q Např. u ethanu rozlišujeme dvě extrémní konformace, zákrytovou a nezákrytovou:
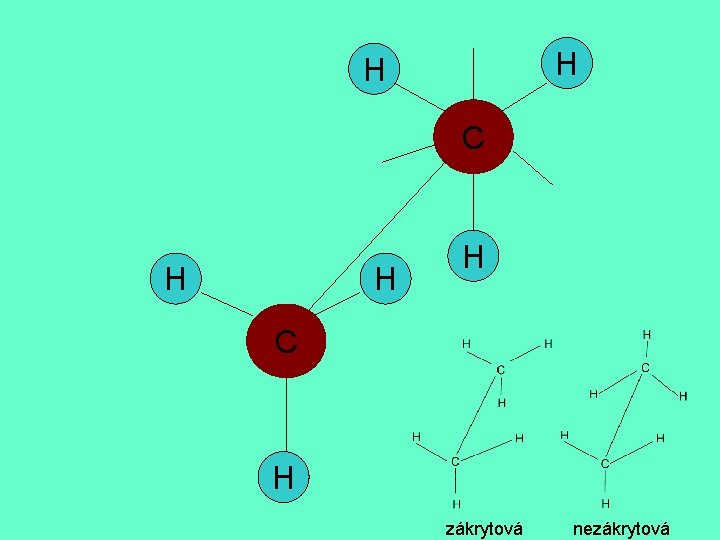
H H C H zákrytová nezákrytová
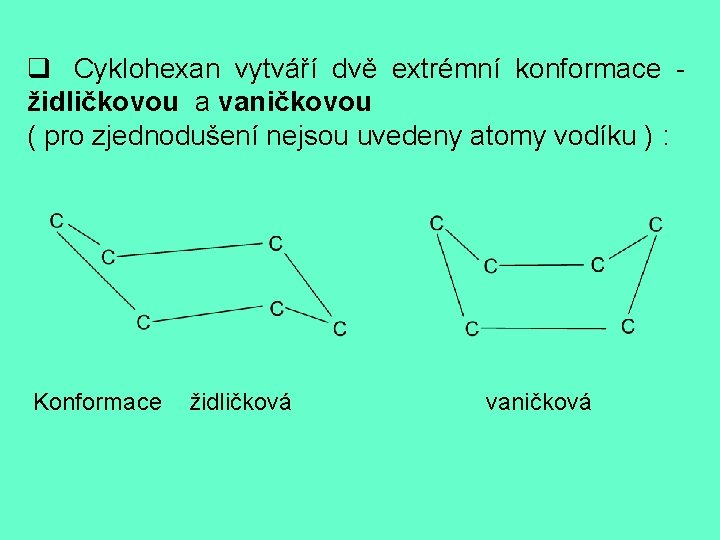
q Cyklohexan vytváří dvě extrémní konformace - židličkovou a vaničkovou ( pro zjednodušení nejsou uvedeny atomy vodíku ) : Konformace židličková vaničková

Příprava alkanů 1. Izolace z přírodních zdrojů ( ropa, zemní plyn, uhlí, humusové sedimenty a živice ). 2. Katalytická hydrogenace nenasycených uhlovodíků ( např. hydrogenace benzenu ). 3. Redukce alkoholů vodíkem ( teplota, katalyzátor ).
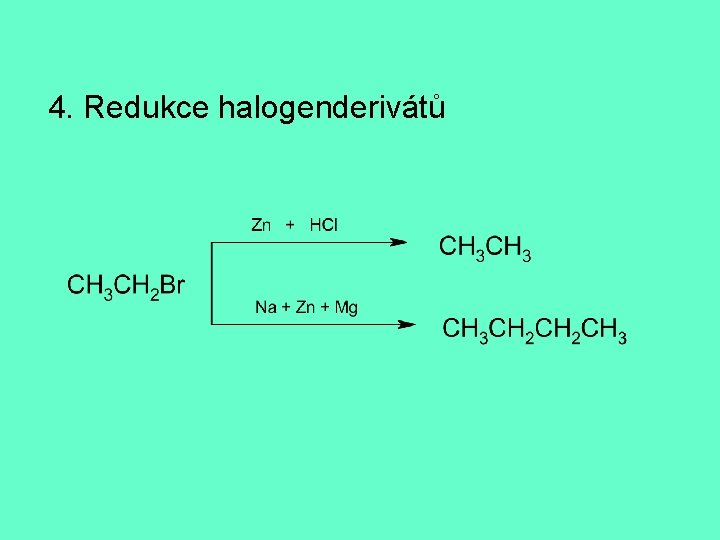
4. Redukce halogenderivátů

Vlastnosti alkanů a cykloalkanů q Methan, propan a butan jsou plyny. q Ostatní alkany jsou kapaliny nebo pevné látky. q Cykloalkany jsou kapaliny nebo pevné látky. q Všechny uhlovodíky jsou hydrofobní látky nemísitelné s vodou, dobře rozpouštějí jiné nepolární látky.

q Protože alkany mají v molekulách jen jednoduché vazby, jsou poměrně málo reaktivní. q Reagují jen za dodání velkého množství energie, reakce probíhají radikálovým mechanismem. q Další charakteristickou reakcí alkanů a cykloalkanů je eliminace. Za velmi vysokých teplot a za přítomnosti katalyzátorů lze z molekuly alkanu odštěpit vodík, proběhne dehydrogenace , alkan se změní na alken, cykloalkan na cykloalken.

q Oxidace Běžnými oxidačními činidly ( dichroman, manganistan ) se alkany a cykloalkany oxidují nesnadno. Silně exotermické a široce využívané jsou oxidace alkanů kyslíkem - hoření. ( Při hoření se štěpí vazby mezi atomy uhlíku a vodíku. )

q Pyrolýza - krakování = rozklad molekul uhlovodíků za vysokých teplot. Z uhlovodíku s delším řetězcem vznikají uhlovodíky s kratším řetězcem. Při krakování se štěpí vazby C - C i vazby C - H. Krakování je složitý proces, který má uplatnění při zpracování frakcí ropy.

Nejdůležitější alkany a cykloalkany q Methan q Ethan q Propan a butan q Cyklopropan a cyklohexan q Isooktan ( 2, 2, 3 -trimethylpentan )

Účinky alkanů a cykloalkanů na organismus q Nasycené uhlovodíky většinou nejsou příliš toxické. q V plynné stavu mají narkotický účinek a některé z nich poškozují plicní tkáň a nervový systém. q Kapalné alkany a cykloalkany se vstřebávají kůží, po požití vyvolávají pálení v ústech, jícnu a žaludku. q Parafinový olej (paraffinum liquidum) jako součást některých přípravků může změkčit stolici. Nelze jej však podávat dlouhodobě, protože se nepatrně vstřebává a kromě toho by zabraňoval vstřebávání v tucích rozpustných vitaminů. q Nebezpečné mohou být akutní otravy motorovým benzinem. Jednak obsahuje určitý podíl aromatických uhlovodíků (včetně benzenu), jednak se stále ještě vyrábí i s příměsí toxického tetraethylolova. Motorový benzin se nikdy nesmí používat jako rozpouštědlo.

Alkeny a alkadieny q Alkeny jsou acyklické nenasycené uhlovodíky, které obsahují v molekule jednu dvojnou vazbu. q Alkadieny jsou acyklické nenasycené uhlovodíky, které obsahují dvě dvojné vazby v molekule.

Struktura alkenů a alkadienů q Ze strukturního hlediska je důležitá vzájemná poloha dvojných vazeb v uhlíkatém řetězci. Mohou nastat tři možnosti: 1. Dvojné vazby jsou izolované dvěma jednoduchými vazbami. 2. Dvojné vazby jsou kumulované. 3. Dvojné vazby konjugované

Izomerie alkenů a alkadienů q Konstituční izomery se mohou lišit uspořádáním řetězce ( nerozvětvený a různé způsoby rozvětvení ) nebo polohou dvojné vazby ( či vazeb ) v řetězci. q Dvojná vazba alkenů a alkadienů je příčinou konfigurační izomerie typu cistrans.
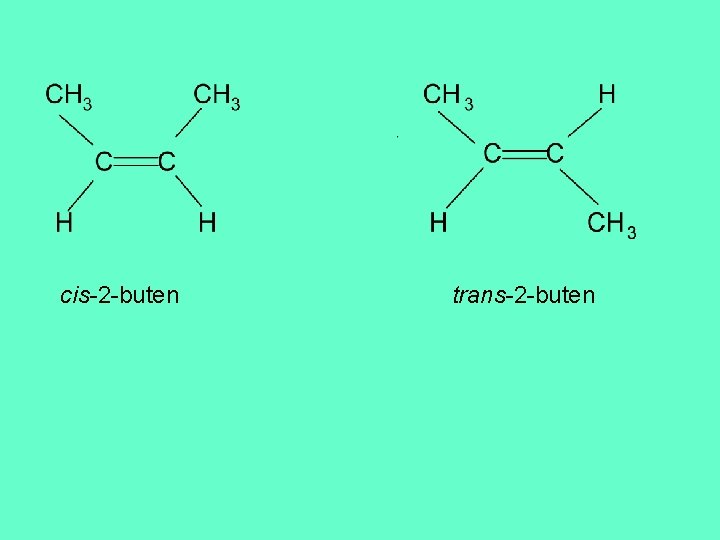
cis-2 -buten trans-2 -buten

Názvosloví alkenů a alkadienů q Název odpovídajícího alkanu, zakončení -an se nahradí zakončením -en. Jestliže poloha dvojné vazby není jednoznačná ( větší počet atomů uhlíku v molekule ), označí se číslem tak, aby číslo označující atom uhlíku, ze kterého dvojná vazba vychází, bylo co nejnižší. q Názvy alkadienů tvoříme obdobně, přítomnost dvou dvojných vazeb vyjádříme dvěma čísly a zakončením -dien.

Příprava alkenů a alkadienů q Alkeny a dieny připravujeme nejčastěji eliminačními reakcemi: 1. Z alkanů 2. Z alkoholů 3. Kučerovova reakce
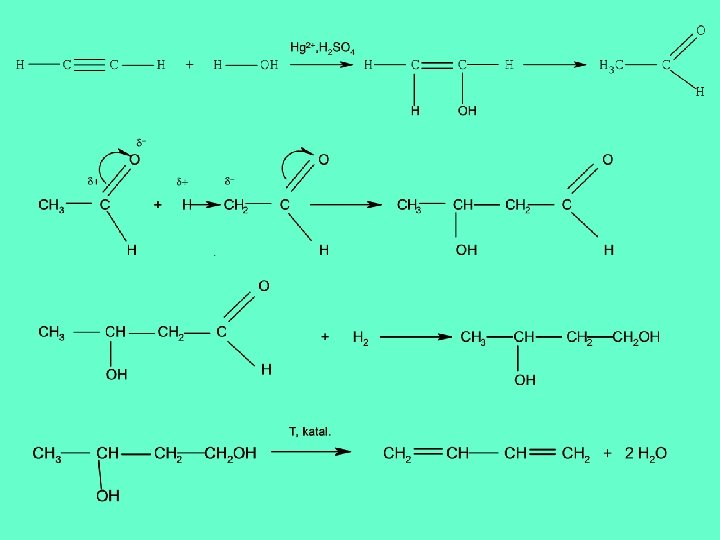

Vlastnosti alkenů a alkadienů q Alkeny a alkadieny jsou nenasycené sloučeniny, dvojná vazba mezi atomy uhlíku je tvořena vazbou σ a vazbou π. q Vazebná energie vazby π je nižší, proto je tato vazba štěpena přednostně.

Charakteristické reakce alkenů a alkadienů 1. Adiční reakce Markovníkovovo pravidlo: Při adici halogenovodíku na dvojnou vazbu se atom vodíku aduje na ten atom uhlíku dvojné vazby, který je na vodík bohatší. Hydrohalogenace Hydratace Halogenace

2. Polymerace 3. Ke štěpení vazby dochází radikálovým mechanismem. Přitom vznikají radikály, které se spojují do větších celků, molekuly monomeru se spojují za vzniku polymeru. 4. Polymerace probíhá ve třech fázích - iniciace, propagace a terminace.

3. Oxidace 4. Nenasycené uhlovodíky jsou mnohem citlivější k oxidaci než uhlovodíky nasycené. Již za nízkých teplot působením alkalického roztoku manganistanu draselného dochází k adici dvou hydroxylových skupin na dvojnou vazbu za vzniku diolu ( dvojsytného alkoholu ):

Za vyšší teploty a při použití kyselého roztoku manganistanu draselného nebo jiných oxidačních činidel ( dichroman draselný, oxid chromový ) stadium diolu již nezachytíme. Dochází totiž k další oxidaci, celá molekula se přitom štěpí a vznikají karboxylové kyseliny : R - CH = CH - R´ + 4 O R - COOH + R´- COOH

4. Substituční reakce Substituce není charakteristická reakce nenasycených uhlovodíků, může však nastat působením halogenů na alkeny ( dieny. . . ) za vysokých teplot ( 500 - 600 o. C ) : CH 3 - CH = CH 2 + Cl 2 CH 2 = CH - CH 2 Cl + HCl propen allylchlorid

Nejdůležitější alkeny a dieny q Ethen ( ethylen ) q Propen ( propylen ) q Buta-1, 3 -dien q 2 -methylbuta-1, 3 -dien, isopren

Alkyny q Alkyny jsou nenasycené acyklické uhlovodíky s jednou trojnou vazbou ( 1 x vazba σ a 2 x vazba π ).

Názvosloví alkynů q Názvosloví alkynů vychází z názvu alkanů, zakončení -an se mění na zakončení -yn. Nejnižší člen homologické řady alkynů je ethyn, triviálním názvem acetylen. q Polohu trojné vazby vyjádříme číslovkou před zakončením –yn.

Příprava alkynů 1. Přímá syntéza z vodíku a uhlíku 2. Rozklad karbidu vápníku vodou 3. Nedokonalá oxidace zemního plynu ( methanu ) 4. Eliminační reakce

Vlastnosti alkinů 1. Adice Při adici vody není produktem alkohol, ale aldehyd nebo keton. q Adicí vody na alkin vzniká zv. enol který je velmi nestálý a snadno přesmykuje na stabilnější aldehyd nebo keton. q Přesmyk dvojné vazby a atomu vodíku je zvratný, v rovnovážném stavu vedle sebe existují dvě rozdílné formy jedné sloučeniny. Tento jev se nazývá tautomerie. V tomto případě se jedná o tzv. keto-enol (nebo oxoenol) tautomerii.
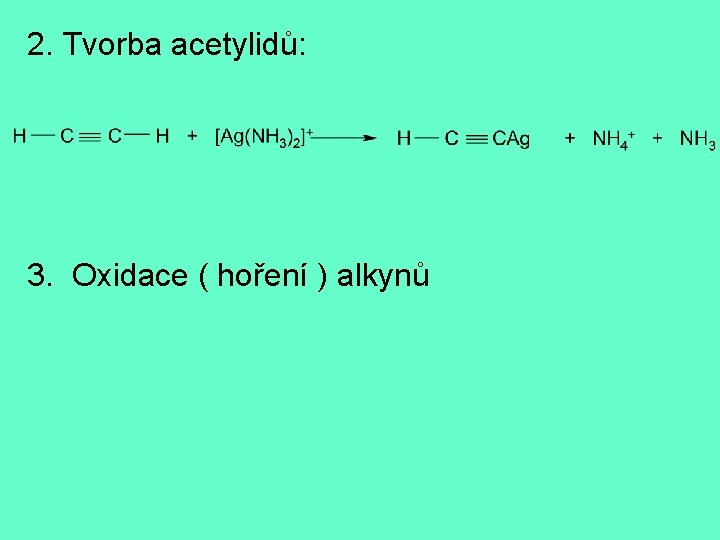
2. Tvorba acetylidů: 3. Oxidace ( hoření ) alkynů
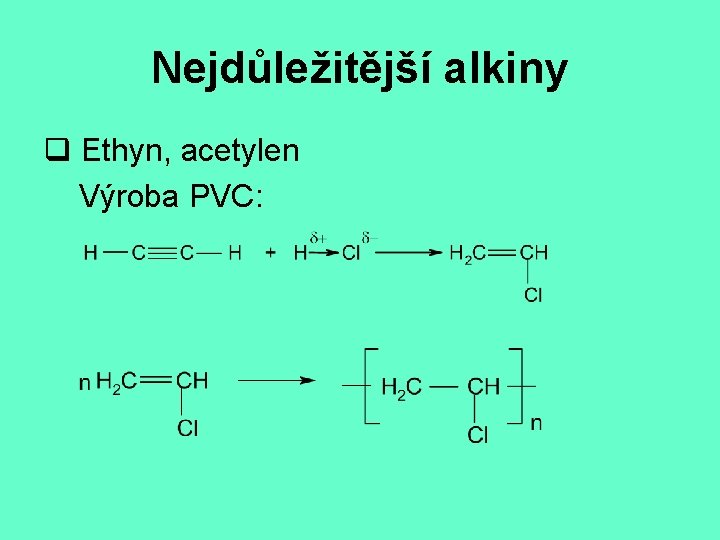
Nejdůležitější alkiny q Ethyn, acetylen Výroba PVC:

Aromatické uhlovodíky, areny q Aromatické uhlovodíky jsou zvláštní skupina cyklických uhlovodíků se systémem dokonale konjugovaných dvojných vazeb, většinou ve formě benzenového jádra nebo několika kondenzovaných kruhů. Toto zvláštní uspořádání jim dodává vlastnosti souhrnně nazývané aromatický charakter.

Názvosloví aromatických uhlovodíků q Jednoduché aromatické uhlovodíky jsou pojmenovány triviálními názvy. q Pokud je na benzenovém jádře navázán substituent ( nahrazuje atom vodíku ), číslujeme cyklus od místa připojení substituentu. Pokud je substituentů více, číslujeme tak, aby polohy navázání substituentů měly nejnižší možná čísla.
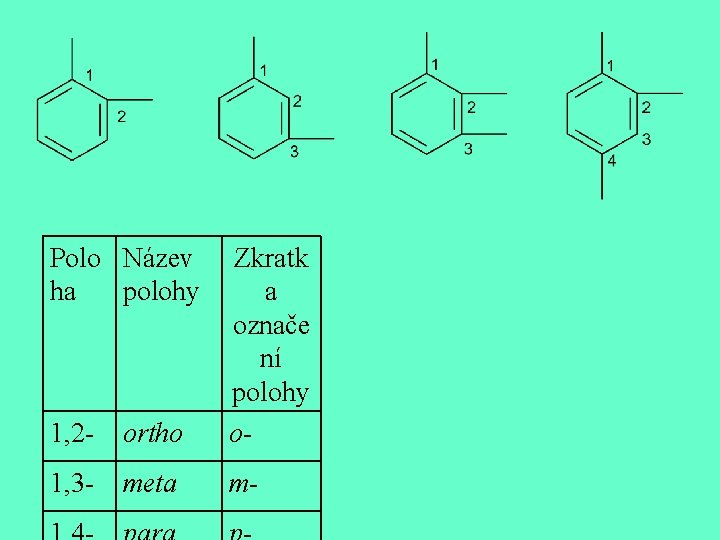
Polo Název ha polohy 1, 2 - ortho Zkratk a označe ní polohy o- 1, 3 - meta m-
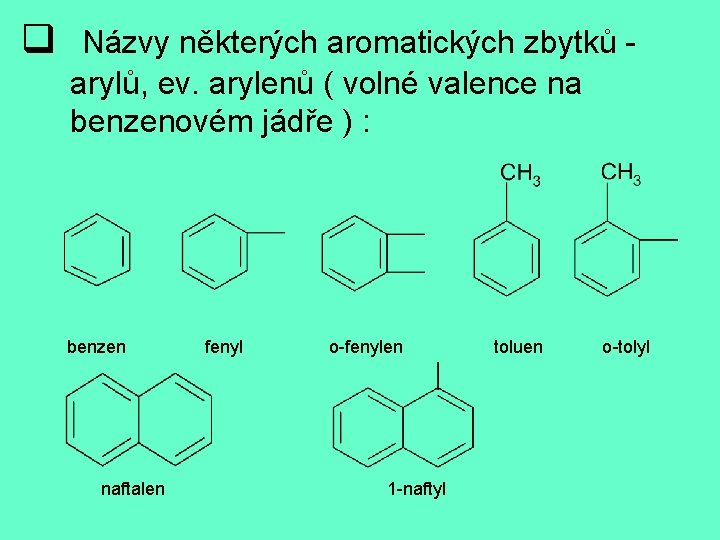
q Názvy některých aromatických zbytků - arylů, ev. arylenů ( volné valence na benzenovém jádře ) : benzen naftalen fenyl o-fenylen 1 -naftyl toluen o-tolyl
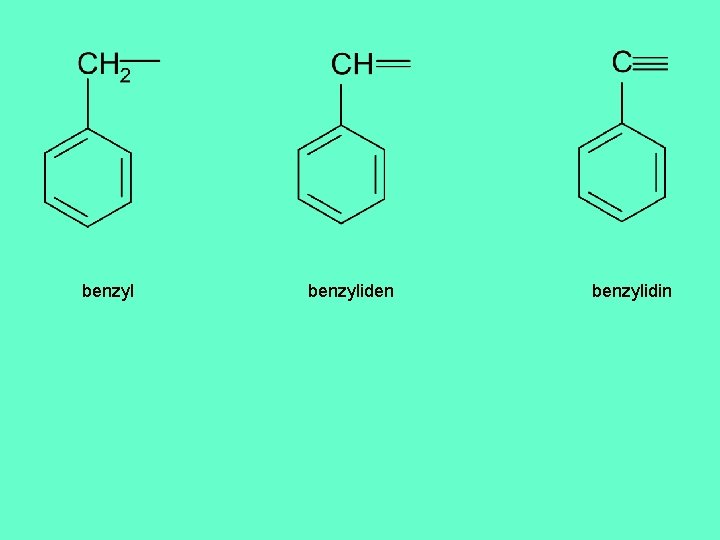
benzyliden benzylidin

Rozdělení arenů q Podle počtu a vzájemného uspořádání benzenových jader: 1. Areny s jedním benzenovým jádrem 2. Areny s kondenzovanými benzenovými jádry 3. Areny s izolovanými benzenovými jádry

Příprava arenů q Frakční destilace černouhelného dehtu: 1. lehký olej ( t. v. 80 - 170 o. C ), 2. střední olej ( t. v. 170 - 240 o. C ), 3. těžký olej ( t. v. 240 - 270 o. C ), 4. anthracenový olej (t. v. 270 - 370 o. C ), 5. destilační zbytek.
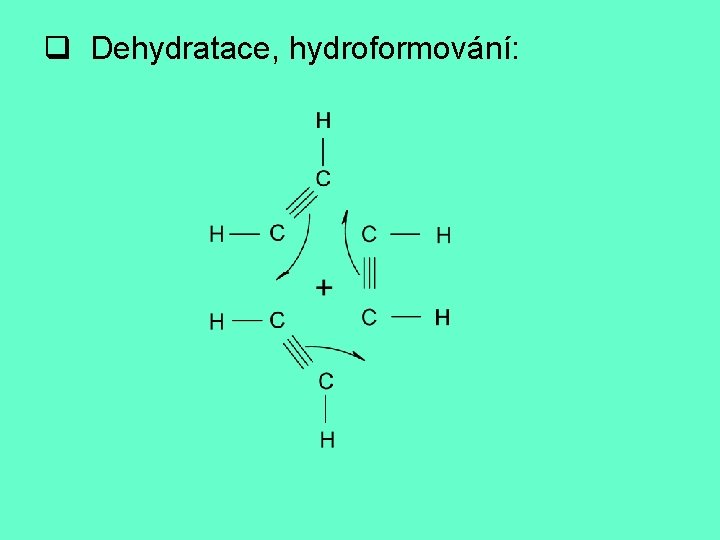
q Dehydratace, hydroformování:

Vlastnosti aromatických uhlovodíků, aromatický charakter q Areny = systémy s dokonalou konjugací dvojných vazeb. Jejich společné rysy: 1. Všechny atomy vázané v kruhu i atomy přímo na ně navázané leží v jediné společné rovině, protože atomy vázané v kruhu jsou v hybridním stavu sp 2.
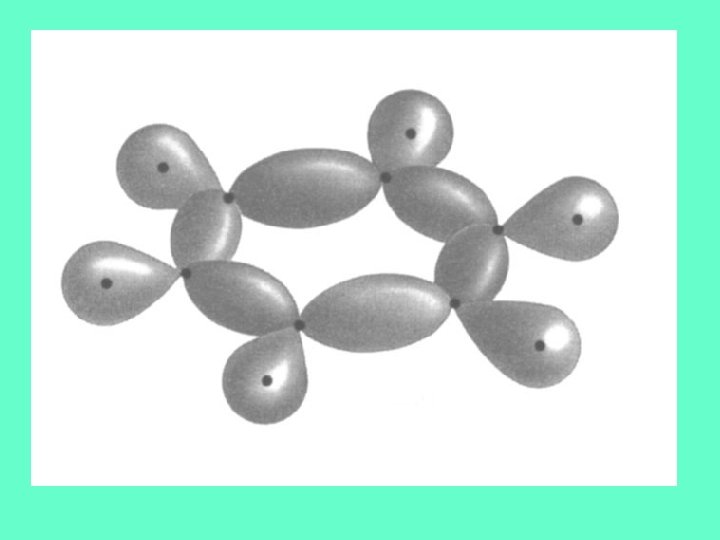
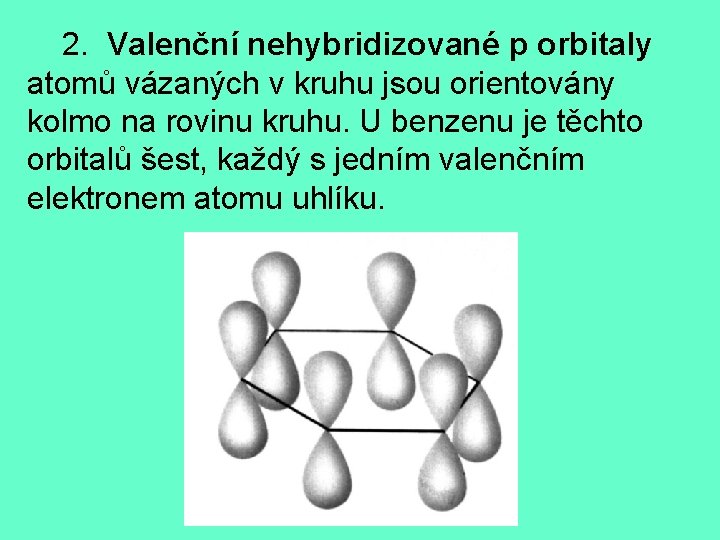
2. Valenční nehybridizované p orbitaly atomů vázaných v kruhu jsou orientovány kolmo na rovinu kruhu. U benzenu je těchto orbitalů šest, každý s jedním valenčním elektronem atomu uhlíku.

Překryvem těchto šesti orbitalů mohou vzniknout tři vazebné orbitaly se třemi vazebnými elektronovými páry, tzn. tři dvojné vazby v konjugovaném uspořádání. Šest vazebných elektronů není lokalizováno v místech tří dvojných vazeb, ale rovnoměrně rozprostřeno po celém kruhovém systému. Vytvořil se jediný molekulový orbital. Jeho polovina je nad, druhá polovina pod rovinou kruhu, v níž leží atomy uhlíku a vodíku.
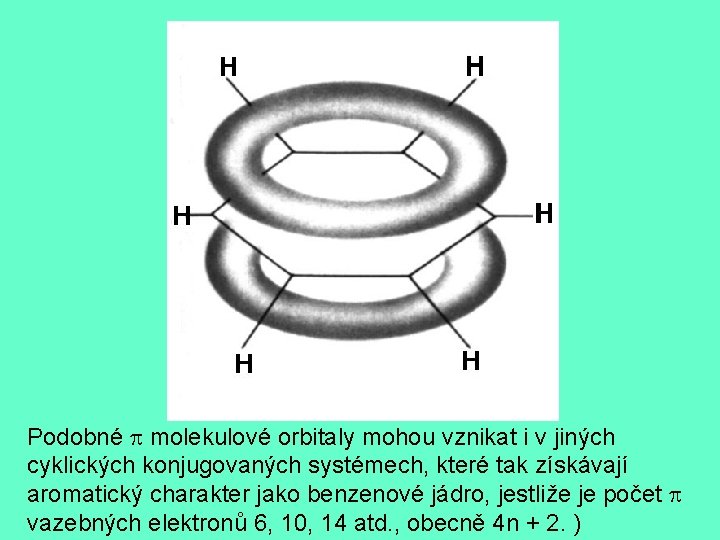
Podobné molekulové orbitaly mohou vznikat i v jiných cyklických konjugovaných systémech, které tak získávají aromatický charakter jako benzenové jádro, jestliže je počet vazebných elektronů 6, 10, 14 atd. , obecně 4 n + 2. )
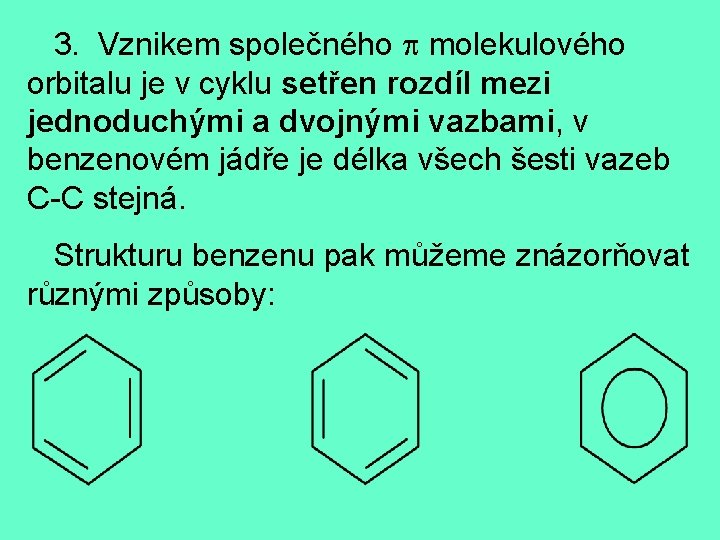
3. Vznikem společného molekulového orbitalu je v cyklu setřen rozdíl mezi jednoduchými a dvojnými vazbami, v benzenovém jádře je délka všech šesti vazeb C-C stejná. Strukturu benzenu pak můžeme znázorňovat různými způsoby:

Fyzikální vlastnosti arenů q Aromatické uhlovodíky s jedním kruhem jsou těkavé látky, nerozpustné ve vodě, dobře rozpustné v organických rozpouštědlech. q Mají charakteristický zápach, většinou jsou jedovaté, akutní účinky jsou centrálně nervové, narkotické. q Při chronických otravách dochází kromě poruch v psychické oblasti k poškozování kostní dřeně a k ubývání krvinek, jsou to krevní jedy. Řada aromatických uhlovodíků ( i benzen ) má rakovinotvorné účinky
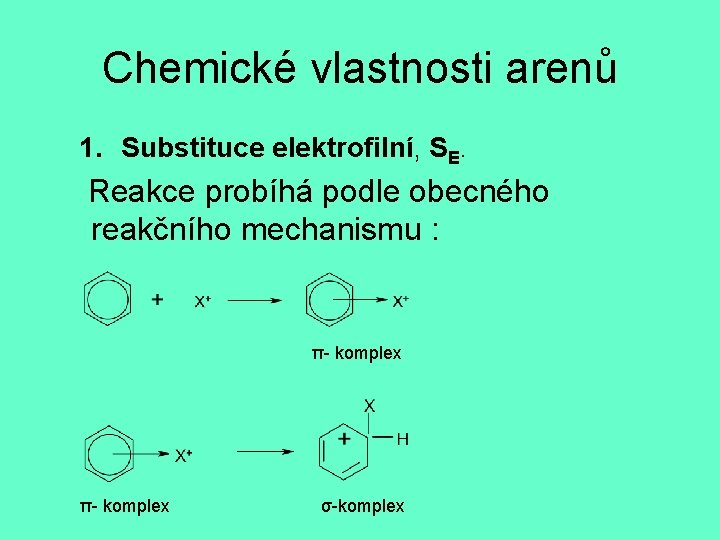
Chemické vlastnosti arenů 1. Substituce elektrofilní, SE. Reakce probíhá podle obecného reakčního mechanismu : π- komplex σ-komplex
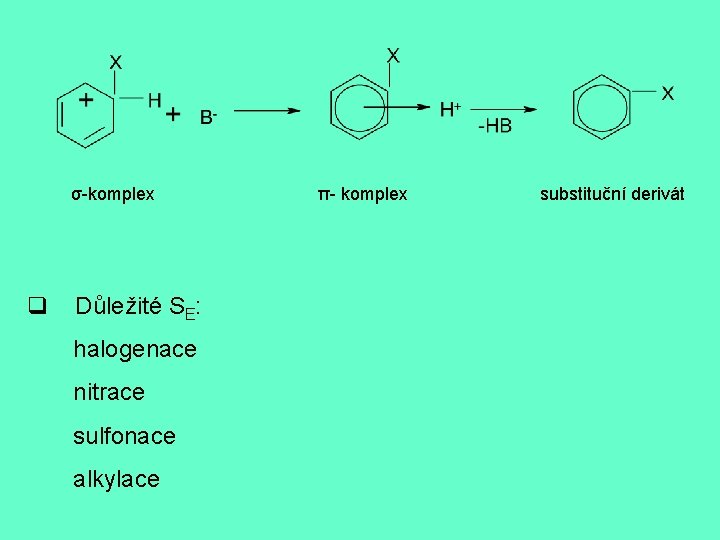
σ-komplex q Důležité SE: halogenace nitrace sulfonace alkylace π- komplex substituční derivát

Substituční pravidla q Přítomnost substituentu na benzenovém jádře má vliv na hustotu elektronů v jeho okolí, vyvolává polarizaci jádra. q Tím je výrazně ovlivněna pravděpodobnost, se kterými atomy uhlíku budou při elektrofilních substitucích reagovat elektrofilní činidla. q Podle toho dělíme substituenty do dvou tříd :
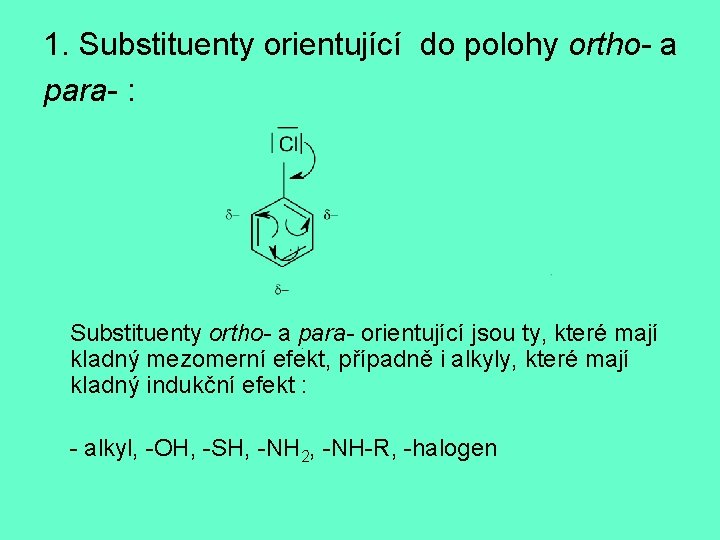
1. Substituenty orientující do polohy ortho- a para- : Substituenty ortho- a para- orientující jsou ty, které mají kladný mezomerní efekt, případně i alkyly, které mají kladný indukční efekt : - alkyl, -OH, -SH, -NH 2, -NH-R, -halogen
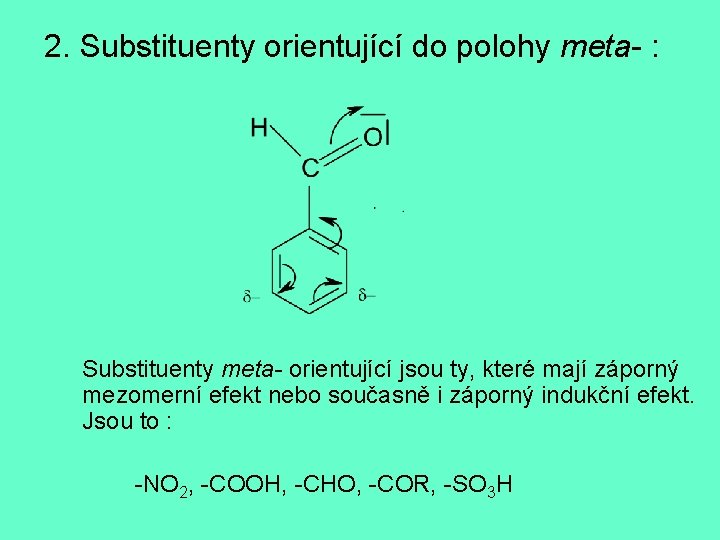
2. Substituenty orientující do polohy meta- : Substituenty meta- orientující jsou ty, které mají záporný mezomerní efekt nebo současně i záporný indukční efekt. Jsou to : -NO 2, -COOH, -CHO, -COR, -SO 3 H
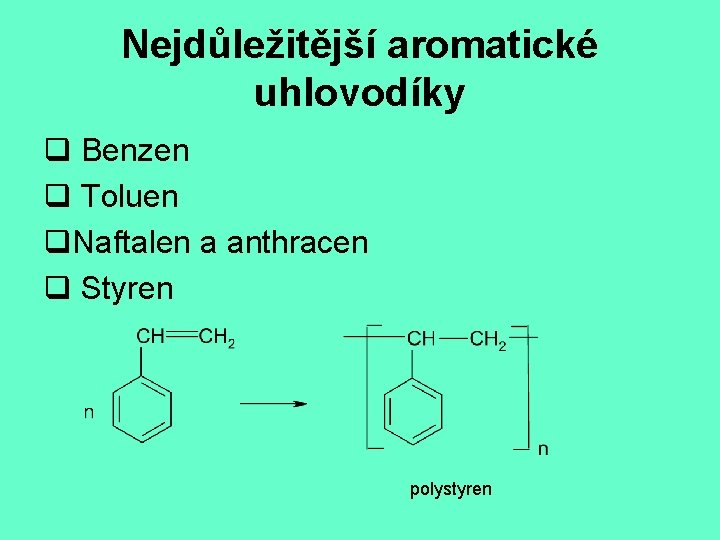
Nejdůležitější aromatické uhlovodíky q Benzen q Toluen q. Naftalen a anthracen q Styren polystyren

Zdroje uhlovodíků q Zdroje uhlovodíků jsou fosilní (ropa, uhlí, zemní plyn ) a recentní ( např. dřevo ). q Frakční destilace ropy ( ropné rafinerie ): 1. benzín ( t. v. 30 - 200 o. C ), 2. petrolej (t. v. 180 - 270 o. C ), 3. plynový olej ( t. v. 250 - 360 o. C ), 4. mazut - destilační zbytek.

Další zpracování produktů destilace – Krakování = přeměna dlouhých uhlovodíkových řetězců na řetězce kratší. Reformování = přeměna nerozvětvených uhlovodíků na rozvětvené a přeměna acyklických uhlovodíků na cyklické. Nejznámější produkty tohoto sekundárního zpracování jsou: 1. Topné oleje - lehký topný olej těžký topný olej 2. Pohonné hmoty - benzin motorová nafta 3. Maziva -mazací oleje a vazelíny 4. Asfalt 5. Plynné produkty - propan butan

Uhlí je hornina složité makromolekulární struktury, převažují prvky C, H, O, N, S. K základním druhům patří černé a hnědé uhlí. Vysokotepelná karbonizace je zahřívání uhlí bez přístupu vzduchu, při tom dochází k rozkladu uhlí za vzniku koksu, dehtu a koksárenského plynu. Dehet patří k nejvýznamnějším surovinovým zdrojům aromatických uhlovodíků a některých jejich derivátů.
- Slides: 69