UGLJENIK http chemnetschool blogspot rs20140901archive html http www
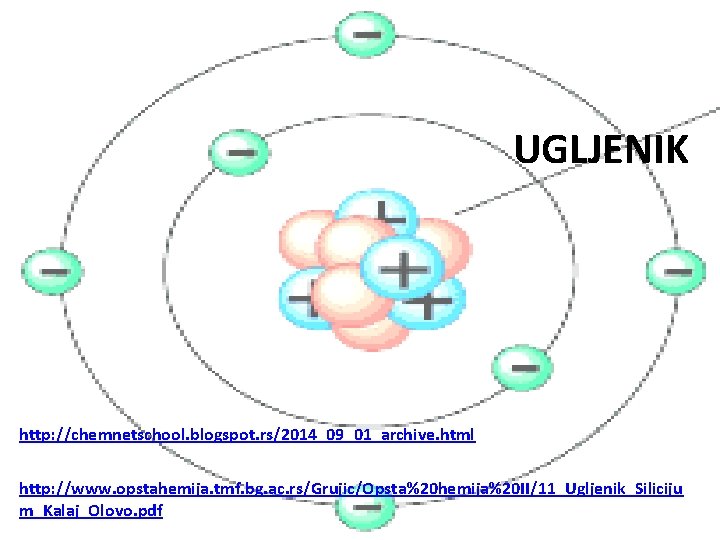
UGLJENIK http: //chemnetschool. blogspot. rs/2014_09_01_archive. html http: //www. opstahemija. tmf. bg. ac. rs/Grujic/Opsta%20 hemija%20 II/11_Ugljenik_Siliciju m_Kalaj_Olovo. pdf

OTKRIĆE UGLJENIKA Poznat još u antičko vreme, ne zna se pronalazač. Devi (Sir Humphry Davy) dokazao da je dijamant ugljenik. https: //prezi. com/0 dtqhyifkx-x/ugljenik/ Hamfri Dejvi (Sir Humphry Davy, 1778 -1829)
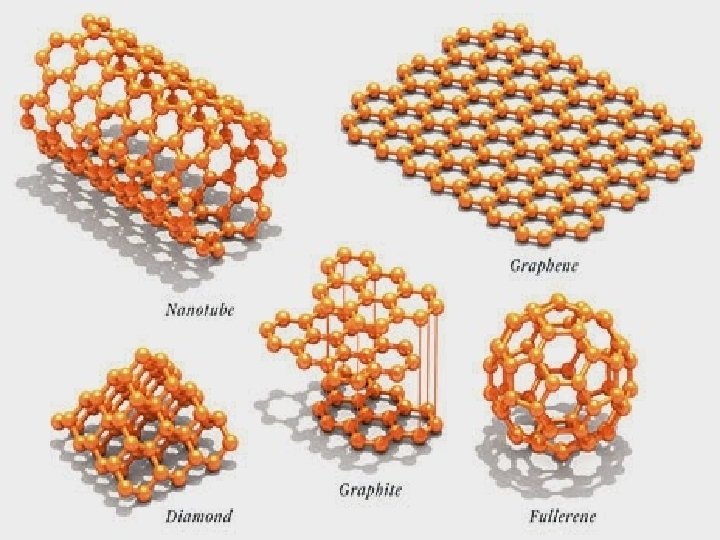
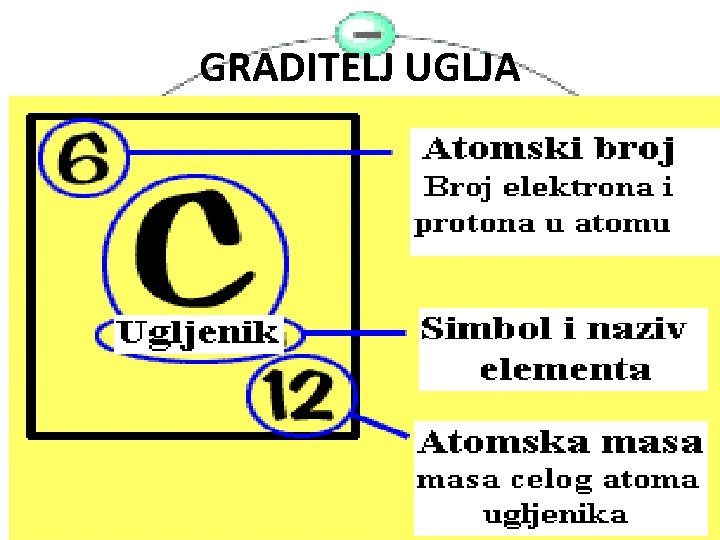
GRADITELJ UGLJA
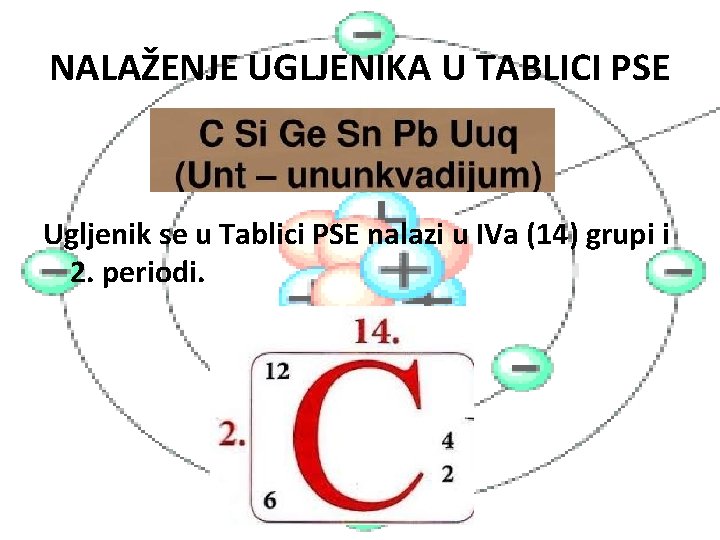
NALAŽENJE UGLJENIKA U TABLICI PSE Ugljenik se u Tablici PSE nalazi u IVa (14) grupi i 2. periodi.
NALAŽENJE UGLJENIKA U PRIRODI - SLOBODNO STANJE: A) Kristalni oblik - grafit, dijamant, fuleren (fudbalen) B) Amorfni oblik (bez oblika) - aktivni ugalj, koks, životinjski ugalj, drveni ugalj - JEDINJENJA : Mineral Oksidi Kiseline Soli - BIOGENI ELEMENT - organska jedinjenja - HEMIJA UGLJENIKOVIH JEDINJENJA ILI ORGANSKA HEMIJA

Ugalj Dijamant http: //www. astronomija. org. rs/nauka/fizika/10145 -q-ugljenik-izgurao-dijamante-na-drugomesto http: //www. nationalgeographic. rs/vesti/7568 -novo-otkrice-dijamant-vise-nije-najjaci-oblikugljenika. html
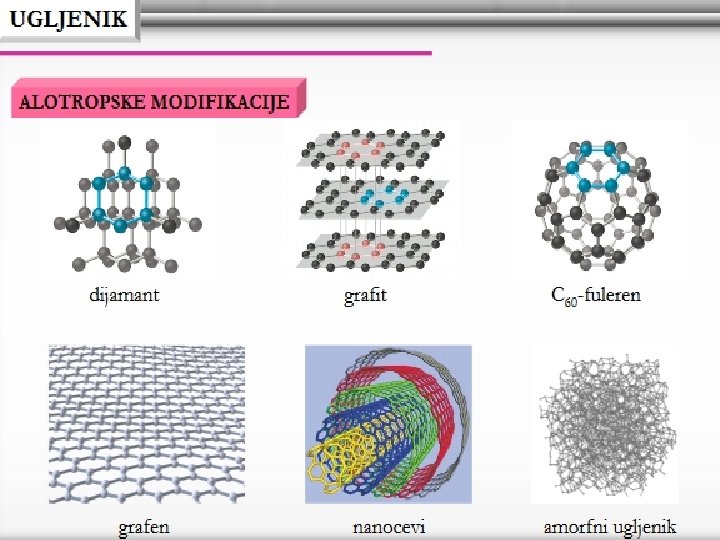

ZANIMLJIVOST Naučnici sa Univerziteta Severna Karolina otkrili su novi oblik čvrstog ugljenika, nazvanog "Qcarbon" koji ima vrlo neuobičajene karakteristike, a od njega se na sobnoj temperaturi mogu praviti dijamanti. Osim što je čvrst i izdržljiv, ovaj materijal obećava kada je u pitanju njegov odgovor na magnetske i svetlosne impulse. Zbog toga bi bio idealan u proizvodnji novih elektronskih displeja. http: //www. astronomija. org. rs/nauka/hemija/10431 -detektovan-ugljenik-u-ranomsvemiru
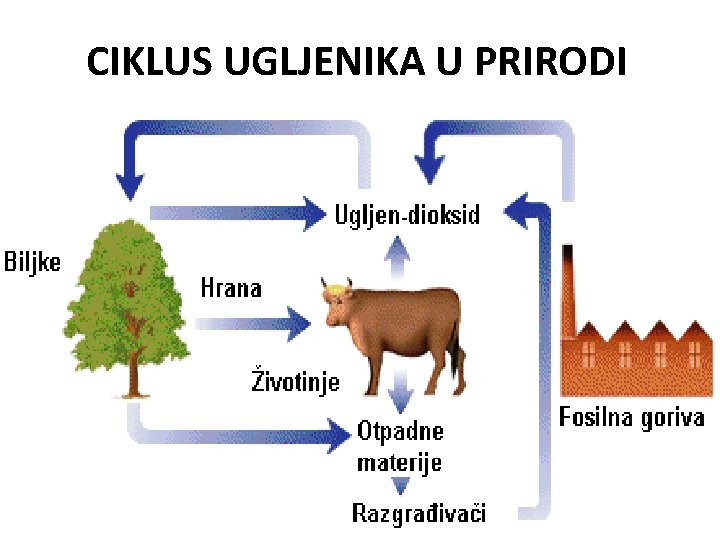
CIKLUS UGLJENIKA U PRIRODI
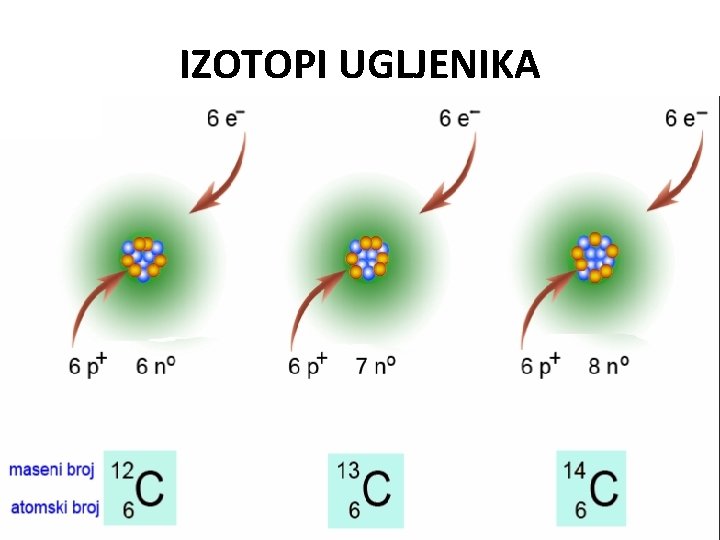
IZOTOPI UGLJENIKA
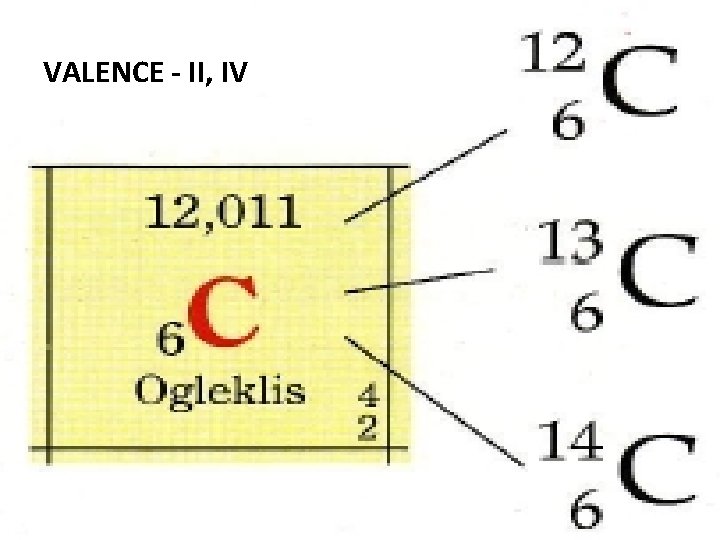
VALENCE - II, IV

DOBIJANJE UGLJENIKA

FIZIČKA SVOJSTVA UGLJENIKA

FIZIČKA SVOJSTVA GRAFITA

FIZIČKA SVOJSTVA DIJAMANTA
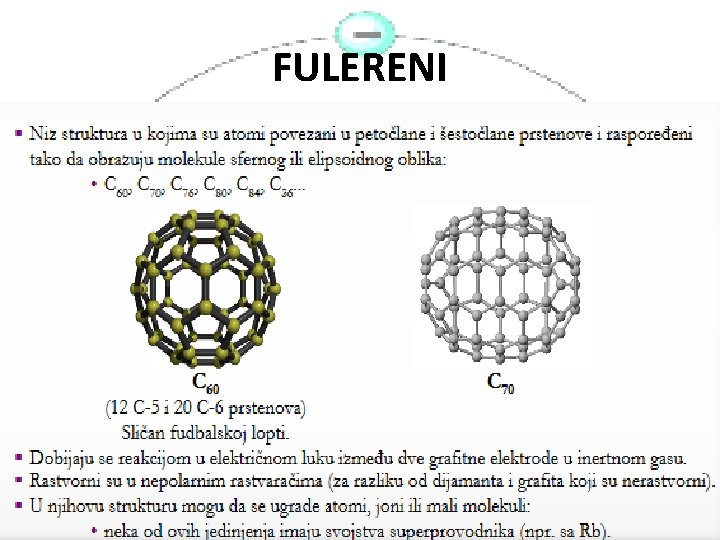
FULERENI


AMORFNI UGLJENICI

FIZIČKA SVOJSTVA JEDINJENJA CO – gas, bez boje ukusa, mirisa, OTROVAN, ZAGUŠLJIV, . CO 2 – gas, bez boje, ukusa, mirisa, u većim količinama izaziva glavobolje, TEŽI OD VAZDUHA.

HEMIJSKA SVOJSTVA UGLJENIKA Slabo reaktivan na sobnoj temperaturi. - Gori : C + O 2 → CO 2 (ugljenik (IV)-oksid ili ugljen-dioksid) 2 CO + O 2 → 2 CO 2 - Nepotpuno sagorevanje: 2 C + O 2 → 2 CO (ugljenik (II)-oksid ili ugljen-monoksid) - Ugljen-dioksid reaguje sa vodom i gradi ugljenu (karbonatnu) kiselinu: CO 2 + H 2 O → H 2 CO 3 - Građenje karbida - jedinjenja sa metalom


UPOTREBA UGLJENIK (II) OKSIDA

UPOTREBA UGLJENIK (IV) OKSIDA


http: //www. slideshare. net/vvli/organska-hemija-uvod-30083238 http: //www. slideshare. net/vvli/presentation 3 -41220703 http: //www. slideshare. net/vvli/alotropske-modifikacije-ugljenika-uenici-41220927

- Slides: 27