U N A M Facultad de Qumica Inorgnica


















![Arsénico (As) Propiedades Valores Z 33 Configuración electrónica [Ar]3 d 104 s 24 p Arsénico (As) Propiedades Valores Z 33 Configuración electrónica [Ar]3 d 104 s 24 p](https://slidetodoc.com/presentation_image/52d92decdd2a67c849092285b39f58f5/image-25.jpg)
















- Slides: 42

U. N. A. M. Facultad de Química Inorgánica. Familia 5 A o 15 Equipo: Darwanzio Alumnos: Caporal Flores Mariana Gonzáles Rodríguez Alejandra Pamela León Domínguez Abraham López Herrera Victor Manuel Pérez Moreno Sheila

NITRÓGENO N

Historia del nitrógeno Su descubrimiento se atribuye a Daniel Rutherford en 1772. Su nombre fue sugerido por Jean Antoine Claude Chaptal en 1970. El nombre de nitrógeno proviene del latín nitrum y éste del griego νίτρον, nitro; y -geno, de la raíz griega γεν generar, El nitrógeno gas fue identificado inicialmente como componente del aire que impedía la respiración o la combustión. Por eso se le dio el nombre de azote (sin vida) en francés.

Propiedades físicas y atómicas Número atómico: 7 Masa atómica: 14. 0067 uma Radio atómico: 56 pm Electronegatividad de Pauling: 3. 04 Configuración electrónica: 1 s 2 2 px 1 2 py 1 2 pz 1 con tres electrones desapareados Isótopos estables: 14 N abundancia 99. 634%, 15 N abundancia 0. 366%

Para el N 2 Punto de fusión: -210º C Punto de ebullición: -195. 8ºC Es incoloro, inodoro, es un gas diamagnético. La molécula es muy poco reactiva a causa del fuerte enlace triple entre los átomos de nitrógeno. El nitrógeno es el elemento más electronegativo de la familia. Así, además de los estados de oxidación típicos de la familia (-3, +3 y +5), el nitrógeno forma compuestos con otros estados de oxidación

Abundancia y distribución Comprende el 78. 1% del volumen de la atmósfera Es poco abundante en las rocas Está presente también en los restos de animales, por ejemplo el guano, usualmente en la forma de urea, ácido úrico y compuestos de ambos. El nitrógeno atmosférico es fijado por: la acción biológica, procesos industriales y por descargas atmosféricas que producen NOX

Obtención El único proceso importante para la producción de nitrógeno a gran escala es la licuefacción y la destilación fraccionada del aire. Otros métodos de obtención son la descomposición térmica del (NH 4)2 Cr 2 O 7, la reacción del NH 3 con bromo, o la reacción a altas temperaturas del NH 3 con Cu. O: (NH 4)2 Cr 2 O 7 N 2 + Cr 2 O 3 + 4 H 2 O 8 NH 3 + 3 Br 2 N 2 + 6 NH 4 Br(aq) 2 NH 3 + 3 Cu. O N 2 + 3 Cu. O + 3 H 2 O

Compuestos La molécula de N 2(g) se vuelve más reactiva a temperaturas elevadas o en presencia de catalizadores. El único elemento químico que reacciona con N 2(g) a temperatura ambiente es el litio, formándose el nitruro de litio: N 2(g) + 6 Li(s) → 2 Li 3 N(s) Con el hidrógeno forma el amoníaco (NH 3) y la hidracina (N 2 H 4). Con el oxígeno forma varios óxidos como el nitroso (N 2 O) o gas de la risa, el óxido nítrico (NO) y el dióxido de nitrógeno (NO 2), estos dos últimos se conocen conjuntamente como NOx y son producto de procesos de combustión contribuyendo a la aparición de episodios contaminantes de smog fotoquímico. Otros óxidos son el trióxido de dinitrógeno (N 2 O 3) y el pentóxido de dinitrógeno (N 2 O 5), ambos muy inestables y explosivos y cuyos ácidos respectivos son el ácido nitroso (HNO 2) y el ácido nítrico (HNO 3) que forman, a su vez, nitritos y nitratos.

El nitrógeno forma compuestos binarios con casi todos los elementos de la tabla periódica. Los métodos de preparación son la reacción directa con N 2 o NH 3 y la descomposición térmica de la amidas metálicas: 3 Ca + N 2 Ca 3 N 2 3 Mg + 2 NH 3 Mg 3 N 2 + 3 H 2 3 Zn (NH 2)2 Zn 3 N 2 + 4 NH 3

Usos En su forma combinada es esencial para todas las formas de vida ya que constituye el 15% del peso de las proteínas. Se emplea para la producción de fertilizantes y otros productos químicos. Los métodos de fijación de nitrógeno atmosférico (procedimiento de Birbeland-Eyde) y los estudiados para el amoníaco (Haber), complementados en la síntesis de Osdwald, tienen enorme importancia industrial y en particular para la agricultura pues las reservas naturales de abonos naturales como el salitre son insuficientes para satisfacer las necesidades de los cultivos, por lo que el aprovechamiento del nitrógeno atmosférico resolvió un problema de capital interés al suministrar nitratos minerales en grandes cantidades y a bajo costo. Los explosivos modernos que han reemplazado a la antigua pólvora negra, son derivados nitratos obtenidos por la acción del ácido nítrico sobre alguna sustancia orgánica: con el algodón forma Algodón Pólvora o nitrocelulosa y se usa para el colodión y celuloide. Con el Tolueno da lugar a la formación del TRINITROTOLUENO (T. N. T. )

El N 2 se utiliza fundamentalmente para los siguientes fines: Para proporcionar atmósferas inertes, exentas de otros gases más reactivos. Protección de componentes electrónicos durante su fabricación o almacenamiento. Se añade a las botellas de vino cuando se les quita el tapón para prevenir la oxidación del vino. También se utiliza en la fabricación de acero, en el purgado de hidrocarburos inflamables en refinerías y oleoductos, etc. Fabricación de amoníaco y otros compuestos nitrogenados. El nitrógeno líquido se utiliza como líquido criogénico para conservar especímenes biológicos. También se utiliza como refrigerante ideal para experiencias que necesiten muy bajas temperaturas: ensayos de superconductividad eléctrica de materiales.


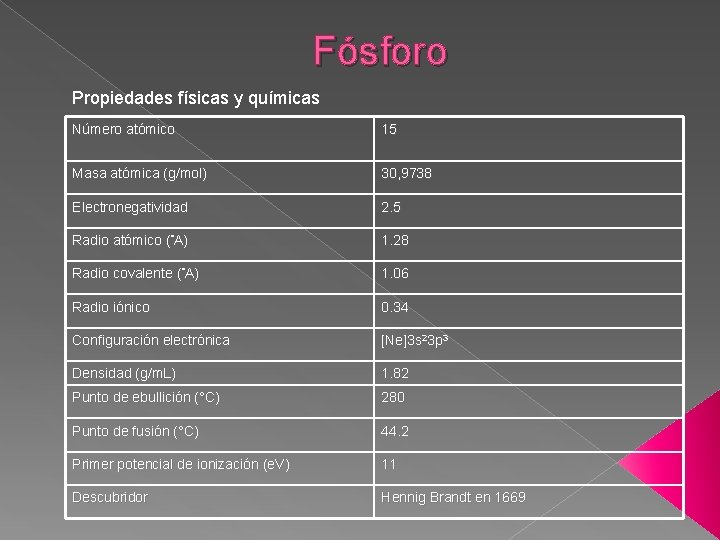
Fósforo Propiedades físicas y químicas Número atómico 15 Masa atómica (g/mol) 30, 9738 Electronegatividad 2. 5 Radio atómico (°A) 1. 28 Radio covalente (°A) 1. 06 Radio iónico 0. 34 Configuración electrónica [Ne]3 s 23 p 3 Densidad (g/m. L) 1. 82 Punto de ebullición (°C) 280 Punto de fusión (°C) 44. 2 Primer potencial de ionización (e. V) 11 Descubridor Hennig Brandt en 1669

Formas alotrópicas - Fósforo blanco Contiene moléculas tetraédricas P 4 Reactivo Se inflama al contacto con el aire Tóxico Blando Soluble en disolvente no polares y poco polares

Fósforo rojo Red sólida - Amorfo - Obtención: P 4 (blanco) P rojo - Fósforo negro Estructura cristalina regular - Más estable - Más denso -

Hidruros de fósforo PH 3 gas incoloro, venenoso P 4(s) + 3 Na. OH (ac) + 3 H 2 O(l) → 3 Na. H 2 PO 3(ac) + PH 3(g) 2 Na 3 P(s) + 6 H 2 O (l)→ 2 PH 3(g) + 6 Na+(ac) + 6 OH-(ac)

Fosfuros n n n Sustancias iónicas Contienen al anión P 3 - (Na 3 P y Ca 3 P 2) Las sales de fosfuro reaccionan vigorosamente con agua. 2 Na 3 P(s) + 6 H 2 O(l)→ 2 PH 3(g) + 6 Na+(ac) + 6 OH-(ac) Fosfuro de aluminio

Óxidos y oxiácidos de fósforo Reacciona con oxígeno formando óxidos con estado de oxidación 3+ y 5+. El P 4 O 6 y P 4 O 10 P 4(s) + 3 O 2→ P 4 O 6(s) P 4(s) +5 O 2→ P 4 O 10(s) § Estados intermedios P 4 O 7, P 4 O 8 y P 4 O 9

P 4 O 10(s) +6 H 2 O → 4 H 3 PO 4(ac) § El H 3 PO 4 experimenta reacciones de condensación formando H 4 P 2 O 7 y H 5 P 3 O 10

Haluros de fósforo Forma los haluros PX 3 Y PX 5 Excepción PI 5 Reaccionan con agua PX 3 + H 2 O H 3 PO 3 (ac) + 3 HX (ac) PX 5 + 4 H 2 O H 3 PO 4 (ac) + 5 HX (ac)

Obtención El fósforo se encuentra en la naturaleza como Ca 3(PO 4)2 y fluoroapatita, Ca 5(PO 4)3 F 2 Ca 3(PO 4)2 (s)+10 C(s)+ 6 Si. O 2 (s) 1500 ºC P 4 (g)+ 10 CO(g)+ 6 Ca. Si. O 3 (l)

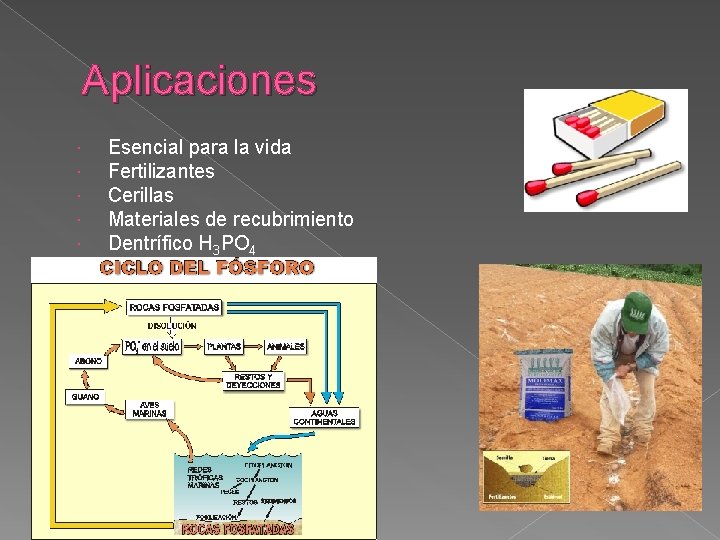
Aplicaciones Esencial para la vida Fertilizantes Cerillas Materiales de recubrimiento Dentrífico H 3 PO 4

Levadura artificial Aditivo de bebidas Fosfatos amónicos como polvo para pagar incendios Bombas de fósforo Recubrimiento interno de lámpara fluorescentes Productos cerámicos Pintura Medicamentos

![Arsénico As Propiedades Valores Z 33 Configuración electrónica Ar3 d 104 s 24 p Arsénico (As) Propiedades Valores Z 33 Configuración electrónica [Ar]3 d 104 s 24 p](https://slidetodoc.com/presentation_image/52d92decdd2a67c849092285b39f58f5/image-25.jpg)
Arsénico (As) Propiedades Valores Z 33 Configuración electrónica [Ar]3 d 104 s 24 p 3 Peso atómico 74. 9216 Volumen atómico 13. 0 Densidad g/m. L 5. 78 Punto de fusión °C 816. 8 Punto de ebullición °C 616 1ª. Energía de Ionización (k. J/mol) 947 Radio covalente A° 1. 19 Radio iónico X 3 - A° 2. 22 Radio iónico X 5+ A° 0. 47 Electronegatividad (Pauling) 2. 18 Abundancia % 5 E-04

Características principales Es el 52º elemento en abundancia de la corteza terrestre con 2 ppm (5· 10 -4 %) . Se encuentra en forma nativa y, principalmente, en forma de sulfuro en una gran variedad de minerales que contienen cobre, plomo, hierro, níquel, cobalto y otros metales. El arsénico presenta tres estados alotrópicos, gris o metálico, amarillo y negro. El arsénico gris(α) es la forma estable en condiciones normales y tiene estructura romboédrica.

Características principales El arsénico amarillo (γ). Presenta fosforescencia a temperatura ambiente. Una tercera forma alotrópica, el arsénico negro (β), tiene propiedades intermedias entre las formas alotrópicas descritas. Se clasifica como METALOIDE. Es un elemento químico esencial para la vida aunque tanto el arsénico como sus compuestos son extremadamente venenosos.

Reacciones con Arsénico AS 2 O 3 + 3 C 2 As + 3 CO AS 4(s) + 5 O 2 (g) 2 As 2 O 5 (s) 4 As(s)+6 CH 3 I(l) 3(CH 3)2 As. I(sol)+As. I 3(sol) As 2 S 3 + H 2 O 2 + OH- As. O 43 - + SO 42 - + H 2 O 2 As+3 RBr As. RBr 2+As. R 2 Br As 2 O 3 + 6 HCl 2 As. Cl 3 + 3 H 2 O 2 As. Cl 3 + 3 H 2 S As 2 S 3 + 6 HCl

Aplicaciones Preservante de la madera (arseniato de cobre y cromo). Aditivo en aleaciones de plomo y latones. Componente del tabaco. Insecticida (arseniato de plomo), herbicidas (arsenito de sodio) y venenos. Decolorante en la fabricación del vidrio (trióxido de arsénico). Algunos compuestos se usan en pirotecnia para la preparación de bengalas. En odontología se usa para destruir la pulpa dentaria.


Antimonio (Sb, del latín stibium) Elemento químico de la serie de metaloides (periodo 5, bloque “p”). En su forma elemental es un sólido cristalino (estructura romboédrica), quebradizo, blanco plateado. Este elemento se parece a los metales en su aspecto y propiedades físicas, pero se comporta quimicamente como un no metal.

Abundancia y obtención El antimonio se encuentra en la naturaleza en numerosos minerales, aunque es un elemento poco abundante. El principal compuesto de antimonio es la antimonita (también llamada estibina), Sb 2 S 3. Mediante la combustión del sulfuro de antimonio se obtiene óxido de antimonio (III), Sb 2 O 3, que se puede reducir con carbono para la obtención de antimonio. 2 Sb 2 O 3 + 3 C → 4 Sb + 3 CO 2 También se puede obtener por reducción directa del sulfuro, por ejemplo con hierro: Sb 2 S 3 + 3 Fe → 2 Sb + 3 Fe. S

Principales aplicaciones El antimonio puro se rompe muy facilmente para ser utilizado por sí sólo Generalmentes se mezcla con plomo, zinc o estaño para formar aleaciones Se utilizan en baterias de almacenamiento (acumuladores) a base de plomo Soldaduras Metal para hacer láminas y tuberias Municiones Peltres (aleación antimonio y estaño) Etc.

Óxidos de antimonio El trióxido de antimonio es el óxido más importante por su utilización (Sb 2 O 3 ). Posee propiedades que retardan la combustión para el caso de materiales plásticos y telas. Se utiliza como catalizador en la producción de fibras plásticas (PET). Elaboración de algunos tintes y pigmentos. Etc.


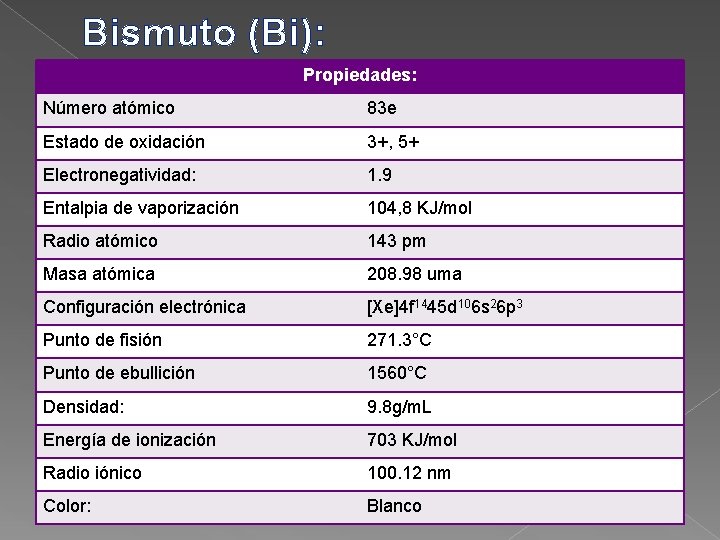
Bismuto (Bi): Propiedades: Número atómico 83 e Estado de oxidación 3+, 5+ Electronegatividad: 1. 9 Entalpia de vaporización 104, 8 KJ/mol Radio atómico 143 pm Masa atómica 208. 98 uma Configuración electrónica [Xe]4 f 1445 d 106 s 26 p 3 Punto de fisión 271. 3°C Punto de ebullición 1560°C Densidad: 9. 8 g/m. L Energía de ionización 703 KJ/mol Radio iónico 100. 12 nm Color: Blanco

Características principales: Es un elemento metálico, en si el mas metálico en este grupo. Metal cristalino blanquizco duro y quebradizo. Se estima que la corteza terrestre contiene cerca de 0. 00002% de bismuto. Existe en la naturaleza como metal libre y en minerales. Los principales depósitos están en Sudamérica, pero en Estados Unidos se obtiene principalmente como subproducto del refinado de los minerales de cobre y plomo. El bismuto metálico no se considera tóxico y presenta una amenaza mínima para el medio ambiente. Lo único que se sabe de este elemento es que se conoce desde la antigüedad, no se sabe ni quien lo descubrió.

Los principales minerales en los que se encuentra el Bismuto son: Bismutita (Bi 2 O 3) Bismutina (Bi 2 S 3)

Sus aplicaciones: En la metalurgia para obtener aleaciones debajo punto de fusión. Como semiconductor en Farmacia y cosmética. En la industria farmacéutica el Bi está presente en astringentes, antisépticos y remedios para males intestinales; el oxicloruro de bismuto (Bi. OCl) es de uso muy común en cosméticos. Debido a lo anteriormente mencionado, el bismuto ha tenido una creciente importancia comercial.

Reacciones de este: El oxido común es básico, se disuelve en ácidos para producir bases de Bismuto (III). Estas sales se hidrolizan para precipitar la sal básica de bismuto. Se emplea para oxidar el Mn 2+ a ion permanganato ( ) en análisis cualitativo.

Bibliografía www. textoscientificos. com/. . . /fosforo-blanco. jpg www. lenntech. es/periodica/elementos/p. htm www. uclm. es/profesorado/afantinolo/Docencia/. . . /Trans_T 8 IQ. pdf www. uva. es/consultas/guia. php? . . . Chang, R. Química , 6 ta. Edición editorial Mc- Graw Hill, México 2000 Witten, Kennet et al. Química General 3 er, edición de la editorial Mc- Graw Hill México 2001

GRACIAS