Two Theories of Bonding MOLECULAR ORBITAL THEORY Robert

Two Theories of Bonding MOLECULAR ORBITAL THEORY — Robert Mullikan (1896 -1986) THUYẾT MO Phương pháp orbital phân tử (MO)

Tính thuận từ cuả O 2

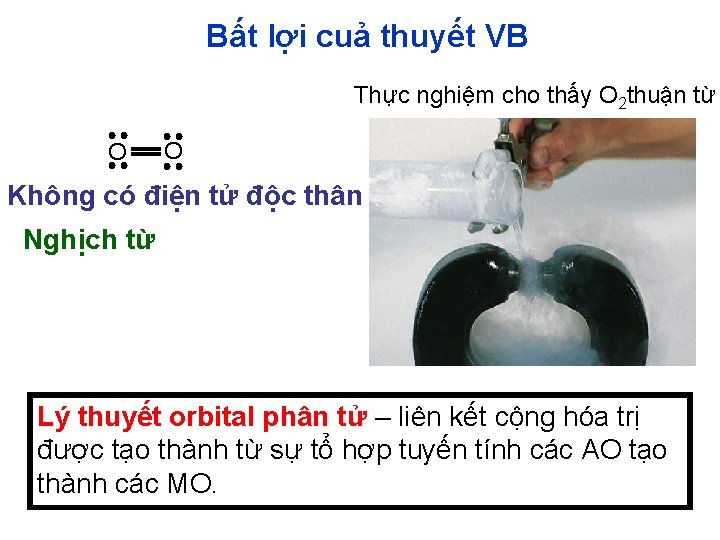
Bất lợi cuả thuyết VB Thực nghiệm cho thấy O 2 thuận từ O O Không có điện tử độc thân Nghịch từ Lý thuyết orbital phân tử – liên kết cộng hóa trị được tạo thành từ sự tổ hợp tuyến tính các AO tạo thành các MO.

LIÊN KẾT CỘNG HÓA TRỊ THEO PHƯƠNG PHÁP MO a. Bài toán ion H 2+ b. Quan niệm của phương pháp MO c. Các luận điểm cơ sở của phương pháp MO c. Áp dụng phương pháp MO cho các phân tử bậc hai
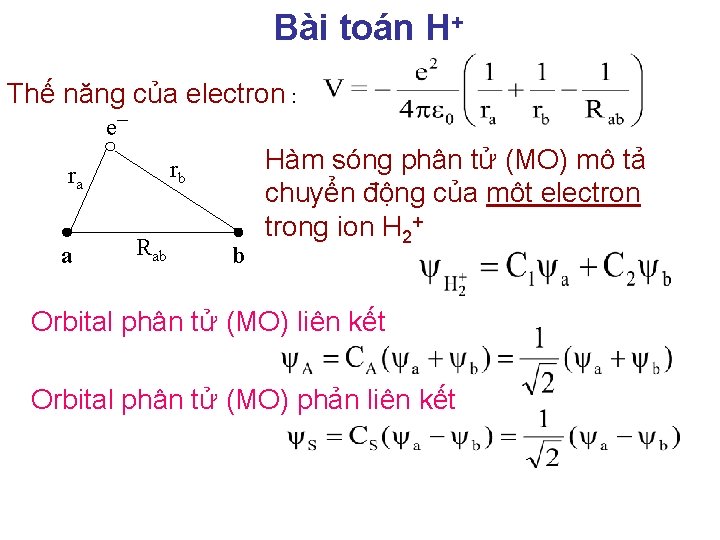
Bài toán H+ Thế năng của electron : e─ rb ra a Rab b Hàm sóng phân tử (MO) mô tả chuyển động của một electrong ion H 2+ Orbital phân tử (MO) liên kết Orbital phân tử (MO) phản liên kết
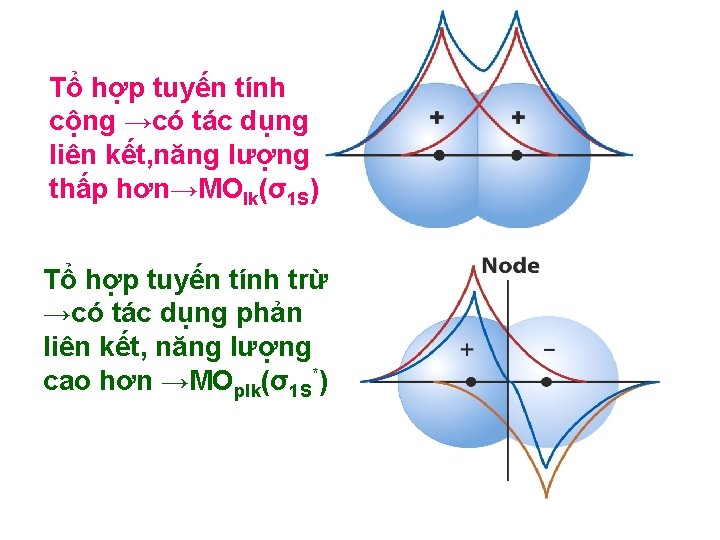
Tổ hợp tuyến tính cộng →có tác dụng liên kết, năng lượng thấp hơn→MOlk(σ1 S) Tổ hợp tuyến tính trừ →có tác dụng phản liên kết, năng lượng cao hơn →MOplk(σ1 S*)

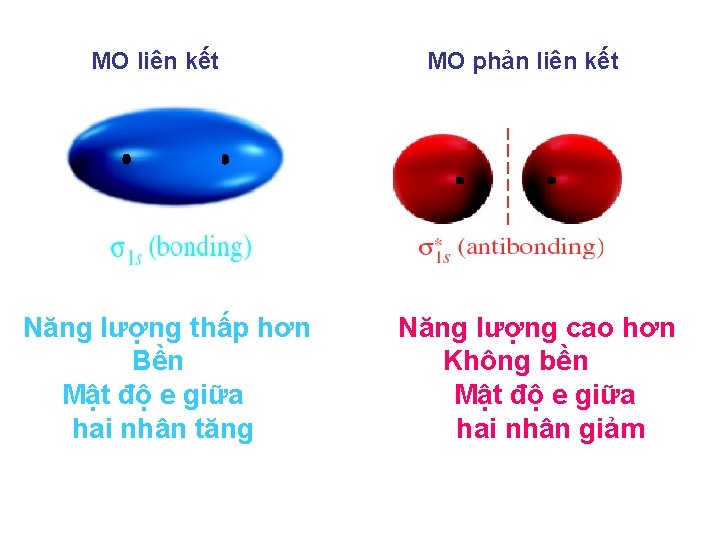
MO liên kết Năng lượng thấp hơn Bền Mật độ e giữa hai nhân tăng MO phản liên kết Năng lượng cao hơn Không bền Mật độ e giữa hai nhân giảm
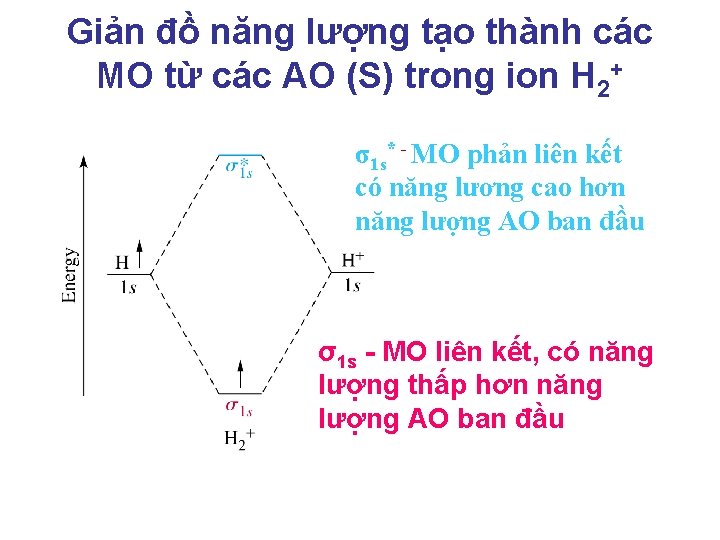
Giản đồ năng lượng tạo thành các MO từ các AO (S) trong ion H 2+ σ1 s* - MO phản liên kết có năng lương cao hơn năng lượng AO ban đầu σ1 s - MO liên kết, có năng lượng thấp hơn năng lượng AO ban đầu

Quan niệm của phương pháp MO • Phân tử là một nguyên tử phức tạp đa nhân. • Mô tả sự chuyển động của từng electron riêng biệt bằng hàm orbital phân tử (MO)

Các luận điểm cơ sở của phương pháp MO Ø Phân tử - tổ hợp thống nhất gồm các hạt nhân và các electron của các nguyên tử tương tác. ØTrạng thái của e được mô tả bằng các MO. Mỗi MO được xác định gần đúng bằng phương pháp tổ hợp tuyến tính các orbital nguyên tử MO = Ci AO ØSố MO tạo thành bằng số AO tham gia tổ hợp tuyến tính

Điều kiện các AO tham gia tổ hợp tuyến tính – Năng lượng gần nhau. – Mức độ che phủ đáng kể. – Cùng tính đối xứng đối với trục liên nhân.

Sự che phủ các AO dọc theo trục liên nhân → MO nhận trục liên nhân làm trục đối xứng Sự che phủ các AO về hai phía trục liên nhân →MO MO có mặt phẳng phản xứng chứa trục liên nhân Năng lượng các MO phụ thuộc vào năng lượng AO và mức độ che phủ giữa các AO đó.

Sự tạo thành các MO từ sự tổ hợp tuyến tính các AO của phân tử bậc hai AO + AO → MO liên kết ( , …), EMO < EAO AO - AO → MO phản liên kết ( * , * …), E MO* > EAO AO → MO không liên kết ( 0, 0 …), EMOo = EAO
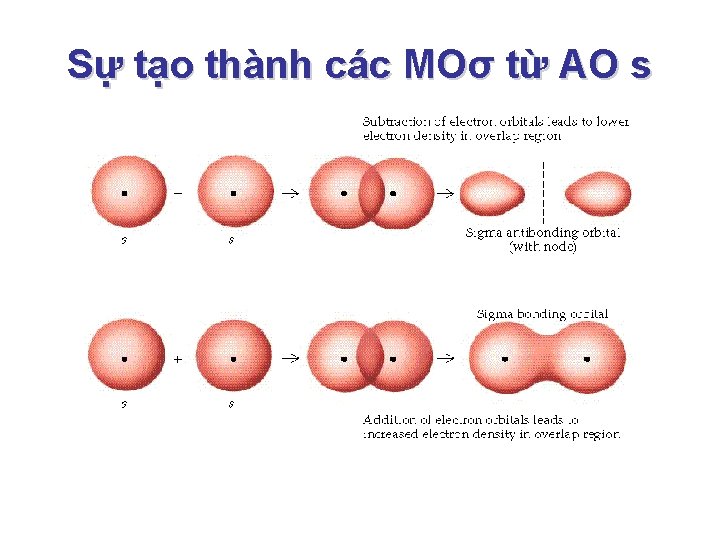
Sự tạo thành các MOσ từ AO s
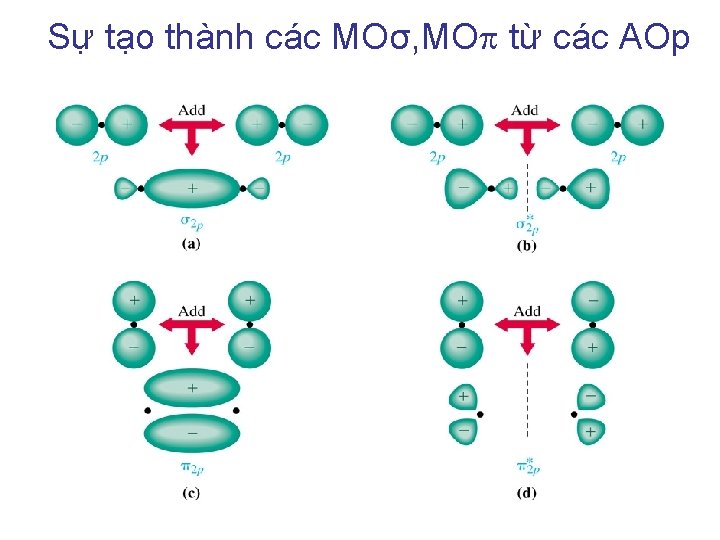
Sự tạo thành các MOσ, MO từ các AOp

Mỗi MO chỉ chứa tối đa 2 e có spin đối song Các e sắp xếp vào các MO tuân theo nl vững bền, nl ngoại trừ Pauli, quy tắc Hund. Trạng thái cuả các e trên các MO được đặc trưng bằng các số lượng tử phân tử | | và tương ứng giống như số lương tử và m trong nguyên tử.


Trong nguyên tử = 0 m = 0 → s 2 Trong phân tử thẳng A 2 (trục z là trục liên nhân) | |=0 → σ s 2 = 1 m = 0, 1 → p 6 | | = 0 , 1 → =0 , 1 → σpx 2 ( py)2 ( pz) 2

Các đặc trưng liên kết –Lk được quyết định bởi các e lk mà không bị triệt tiêu. –Một bậc lk ứng với một cặp e lk không bị triệt tiêu –Cho lk 2 tâm: Bậc lk –Tên của lk được gọi bằng tên của cặp e lk không bị triệt tiêu –Bậc lk tăng thì năng lượng lk tăng còn độ dài lk giảm

• Thuyết MO coi sự hình thành liên kết hóa học là sự chuyển điện tử (hóa trị) từ các AO cuả các nguyên tử tương tác về các orbital phân tử thuộc chung toàn bộ phân tử.

Việc mô tả cấu trúc phân tử gồm các bước üBước 1: Xét sự tạo thành MO từ các AO üBước 2: Sắp xếp các MO theo thứ tự năng lượng tăng dần üBước 3: Xếp các electron vào các MO üBước 4: Xét các đặc trưng liên kết

Các phân tử bậc hai thuộc chu kỳ 1 1 S → σ1 s , σ1 s E : σ1 s < σ1 s* *
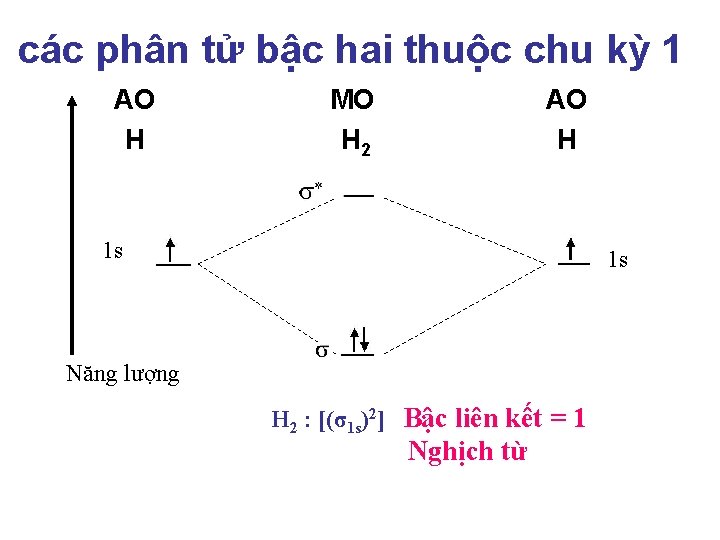
các phân tử bậc hai thuộc chu kỳ 1 AO H MO H 2 AO H 1 s 1 s Năng lượng H 2 : [(σ1 s)2] Bậc liên kết = 1 Nghịch từ
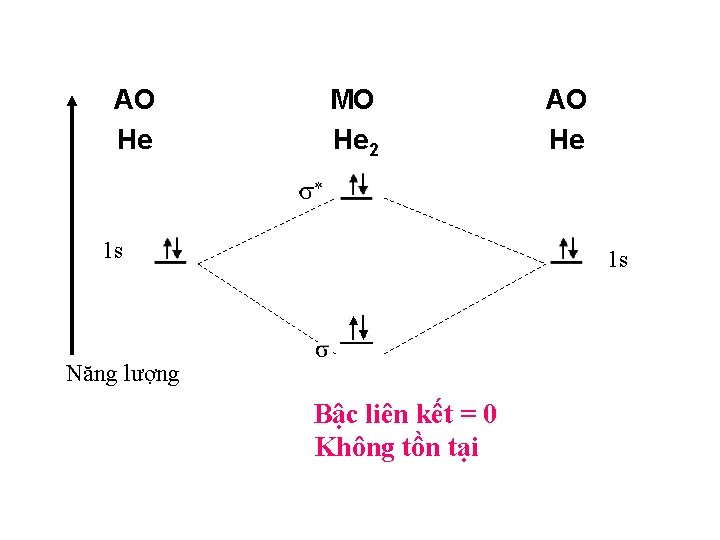
AO He MO He 2 1 s AO He 1 s Năng lượng Bậc liên kết = 0 Không tồn tại
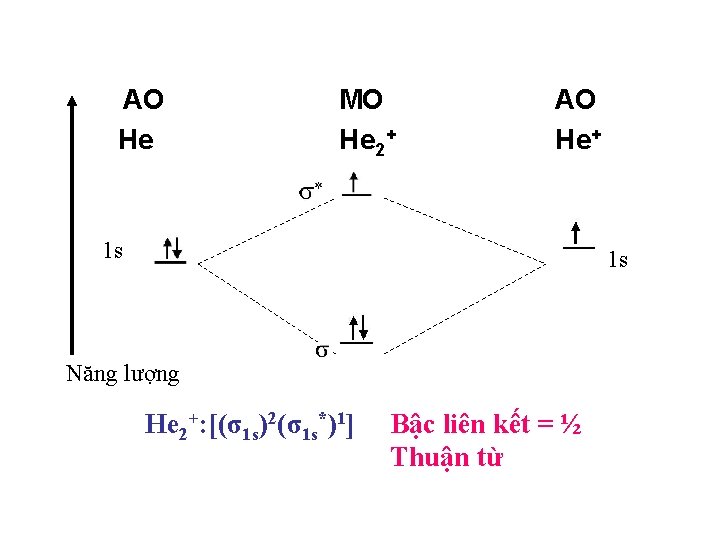
AO He MO He 2+ AO He+ 1 s 1 s Năng lượng He 2+: [(σ1 s)2(σ1 s*)1] Bậc liên kết = ½ Thuận từ

Áp dụng phương pháp MO cho các phân tử bậc hai chu kỳ hai • Các phân tử hai nguyên tử của các nguyên tố cuối chu kỳ II • Các phân tử hai nguyên tử cùng loại của những nguyên tố đầu chu kỳ II • Các phân tử hai nguyên tử khác loại của những nguyên tố chu kỳ II

Các phân tử bậc hai thuộc chu kỳ 2 (trục x là trục liên nhân ) 1 S 2 S 2 S 2 px 2 py 2 pz → σ1 s , σ1 s* → σ2 s , σ2 s* → σ2 px , σ2 px* → 2 py , 2 py* → 2 pz , 2 pz* E : σ1 s< σ1 s*<σ2 s*<σ2 px< 2 py = 2 pz< 2 py* = 2 pz* < σ2 px*
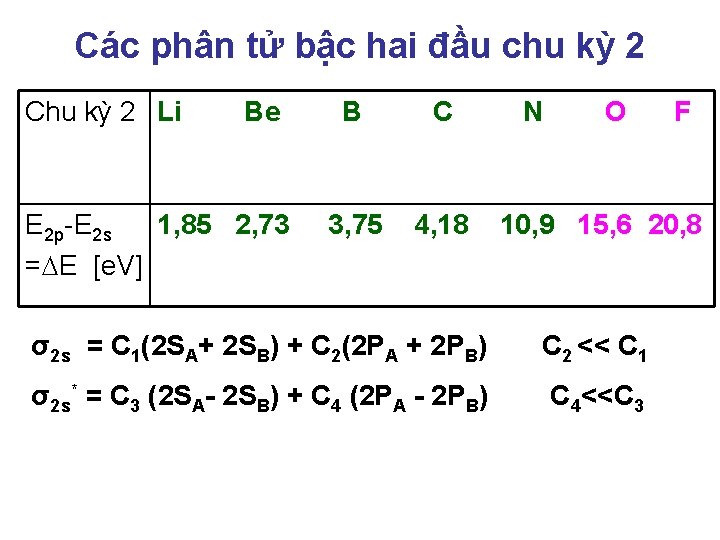
Các phân tử bậc hai đầu chu kỳ 2 Chu kỳ 2 Li Be E 2 p-E 2 s 1, 85 2, 73 = E [e. V] B C 3, 75 4, 18 N O F 10, 9 15, 6 20, 8 σ2 s = C 1(2 SA+ 2 SB) + C 2(2 PA + 2 PB) C 2 << C 1 σ2 s* = C 3 (2 SA- 2 SB) + C 4 (2 PA - 2 PB) C 4<<C 3

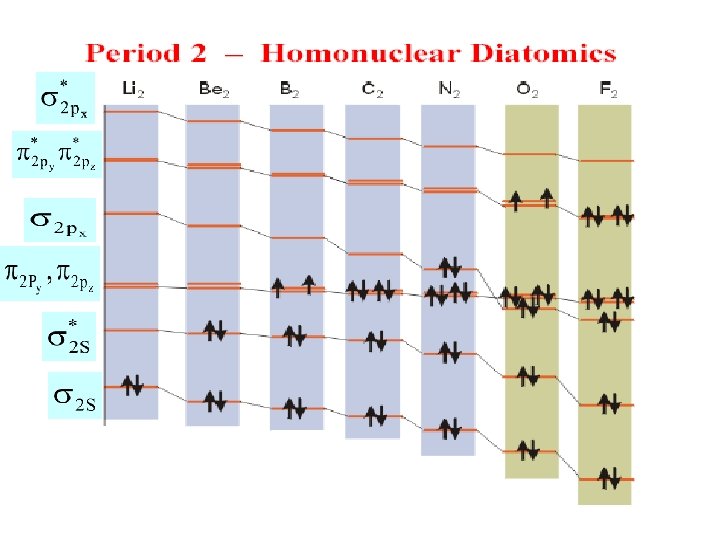
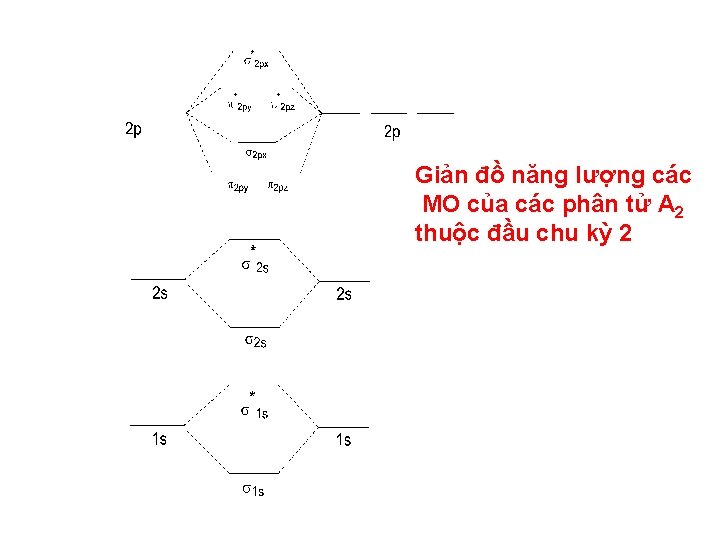
Giản đồ năng lượng các MO của các phân tử A 2 thuộc đầu chu kỳ 2
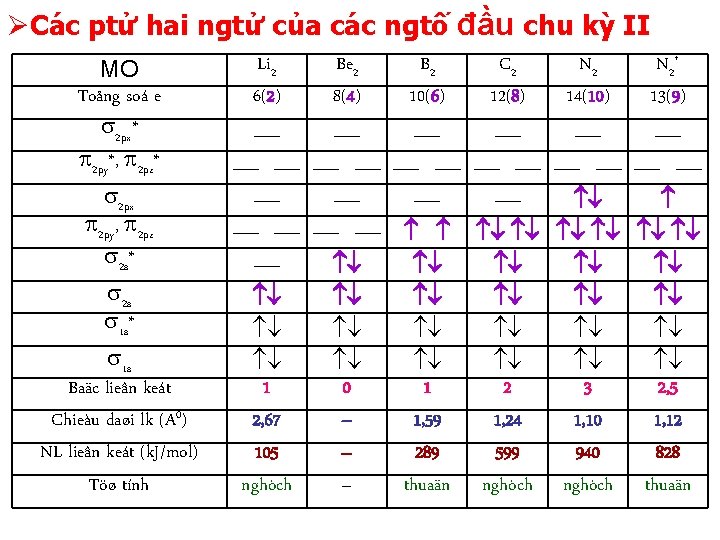
ØCác ptử hai ngtử của các ngtố đầu chu kỳ II MO Toång soá e 2 px* 2 py*, 2 pz* 2 px 2 py, 2 pz 2 s* 2 s 1 s* 1 s Baäc lieân keát Chieàu daøi lk (A 0) NL lieân keát (k. J/mol) Töø tính Li 2 6(2) Be 2 8(4) B 2 10(6) C 2 12(8) N 2 14(10) N 2+ 13(9) 1 0 1 2 3 2, 5 2, 67 – 1, 59 1, 24 1, 10 1, 12 105 – 289 599 940 828 nghòch – thuaän nghòch thuaän
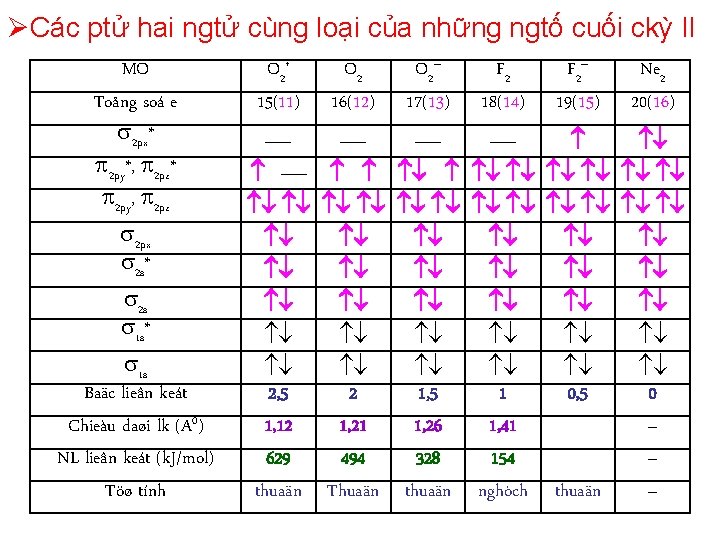
ØCác ptử hai ngtử cùng loại của những ngtố cuối ckỳ II MO Toång soá e 2 px* 2 py*, 2 pz* 2 py, 2 pz 2 px 2 s* 2 s 1 s* 1 s Baäc lieân keát Chieàu daøi lk (A 0) NL lieân keát (k. J/mol) Töø tính O 2+ 15(11) O 2 16(12) O 2– 17(13) F 2 18(14) F 2– 19(15) Ne 2 20(16) 2, 5 2 1, 5 1 0, 5 0 1, 12 1, 21 1, 26 1, 41 – 629 494 328 154 – thuaän Thuaän thuaän nghòch thuaän –
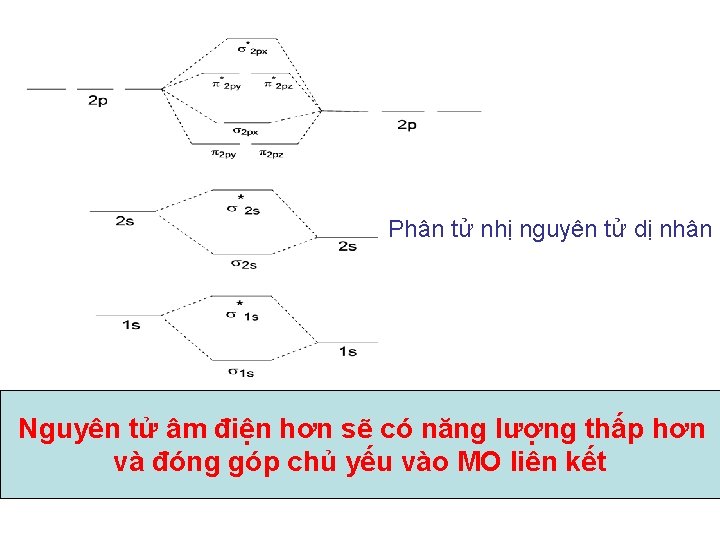
Phân tử nhị nguyên tử dị nhân Nguyên tử âm điện hơn sẽ có năng lượng thấp hơn và đóng góp chủ yếu vào MO liên kết
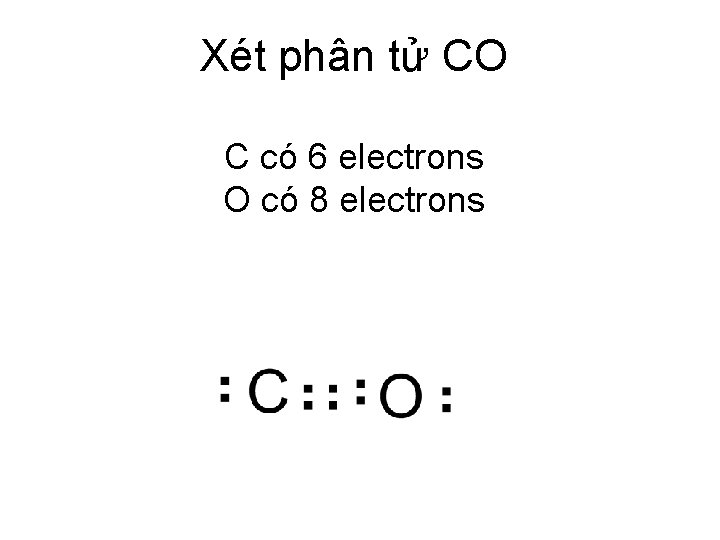
Xét phân tử CO C có 6 electrons O có 8 electrons
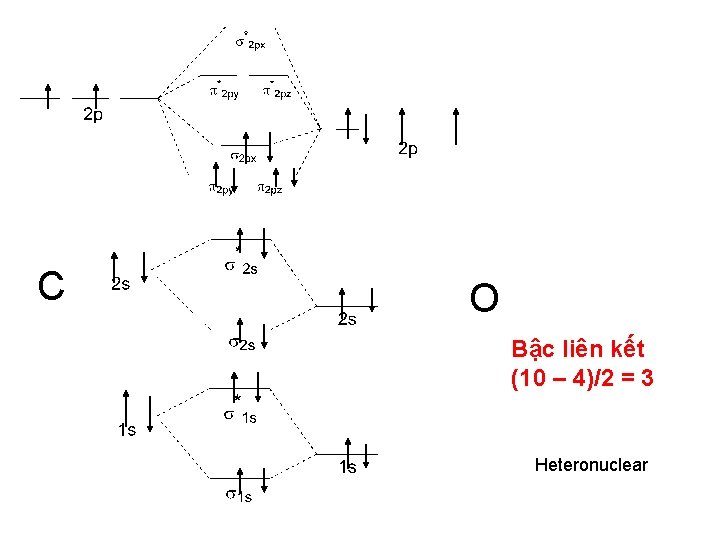
C O Bậc liên kết (10 – 4)/2 = 3 Heteronuclear
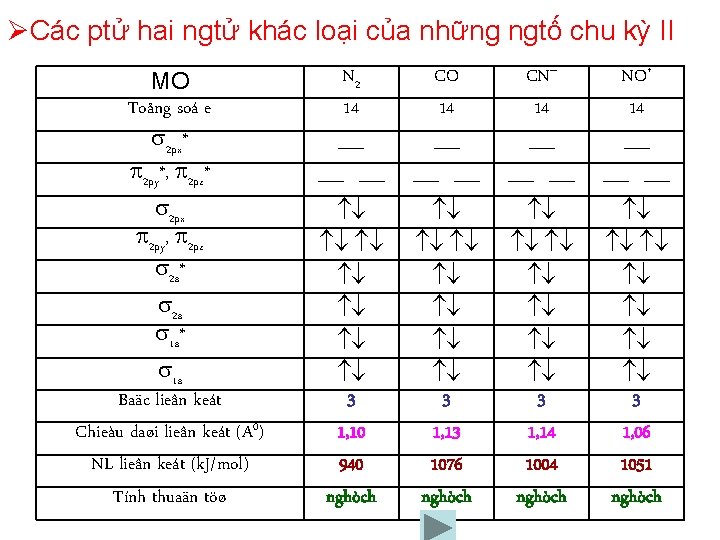
ØCác ptử hai ngtử khác loại của những ngtố chu kỳ II MO Toång soá e 2 px* 2 py*, 2 pz* 2 px 2 py, 2 pz 2 s* 2 s 1 s* 1 s Baäc lieân keát Chieàu daøi lieân keát (A 0) NL lieân keát (k. J/mol) Tính thuaän töø N 2 14 CO 14 CN– 14 NO+ 14 3 1, 10 940 nghòch 3 1, 13 1076 nghòch 3 1, 14 1004 nghòch 3 1, 06 1051 nghòch
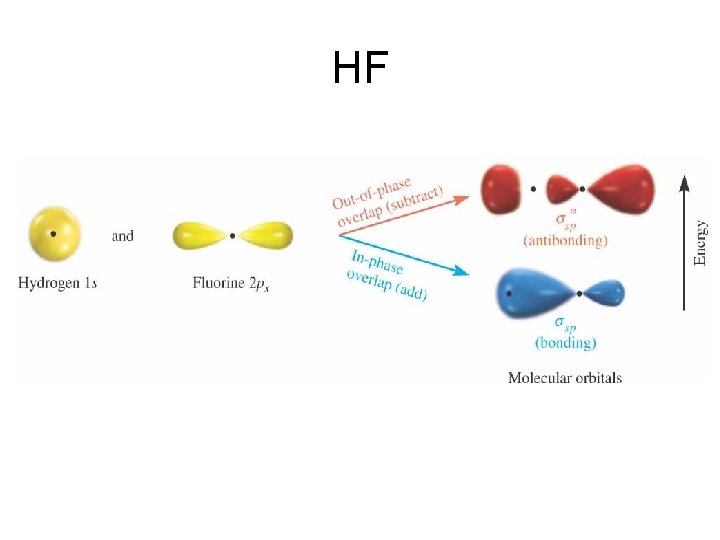
HF
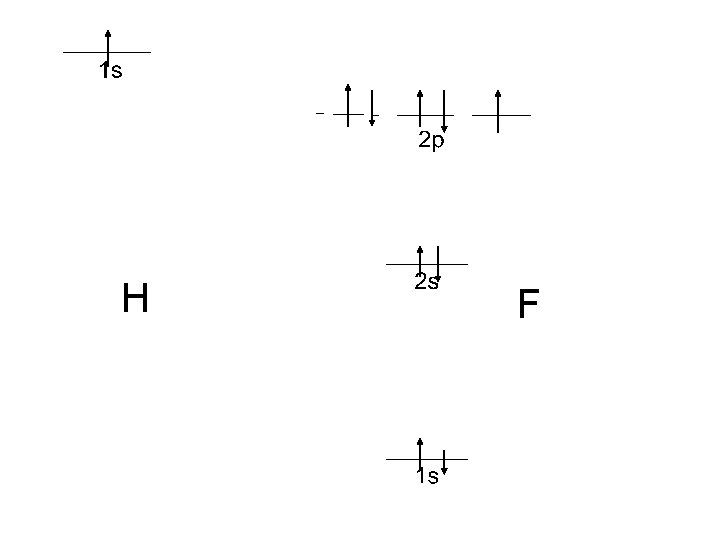
H F
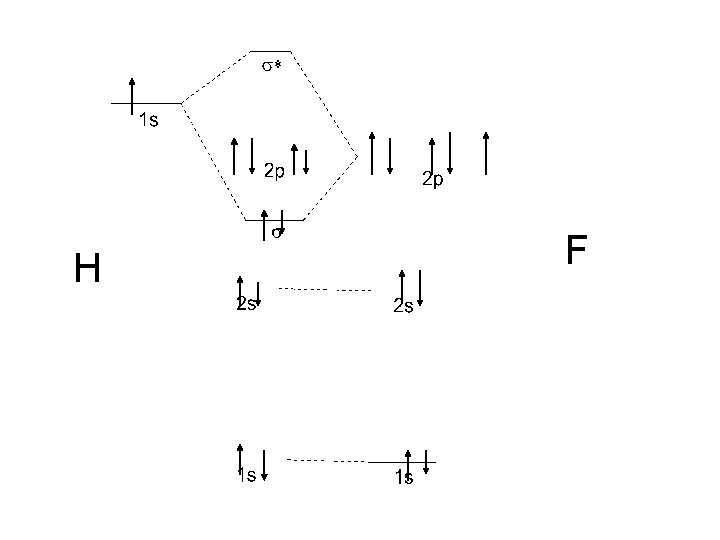
H F
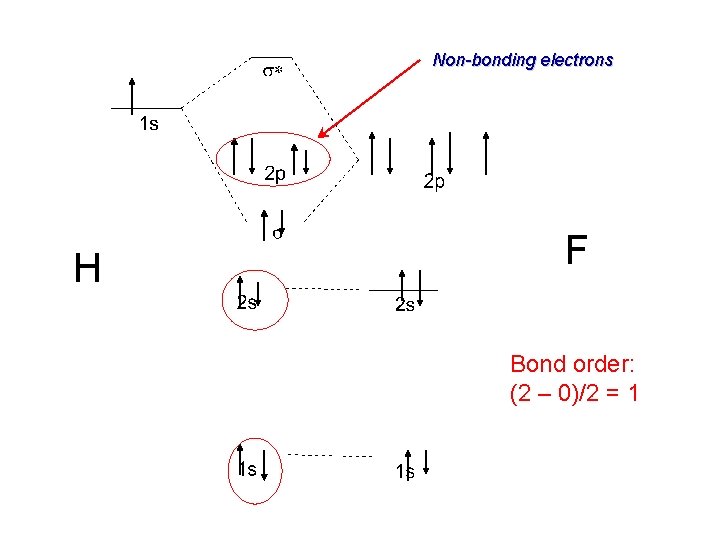
Non-bonding electrons H F Bond order: (2 – 0)/2 = 1

LIÊN KẾT KIM LỌAI Các tính chất của kim loại Không trong suốt Có ánh kim Dẫn nhiệt, dẫn điện tốt Dẻo …
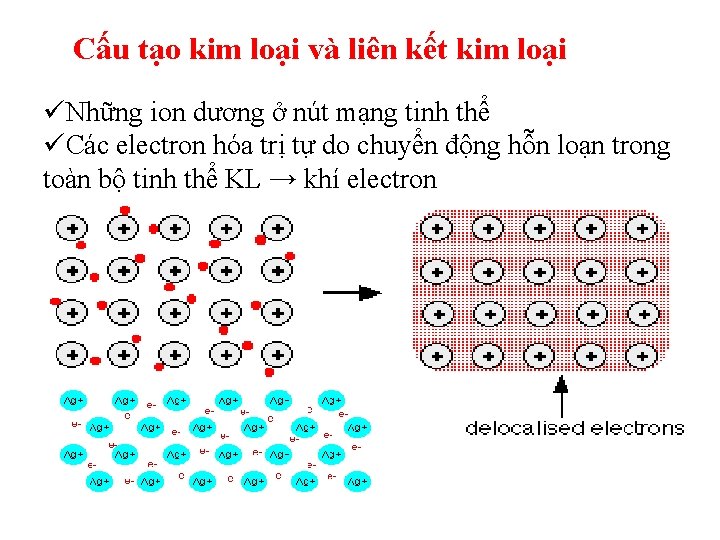
Cấu tạo kim loại và liên kết kim loại üNhững ion dương ở nút mạng tinh thể üCác electron hóa trị tự do chuyển động hỗn loạn trong toàn bộ tinh thể KL → khí electron
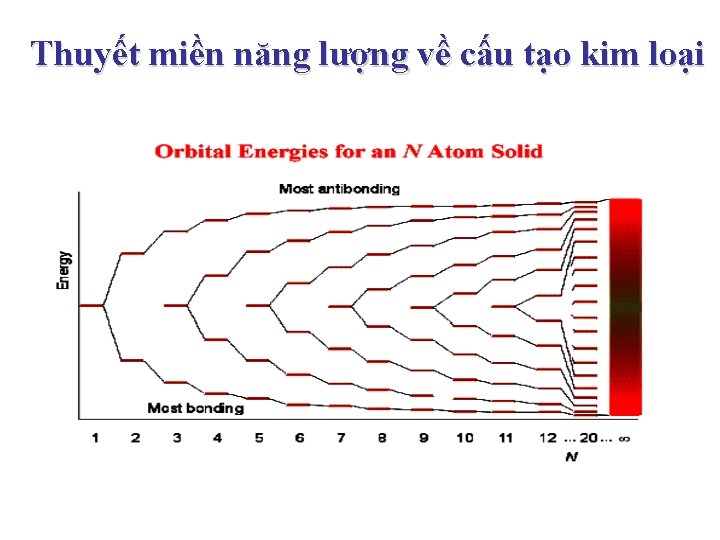
Thuyết miền năng lượng về cấu tạo kim loại

• MIỀN HÓA TRỊ - HOMO miền chứa electron hóa trị • MIỀN DẪN – LUMO miền nằm trên miền hóa trị • MIỀN CẤM là khoảng cách giữa hai miền trên nếu có
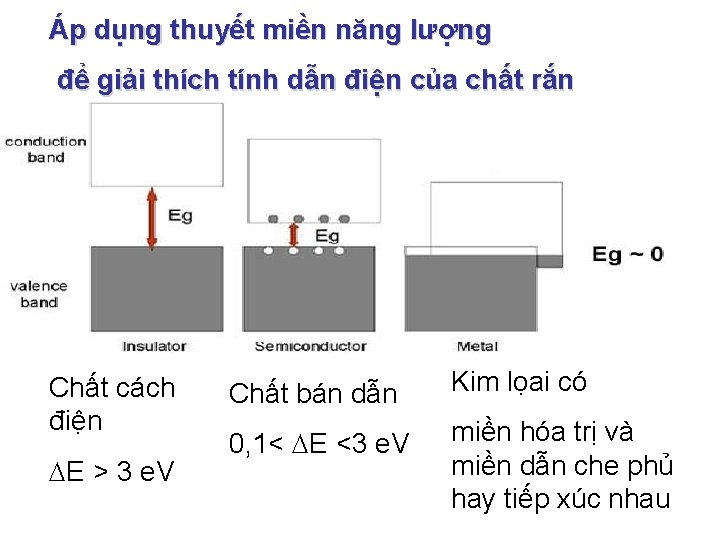
Áp dụng thuyết miền năng lượng để giải thích tính dẫn điện của chất rắn Chất cách điện E > 3 e. V Chất bán dẫn Kim lọai có 0, 1< E <3 e. V miền hóa trị và miền dẫn che phủ hay tiếp xúc nhau
- Slides: 48