TUN 24 bi 44 Luyn tp 2 TIT

TUẦN 24 bµi 44 LuyÖn tËp (2 TIẾT) Hi®rocacbon kh «ng no ANKEN ANKADIEN ANKIN GV: HUỲNH THU TRÚC

Hiđrocacbon không no Anken Ankađien Ankin
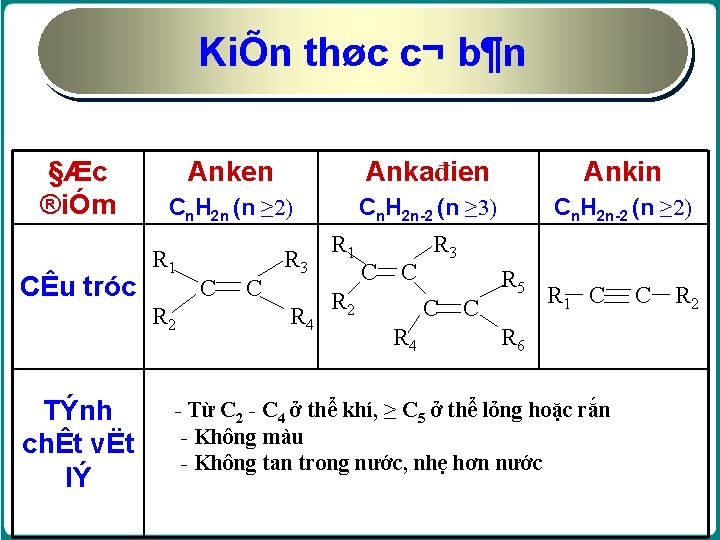
KiÕn thøc c¬ b¶n §Æc ®iÓm Anken Ankađien Ankin Cn. H 2 n (n ≥ 2) Cn. H 2 n 2 (n ≥ 3) Cn. H 2 n 2 (n ≥ 2) R 1 R 3 C C R 5 CÊu tróc C C R 1 C C R 2 C C R 2 R 4 R 6 TÝnh chÊt vËt lÝ - Từ C 2 - C 4 ở thể khí, ≥ C 5 ở thể lỏng hoặc rắn - Không màu - Không tan trong nước, nhẹ hơn nước
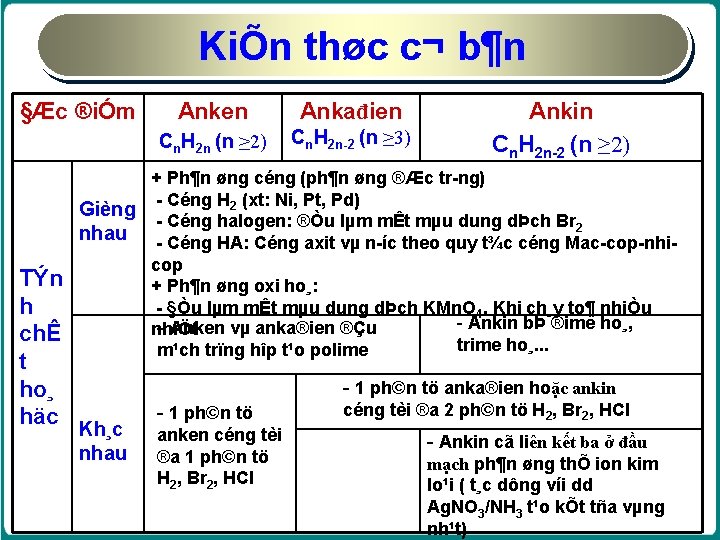
KiÕn thøc c¬ b¶n §Æc ®iÓm TÝn h chÊ t ho¸ häc Anken Ankađien Cn. H 2 n (n ≥ 2) Cn. H 2 n 2 (n ≥ 3) Ankin Cn. H 2 n 2 (n ≥ 2) + Ph¶n øng céng (ph¶n øng ®Æc tr ng) Céng H 2 (xt: Ni, Pt, Pd) Gièng Céng halogen: ®Òu lµm mÊt mµu dung dÞch Br 2 nhau Céng HA: Céng axit vµ n íc theo quy t¾c céng Mac cop nhi cop + Ph¶n øng oxi ho¸: §Òu lµm mÊt mµu dung dÞch KMn. O 4. Khi ch¸y to¶ nhiÒu - Ankin bÞ ®ime ho¸, - Anken vµ anka®ien ®Çu nhiÖt trime ho¸. . . m¹ch trïng hîp t¹o polime - 1 ph©n tö anka®ien hoặc ankin Kh¸c nhau - 1 ph©n tö anken céng tèi ®a 1 ph©n tö H 2, Br 2, HCl céng tèi ®a 2 ph©n tö H 2, Br 2, HCl - Ankin cã liên kết ba ở đầu mạch ph¶n øng thÕ ion kim lo¹i ( t¸c dông víi dd Ag. NO 3/NH 3 t¹o kÕt tña vµng nh¹t)
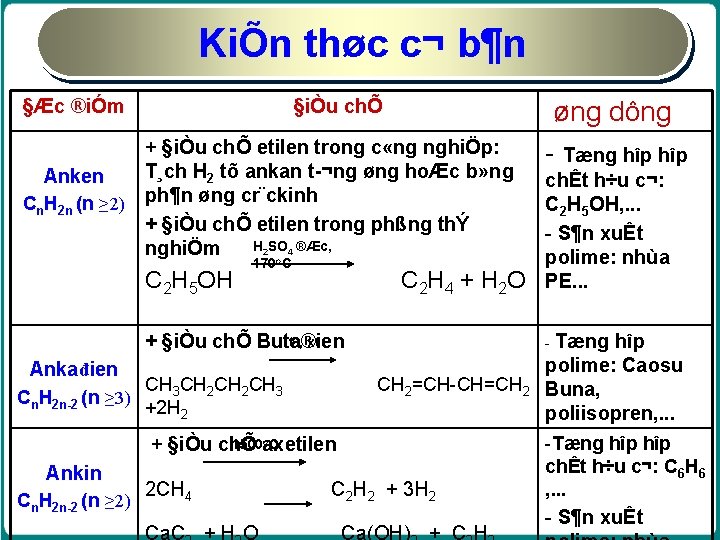
KiÕn thøc c¬ b¶n §Æc ®iÓm §iÒu chÕ + §iÒu chÕ etilen trong c «ng nghiÖp: T¸ch H 2 tõ ankan t ¬ng øng hoÆc b» ng Anken Cn. H 2 n (n ≥ 2) ph¶n øng cr¨ckinh + §iÒu chÕ etilen trong phßng thÝ H 2 SO 4 ®Æc, nghiÖm o C 2 H 5 OH 170 C C 2 H 4 + H 2 O to, xt + §iÒu chÕ Buta®ien Ankađien CH 3 CH 2 CH 3 Cn. H 2 n 2 (n ≥ 3) +2 H 2 Cn. H 2 n 2 (n ≥ 2) 2 CH 4 chÊt h÷u c¬: C 2 H 5 OH, . . . - S¶n xuÊt polime: nhùa PE. . . - Tæng CH 2=CH-CH=CH 2 o. C 1500 axetilen + §iÒu chÕ Ankin øng dông - Tæng hîp C 2 H 2 + 3 H 2 hîp polime: Caosu Buna, poliisopren, . . . -Tæng hîp chÊt h÷u c¬: C 6 H 6 , . . . - S¶n xuÊt
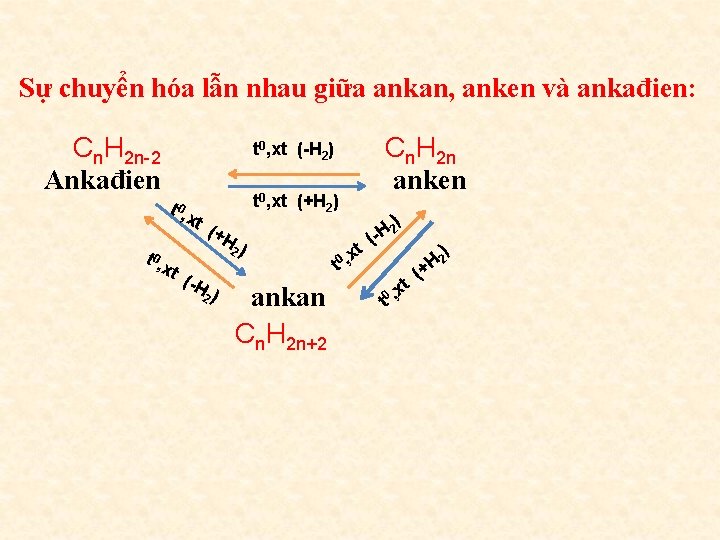
Sự chuyển hóa lẫn nhau giữa ankan, anken và ankađien: Cn. H 2 n-2 Ankađien Cn. H 2 n anken t 0, xt ( H 2) t 0, xt (+H 2) t 0, x t ( H 2) ankan Cn. H 2 n+2 t 0 , x t ) 2 H ( t 0 , xt ( ) 2 H +

BÀI TẬP 1 Viết các phương trình hoá học (nếu có) khi cho lần lượt các chất: etilen, butađien, axetilen tác dụng với các chất sau: HCl (tỉ lệ 1: 1), dd Br 2 dư, dd Ag. NO 3/NH 3, phản ứng trùng hợp ( ghi rõ điều kiện phản ứng nếu có)

Hướng dẫn bài tập 1 + Etilen CH 2 = CH 2 + HCl CH 2=CH 2 + Br 2 + Butađien CH 2 Br-CH 2 Br to, p, xt n. CH 2 = CH 2 CH 3 CH 2 Cl CH – CH n 2 CH 2 = CH-CH=CH 2 + HCl 1: 1 2 CH 3 -CHCl-CH=CH 2 CH 3 -CH=CH-CH 2 Cl CH 2=CH-CH=CH 2 + 2 Br 2 n. CH 2 = CH-CH=CH 2 + Axetilen CH CH + HCl CH CH + 2 Br 2 HC CH 2 Br–CHBr- CH 2 Br CH -CH=CH- CH n to, p, xt 2 Hg. Cl 2 , 150 200 o. C 2 CH 2 = CHCl CHBr 2 -CHBr 2 CH + [Ag(NH 3)2]OH Ag. C CAg + 2 NH 3 + H 2 O

Bài tập 2: Bài tập nhận biết Bằng phương pháp hoá học em hãy nhận biết 3 lọ chứa chất lỏng mất nhãn sau: hexan, hex-1 -en, hex-1 -in
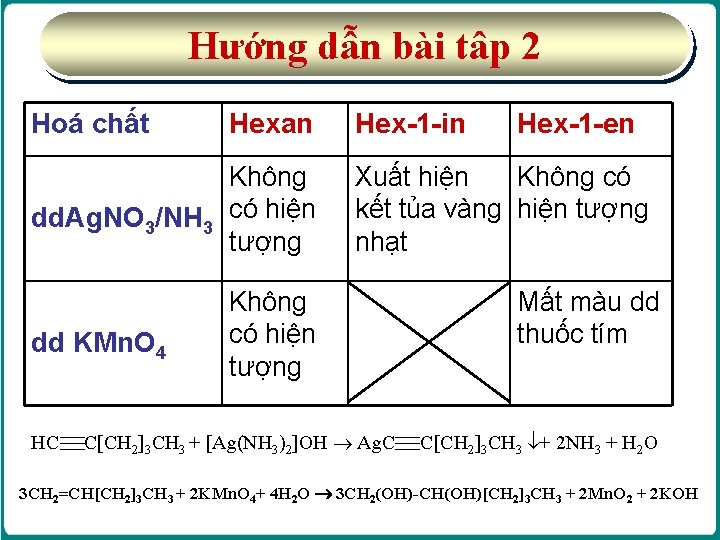
Hướng dẫn bài tâp 2 Hoá chất Hexan Không dd. Ag. NO 3/NH 3 có hiện tượng dd KMn. O 4 Không có hiện tượng Hex 1 in Hex 1 en Xuất hiện Không có kết tủa vàng hiện tượng nhạt Mất màu dd thuốc tím HC C[CH 2]3 CH 3 + [Ag(NH 3)2]OH Ag. C C[CH 2]3 CH 3 + 2 NH 3 + H 2 O 3 CH 2=CH[CH 2]3 CH 3 + 2 KMn. O 4+ 4 H 2 O 3 CH 2(OH)-CH(OH)[CH 2]3 CH 3 + 2 Mn. O 2 + 2 KOH
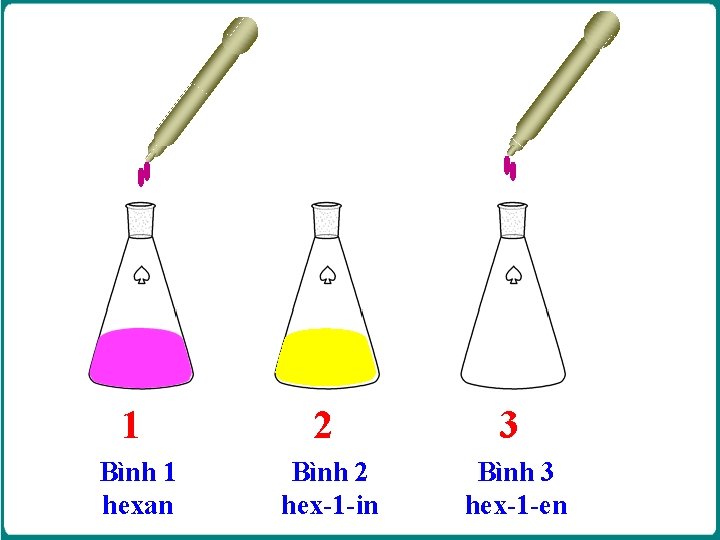
1 2 3 Bình 1 hexan Bình 2 hex-1 -in Bình 3 hex-1 -en

Bài 3: Viết đồng phân cấu tạo ứng với công thức phân tử C 5 H 10 và C 5 H 8 và gọi tên theo tên thay thế? * C 5 H 10 Giải CH 2=CH-CH 2 -CH 3 Pent-1 -en CH 3 -CH=CH-CH 2 -CH 3 Pent-2 -en 2 -metylbut-1 -en 3 -metylbut-1 -en 2 -metylbut-2 -en

*C 5 H 8 2 3 1 4 CH 3 -CH=C=CH-CH 3 và CH 2=CH-CH 2 -CH=CH 2 penta-2, 3 -đien penta-1, 4 -đien 1 2 1 3 CH 2=C=CH-CH 2 -CH 3 và CH 2=CH-CH 3 penta-1, 2 -đien penta-1, 3 -đien 1 2 1 3 CH 2=C=C -CH 3 và CH 2=CH-CH=CH 2 CH 3 3 -metylbuta-1, 2 -đien 2 -metylbuta-1, 3 -đien

Bài 4: Viết CTCT các anken có tên gọi sau: a. Butilen, 2 - metylbut-2 -en, pent -1 -en, 2, 3đimetylpent-2 -en. b. Propilen, hex-1 -en, etilen, 2 -metylpent-1 -en. Giải Hướng dẫn giải: a. CH 2=CH-CH 2 -CH 3 -C(CH 3)=CH-CH 3 CH 2=CH-CH 2 -CH 3 -C(CH 3)=C(CH 3)-CH 2 -CH 3

b. Propilen, hex-1 -en, etilen, 2 -metylpent-1 -en. CH 2=CH-CH 3 CH 2=CH-CH 2 -CH 3 CH 2=CH 2=C(CH 3)-CH 2 -CH 3

Bài 5: Nhận biết các chất sau bằng phương pháp hóa học: CH 4, C 2 H 4. Hướng dẫn giải + Dẫn hai mẫu khí vào dung dịch Br 2, nếu thấy khí nào làm mất màu dung dịch Br 2 là C 2 H 4. + Còn lại là khí CH 4

Bài 6: Cho 4, 48 lít hỗn hợp khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 1, 12 lít khí thoát ra. Các thể tích đo ở điều kiện tiêu chuẩn. Thành phần trăm thể tích của khí metan trong hỗn hợp là ? Hướng dẫn giải: Công thức tính thành phần trăm: %về thể tích =% về số mol Vkhí. 100% nkhí. 100% %Khí = Vhỗn hợp nhỗn hợp Chỉ có khí etilen phản ứng khí thoát ra là khí metan Vmetan =1, 12 ml 1, 12. 100% %CH 4 = 4, 48 = 25%

Bài 7 : Hỗn hợp A gồm hai chất kế tiếp nhau trong dãy đồng đẳng của etilen. Cho 3, 36 lít (đktc) hỗn hợp khí trên phản ứng hoàn toàn với Br 2 trong CCl 4 thì thấy trong bình chứa brom tăng thêm 7. 7 g a. Xác định CTPT của hai anken. b. Xác định thành phần % về thể tích của hỗn hợp A. Hướng dẫn giải a. Ta có nhh=3. 36/22, 4=0, 15 (mol) Gọi CT chung của anken là: Cn. H 2 n 0, 15 ---> 0, 15 Khối lượng bình tăng chính là khối lượng của hai anken. MA=7. 7/0, 15=51, 3 (g/mol) 14 n=51, 3 n=3, 66 Vậy 2 anken kế tiếp nhau là : C 3 H 6 và C 4 H 8

b. -Gọi số mol của C 3 H 6: a (mol) C 4 H 8: b (mol) - Ta có hệ: a+b=0, 15 42 a+56 b=7, 7 Giải hệ phương trình , ta được: a=0, 05 ; b=0, 1 %VC 3 H 6 = %VC 4 H 8=66, 67%

+ Ba i ho c: - Biết công thức chung, cÊu t¹o vµ hiểu tính chất hoá học, cách điều chế anken, ankađien, ankin tõ ®ã vận dụng làm c¸c bµi tËp nhËn biÕt , ®iÒu chÕ, t¸ch chÊt vµ gi¶i c¸c bµi tËp to¸n liªn quan. + Bài tập rèn luyện thêm: + 3, 6, 8 /SGK. tr 181, 182 + 6. 39 6. 43/SBT. tr 53, 54

CHÚC c¸c em häc sinh HỌC TỐT
- Slides: 22