TUMORS of the BLADDER MGE KALAYCIOLU ECE TOPRAKI

TUMORS of the BLADDER MÜGE KALAYCIOĞLU ECE TOPRAKÇI GÖKALP ARİF UTKUGÜN
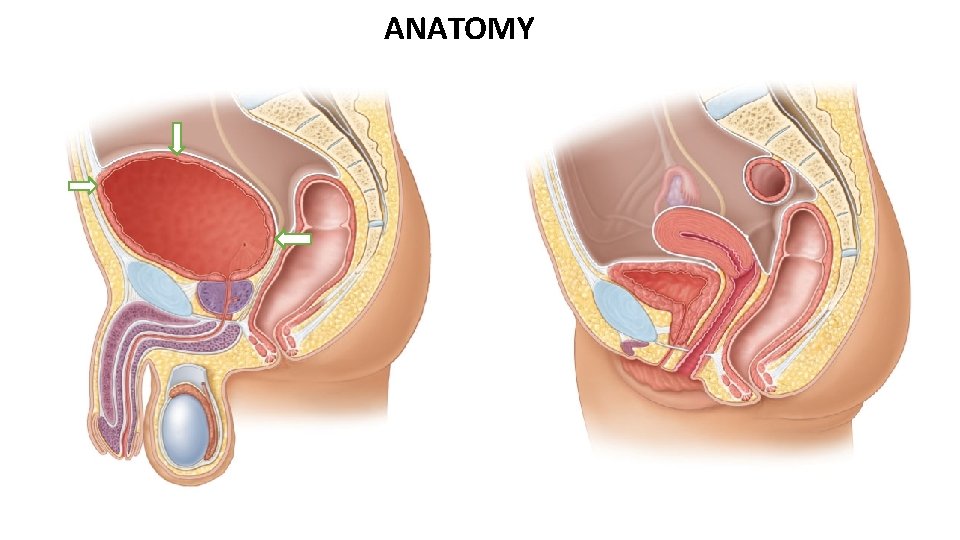
ANATOMY
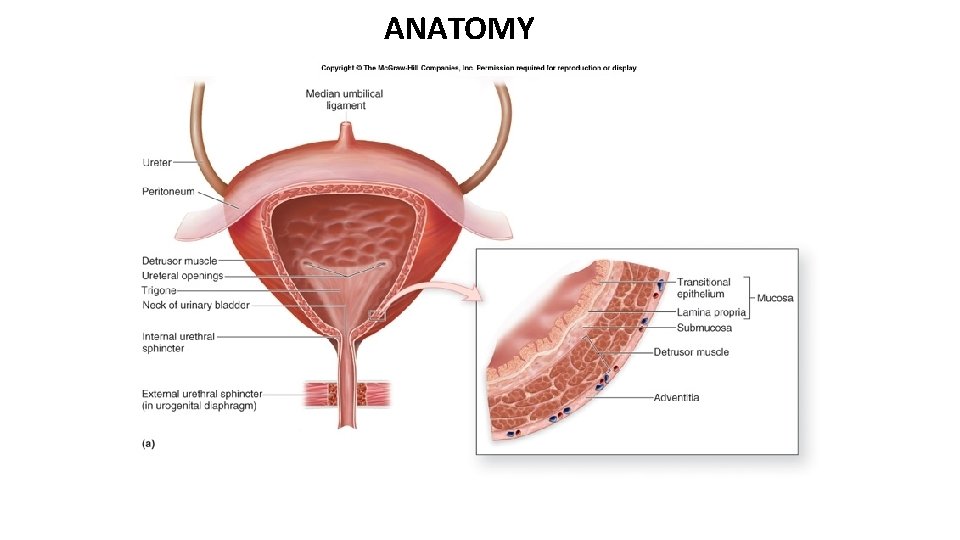
ANATOMY
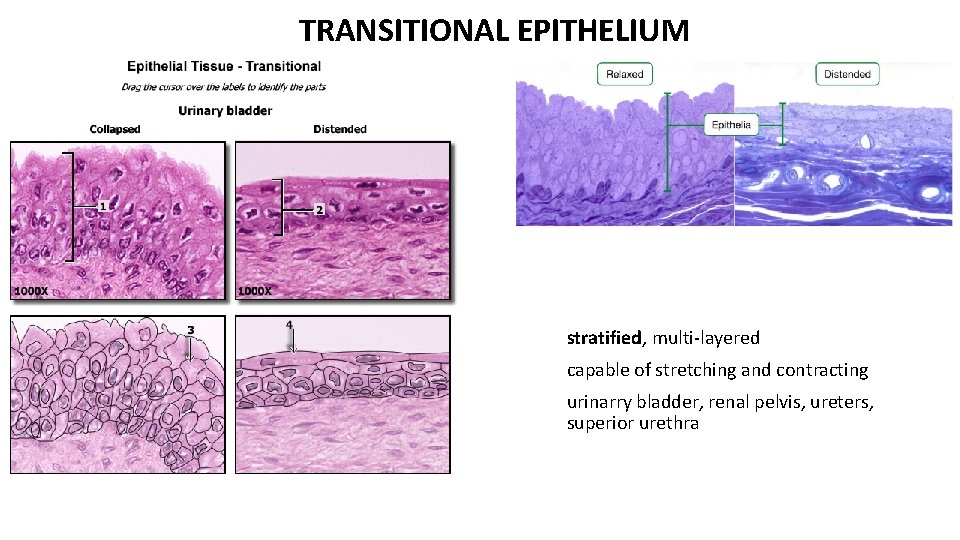
TRANSITIONAL EPITHELIUM stratified, multi-layered capable of stretching and contracting urinarry bladder, renal pelvis, ureters, superior urethra
• Arterial Supply: superior vesical a. inferior vesical a. • Venous Drainage venous plexus internal iliac v. prostatic

BENIGN TUMORS of the BLADDER • epithelial metaplasia • leukoplakia • inverted papilloma • nephrogenic adenoma • leiomyoma • cystitis cystica and cystitis glandularis
LEIOMYOMA • most common benign neoplasm • non-infiltrative smooth muscle tumour lacking mitotic activity, cellular atypia, and necrosis • in the submucosa • Focal excision of the mass

İNSİDANS • Mesane kanseri genitoüriner sistemde görülen 2. en sık kanserdir. • Erkeklerde yeni vakaların %7’sini , bayanlarda %2’sini oluşturur. • Sosyoekonomik düzey arttıkça her iki cinsiyet için de kanser görülme sıklığı artıyor. • En sık 65 yaş ve üzerinde görülür. Erkeklerde görülme sıklığı bayanlara göre 4 kat daha fazladır. • Tanı alan hastaların %75’inde mesaneye sınırlıdır, %25’inde lenf nodu ve uzak yayılım görülür.

Risk Faktörleri • 1)Sigara: Mesane kanseri riskini 2 -3 kat arttırır. En önemli risk faktörüdür. • Etken maddesi alpha- ve beta-naphtylamine idrar ile atıldığı için riski arttırır. • Sigara kullanımının bırakılmasıyla risk azalır ama hiç kullanmayan bireyden daha yüksek risk taşır.

2)Mesleki Maruziyet • Boya endüstrisinde çalışanlar • Tekstil üreticileri(kauçuk, deri) • Basımevlerinde çalışanlar • Kimyasal maddelere maruziyeti olanlar risk altındadır. 3)Yaş: 65 yaş ve üzerinde risk artmaktadır.

• 4)Cinsiyet: Erkeklerin mesane kanserine yakalanma riski kadınlara göre üç ya da dört kat daha yüksektir. Ancak kadınların mesane kanserinden ölme olasılığı erkeklerden daha yüksektir. • 5)Genetik: Ailede mesane kanseri öyküsü • 6) Kronik idrar yolu enfeksiyonu, böbrek ve mesane taşı gibi mesanede kronik irritasyona yol açan etkenler • 7)Kemoterapi ve Radyoterapi Öyküsü • 8)Arsenik Maruziyeti: İçme suyunda tüketilmesi ile oluşabilmektedir.

KLİNİK • Hastaların %85 -90’ında görülen en sık semptom hematüridir. Hematüri ağrısız ve pıhtılıdır. Sürekli olmaktan ziyade aralıklıdır. • Gross veya mikroskobik hematüri olabilir. • Mikroskobik hematüri idrar testi ile tespit edilir.

• İdrar yaparken yanma ya da ağrı • Sık idrara çıkma • Gece boyunca birçok kez idrara çıkma ihtiyacı hissetme • İdrara çıkma ihtiyacı hissetme ama idrarın olmaması • Vücudun bir tarafında alt sırt ağrısı

• Metastaz varlığında • Kanser akciğerlere yayıldığında, öksürük veya nefes darlığına neden olabilir. • Karaciğere yayıldığında karın ağrısı ve sarılığa neden olabilir. • Kemiğe yayıldığı zaman ise, kemik ağrısı, sırt ağrısı ve kemik kırıklarına neden olabilir.

TANI • Fizik Muayene, Anamnez • İdrar analizi: Büyütme sahasında 4 ten fazla eritrosit olması mikroskobik hematüri anlamına gelir. İdrar sitolojisi ile hücrelerin tümör içerip içermediğine mikroskop altında bakılır. • USG: Hematürisi olan hastaya yapılacak ilk görüntüleme yöntemidir. Kitlelerin karakterleri ve mesanedeki dolma defektleri saptanabilir.

• Sistoskopi: USG’de kitle saptanırsa yapılacak ilk görüntüleme yöntemidir. Mesanenin direkt görsel incelenmesidir. Sistoskop ile mesanenin iç tabakalarını görme ve kanser belirtisi olup olmadığını inceleme mümkün hale gelir. Mesanede büyümeleri algılar ve biyopsi veya cerrahi ihtiyacı belirleyebilir. Mesane tümörü tanı ve takibinde altın standart tanı yöntemidir.

• Mesane Tümörünün Transüretral Rezeksiyonu (TURMT): Eğer sistoskopi sırasında anormal doku bulunursa biyopsi ile doku örneği alınarak incelenir.

• Bilgisayarlı tomografi taraması (BT): • Manyetik rezonans görüntüleme (MR): Ø Kasa invaze ve metastatik mesane tümörlerinde Ø BT ve MR ile tümörün evrelemesi yapılmaktadır. Ø Lenf nodüllerinin değerlendirmesinde Ø Karaciğer ve akciğer metastazları için Ø Kemik metastazlarının saptanmasında MR görüntüleme daha sensitiftir. • Pozitron Emisyon Tomografisi(PET): Mesane kanserinin yayılıp yayılmadığını öğrenmek ve evresini belirlemeye yardımcı olmak için kullanılabilir.
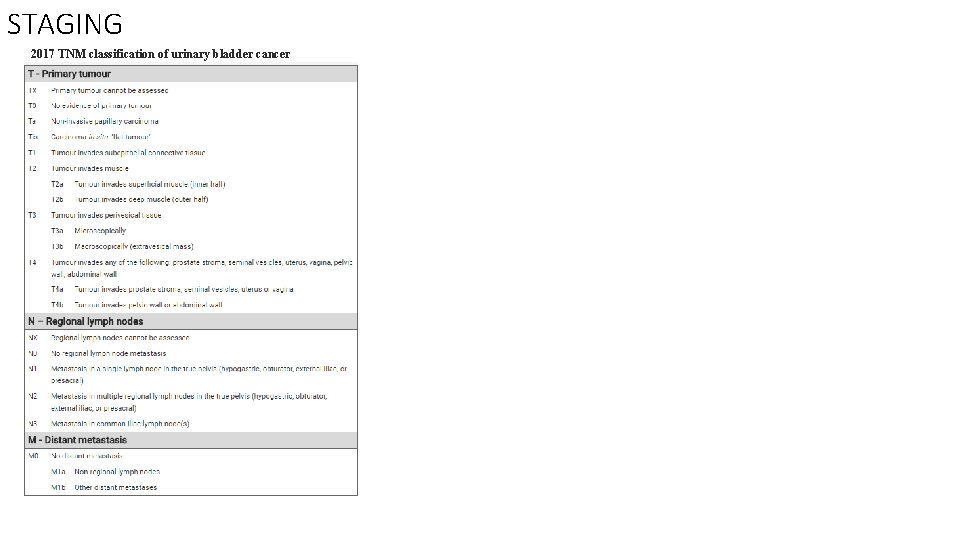
STAGING 2017 TNM classification of urinary bladder cancer
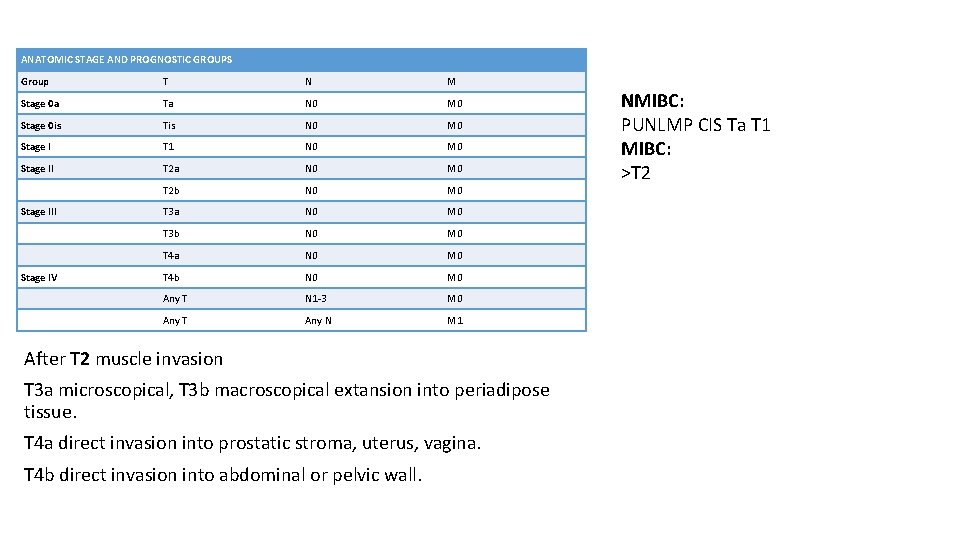
ANATOMIC STAGE AND PROGNOSTIC GROUPS Group T N M Stage 0 a Ta N 0 M 0 Stage 0 is Tis N 0 M 0 Stage I T 1 N 0 M 0 Stage II T 2 a N 0 M 0 T 2 b N 0 M 0 T 3 a N 0 M 0 T 3 b N 0 M 0 T 4 a N 0 M 0 T 4 b N 0 M 0 Any T N 1 -3 M 0 Any T Any N M 1 Stage III Stage IV After T 2 muscle invasion T 3 a microscopical, T 3 b macroscopical extansion into periadipose tissue. T 4 a direct invasion into prostatic stroma, uterus, vagina. T 4 b direct invasion into abdominal or pelvic wall. NMIBC: PUNLMP CIS Ta T 1 MIBC: >T 2
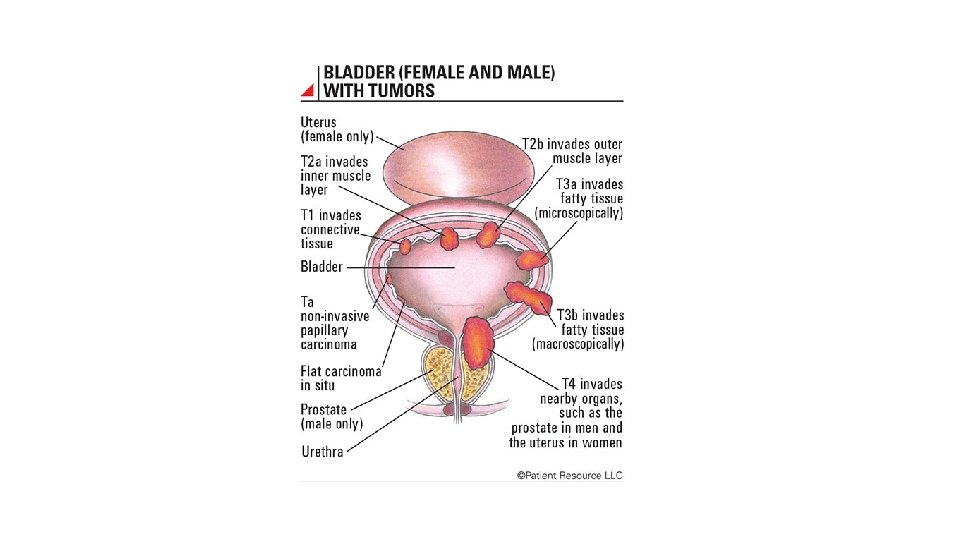

Bladder Cancer types and treatment

Bladder cancer types • Papilloma • Transitional cell carcinoma • Nontransitional cell carcinomas: • adenocarcinoma • squamous cell carcinoma • undifferentiated carcinomas • mixed carcinoma • Rare epithelial and nonepithelial cancers

Papilloma • Benign proliferative growth in the bladder, composed of delicate stalks lined by normal-appearing urothelium • Rarely have mitotic figures • Lack markers of aggressive growth (TP 53 or RB mutations) • 75% of these tumors have mutations in FGFR-3 • May recur, but they do not progress or invade!

Transitional cell ca • 90% of all bladder cancers • Papillary, exophytic lesions • May be sessile or ulcerated

Squamous cell ca • 5 -10% of all bladder cancers in US, often asso. w history of chr infection, vesical calculi or chr catheter use • Schistosoma haematobium: Egypt, parts of Africa, Middle East • Often nodular and invasive at the time of dx • Poorly differentiated neoplasms composed of polygonal cells w intercellular bridges
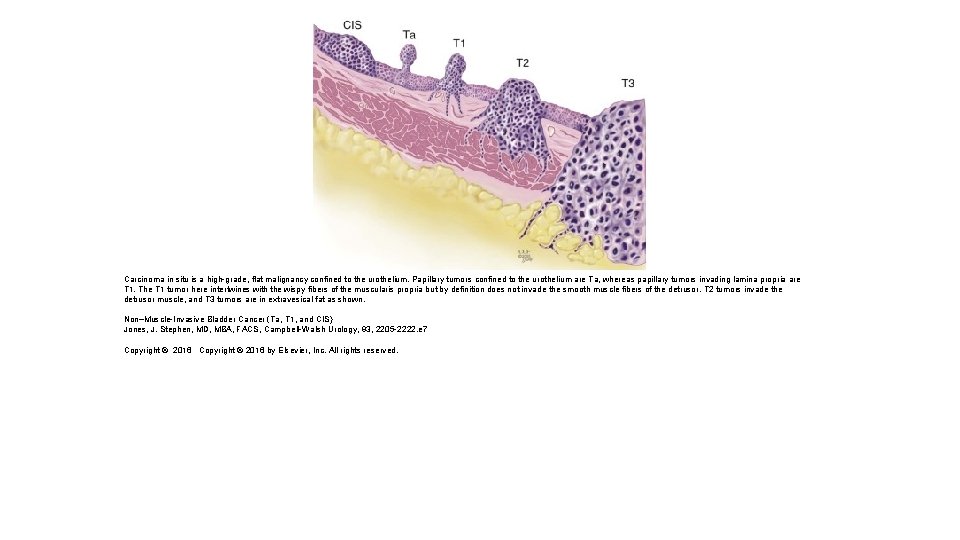
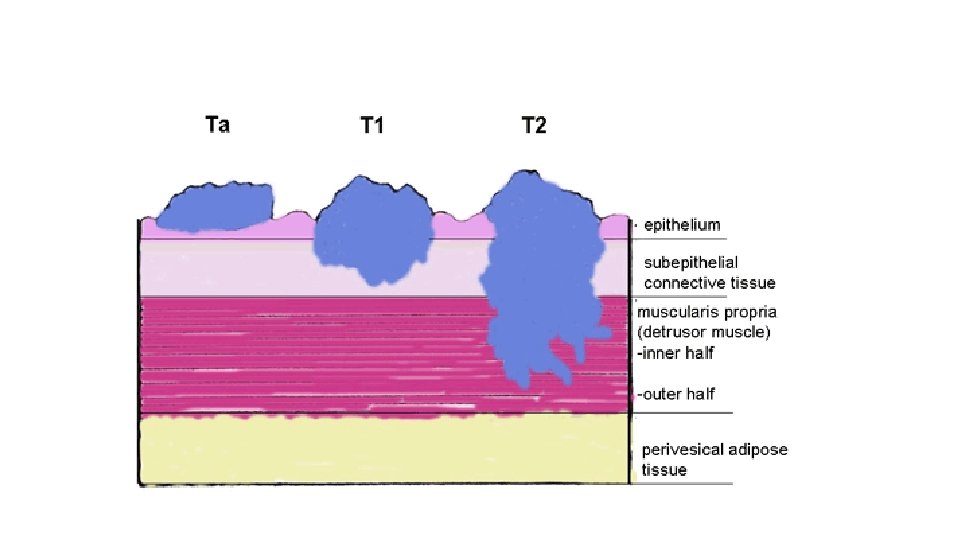
Carcinoma in situ is a high-grade, flat malignancy confined to the urothelium. Papillary tumors confined to the urothelium are Ta, whereas papillary tumors invading lamina propria are T 1. The T 1 tumor here intertwines with the wispy fibers of the muscularis propria but by definition does not invade the smooth muscle fibers of the detrusor. T 2 tumors invade the detrusor muscle, and T 3 tumors are in extravesical fat as shown. Non–Muscle-Invasive Bladder Cancer (Ta, T 1, and CIS) Jones, J. Stephen, MD, MBA, FACS, Campbell-Walsh Urology, 93, 2205 -2222. e 7 Copyright © 2016 by Elsevier, Inc. All rights reserved.
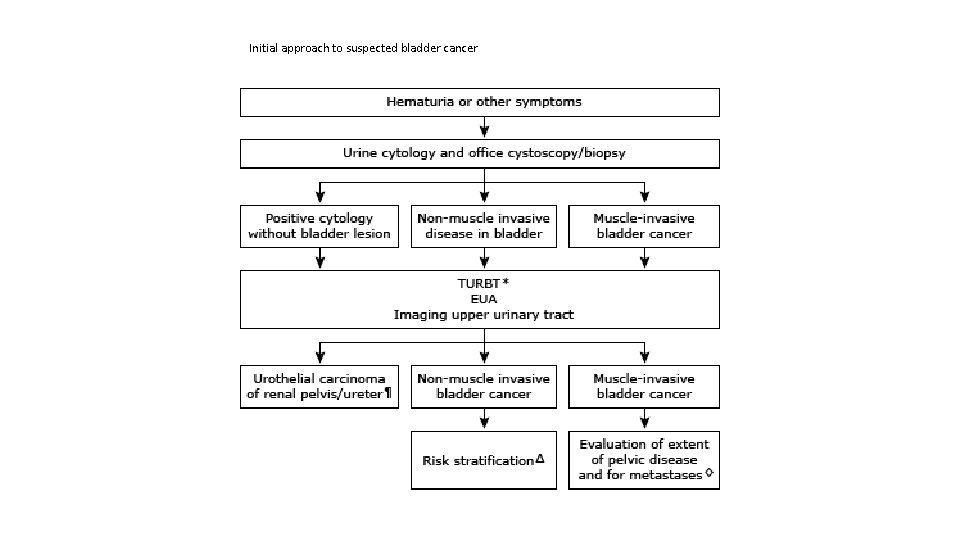
Initial approach to suspected bladder cancer
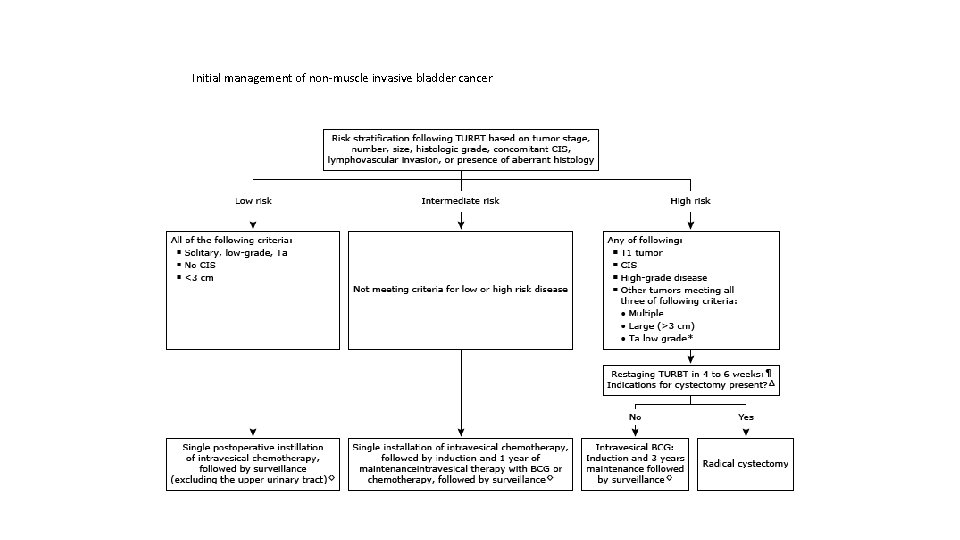
Initial management of non-muscle invasive bladder cancer
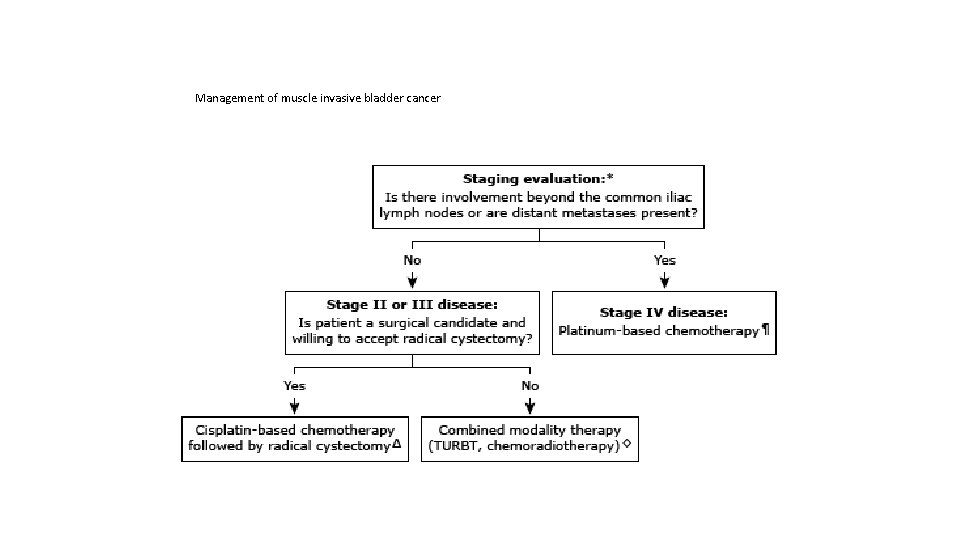
Management of muscle invasive bladder cancer
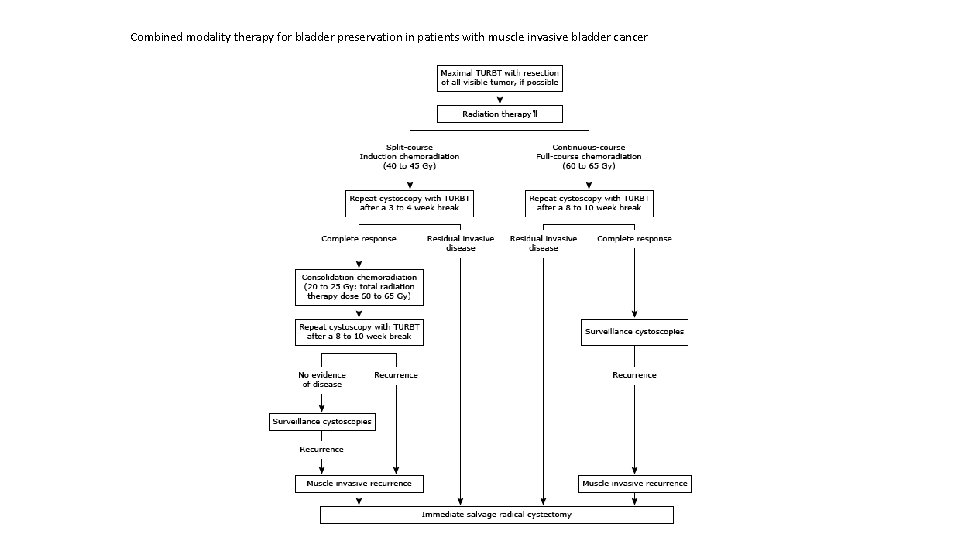
Combined modality therapy for bladder preservation in patients with muscle invasive bladder cancer
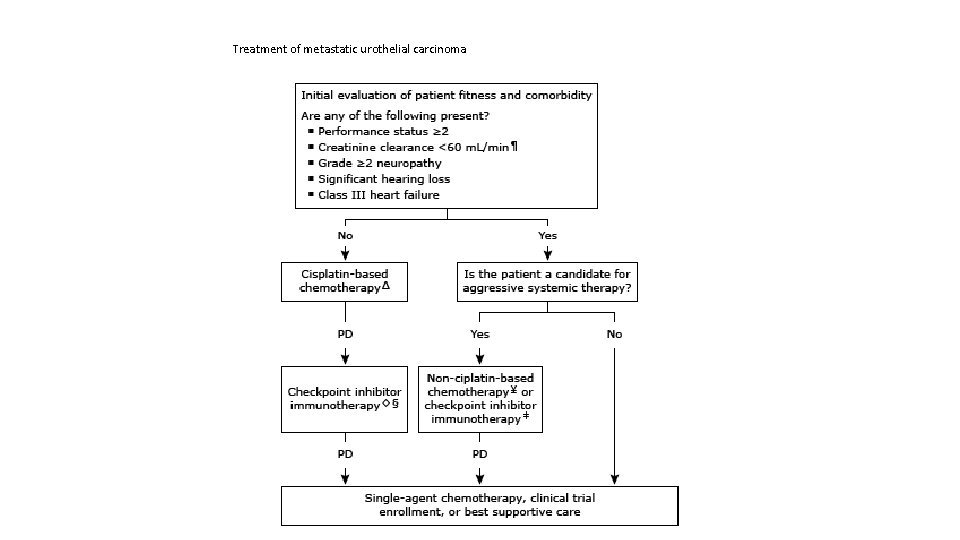
Treatment of metastatic urothelial carcinoma

Treatment • Intravesical chemotherapy • Surgery • Radiotherapy • Chemotherapy • Combination therapy

Intravesical chemotherapy • Immunotherapeutic or chemotherapeutic agents can be instilled into the bladder via catheter • Prophylactic or therapeutic • Local toxicity relatively common: irritative voiding sx • Mitomycin C, thiotepa, BCG

Surgery • TUR • Partial cystectomy • Radical cystectomy: removal of bladder w surrounding fat (prostate/seminal vesicles in male; uterus/fallopian tubes/ovaries/cervix in female)

Radiotherapy • External beam irradiation over 5 -8 week period • Alternative to radical cystectomy in selected pt w deeply infiltrating bladder ca • 15% of pts may have significant bowel, bladder, rectal cx • 5 year survival for T 2 and T 3 18 -41% • Local recurrence common • Offered only to poor surgical candidates

Chemotherapy • Single most active agent is cisplatin • MVAC regimen (methotrexate, vinblastine, adriamycin, cisplatin) • 13 -35% of pts receiving such regimens attain complete response • Median survival time approximately one year

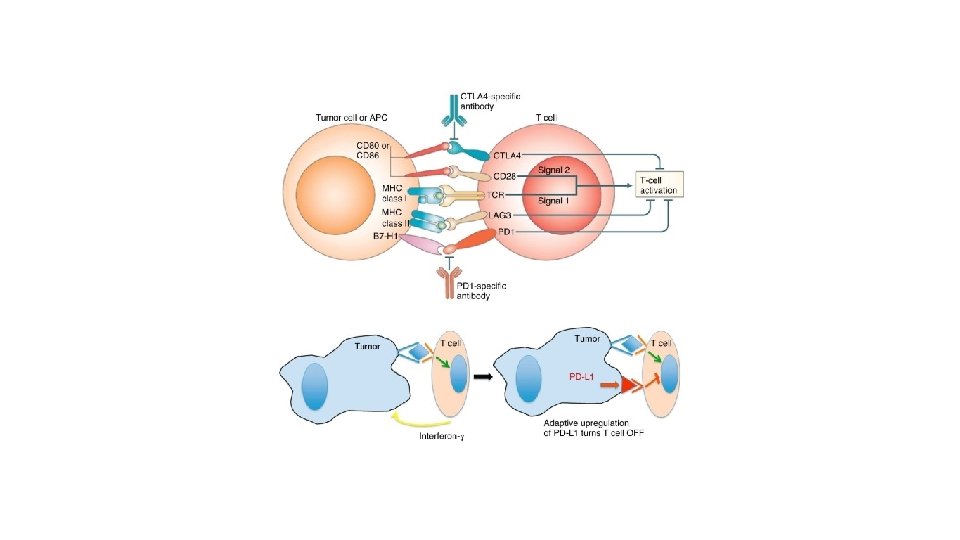
Immunotherapy • Checkpoint inhibitors • • • Pembrolizumab Atezolizumab Nivolumab Avelumab Durvalumab
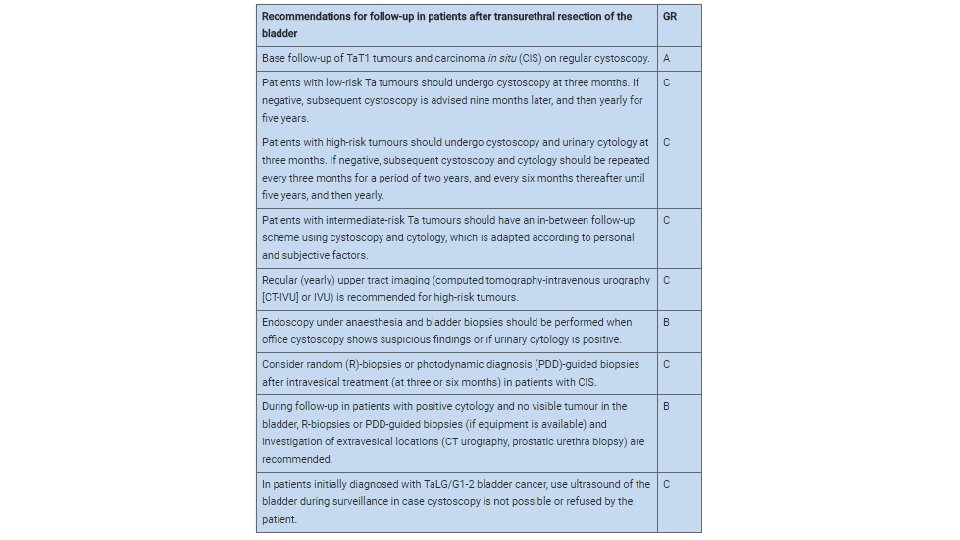

Follow-up of NMIBC As a result of the risk of recurrence and progression, patients with NMIBC need to be followed-up. When planning the follow-up schedule and methods, the following aspects should be considered: • The prompt detection of muscle-invasive and HG/G 3 non-muscle-invasive recurrence is crucial because a delay in diagnosis and therapy can be life-threatening. • The first cystoscopy after TURB at three months is a very important prognostic indicator for recurrence and progression. Therefore, the first cystoscopy should always be performed three months after TURB in all patients with Ta. T 1 tumours and CIS. • In tumours originally intermediate- or high risk, recurrences after ten years tumour-free are not unusual. Therefore, life-long follow-up is recommended. • The follow-up strategy must reflect the risk of extravesical recurrence (prostatic urethra in men and upper urinary tract in both genders). • The risk of upper urinary tract recurrence increases in patients with multiple and high-risk tumours. • Positive urine test results have a positive impact on the quality of performed follow-up cystoscopy. It supports the adjunctive role of urine tests during follow-up. • In patients initially diagnosed with Ta. LG/G 1 -2 BC, ultrasound of the bladder may be a mode of surveillance in case cystoscopy is not possible or refused by the patient.

Follow-up of MIBC • Cystectomy – Metabolic abnormalities, including electrolyte abnormalities and acidosis, are common, and patients with chronic kidney disease and obstructive uropathy may be at increased risk. Chronic acidosis is a risk factor for osteopenia and osteoporosis, so regular monitoring may identify at-risk patients for pharmacologic intervention. For patients treated with cystectomy, we perform laboratory evaluations (ie, urine cytology, liver and renal function tests, and electrolytes) every three months for the first year, every six months for the second and third years, and then annually up to year 5. After year 5, they should be performed as clinically indicated. In addition, computed tomography (CT) imaging (chest, abdomen, and pelvis) is reasonably performed every six months for the first three years, then annually to year 5, and then only as clinically indicated. • Combined-modality approaches – Combined-modality bladder preservation approaches require careful surveillance following therapy for evidence of local recurrence and for detection of new urothelial cancers. For patients who fail to achieve a complete response and for those who subsequently relapse with muscle invasive disease, salvage cystectomy is indicated.
- Slides: 44