tude SAVOR Diabte de type 2 maladie CV
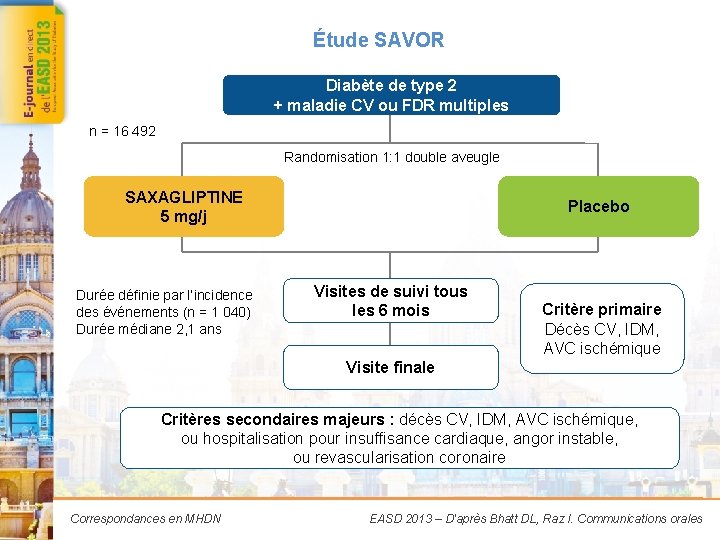
Étude SAVOR Diabète de type 2 + maladie CV ou FDR multiples n = 16 492 Randomisation 1: 1 double aveugle SAXAGLIPTINE 5 mg/j Durée définie par l’incidence des événements (n = 1 040) Durée médiane 2, 1 ans Placebo R Visites de suivi tous les 6 mois Critère primaire Décès CV, IDM, AVC ischémique Visite finale Critères secondaires majeurs : décès CV, IDM, AVC ischémique, ou hospitalisation pour insuffisance cardiaque, angor instable, ou revascularisation coronaire Correspondances en MHDN EASD 2013 – D'après Bhatt DL, Raz I. Communications orales
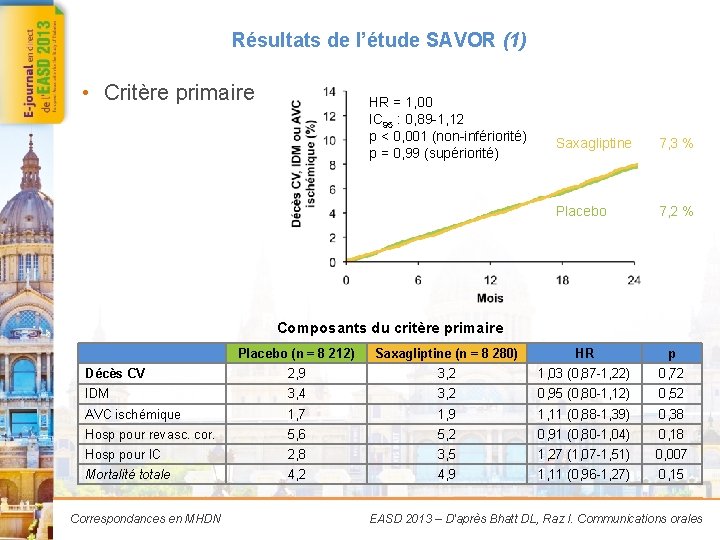
Résultats de l’étude SAVOR (1) • Critère primaire HR = 1, 00 IC 95 : 0, 89 -1, 12 p < 0, 001 (non-infériorité) p = 0, 99 (supériorité) Saxagliptine 7, 3 % Placebo 7, 2 % RComposants du critère primaire Placebo (n = 8 212) Saxagliptine (n = 8 280) HR p Décès CV 2, 9 3, 2 1, 03 (0, 87 -1, 22) 0, 72 IDM 3, 4 3, 2 0, 95 (0, 80 -1, 12) 0, 52 AVC ischémique 1, 7 1, 9 1, 11 (0, 88 -1, 39) 0, 38 Hosp pour revasc. cor. 5, 6 5, 2 0, 91 (0, 80 -1, 04) 0, 18 Hosp pour IC 2, 8 3, 5 1, 27 (1, 07 -1, 51) 0, 007 Mortalité totale 4, 2 4, 9 1, 11 (0, 96 -1, 27) 0, 15 Correspondances en MHDN EASD 2013 – D'après Bhatt DL, Raz I. Communications orales
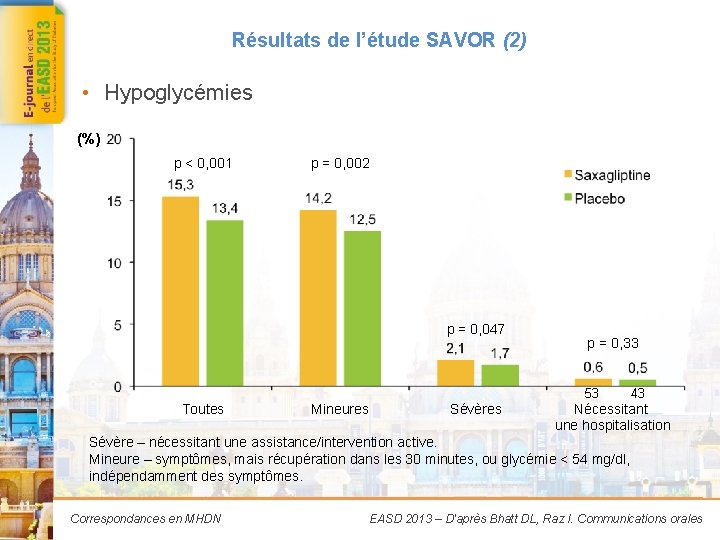
Résultats de l’étude SAVOR (2) • Hypoglycémies (%) p < 0, 001 p = 0, 002 R p = 0, 047 1 264 1 104 Toutes 1 172 1 028 Mineures 177 p = 0, 33 140 Sévères 53 43 Nécessitant une hospitalisation Sévère – nécessitant une assistance/intervention active. Mineure – symptômes, mais récupération dans les 30 minutes, ou glycémie < 54 mg/dl, indépendamment des symptômes. Correspondances en MHDN EASD 2013 – D'après Bhatt DL, Raz I. Communications orales
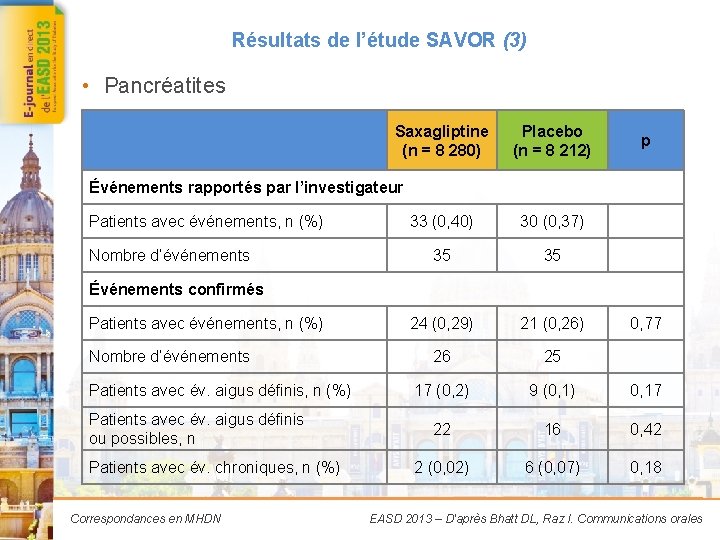
Résultats de l’étude SAVOR (3) • Pancréatites Saxagliptine (n = 8 280) Placebo (n = 8 212) p Événements rapportés par l’investigateur Patients avec événements, n (%) Nombre d’événements 33 (0, 40) 30 (0, 37) 35 35 24 (0, 29) 21 (0, 26) 26 25 17 (0, 2) 9 (0, 1) 0, 17 22 16 0, 42 2 (0, 02) 6 (0, 07) 0, 18 Événements confirmés R n (%) Patients avec événements, Nombre d’événements Patients avec év. aigus définis, n (%) Patients avec év. aigus définis ou possibles, n Patients avec év. chroniques, n (%) Correspondances en MHDN 0, 77 EASD 2013 – D'après Bhatt DL, Raz I. Communications orales
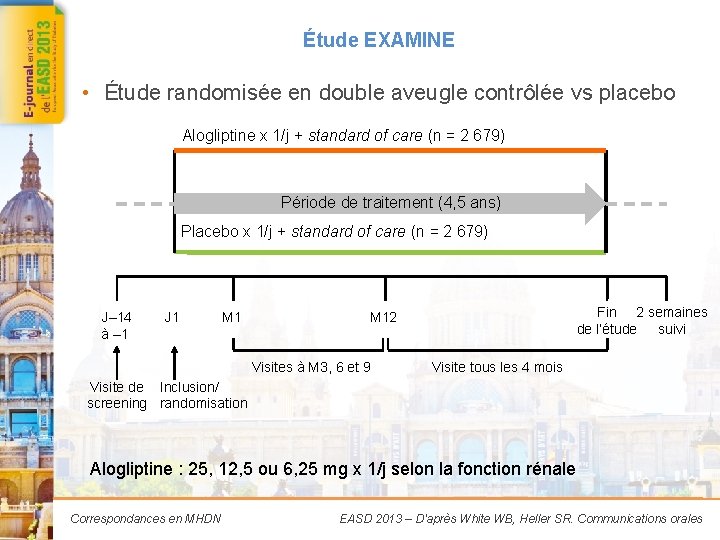
Étude EXAMINE • Étude randomisée en double aveugle contrôlée vs placebo Alogliptine x 1/j + standard of care (n = 2 679) Période de traitement (4, 5 ans) Placebo x 1/j + standard of care (n = 2 679) J– 14 à – 1 J 1 M 1 R Fin 2 semaines de l’étude suivi M 12 Visites à M 3, 6 et 9 Visite tous les 4 mois Visite de Inclusion/ screening randomisation Alogliptine : 25, 12, 5 ou 6, 25 mg x 1/j selon la fonction rénale Correspondances en MHDN EASD 2013 – D'après White WB, Heller SR. Communications orales
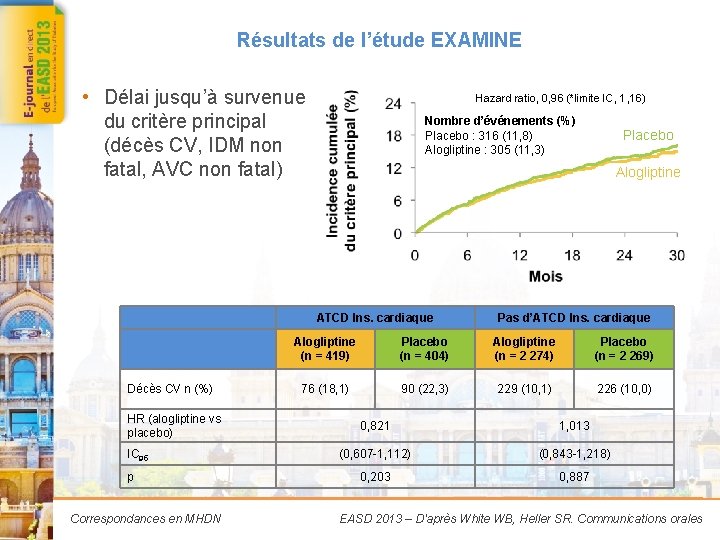
Résultats de l’étude EXAMINE • Délai jusqu’à survenue du critère principal (décès CV, IDM non fatal, AVC non fatal) R Décès CV n (%) HR (alogliptine vs placebo) IC 95 p Correspondances en MHDN Hazard ratio, 0, 96 (*limite IC, 1, 16) Nombre d’événements (%) Placebo : 316 (11, 8) Alogliptine : 305 (11, 3) Placebo Alogliptine ATCD Ins. cardiaque Pas d’ATCD Ins. cardiaque Alogliptine (n = 419) Placebo (n = 404) Alogliptine (n = 2 274) Placebo (n = 2 269) 76 (18, 1) 90 (22, 3) 229 (10, 1) 226 (10, 0) 0, 821 1, 013 (0, 607 -1, 112) (0, 843 -1, 218) 0, 203 0, 887 EASD 2013 – D'après White WB, Heller SR. Communications orales
- Slides: 6