tude de phase II islatravir doravirine rsultats S
- Slides: 4

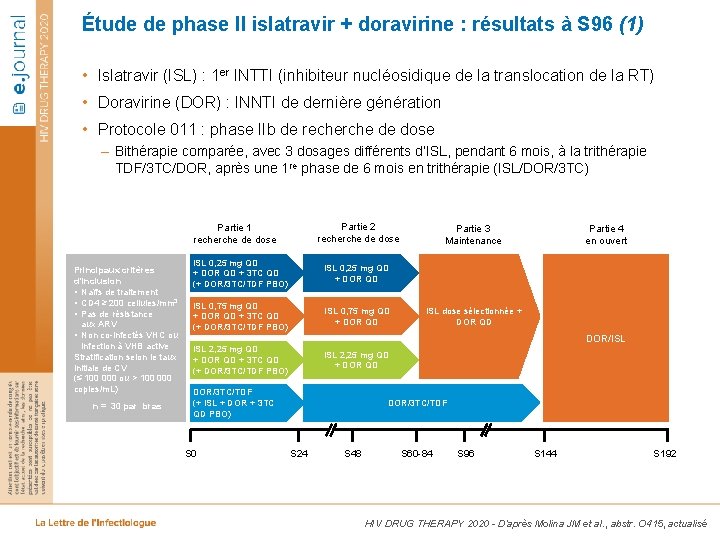
Étude de phase II islatravir + doravirine : résultats à S 96 (1) • Islatravir (ISL) : 1 er INTTI (inhibiteur nucléosidique de la translocation de la RT) • Doravirine (DOR) : INNTI de dernière génération • Protocole 011 : phase IIb de recherche de dose – Bithérapie comparée, avec 3 dosages différents d’ISL, pendant 6 mois, à la trithérapie TDF/3 TC/DOR, après une 1 re phase de 6 mois en trithérapie (ISL/DOR/3 TC) Partie 2 recherche de dose Partie 1 recherche de dose Principaux critères d’inclusion • Naïfs de traitement • CD 4 ≥ 200 cellules/mm 3 • Pas de résistance aux ARV • Non co-infectés VHC ou infection à VHB active Stratification selon le taux initiale de CV (≤ 100 000 ou > 100 000 copies/m. L) n = 30 par bras ISL 0, 25 mg QD + DOR QD + 3 TC QD (+ DOR/3 TC/TDF PBO) ISL 0, 25 mg QD + DOR QD ISL 0, 75 mg QD + DOR QD + 3 TC QD (+ DOR/3 TC/TDF PBO) ISL 0, 75 mg QD + DOR QD Partie 3 Maintenance Partie 4 en ouvert ISL dose sélectionnée + DOR QD DOR/ISL 2, 25 mg QD + DOR QD + 3 TC QD (+ DOR/3 TC/TDF PBO) ISL 2, 25 mg QD + DOR QD DOR/3 TC/TDF (+ ISL + DOR + 3 TC QD PBO) S 0 DOR/3 TC/TDF S 24 S 48 S 60 -84 S 96 S 144 S 192 HIV DRUG THERAPY 2020 - D’après Molina JM et al. , abstr. O 415, actualisé

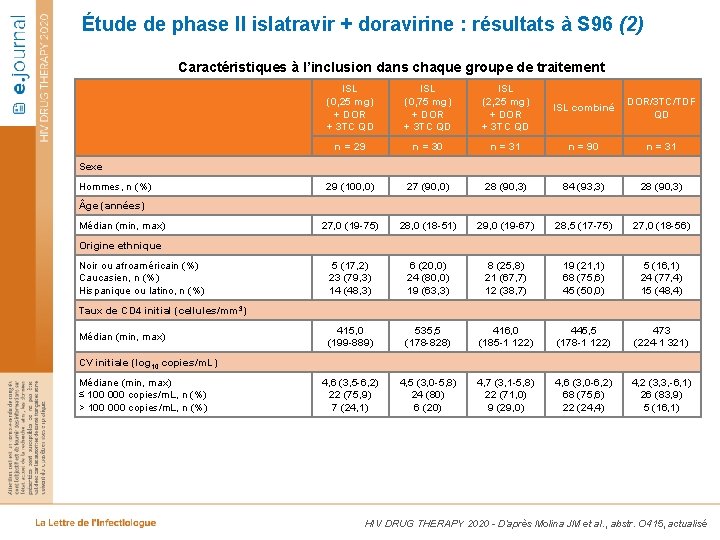
Étude de phase II islatravir + doravirine : résultats à S 96 (2) Caractéristiques à l’inclusion dans chaque groupe de traitement ISL (0, 25 mg) + DOR + 3 TC QD ISL (0, 75 mg) + DOR + 3 TC QD ISL (2, 25 mg) + DOR + 3 TC QD ISL combiné DOR/3 TC/TDF QD n = 29 n = 30 n = 31 n = 90 n = 31 29 (100, 0) 27 (90, 0) 28 (90, 3) 84 (93, 3) 28 (90, 3) 27, 0 (19 -75) 28, 0 (18 -51) 29, 0 (19 -67) 28, 5 (17 -75) 27, 0 (18 -56) 5 (17, 2) 23 (79, 3) 14 (48, 3) 6 (20, 0) 24 (80, 0) 19 (63, 3) 8 (25, 8) 21 (67, 7) 12 (38, 7) 19 (21, 1) 68 (75, 6) 45 (50, 0) 5 (16, 1) 24 (77, 4) 15 (48, 4) 415, 0 (199 -889) 535, 5 (178 -828) 416, 0 (185 -1 122) 445, 5 (178 -1 122) 473 (224 -1 321) 4, 6 (3, 5 -6, 2) 22 (75, 9) 7 (24, 1) 4, 5 (3, 0 -5, 8) 24 (80) 6 (20) 4, 7 (3, 1 -5, 8) 22 (71, 0) 9 (29, 0) 4, 6 (3, 0 -6, 2) 68 (75, 6) 22 (24, 4) 4, 2 (3, 3, -6, 1) 26 (83, 9) 5 (16, 1) Sexe Hommes, n (%) ge (années) Médian (min, max) Origine ethnique Noir ou afroaméricain (%) Caucasien, n (%) Hispanique ou latino, n (%) Taux de CD 4 initial (cellules/mm 3) Médian (min, max) CV initiale (log 10 copies/m. L) Médiane (min, max) ≤ 100 000 copies/m. L, n (%) > 100 000 copies/m. L, n (%) HIV DRUG THERAPY 2020 - D’après Molina JM et al. , abstr. O 415, actualisé

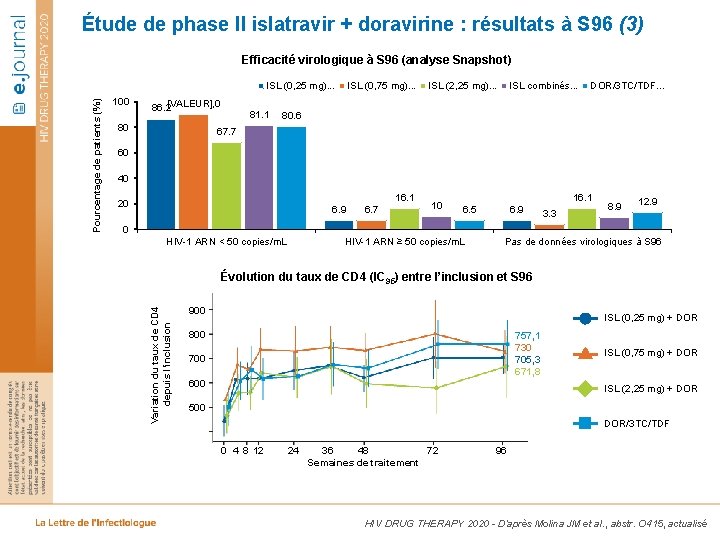
Étude de phase II islatravir + doravirine : résultats à S 96 (3) Efficacité virologique à S 96 (analyse Snapshot) 100 86. 2[VALEUR], 0 80 81. 1 ISL (0, 75 mg). . . ISL (2, 25 mg). . . ISL combinés. . . DOR/3 TC/TDF. . . 80. 6 67. 7 60 40 16. 1 20 6. 9 6. 7 10 16. 1 6. 9 6. 5 3. 3 8. 9 12. 9 0 HIV-1 ARN < 50 copies/m. L HIV-1 ARN ≥ 50 copies/m. L Pas de données virologiques à S 96 Évolution du taux de CD 4 (IC 95) entre l’inclusion et S 96 Variation du taux de CD 4 depuis l’inclusion Pourcentage de patients (%) ISL (0, 25 mg). . . 900 ISL (0, 25 mg) + DOR 800 757, 1 730 705, 3 671, 8 700 600 ISL (0, 75 mg) + DOR ISL (2, 25 mg) + DOR 500 DOR/3 TC/TDF 0 4 8 12 24 36 48 72 Semaines de traitement 96 HIV DRUG THERAPY 2020 - D’après Molina JM et al. , abstr. O 415, actualisé

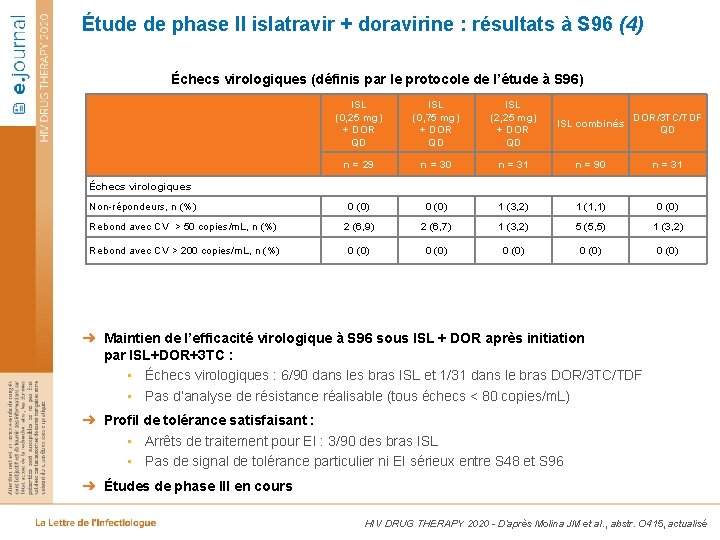
Étude de phase II islatravir + doravirine : résultats à S 96 (4) Échecs virologiques (définis par le protocole de l’étude à S 96) ISL (0, 25 mg) + DOR QD ISL (0, 75 mg) + DOR QD ISL (2, 25 mg) + DOR QD ISL combinés DOR/3 TC/TDF QD n = 29 n = 30 n = 31 n = 90 n = 31 0 (0) 1 (3, 2) 1 (1, 1) 0 (0) Rebond avec CV > 50 copies/m. L, n (%) 2 (6, 9) 2 (6, 7) 1 (3, 2) 5 (5, 5) 1 (3, 2) Rebond avec CV > 200 copies/m. L, n (%) 0 (0) 0 (0) Échecs virologiques Non-répondeurs, n (%) ➜ Maintien de l’efficacité virologique à S 96 sous ISL + DOR après initiation par ISL+DOR+3 TC : • Échecs virologiques : 6/90 dans les bras ISL et 1/31 dans le bras DOR/3 TC/TDF • Pas d’analyse de résistance réalisable (tous échecs < 80 copies/m. L) ➜ Profil de tolérance satisfaisant : • Arrêts de traitement pour EI : 3/90 des bras ISL • Pas de signal de tolérance particulier ni EI sérieux entre S 48 et S 96 ➜ Études de phase III en cours HIV DRUG THERAPY 2020 - D’après Molina JM et al. , abstr. O 415, actualisé