TS chimie chapitre 7 CINTIQUE ET CATALYSE Observer

TS chimie chapitre 7 CINÉTIQUE ET CATALYSE

Observer des réactions lentes et rapides. • Les transformations chimiques ne se produisent pas toujours instantanément. (ex : formation de la rouille : oxydation du Fer) • Comment évaluer leur durée ? Est-il possible de la modifier ?

Observer des réactions lentes et rapides • Protocole expérimental : • Introduire 10 m. L d’une solution aqueuse de permanganate de potassium acidifiée (2, 0. 10 -2 mol. L-1) dans deux béchers de 100 m. L. • Ajouter simultanément 10 m. L d’une solution aqueuse de peroxyde d’hydrogène (1, 0. 10 -1 mol. L-1) (H 2 O 2 eau oxygénée)dans un bécher, et 10 m. L d’une solution aqueuse d’acide oxalique (1, 0. 10 -1 mol. L-1) dans un autre bécher et relever la durée nécessaire pour observer la décoloration totale de la solution.

X 2 X 5

Parmi les espèces mises en jeu, seuls les ions permanganate colorent le milieu. Expliquer pourquoi la durée nécessaire à la décoloration de la solution coïncide avec la durée de réaction Les ions permanganates réagissent avec le peroxyde d’hydrogène ou avec l’acide oxalique et sont les réactifs limitant. Les réactions s’arrêtent donc quand les ions permanganates sont consommés, et donc lorsque les solutions deviennent incolores.

www. youtube. com/embed/_ge. DJJdwens 1. Quelle est la transformation chimique la plus rapide ? Permanganate de potassium + peroxyde d’hydrogène : rapide (quasiment instantanée) Permanganate de potassium + acide oxalique : 4 min

Modifier la durée de réaction. • Divers paramètres, appelés facteurs cinétiques, agissent sur la rapidité d’évolution d’un système chimique. Quels peuvent être ces facteurs ? Ces facteurs peuvent être la concentration, la température.

Premier facteur cinétique : La concentration • Proposer un protocole permettant de mettre en œuvre l’influence d’un de ces facteurs. On étudie la réaction lente entre les ions permanganate et les l’acide oxalique, on fait varier les concentrations de ces solutions puis on mesure le temps nécessaire pour que les réactions s’effectuent complètement. On dilue au 1/10 e chacune des solutions de façon à avoir deux nouvelles solutions moins concentrées. Protocole de la dilution à faire écrire aux élèves.

PROTOCOLE DE DILUTION Le facteur de dilution étant de 10, le rapport entre le volume de solution fille préparée (fiole jaugée) et le volume de solution mère prélevée (pipette jaugée) doit entre de 10 • A l’aide d’une pipette jaugée de 10 m. L, préalablement rincée avec la solution, on prélève 10 m. L de solution mère de permanganate de potassium que l’on introduit dans une fiole jaugée de 100 m. L • On ajoute de l’eau distillée jusqu’à la moitié (ou ¾ ) de la fiole ; on bouche et on agite. On complète avec de l’eau distillée jusqu’au trait de jauge, on bouche et on homogénéise la solution

Mettre en œuvre le protocole et noter vos résultats sous forme de tableau t 2, 0. 10 -2 mol. L-1 1, 0. 10 -1 mol. L-1 4 min 2, 0. 10 -3 mol. L-1 1, 0. 10 -2 mol. L-1 26 min 2, 0. 10 -4 mol. L-1 1, 0. 10 -3 mol. L-1 Encore plus long Conclusion : La durée de la réaction augmente lorsque la concentration des réactifs en solution diminue. On a garder le même rapport entre les quantités d’ions permanganate et d’acide oxalique

Deuxième facteur cinétique : La température • Proposer un protocole permettant de mettre en œuvre l’influence d’un de ces facteurs. On reprend la première expérience avec les ions permanganate et l’acide oxalique et on fait varier la température : bain de glace et bain marie (eau chaude du robinet).
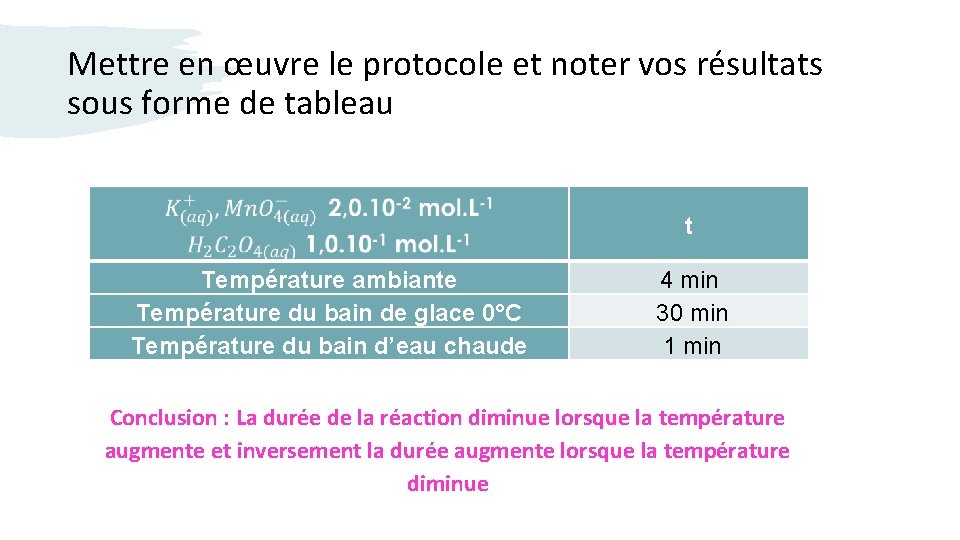
Mettre en œuvre le protocole et noter vos résultats sous forme de tableau t Température ambiante Température du bain de glace 0°C Température du bain d’eau chaude 4 min 30 min 1 min Conclusion : La durée de la réaction diminue lorsque la température augmente et inversement la durée augmente lorsque la température diminue

La catalyse https: //www. youtube. com/embed/55 p 4 A 1 IGGp. A La catalyse • Un catalyseur est un corps qui accélère une transformation chimique, sans être modifié ou en étant consommé puis régénéré. Il peut accélérer une transformation spontanée mais il ne peut en aucun cas déclencher une transformation impossible. • Il existe trois types de catalyse : • La catalyse hétérogène si les réactifs et le catalyseur n’appartient pas à la même phase. • La catalyse homogène si les réactifs et le catalyseur sont miscibles entre eux et ne forment qu’une seule phase. • La catalyse enzymatique : Les molécules biologiques agissant comme catalyseur sont appelées enzymes: ce sont des protéines. La catalyse enzymatique est un cas particulier de la catalyse hétérogène : les réactifs sont en solution dans la même phase que le catalyseur. Au niveau mécanisme, elle s’apparente à la catalyse hétérogène.


Protocole expérimental : Dans trois béchers marqués A, B et C verser 10 m. L d’eau oxygénée à 20 volumes. Le bécher A sert de témoin. Dans le bécher B, introduire un petit cylindre de platine utilisé pour la désinfestation et le nettoyage des lentilles cornéennes. Dans le bécher C, introduire quelques gouttes de chlorure de fer (III) à 1, 0 mol. L -1. Dans un quatrième bécher marqué D, introduire un petit morceau de radis et de l’eau oxygénée à l’aide d’une pipette plastique.

Observations expérimentales • Bécher A Pourquoi n’observe-t-on pas ou très peu de dégagement de dioxygène dans ce bécher ? La décomposition de l’eau oxygénée est une réaction très lente, donc pas ou très peu de dégagement gazeux. verser 10 m. L d’eau oxygénée à 20 volumes. Le bécher A sert de témoin.

Observations expérimentales verser 10 m. L d’eau oxygénée à 20 volumes. Dans le bécher B, introduire un petit cylindre de platine utilisé pour la désinfestation et le nettoyage des lentilles cornéennes. https: //www. youtube. com/embed/4 vqnz 9 OTRbg • Bécher B Qu’observe-t-on ? Où se produit la réaction chimique ? Comment optimiser l’effet du catalyseur. • On observe un dégagement gazeux à la surface du platine. On peut augmenter la surface du platine pour augmenter la surface de contact et optimiser son effet. Catalyse hétérogène.

Observations expérimentales • Bécher C verser 10 m. L d’eau oxygénée à 20 volumes. https: //www. youtube. com/emb ed/c. Zk. G 4 Rm 64 Yk quelques gouttes de chlorure de fer (III) Qu’observe-t-on ? Expliquer pourquoi on peut considérer que les ions Fe 3+, bien que non consommées, permettent à la réaction d’avoir lieu ? • On observe un dégagement gazeux important. • Changement de couleur : jaune-orange (fer III) puis teinte brune (fer II) puis redevient jaune-orange quand le dégagement cesse • les ions Fe 3+ permettent d’accélérer la réaction (de décomposition de l’eau oxygénée) : dégagement O 2 très important • les ions Fe 3+ sont régénérés à fin de réaction car lorsque l’effervescence Fe 3+ cesse la solution redevient orange catalyseur • les ions Fe 3+ n’apparaissent pas dans équation bilan (faible quantité)

Observations expérimentales verser 10 m. L d’eau oxygénée à 20 volumes. + un morceau de radis https: //www. youtube. com/embed/f. Hm_Qs 3 x_VQ • Bécher D Qu’observe-t-on ? On observe un dégagement gazeux à la surface du radis. Catalyse enzymatique. Catalyse hétérogène. Le radis contient une enzyme la catalase également présente dans le sang. Expliquer pourquoi une effervescence se produit si l’eau oxygénée est versée sur une blessure et pas sur une peau saine. Le sang contient de la catalase qui est une enzyme et permet la décomposition de l’eau oxygénée d’où l’apparition d’une effervescence, ce qui permet de nettoyer les plaies mais ne les désinfecte pas.

Bilan : Facteurs cinétiques • Les paramètres contrôlables susceptibles de modifier la durée d’une transformation chimique sont appelés facteurs cinétiques • Parfois on cherche à diminuer la durée des transformations dans le cas par exemple de synthèse industrielle afin de réduire les coûts énergétiques. • Par contre on veut parfois augmenter la durée d’une transformation. Par exemple pour permettre une conservation plus longue des aliments, on veut augmenter la durée des réactions de dégradation. • Attention un facteur cinétique ne change pas l’état final de la réaction

Bilan : Facteurs cinétiques • Influence de la température • Influence de la concentration Tous les autres paramètres du système étant maintenus constant, plus la température du milieu réactionnel est élevée, plus la durée de la transformation diminue. La température est un facteur cinétique. Tous les autres paramètres du système étant maintenus constant, l’augmentation de la concentration d’au moins un des réactif diminue la durée de la transformation. La concentration est un facteur cinétique.

Bilan : Facteurs cinétiques • Influence du milieu Le solvant est le lieu de la réaction. Présent en excès il n’intervient pas mais il peut à l’échelle microscopique favoriser ou défavoriser la rencontre des réactifs et ainsi modifier la durée de la transformation. Le solvant est un facteur cinétique. • cas particulier de la catalyse

Suivi cinétique https: //www. youtube. com/embed/55 p 4 A 1 IGGp. A
- Slides: 23