TROMBOSE VENOSA EM NEONATOLOGIA Relato de caso clnico

TROMBOSE VENOSA EM NEONATOLOGIA Relato de caso clínico Apresentação: Louise Daameche (R 2 em Pediatria-HUB) Coordenação: Márcia Pimentel de Castro Universidade de Brasília 29/7/2017 www. paulomargotto. com. br

DADOS MATERNOS E GESTACIONAIS: - Idade: 27 anos, G 2 A 0 P 0 C 1 - Tipo sanguíneo: A+ - Patologias maternas: Nega - Complicações nesta gestação: Apresentou ITU no último mês da gestação, RCIU não identificado, oligâmnio, bradicardia fetal severa. - Realizou 8 consultas de pré-natal. - Sorologias: Sorologias maternas: VDRL e HIV ( teste rápido): não reagente

CONDIÇÕES DE NASCIMENTO E DADOS DO RN Data de nascimento: 20/06/2017 às 22: 10 h no Hospital da Rede Hospitalar do DF Parto: cesariano /// BR: no ato Líquido amniótico: meconial Apresentação: cefálica Peso: 2290 kg /// Comprimento: 47 cm /// PC: 29 cm (? ) Sexo: masculino /// Apgar: 1º [2 ] 5º [ 7 ] 10° [8] Idade gestacional: 38 semanas Classificação: RN TERMO+ PIG ASSIMÉTRICO + BAIXO Curva de Margotto PR, 1995 PESO

Condições do nascimento do RN Relato de ter nascido em morte aparente com Apgar 2/7/8. RN recebido em campo estéril, aspirado VAS e entubado na sequência. Saída de pouca quantidade de mecônio da traquéia. Seguido com VPP com O 2 e recuperação da FC e da cor. Houve relato de melhora da FR e tônus gradualmente. Foi extubado na Sala de Parto, colocado sob ventilação não invasiva (VNI) na primeira hora de vida. Realizado cateterismo venoso umbilical com sonda devido falta de cateter adequado no Hospital de origem. Evoluiu grave, taquidispneico, cianótico, sem sopros, Sat O 2 82/84%, com Fi. O 2 de 60%, pulsos não palpáveis. Optado por intubação orotraqueal , iniciado dobutamina, ampicilina + gentamicina + HV. Feita expansão com SF 0, 9% 20 ml/kg. Gasometria após intubação p. H: 7, 05; PCO 2: 25; PO 2: 174; HCO 3: 9, 1 , recebeu nova expansão após resultado de gasometria e uma correção com bicarbonato de sódio.

Paciente admitido dia 21/06/2017 na UTIN do HUB as 16: 30 h ( 18 h de vida ) - Em uso: Ampicilina + gentamicina D 1 Dobutamina 6, 5 mcg/kg/min Adrenalina 0, 27 mcg/kg/min ( dose foi reduzida gradualmente, sendo suspensa a medicação no mesmo dia ) Fentanil 1 mcg/kg/h - Intubado - Edema de tronco superior - Apresentava lesão importante em membro superior direito com edema e sinais de flictema com intensa dor à mobilização. Devido admissão no Hospital Universitário de Brasília (HUB) ter ocorrido com > 6 h de vida, não foi possível a realização do protocolo de hipotermia terapêutica.
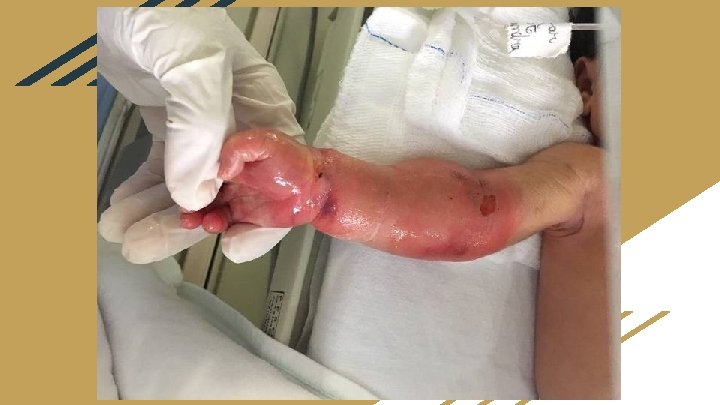
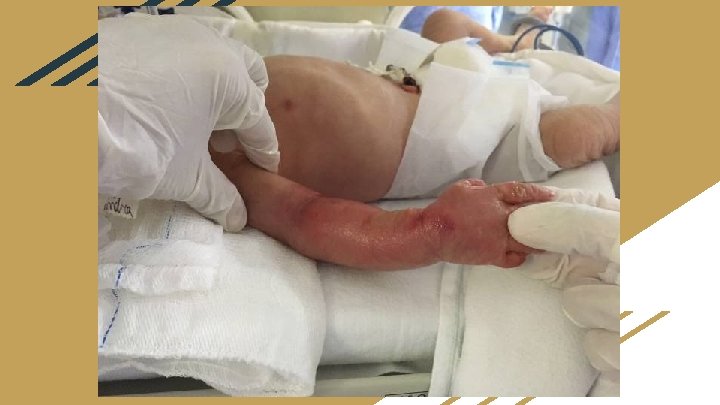
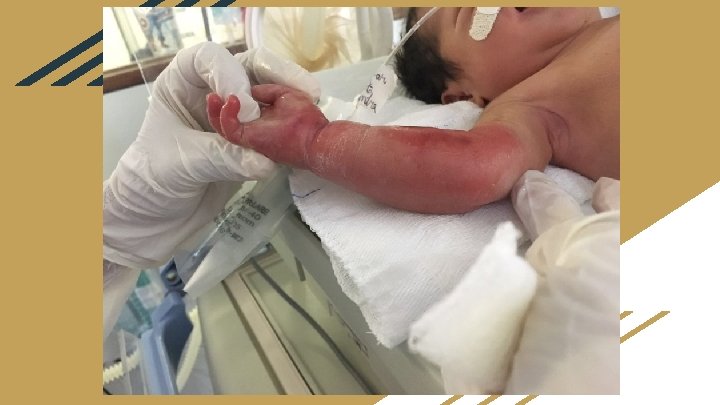

com 48 h de vida. . . ● Retirado sonda umbilical e introduzido novo cateter umbilical, devido impossibilidade de outro acesso. ● Reduzido a dose de dobutamina para 5 ● Iniciado vancomicina ● Realizado 1 dose de oxacilina apenas ● Extubado e iniciado VNI ● Apresentou tremores iniciado fenobarbital com 72 h de vida … ● Suspenso dobutamina e ampicilina ● Houve melhora do padrão respiratório ao ser mantido em ar ambiente.

Com 5 dias de vida … ●Realizado punção de acesso venoso profundo em veia subclávia direita Com 6 dias de vida … ●Apresentou piora do edema de tronco e face sendo necessário furosemida 0, 4 mg/kg/dia. Com 7 dias de vida … ●Foi suspenso nutrição parenteral total (NPT) ●Suspenso Gentamicina ●Aumentado a dose da furosemida 0, 5

Com 8 dias de vida … ●Ultrassonografia (USG) de membro superior direito (MSD) com Doppler sem alterações aparentes. ●USG cerebral: hiperecogenicidade na substância banca cerebral sendo mais importante no hemisfério encefálico direito, associado a desvio faz estruturas da linha média para a esquerda, provavelmente relacionado á hemorragia intracraniana. Recomenda-se, a critério clínico, controle ecográfico. Com 10 dias de vida … ●O RN não apresentou novas crises convulsivas sendo possível suspensão do fenobarbital. Com 11 dias de vida … ●Iniciado cefepima ( pois a lesão em MSD não apresentava melhora ) ●Logo foi evidenciado crescimento de Coco Gram Positivo (CGP) na hemocultura (30/6) sendo suspenso o cefepima com 14 dias de vida.

Com 14 dias de vida … ●Eco. Doppler renal também sem alterações aparentes. ●Após discussão com CCIH foi possível a retirada do CVC em subclávia direita e solicitado novo cateter em outra localização conforme orientações da CCIH devido o crescimento de CGP. Com 15 dias de vida … ●Realizado Ecocardiograma : coarctação de aorta discreta com FOP, e solicitado pela Cardiopediatra Angio TC de tórax para complementar a investigação. ●USG Cerebral: discreta redução da hiperecogenicidade difusa da substância branca cerebral do hemisfério encefálico direito e têmporo-parietal do hemisfério encefálico esquerdo sem desvio significativo das estruturas da linha média. Observam-se pequenas áreas anecogênicas periventriculares à direita, sugestiva de encefalomalácia. Leve dilatação dos ventrículos laterais associado à assimetria desses, sendo menor o direito. Com 16 dias de vida … ●Angio TC de tórax : -Moderada ectasia biliar intra-hepática no lobo esquerdo e leve edema do tecido periportal, opacificação tardia da veia supra-hepática direita. -Áreas focais de hiporrealce no baço, em faixa nos terços superior e inferior, outra subcapsular no terço inferior, provavelmente correspondendo a infartos. Espessamento regular difusa das glândulas adrenais, que exigem hiporrealce medular. -Duplicação da veia cava superior a esquerda drenando também no átrio direito. -Provável trombo luminal central na confluência das veias jugular interna e subclávia esquerdas, bem como no segmento distal da veia subclávia direita. -Trombos luminais centrais nos segmentos proximal e distal da artéria subclávia direita e no segmento proximal da artéria axilar ipsilateral.
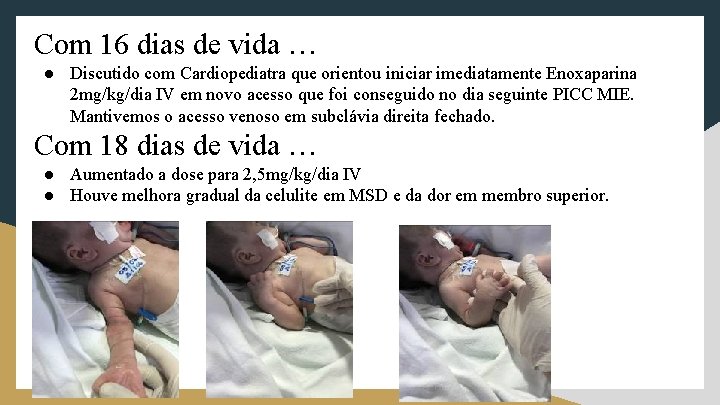
Com 16 dias de vida … ● Discutido com Cardiopediatra que orientou iniciar imediatamente Enoxaparina 2 mg/kg/dia IV em novo acesso que foi conseguido no dia seguinte PICC MIE. Mantivemos o acesso venoso em subclávia direita fechado. Com 18 dias de vida … ● Aumentado a dose para 2, 5 mg/kg/dia IV ● Houve melhora gradual da celulite em MSD e da dor em membro superior.

Com 21 dias de vida … ● Discutido com CCIH o resultado que orientou manter o uso da vancomicina até D 28 devido o risco de tromboflebite séptica, e retirar o cateter venoso central em subclávia direita. ● RM de crânio: com extensa encefalomalácia multicística envolvendo os hemisférios cerebrais, sobretudo os lobos frontais, parietais e temporal direito. Considerar a possibilidade de injúria hipóxico-isquêmica. Produtos de degradação da hemoglobina nos hemisférios cerebrais, sobretudo a direita. Hipersinal de T 1 dos seios sagital superior, reto e transverso esquerdo, que pode estar relacionado a trombose venosa.

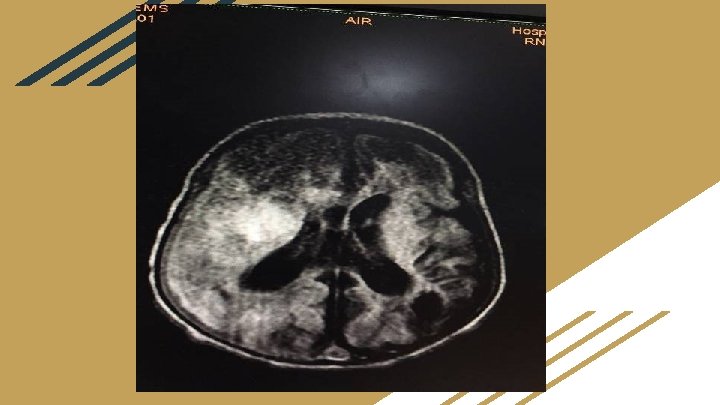
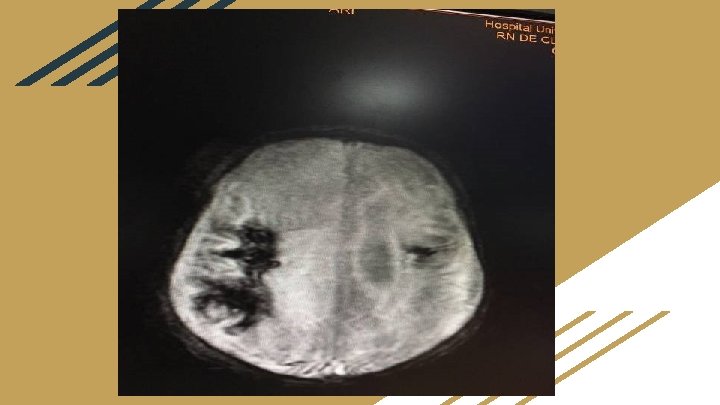
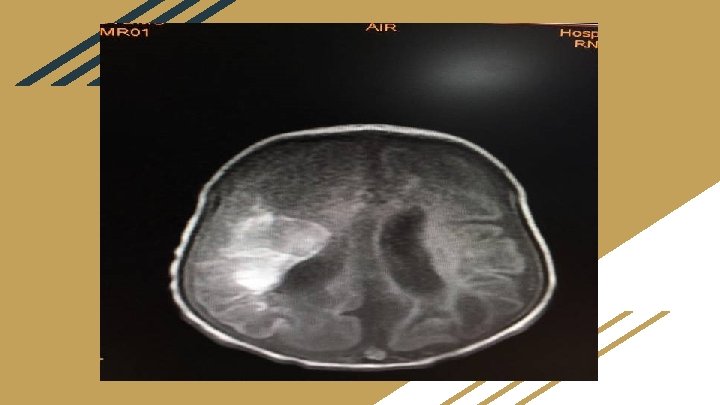

Com 21 dias de vida … ●Após o uso da Enoxaparina houve melhora importante do edema de tronco superior e discretamente da hipertensão. ●Nesse mesmo dia foi discutido com Hematologista sobre o quadro do paciente que orientou a coleta de exames que foram enviados ao Hemocentro com o resultado: -Tempo de protrombina: paciente 11, 7 seg / controle 11, 0 seg/ atividade: 93% ( VR: 70 a 100% )/ relação P/C: 1, 064 ( VR: até 1, 30 ) -RNI 1, 062 ( VR: 1, 08 ) -TTPa: 34, 8 seg ( VR: 25, 2 a 37, 9 seg ) -Fibrinogênio: 271 mg/dl ( VR: 220 a 496 mg/dl ) -Tempo de trombina: TT 19, 8 seg ( VR: 12, 7 a 17, 6 s)/ plasma controle: 14 ( VR: 12, 7 a 17, 6 s ) -Pesquisa de inibidor: TTPa pool plasma normal 30, 5 seg / TTPa paciente: 37, 0 / TTPa 50%: 36, 4 seg / correção em segundos: 0, 5 seg / conclusão: negativo -Anticoagulante lúpico: negativo.

Com 21 dias de vida … ●Realizado TC de crânio e tórax a pedido do Hematologista, pois se houvesse piora do sangramento seria possível o uso de fibrinogênio, exame sem alteração dos anteriores. ●Optado após a discussão de manter Enoxaparina 2 mg/kg/dia SC. Com 27 dias de vida … ●Identificamos CGP = S. epidermidis Com 28 dias de vida … ●Realizado exame no Hemocentro com seguinte resultado: -Fator XIII: presente, o que descartou a disfibrinogenemia. Com 29 dias de vida … ●Exame realizado no Sabin: Anticardiolipina Ig. G e Ig. M negativo. Com 1 mês e 1 dia de vida … ●Foi suspenso a Vancomicina em seu D 28 e suspenso o PICC MIE.

Exames laboratoriais
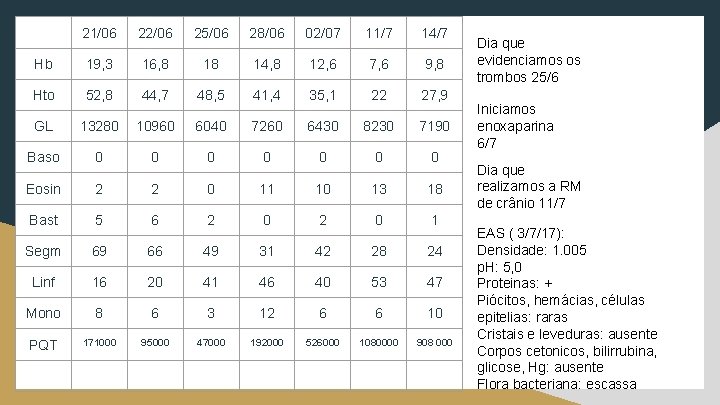
21/06 22/06 25/06 28/06 02/07 11/7 14/7 Hb 19, 3 16, 8 18 14, 8 12, 6 7, 6 9, 8 Hto 52, 8 44, 7 48, 5 41, 4 35, 1 22 27, 9 GL 13280 10960 6040 7260 6430 8230 7190 Baso 0 0 0 0 Eosin 2 2 0 11 10 13 18 Bast 5 6 2 0 1 Segm 69 66 49 31 42 28 24 Linf 16 20 41 46 40 53 47 Mono 8 6 3 12 6 6 10 PQT 171000 95000 47000 192000 526000 1080000 908 000 PCR 1, 88 0, 43 Dia que evidenciamos os trombos 25/6 Iniciamos enoxaparina 6/7 Dia que realizamos a RM de crânio 11/7 EAS ( 3/7/17): Densidade: 1. 005 p. H: 5, 0 Proteinas: + Piócitos, hemácias, células epitelias: raras Cristais e leveduras: ausente Corpos cetonicos, bilirrubina, glicose, Hg: ausente Flora bacteriana: escassa
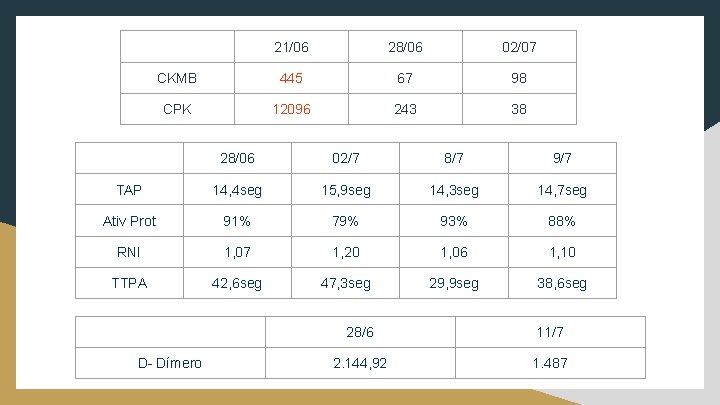
21/06 28/06 02/07 CKMB 445 67 98 CPK 12096 243 38 28/06 02/7 8/7 9/7 TAP 14, 4 seg 15, 9 seg 14, 3 seg 14, 7 seg Ativ Prot 91% 79% 93% 88% RNI 1, 07 1, 20 1, 06 1, 10 TTPA 42, 6 seg 47, 3 seg 29, 9 seg 38, 6 seg D- Dímero 28/6 11/7 2. 144, 92 1. 487

Trombose em Neonatologia

A trombose neonatal pode resultar na morte ou em grave morbidade para o RN por causa de lesões irreversíveis aos órgãos. ( Cérebro / Hepático / Esplênico ) Incidência de tromboembolismo venoso sintomático em neonatos é de 0, 24/10. 000. Trombos ocorrem em cerca de 30% de todos os cateterismos venosos umbilicais, mas em sua grande maioria são assintomáticos. A trombose venosa renal é a modalidade de trombose mais frequentemente diagnosticada nas UTI neonatais. 89% estão associadas com a presença de cateter venoso central e 29% com infecção sistêmica. As veias femorais são o segundo sítio mais comum de trombose associada a cateter venoso. Vasos afetados mais raramente incluem a braquiocefálica, subclávia, jugular e ilíacas.

As tromboses arteriais são em sua maioria iatrogênicas e afetam tipicamente a aorta ou as artérias ilíacas e femorais. Quando é feito cateterismo arterial umbilical, a trombose pode ser encontrada em 23% dos bebês, mas a maioria é assintomática e não requer tratamento. A mortalidade é de 5% para trombose venosa renal (TVR), 18% para outros tipos de tromboses, 21% para as tromboses arteriais e 25% para as tromboses mistas (venosas e arteriais). QUADRO CLÍNICO Edema do membro afetado, da cabeça, região cervical ou tórax. Insuficiência respiratória, apnéias e bradicardia, trombocitopenia e sepse persistente são sintomas menos comuns. A trombose arterial leva a diminuição de pulsos e descoloração do membro afetado. A trombose da aorta pode levar a hipertensão sistêmica ou a uma clínica de redução dos pulsos e da perfusão que mimetiza uma coarctação de aorta, mas com ecocardiograma normal. Os distúrbios específicos da coagulação são raros.

DIAGNÓSTICO: A ultrassonografia com Doppler é o método mais usado para o diagnóstico (68% dos casos) por ser não invasiva e pode ser realizada a beira do leito. A venografia é o exame complementar de diagnóstico clássico. Não podemos esquecer que também pode ser utilizado a Angio TC para identificação do trombo. TRATAMENTO Neonatos com Tromboembolismo Venoso: devem ser removidos, se possível, após 3 a 5 dias de anticoagulação, com o objetivo de evitar a liberação de êmbolos (essa recomendação não tem evidência em estudos clínicos).

Cateter Umbilical Arterial: Para manter a patência do cateter umbilical arterial, manter infusão de dose baixa de heparina convencional (0, 25 a 1 U/m. L). heparina ou enoxaparina por pelo menos 10 dias e remover o cateter. Para neonatos com trombose relacionada a cateter umbilical arterial comprometimento grave da perfusão de membros ou órgãos, iniciar trombólise com t. PA ( ativador de plasminogênio tecidual ). Se a trombólise for contraindicada, realizar trombectomia cirúrgica. Manter o cateter arterial umbilical em posição alta em vez de baixa.
Trombose de seio venoso cerebral: Para neonatos com trombose de seio venoso cerebral (TSVC) sem hemorragia intracraniana significativa, iniciar heparina convencional ou enoxaparina e depois manter enoxaparina por pelo menos 6 semanas, mas durante não mais que 3 meses. Para neonatos com TSVC com hemorragia significativa, manter monitorização radiológica durante 5 a 7 dias e anticoagulante se houver propagação do trombo. Cirurgia está recomendada para os neonatos com hidrocefalia ou hematomas cerebrais grandes com efeito de massa. Acidente vascular cerebral isquêmico: Trombose neonatal Alexandre Peixoto Serafim (Capítulo do Livro Assistência ao Recém-Nascido de Risco, ESCS, Brasília, 3ª Edição, 2013) Link Para Download: https: //drive. google. com/open? id=0 B 5 b 9 f. O W 0 r. J 3 SRk. Rp. UFMw. VUx. JZj. A (ponha no seu Smartphone!)

SÍNDROME DO ANTICORPO ANTIFOSFOLÍPIDE

SAF …. vamos ver no geral. . . Anticorpos antifosfolípides consistem de ambos, anticorpos anticoagulante lúpico e anticardiolipina e são um grupo heterogêneo de anticorpos que reagem com proteínas ligadas aos fosfolipídios e interfere com os testes de coagulação. Na verdade ele não atua como anticoagulante e está associado a fenômenos trombóticos, sendo uma causa importante de trombofilia adquirida. O mecanismo pelo qual o anticorpo antifosfolípide causa trombose não está totalmente estabelecido (a interação dos anticorpos anticardiolipina com a beta 2 -glicoproteína I, levando a inibição da proteína C, proteína S, plaquetas e outros fatores da coagulação e a interação dos anticorpos lúpicos com lipídeos ligados a protrombina, levando a inibição da proteína C, cria um estado hipercoagulante). Os dados laboratoriais para o diagnóstico incluem a presença de anticardiolipina do tipo Ig. G em título maior que 10 Unidades GPL ou presença de anticoagulante lúpico ou ainda a presença de anticardiolipina Ig. M associada ao anticoagulante lúpico.

No estudo de de. Veber e cl, envolvendo 92 crianças (RN a 18 anos de idade) com tromboembolismo cerebral, o anticorpo anticardiolipina esteve presente em 33% dos casos (23 pacientes), constituindo a mais freqüente anormalidade protrombótica. O papel dos anticorpos antifosfolípides adquiridos por passagem transplacentária no desencadeamento de trombose, segundo Ravelli e Martini, não está ainda totalmente esclarecido. Excetuando a trombose renal, a trombose de forma geral é rara nestes pacientes com estes anticorpos adquiridos via transplacentária. Na maioria das vezes está associada a cateteres (fator trombofílico). Hemorragia intraventricular e talâmica em um recém-nascido a termo com aumento de anticorpos antifosfolípides Paulo R. Margotto

SAF em neonatologia ● Anticorpo antifosfolípide (APA) é a designação genérica que descreve o grupo heterogêneo de auto-anticorpos contra fosfolípides de carga negativa ou proteína-ligantes plasmáticas. ● A síndrome de anticorpo antifosfolípide ou síndrome antifosfolípide (SAF) é caracterizada por trombose arterial, venosa ou microvascular associadas com a persistência de anticorpos antifosfolípides circulantes.

Critérios diagnósticos: (2) e revisados critérios de Sapporo recentemente em Sidney Define-se a SAF pela presença de um critério clínico: - trombose vascular e um critério laboratorial: - títulos médios ou altos de anticorpo anticardiolipina Ig. G e/ou Ig. M com título clinicamente significativo (> 40 GPL ou MPL), teste do anticoagulante lúpico ou anticorpo anti-beta 2 glicoproteína I (anti. B 2 GPI) de classe Ig. G e/ou Ig. M.

SAF na atualidade. . . A SAF primária é rara, assim como a SAF na faixa etária pediátrica. Em um estudo de coorte, o início da SAF ocorreu antes dos 15 anos em 2, 8% dos pacientes. Ainda não há critérios válidos para o diagnóstico da SAF pediátrica , mas análise das séries de casos publicados até o presente indica as suas características singulares. Um registro internacional de SAF pediátrica foi recentemente proposto na Paediatric Rheumatology European Society (PRES), com base nos critérios de Sidney


Viabilidade e segurança da dosagem de enoxaparina em miligramas inteiros em prematuros e recém-nascidos a termo Feasibility and safety of enoxaparin whole milligram dosing in premature and term neonates. Goldsmith R, Chan AK, Paes BA, Bhatt MD; Thrombosis and Hemostasis in Newborns (THi. N) Group. J Perinatol. 2015 Oct; 35(10): 852 -4 A terapia anti-trombótica foi iniciada com enoxaparina subcutânea na dose inicial de 1, 5 mg/kg para recém nascidos a termo e 1, 7 mg/kg para recém-nascidos prematuro, arredondado para o miligrama mais próximo, sendo administrada duas vezes ao dia. Enoxaparina foi subsequentemente titulada para manter um nível de anti-Xa compreendido entre 0, 5 e 1, 0 UI /L. Este é o primeiro estudo a relatar especificamente sobre a viabilidade e segurança da dosagem em miligrama da enoxaparina em recém-nascidos quais 47, 5% eram prematuros. Apesar de ser menor em peso em comparação com neonatos a termo, recém-nascidos prematuros podem tolerar arredondamento das doses de enoxaparina para miligramas inteiros sem aumento dos níveis supraterapêuticos ou episódios hemorrágicos Viabilidade e segurança da dosagem de enoxaparina em miligramas inteiros em prematuros e recém-nascidos a termo R Goldsmith, AK Chan, BA Paes, MD Bhatt. Apresentação: Dhouglas Diniz Mota, Paula Nunes Pinto Jubé, Paulo R. Margotto

Um raro caso de Sd Antifosfolípide Neonatal Estudo sobre uma criança de 6 meses com história de convulsões, atraso no desenvolvimento psicomotor, hemiparesia D e diminuição da acuidade a direita. Nasceu com 38 semanas de parto normal com apgar 9/9. A mãe notou hipotrofia facial E desde o primeiro dia de vida e diminuição do uso de MSD. Com 3 meses de vida apresentou estrabismo divergente e convulsão. Com RM cerebral apresentando isquemia cerebral em hemisfério cerebral E em território arterial. Com anticardiolipina Ig. G aumentada 17 UI/ml e Ig. G beta GL P 1 aumentado 59 UI/ml e houve mutação genética G 1691 do fator V de Leiden.

Desfecho do caso clínico Paciente encontra-se estável hemodinamicamente, sem acesso venoso, em ar ambiente, fazendo uso de enoxaparina, com boa aceitação da dieta associado ao seio materno, continuará o acompanhamento com a equipe de Pediatria, Hematologia e Cardiopediatria após a alta hospitalar. Ainda em investigação: Mutação do Fator V de Leiden e da protrombina.

Conclusão -O diagnóstico ficou mesmo com sepse por Staphylococcus associada a cateterismo venoso feito com SONDA no Hospital de origem e repetido com 36 h no HUB com cateter apropriado (cateterismo venoso tardio). -As principais etiologias: infecção e cateter venoso profundo. -A punção de VEIA SUBCLÁVIA DIREITA foi do lado que tinha a lesão do braço. O cateter foi trocado e repuncionado na mesma veia !!!! -Parece-nos que foram todos esses fatores que contribuíram para a trombose. No entanto, ainda em investigação: Mutação do Fator V de Leiden e da protrombina

REFERÊNCIAS 1. Serafim, A. Trombose neonatal In. Margotto PR. Assistência ao Recém-Nascido de Risco, Brasília, ESCS, 3ª Edição, 2013 pg. 317 -321 2. Hemorragia Intraventricular e talâmica em um recém-nascido a termo com aumento de anticorpos antifosfolípides: Paulo R. Margotto (dispnível em www. paulomargotto. com. br) 3. Michaels LA, Gurian M, Hegyi T, Drachtman RA. Low molecular weight heparin in the treatment of venous and arterial thromboses in the premature infant. Pediatrics. 2004; 114(3): 703 -7. 4. Sato JO, Carvalho SM, Magalhães CS. Apresentação pediátrica da síndrome antifosfolípide. Rev. Bras. Reumatol 2008; 48 (6): 366 -372 5. Um raro caso de Sd Antifosfolípide neonatal. 6. Palaré, MJ, Mendes P, Ferrão A et al. Trombose Venosa Profunda em Pediatria: Acta Pediatr. Port 2002 (5); 33: 363 -67

Nota do Editor do site, Dr. Paulo R. Margotto. Consultem também! Aqui e Agora! Estudando Juntos! pmargotto@gmail. com
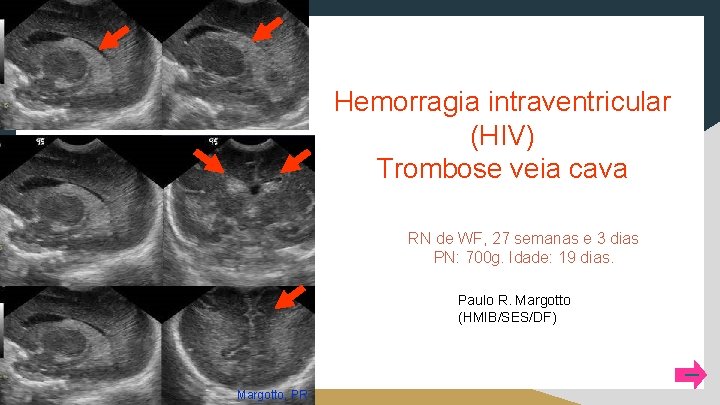
Hemorragia intraventricular (HIV) Trombose veia cava RN de WF, 27 semanas e 3 dias PN: 700 g. Idade: 19 dias. Paulo R. Margotto (HMIB/SES/DF) Margotto, PR

Neonatal venous cerebral hemorrhage. Report of two cases. Misra SN, Misra AK. Neurosurg Focus. 2003 Oct 15; 15(4): E 5. PMID: 15344898. (Austrália) RN de 27 semanas com acesso jugular-HIV com 36 dias-Trombose na veia cava superior. Heparina de baixo Peso molecular-1, 5 mg/kg subcutânea 2 x/dia- Melhora da HIV 4 semanas depois da remoção do cateter RN de 38 semanas com cateter femoral-HIV com 24 dias-Trombose na veia cava inferior Com heparina de baixo peso molecular, resolução da HIV com 2 semanas A presença de hipertensão venosa com pressão retrógrada no tecido cerebral predispõe a alterações intracranianas. Investigações cardiovasculares neonatais demonstraram que 49% do débito cardíaco em recém-nascidos é do retorno da veia cava superior. Há um significante fluxo de retorno cerebral via veia cava inferior com o potencial para congestão retrógrada Por outro lado trombose na cava inferior resulta em congestão venosa retrógrada Elevação da pressão da veia cava superior tem sido associada com elevação da pressão do LCR
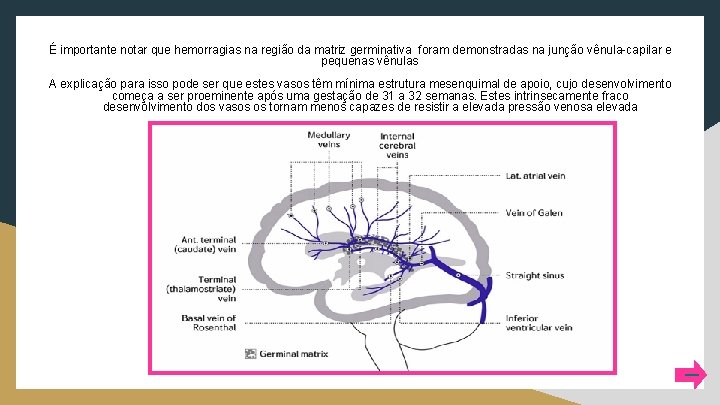
É importante notar que hemorragias na região da matriz germinativa foram demonstradas na junção vênula-capilar e pequenas vênulas A explicação para isso pode ser que estes vasos têm mínima estrutura mesenquimal de apoio, cujo desenvolvimento começa a ser proeminente após uma gestação de 31 a 32 semanas. Estes intrinsecamente fraco desenvolvimento dos vasos os tornam menos capazes de resistir a elevada pressão venosa elevada

Portanto. . A causa da hemorragia intracraniana foi atribuído à congestão venosa cerebral retrógrada devido a trombose tanto da veia cava superior como inferior! EXOXAPARINA (Clexane. R): Heparina de baixo peso molecular é a forma de anticoagulação mais usada nas UTI neonatais atualmente. As vantagens supostas incluem farmacocinética previsível, administração subcutânea, ausência de interferência por outras drogas ou dieta, risco diminuído de trombocitopenia e de osteoporose. Pré-termos: Dose: 2 mg/kg/dose cada 12 horas /Termos: SC 1, 7 mg/kg/dose cada 12 horas SCSC: subcutâneo Devido à alta concentração da enoxaparina, a administração de doses decimais é sujeita a grande incidência de erros. A enoxaparina pode ser diluída para uma concentração de 20 mg/m. L em cloreto de sódio a 0, 9% e permanece estável por até 43 dias em temperatura ambiente (22 -26ºC) ou sob refrigeração. A monitorização deve ser feita com o nível de atividade antifator Xa entre 0, 5 a 1, 0 U/ml em uma amostra colhida de 4 a 6 horas após a injeção subcutânea.

Avaliação e manejo da trombose pós-natal M A Saxonhouse and D J Burchfield. Apresentação: Antenor Couto Neto, Márcio Teixeira de Campos, Ciro Mendes Vargas, Leonardo Alves, Paulo R. Margotto The evaluation and management of postnatal thromboses. Saxonhouse MA, Burchfield DJ. J Perinatol. 2009 Jul; 29(7): 467 -78. doi: 10. 1038/jp. 2009. 14. Epub 2009 Mar 12. Review. PMID: 19279647. Artigo Integral! Na população pediátrica, os neonatos têm o maior risco de tromboembolismo (TE), provavelmente devido ao uso freqüente de cateteres. Este risco aumentado é atribuído a vários fatores de risco. Os ensaios clínicos randomizados que lidam com o manejo de tromboses pós-natais não existem e assim, as opiniões diferem quanto intervenções diagnósticas e terapêuticas ideais. Esta avaliação começa com um estudo de caso real que ilustra a complexidade e a gravidade desses tipos de casos e, em seguida, avalia o sistema hemostático neonatal com discussão sobre os locais comuns de trombose pósparto, fatores de risco perinatais e pró-trombóticos e opções de tratamento potenciais. Uma avaliação passo a passo proposto para os recém-nascidos com tromboses pósnatais sintomáticos serão sugeridas, bem como futuras direções de pesquisa e de registro. Devido à complexidade de acidente vascular cerebral isquêmico perinatal, este tópico não será revisto.


Trombose venosa relacionada a cateter (não cardíaco) -Trombose venosa sintomática tem incidência de 0, 24/ 10000 admissões na UTI, a maioria está relacionada a cateter vemoso (CV). -Mecanismos: lesão de endotélio, alteração do fluxo, infusão de substâncias e materiais trombogênicos. -Cateter umbilical geralmente substituído na 1ª semana, risco de trombose de Veia porta. -Quanto menor o tempo de permanência do cateter menor o risco de trombose. -Padrão ouro é o venograma, porém o mais usado é o ultrassom ( falso negativos). -Complicações da trombose venosa: obstrução venosa crônica, quilo tórax, hipertensão portal e embolismo. -Manejo requer retirada do cateter( 3 -5 dias de terapia anticoagulante).

Fatores Adquiridos Fatores de risco para o tromboembolismo -A presença de cateter venoso central e cateteres arteriais são os maiores riscos adquirido para trombose pós-natal. -Outros fatores de riscos: Vários fatores coexistentes.

Fatores genéticos Avaliação laboratorial para distúrbio protrombótico -Os estudos genéticos enfatizam mutações que resultam em falta ou deficiência severa de fatores inibidores de hemostase. -Desordens homozigóticas protrombóticas (proteína C, S ou antitrombina) -Desordens heterozigóticas protrombóticas

Avaliação da trombose pós-natal clinicamente sintomática -É confuso devido limitado número de estudos -Recomendado: Detalhada história familiar (desordens, história gestacional, etc) -Extensiva pesquisa laboratorial de desordem protrombótica. Avaliação laboratorial para distúrbio protrombótico Prevalência de certos fatores protrombóticos

Manejo da trombose -A complicação mais temida na terapia antitrombótica é a hemorragia intracraniana. Contraindicações absolutas para a terapia antitrombótica: Cirurgias do SNC, asfixia( nos primeiros 10 dias) sangramento ativo, procedimentos invasivos dentro de 3 dias, convulsões Contraindicações: plaquetopenia(abaixo de 50 mil/mm 3), fibrinogênio <100 mg%, INR >2, deficiência severa de coagulação, alergia ao agente entitrombótico Monitorização laboratorial: vide tabela Monitorização laboratorial durante a terapia antitrombótica

Hemorragia intraventricular e talâmica em um recém-nascido a termo com aumento de anticorpos antifosfolípides Paulo R. Margotto RN de ECB, registro. 180704, de parto cirúrgico por parada de progressão, Apgar de 9/10, 40 semanas 3 dias de idade gestacional, peso ao nascer de 3640 g, 7 consultas pré-natais, sem intercorrências na gravidez. No 4º dia de vida apresentou convulsão tônica, seguida de irritabilidade. Na internação, a punção lombar revelou líquido céfaloraquidiano hemorrágico. Usou ampicilina e gentamicina por 4 dias, sendo suspenso quando se afastou infecção. Usado fenobarbital endovenoso para o controle das crises convulsivas. A primeira ecografia cerebral Doppler com transdutor de 5 Mhz foi realizada no 8º dia de vida revelou hemorragia peri/intraventricular grau III bilateral, além de hemorragia talâmica á esquerda. A 2ª ecografia cerebral Doppler com transdutor de 5 MHz, foi realizada 7 dias após (com 15 dias de vida) revelou coágulos em ambos os ventrículos e cisto porencefálico no tálamo esquerdo. A ressonância magnética, realizada no dia 13/8/04, 22 dias após a ocorrência da hemorragia intraventricular, revelou: lesão hemorrágica de 2, 5 x 2 cm no tálamo esquerdo de comportamento hipertenso em todas as seqüências obtidas, traduzindo, portanto, fase subaguda (acima de duas semanas). Observa-se extensão da hemorragia para a região da matriz germinativa, situada na região caudo-talâmica esquerda. Grande dilatação simétrica dos ventrículos laterais, terceiro e quarto ventrículos. Conclusão: hemorragia da matriz germinativa, ocupando o tálamo esquerdo e região caudo-talâmica ipsilateral; moderada hidrocefalia comunicante provavelmente por obstrução da drenagem liquórica nas granulações aracnóides. ( A investigação laboratorial incluiu: plasminogênio, Fator VIII, Fator IX, Fator VII, Tempo de tromboplastina parcial, Tempo de Atividade de Protrombina, contagem de plaquetas (valores normais), Fator V Leiden (negativo), Anticoagulante Lúpico Positivo, Antitrombina III (68%-normal de 80 a 120%), Proteína S (normal), Homocisteína (normal), Anti-cardiolipina Ig. G (normal), Auto-anticorpos anti-cardiolipina Ig. M (elevado) e Teste do pezinho Plus normal (17 -OH progesterona, TSH neonatal, Toxoplasmose Ig. M, ácido fenilpirúvico ou fenilalanina, T 4 neonatal, galactose, biotinidasee, galactose e cromatografia de aminoácidos). Foram realizadas pesquisas da mutação do gene da protrombina, do gene da anti-trombina III e do gene da tetrahidrofolatoredutase, tanto no RN como na mãe, sendo negativas. Os anticorpos antifosfolípides (anticardiolipina Ig. G e anticardiolipina Ig. M) na mãe estavam elevados.

Hemorragia intraventricular no recém-nascido a termo Paulo R. Margotto Capítulo do Livro Assistência ao Recém-Nascido de Risco ESCS, Brasília, 3ª Edição, 2013 Investigação laboratorial para distúrbios trombóticos -tempo de tromboplastina parcial, tempo de atividade de protrombina, fibrinogênio, antitrombina, atividade da proteína S, atividade da proteína C, fatores V, VIII, X e fator Von Willebrand -níveis de plasminogênio-homocisteína -anticorpos maternos anti-fosfolipídicos -análise genética para as deficiências associadas à trombose, incluindo a análise do DNA para a mutação da termolábil metilenotetrahidrofolato redutase Link Para Download: https: //drive. google. com/open? id=0 B 5 b 9 f. OW 0 r. J 3 SRk. Rp. UFMw. VUx. JZj. A (ponha no seu Smartphone!)

Grow e cl descreveram 1 RN de 42 semanas de idade gestacional, 3700 g de peso ao nascer, com convulsões tônico-clônicas generalizadas na 6ª hora de vida, com trombose no seio venoso cerebral associado a homozigoto termolábil metilenotetrahidrofolato redutase (termolábil MTHFR), tanto no recém-nascido como na mãe. A literatura adulta cita que 12 a 21% da população geral é homozigoto para este defeito e 35% da população tem o genótipo heterozigoto. A termolátil MTHRF resulta em hiperhomocisteínemia que tem sido associada à trombose (níveis elevados de homocisteína intra-útero podem levar a injúria oxidativa com conseqüentes anormalidades no endotélio dos seios cerebrais). Os autores enfatizam que atividade convulsiva inexplicada deve orientar para a investigação de fatores de risco protrombóticos (considerar a análise do DNA para mutação da MTHFR, tanto na mãe como no neonato).
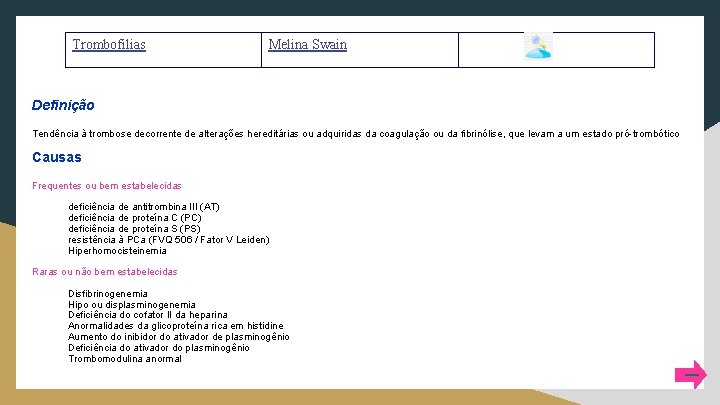
Trombofilias Melina Swain Definição Tendência à trombose decorrente de alterações hereditárias ou adquiridas da coagulação ou da fibrinólise, que levam a um estado pró-trombótico Causas Frequentes ou bem estabelecidas deficiência de antitrombina III (AT) deficiência de proteína C (PC) deficiência de proteína S (PS) resistência à PCa (FVQ 506 / Fator V Leiden) Hiperhomocisteinemia Raras ou não bem estabelecidas Disfibrinogenemia Hipo ou displasminogenemia Deficiência do cofator II da heparina Anormalidades da glicoproteína rica em histidine Aumento do inibidor do ativador de plasminogênio Deficiência do ativador do plasminogênio Trombomodulina anormal

Hiperhomocisteinemia Resultante de anormalidades funcionais das enzimas do metabolismo da metionina ou da deficiência de cofatores enzimáticos com vitamina B 6, B 12 ou ácido fólico. Aumento moderado de homocisteína – variante termolábil da enzima metileno tetrahidrofolato (MTHFR). Transição 677 C →T no gene da MTHFR mudança de Ala-Val → redução na ligação com o ác. Fólico → níveis inferiores aos normais de ác. fólico ativo (que apresenta atividade cofatora no metabolismo da homocisteina). atividade funcional inferior a 50% da forma normal O risco para o desenvolvimento de trombose é variado entre as distintas populações.

Diagnóstico A Avaliação global da coagulação pelo tempo de tromboplastina parcial ativado ou tempo de protrombina não permite identificar pacientes com trombofilia hereditárias (TH). Necessidade da utilização de métodos específicos para cada fator custo elevado limitado a determinados centros. Seleção dos casos Baseado no quadro clínico Reservada para casos onde não há associação com doenças sistêmicas como neoplasias, doenças autoimunes ou síndrome antifosfolípide. A ausência de história familiar não exclui a possibilidade de TH

Testes laboratoriais específicos Testes diagnósticos iniciais Hemograma e esfregaço periférico Tempo de protrombina TTPA Tempo de trombina e Screening para Lupus Anticardiolipina e anticorpo anti β 2 glicoproteina Proteina C ativada Fibrinogênio Protrombina mutante (G 20210 GA) homocisteína

Testes adicionais específicos Mutação do fator V leiden Antitrombina Atividade Proteína C Atividade Proteína S Atividade do Plasminogênio Teste de trombocitopenia induzido por heparina Mutação JAK 2 por PCR

OBRIGADO! Drs. Rafael Saldanha, Márcia Pimentel de Castro e Louise Daameche
- Slides: 63