Troisimes collge Lamartine Hondschoote QCM Chapitre 9 Approche















- Slides: 16

Troisièmes collège Lamartine Hondschoote QCM Chapitre 9 Approche de l’énergie chimique : La pile électrochimique Mr Malfoy

Q 1 Quel métal est utilisé dans la pile de Volta ? A: Le Fer B: Le Nickel C: Le cuivre D: L’or E: Le Plomb Aide: livre p 92

Q 2 Quel métal est utilisé dans la pile de Volta ? A: chrome B: Le Nickel C: Le Zinc D: L’or E: Le Plomb Aide: livre p 92

Q 3 En quelle année Volta a-t-il présenté sa pile ? A: 1600 B: 1700 C: 1800 D: 1900 E: 2000 Aide: livre p 92

Q 4 Comment doit on appeler la solution comprises entre les deux lames de métal ? A: Electrocardiogramme B: Electrode C: Electrolyte D: Electrolitre E: Electromythe Aide: livre p 86

Q 5 Comment doit on appeler les deux lames de métal ? A: Electrocardiogrammes B: Electrodes C : Electrolytes D: Electrolitres E: Electromythes Aide: livre p 86

Q 6 Qu’est-ce qui donne sa couleur à une solution de sulfate de cuivre? A: Les ions cuivre B: Le ciel C: Les ions zinc D: Les ions sulfate E: Les ions fer Aide: livre p 82

Q 7 Comment appelle-t-on les espèces chimiques présentent avant une transformation chimique? A: Des produits B: Des réactants C: Des machins D: Des réactifs E: Des liquides Aide: cours 4ème

Q 8 Comment appelle-t-on les espèces chimiques qui se forment pendant une transformation chimique? A: Des produits B: Des réactants C: Des machins D: Des réactifs E: Des liquides Aide: cours 4ème

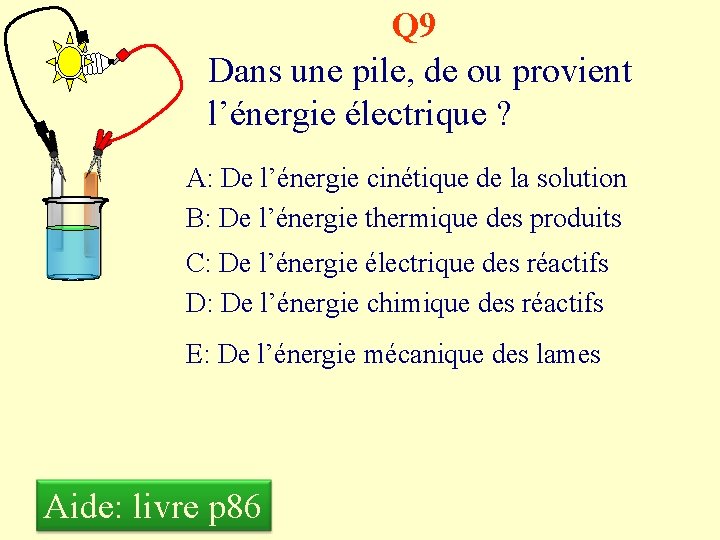
Q 9 Dans une pile, de ou provient l’énergie électrique ? A: De l’énergie cinétique de la solution B: De l’énergie thermique des produits C: De l’énergie électrique des réactifs D: De l’énergie chimique des réactifs E: De l’énergie mécanique des lames Aide: livre p 86

Q 10 Pourquoi une pile s’use ? A: Les produits sont consommés B: Des réactifs apparaissent C: Des réactifs sont consommés D: Le cuivre disparait E: Les ions zinc ont une courte durée de vie Aide: livre p 87

Q 11 Quel ensemble constitue une pile ? A: 2 lames de zinc une solution de Zn. SO 4 B: 2 lames de zinc une solution de Cu. SO 4 C: 1 lame de zinc, 1 lame de cuivre et une solution d’eau déminéralisée D: 2 lames de cuivre une solution de Cu. SO 4 E: 1 lame de zinc, 1 lame de cuivre et une solution de Cu. SO 4 Aide: livre p 86

Q 12 Une pile électrochimique fournit de l’énergie sous forme d’énergie A: cinétique B: déformation C: électrique D: mécanique E: De position Aide: livre p 86

Q 13 Quelle est l’espèce chimique 1 ? A: Fe B: Fe 2+ C: Cu 2+ D: Zn 2+ E: Zn 3+ Aide: livre p 86

Q 14 Quelle est l’espèce chimique 2 ? A: Fe B: Fe 2+ C: Cu 2+ D: Zn 2+ E: Zn 3+ Aide: livre p 86

Q 15 Quelle est la borne positive de la pile? A: Le fil de cuivre B: La solution de sulfate de cuivre C: La lame de zinc D: La lame de cuivre E: La lampe Aide: livre p 86