TRNG THCS TRN HNG O GV NGUYN TH
















- Slides: 30

TRƯỜNG THCS TRẦN HƯNG ĐẠO GV: NGUYỄN THỊ NGỌC OANH Hóa học 9 Chủ đề 3. Hidrocacbon Chủ đề này có 2 bài : Metan và Etilen Các em nên chia vở làm 3 cột theo mẫu sau Nội dung I. Tính chất vật lí II. Cấu tạo phân tử III. Tính chất hóa học IV. Ứng dụng Metan Etilen

Nội dung bài học • • I. Tính chất vật lí II. Cấu tạo phân tử III. Tính chất hóa học IV. Ứng dụng

I. Trạng thái thiên nhiên- tính chất vật lý • Quan sát các hình ảnh sau, em hãy cho biết khí Metan có nhiều ở đâu? MỎ DẦU Khí hầm biogas MỎ THAN

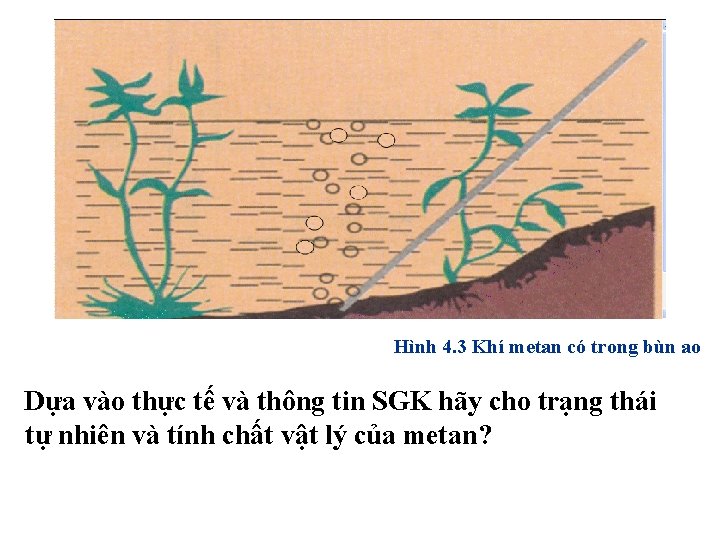
Hình 4. 3 Khí metan có trong bùn ao Dựa vào thực tế và thông tin SGK hãy cho trạng thái tự nhiên và tính chất vật lý của metan?

I. Trạng thái tự nhiên-Tính chất vật lí - Metan có nhiều trong các mỏ khí, mỏ dầu, mỏ than, trong bùn ao, trong khí biogas. - Metan là chất khí, không màu, không mùi, nhẹ hơn không khí ( d = 16/29 ), rất ít tan trong nước.

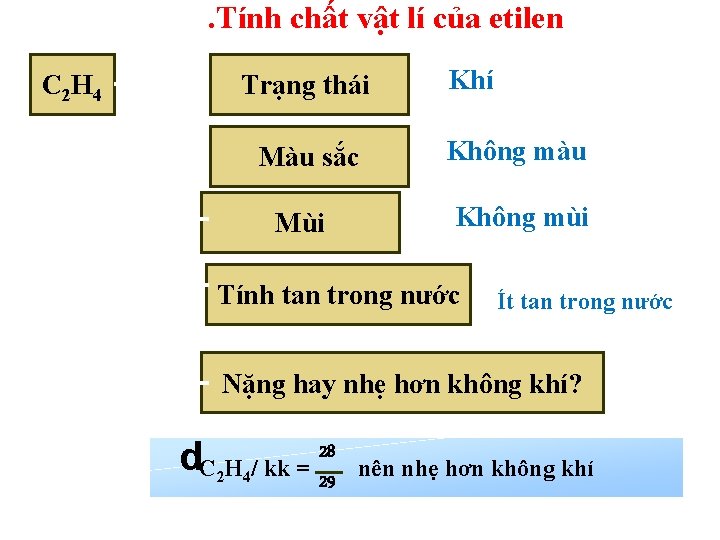
. Tính chất vật lí của etilen C 2 H 4 Trạng thái Màu sắc Mùi Khí Không màu Không mùi Tính tan trong nước Ít tan trong nước Nặng hay nhẹ hơn không khí? d. C H / kk = 2829 2 4 nên nhẹ hơn không khí

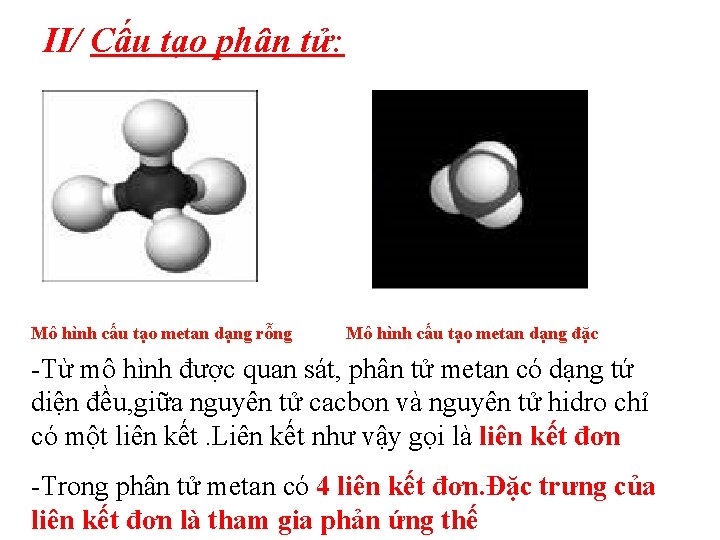
II/ Cấu tạo phân tử: Mô hình cấu tạo metan dạng rỗng Mô hình cấu tạo metan dạng đặc -Từ mô hình được quan sát, phân tử metan có dạng tứ diện đều, giữa nguyên tử cacbon và nguyên tử hidro chỉ có một liên kết. Liên kết như vậy gọi là liên kết đơn -Trong phân tử metan có 4 liên kết đơn. Đặc trưng của liên kết đơn là tham gia phản ứng thế

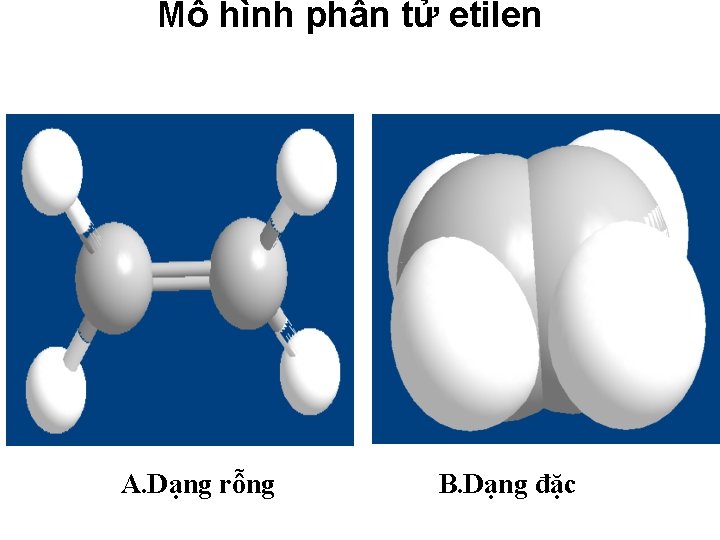
Mô hình phân tử etilen A. Dạng rỗng B. Dạng đặc

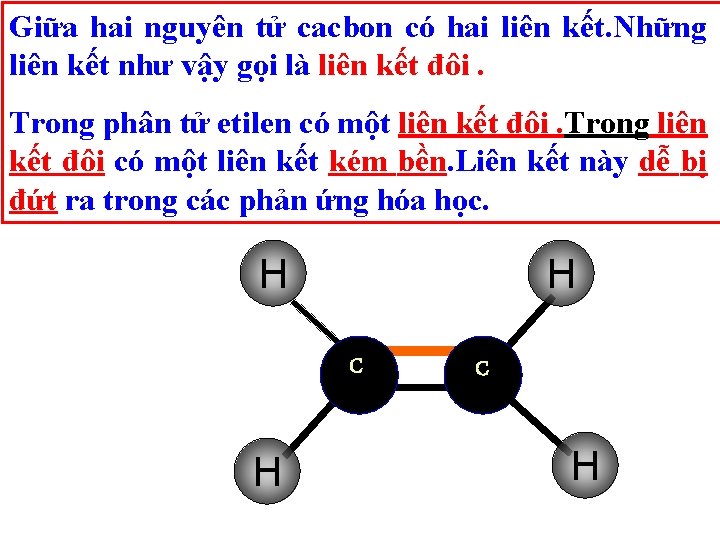
Giữa hai nguyên tử cacbon có hai liên kết. Những liên kết như vậy gọi là liên kết đôi. Trong phân tử etilen có một liên kết đôi. Trong liên kết đôi có một liên kết kém bền. Liên kết này dễ bị đứt ra trong các phản ứng hóa học. H H CC H

III / Tính chất hóa học : • 1)Tác dụng với oxi: (phản ứng cháy của metan)

Dựa vào thí nghiệm mô phỏng và nội dung SGK, trả lời các câu hỏi sau 1. Metan tác dụng với oxi ở điều kiện nào? 2. Metan cháy trong oxi với ngọn lửa màu gì? 3. Metan tác dụng với oxi tạo ra sản phẩm nào? 4. Viết PTHH

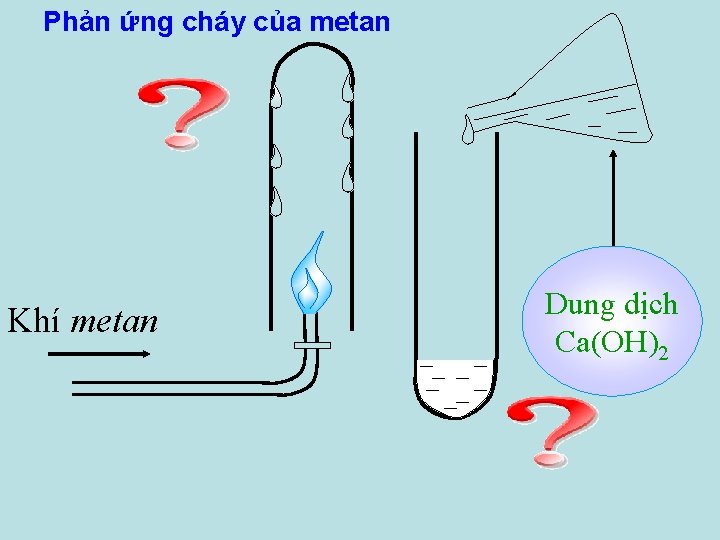
Phản ứng cháy của metan Khí metan Dung dịch Ca(OH)2

Trả lời 1. Metan tác dụng với oxi ở điều kiện nào? khi cung cấp nhiệt độ 2. Metan cháy trong oxi với ngọn lửa màu gì? màu xanh 3. Metan tác dụng với oxi tạo ra sản phẩm nào? khí cacbon đioxit và nước 4. Viết PTHH CH 4 + 2 O 2 t 0 CO 2 + 2 H 2 O

Tỉ lệ VCH : VO = 1 : 2 ( PƯ nổ mạnh nhất ) 4 2

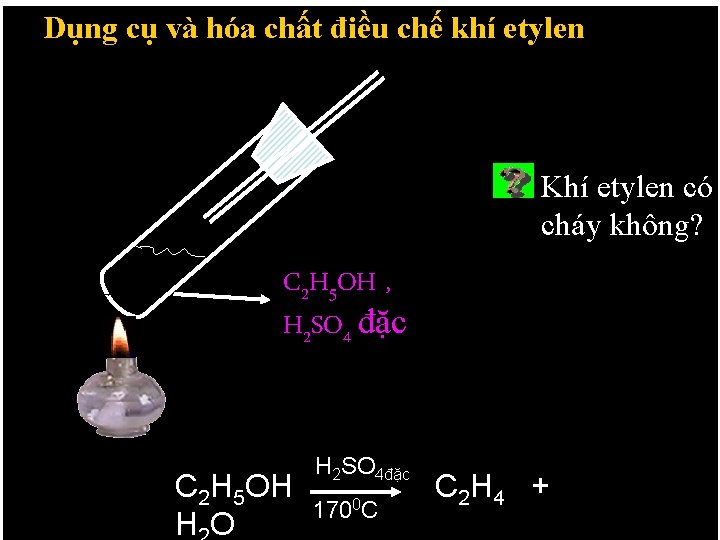
cụÖÙNG và hóa. OXI chất điều chế khí etylen 3. Dụng PHAÛN HOAÙ Khí etylen có cháy không? C 2 H 5 OH , H 2 SO 4 đặc C 2 H 5 OH HO H 2 SO 4đặc 1700 C C 2 H 4 +

III. Tính chất hóa học 1. Phản ứng cháy của etilen Đốt cháy khí etilen Hiện tượng : khí etylen cháy tạo ra khí cacbonic , hơi nước và tỏa nhiệt PTHH: C 2 H 4 + 3 O 2 2 CO 2 + 2 H 2 O

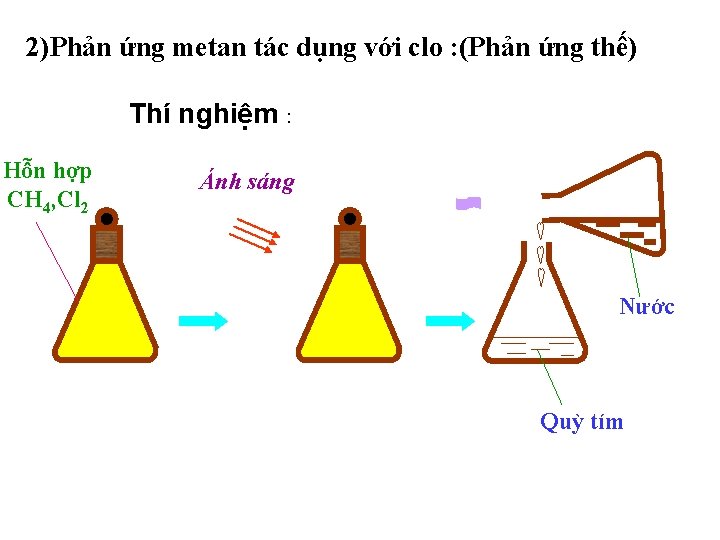
2)Phản ứng metan tác dụng với clo : (Phản ứng thế) Thí nghiệm : Hỗn hợp CH 4, Cl 2 Ánh sáng Nước Quỳ tím

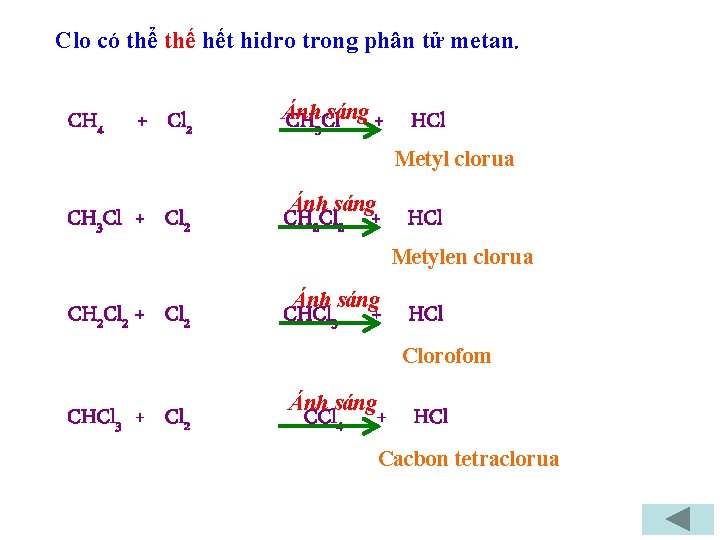
Clo có thể thế hết hidro trong phân tử metan. CH 4 + Cl 2 Ánh CH Clsáng + 3 HCl Metyl clorua CH 3 Cl + Cl 2 Ánh sáng CH 2 Cl 2 + HCl Metylen clorua CH 2 Cl 2 + Cl 2 Ánh sáng CHCl 3 + HCl Clorofom CHCl 3 + Cl 2 Ánh sáng CCl 4 + HCl Cacbon tetraclorua

2 Etilen có làm mất màu dung dịch brom không? Etilen làm mất màu da cam của dung dịch brom. Etilen đã phản ứng với brom trong dung dịch Dung dÞch Br 2

Cơ chế phản ứng giữa Etilen và Brom: H H C H H + C H Br Br H C H Phản ứng trên được gọi là phản ứng cộng. Phản ứng cộng là phản ứng đặc trưng của etilen Các chất có liên kết đôi dễ tham gia phản ứng cộng

► Ngoài Brom, trong những điều kiện thích hợp, etilen còn có phản ứng cộng với một số chất khác như Hiđro, Clo, nước axit clohiđric……

PTHH xảy ra khi cho etylen phản ứng cộng với khí hidro , clo CH 2= CH 2 + H-H Ni, t 0 CH 3 – CH 3 (Etan) CH 2= CH 2 + Cl-Cl Cl-CH 2 -Cl (đicloetan)

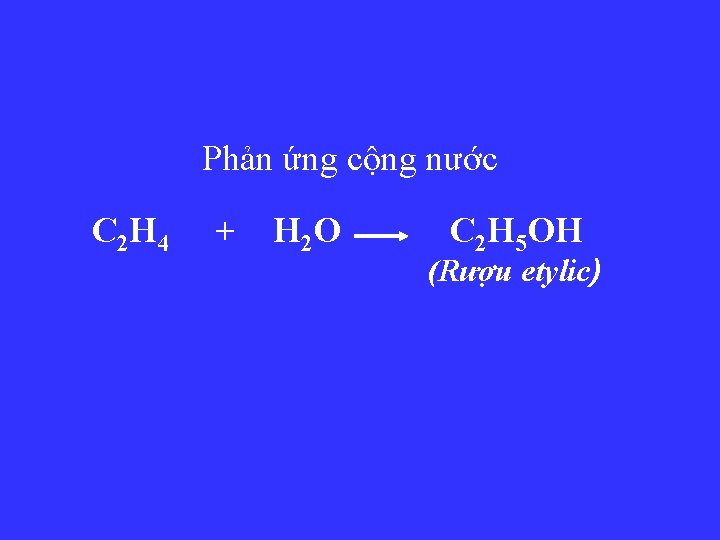
Phản ứng cộng nước C 2 H 4 + H 2 O C 2 H 5 OH (Rượu etylic)

►Etilen có phản ứng cộng là do trong phân tử Etilen có liên kết đôi.

3. Các phân tử etilen có kết hợp được với nhau không?

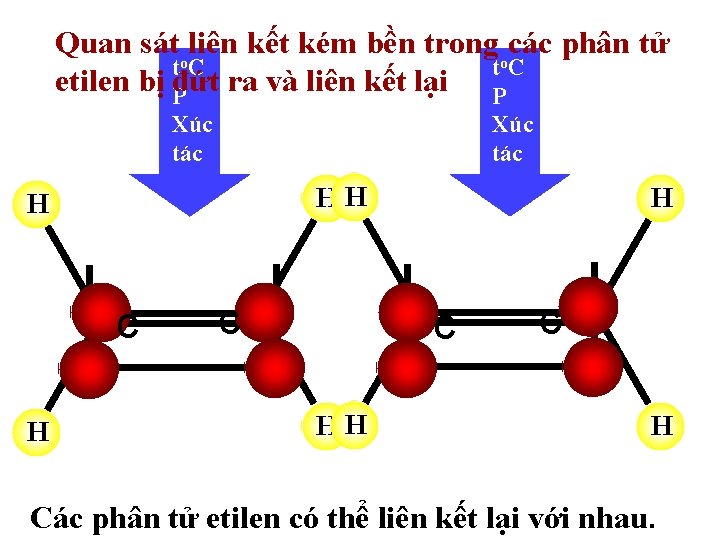
Quan sátoliên kết kém bền trong ocác phân tử t. C etilen bị Pđứt ra và liên kết lại P Xúc tác HH H c H c H Các phân tử etilen có thể liên kết lại với nhau.

Viết gọn: n. CH 2=CH 2 Xúc tác Áp suất, to CH 2 n Polietilen(PE) ► Polietilen là chất rắn, không tan trong nước, không độc. Nó là nguyên liệu quan trọng trong công nghiệp chất dẻo. Phản ứng trên được gọi là phản ứng trùng hợp

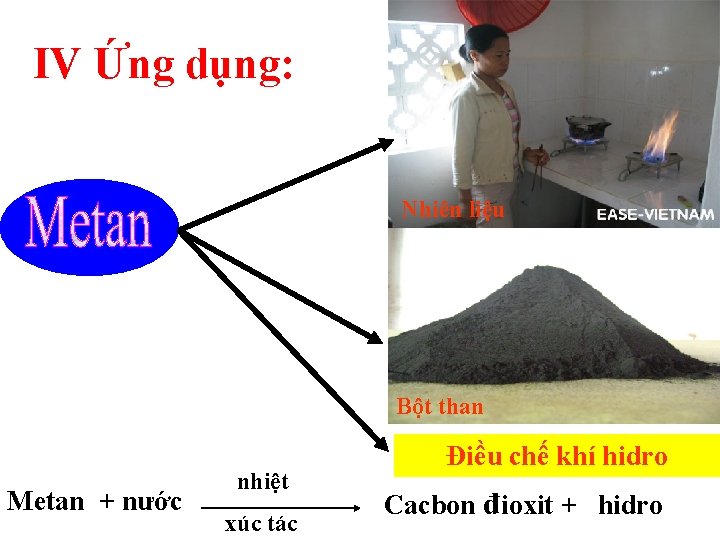
IV Ứng dụng: Nhiên liệu Bột than Metan + nước nhiệt xúc tác Điều chế khí hidro Cacbon đioxit + hidro

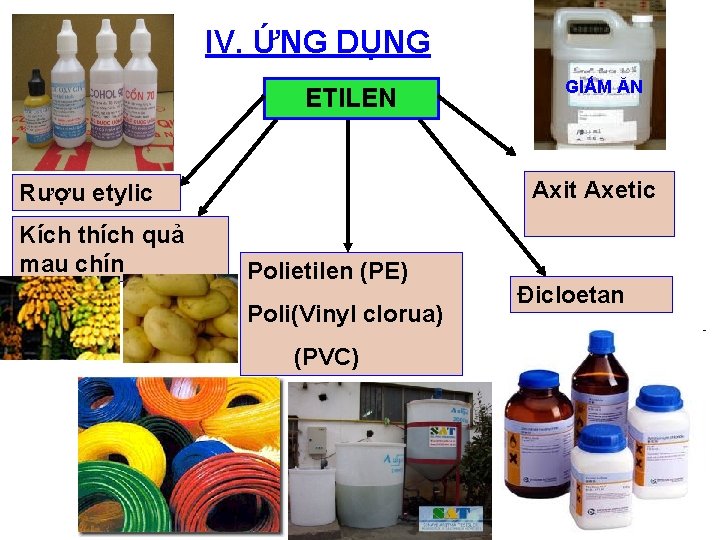
IV. ỨNG DỤNG ETILEN Axit Axetic Rượu etylic Kích thích quả mau chín GIẤM ĂN Polietilen (PE) Poli(Vinyl clorua) (PVC) Đicloetan

+Chép nội dung trong ghi nhớ SGK trang 115 và 119 vào vở học và học thuộc bài ghi Lập bảng so sánh tính chất vật lí, cấu tạo phân tử, tính chất hóa học, ứng dụng của metan và etilen + Làm bài tập 1, 2, 3, 4 (SGK/119) + Chuẩn bị bài sau: Luyện tập (có làm bài kiểm tra số 2)