TRNG THCS HON KIM BI GING IN T

TRƯỜNG THCS HOÀN KIẾM BÀI GIẢNG ĐIỆN TỬ HOÁ HỌC LỚP 8 THEO CHƯƠNG TRÌNH ĐỔI MỚI Giáo viên thực hiện: Nguyễn Kim Dung

KIỂM TRA BÀI CŨ q Trong phản ứng hóa học nguyên nhân nào làm cho chất bị biến đổi ? Đáp án: Trong phản ứng hóa học liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác ( Chất này biến đổi thành chất khác )
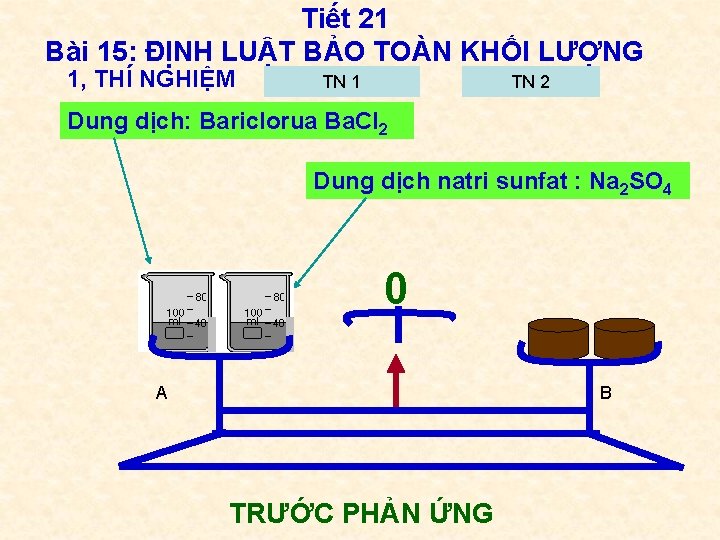
Tiết 21 Bài 15: ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG 1, THÍ NGHIỆM TN 1 TN 2 Dung dịch: Bariclorua Ba. Cl 2 Dung dịch natri sunfat : Na 2 SO 4 0 A B TRƯỚC PHẢN ỨNG
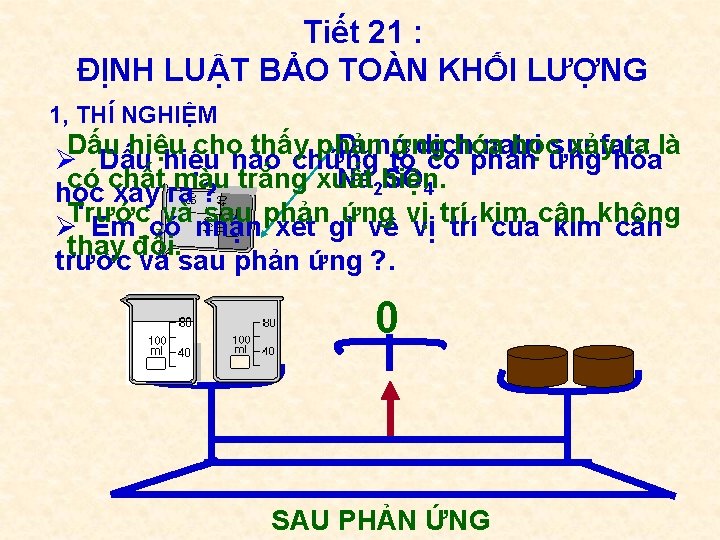
Tiết 21 : ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG 1, THÍ NGHIỆM Dấu hiệu cho thấy phản Dung ứng dịch hóa natri họcsunfat xảy ra: là Ø Dấu hiệu nào chứng tỏ có phản ứng hóa có chất màu trắng xuất Na 2 hiện. SO 4 học xảy ra ? Trước và sau phản ứng vị trí kim cân không Ø Em có nhận xét gì về vị trí của kim cân thay đổi. trước và sau phản ứng ? . 0 SAU PHẢN ỨNG

Tiết 21: ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG 1, Thí nghiệm q Biết hai chất mới sinh ra là Bari sunfat và Natri clorua. Hãy viết phương trình chữ của phản ứng trong thí nghiệm trên ? Trả lời : Phương trình chữ của phản ứng: Bari clorua + Natri sunfat → Bari sunfat + Natri clorua

v Kim cân trước và sau phản ứng không thay đổi chứng tỏ điều gì ? v. Qua thí nghiệm em thử rút ra nội dung định luật ? Ø Kim cân trước và sau phản ứng không thay đổi chứng tỏ khối lượng các chất sản phẩm bằng khối lượng các chất tham gia phản ứng. ØĐịnh luật : “ Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng”.

Tiết 21: ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG 1, Thí nghiệm: Phương trình chữ của phản ứng: Bari clorua + Natri sunfat Bari sunfat + Natri clorua 2, ĐỊNH LUẬT: a, Phát biểu: “ Trong một phản ứng hóa học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng”
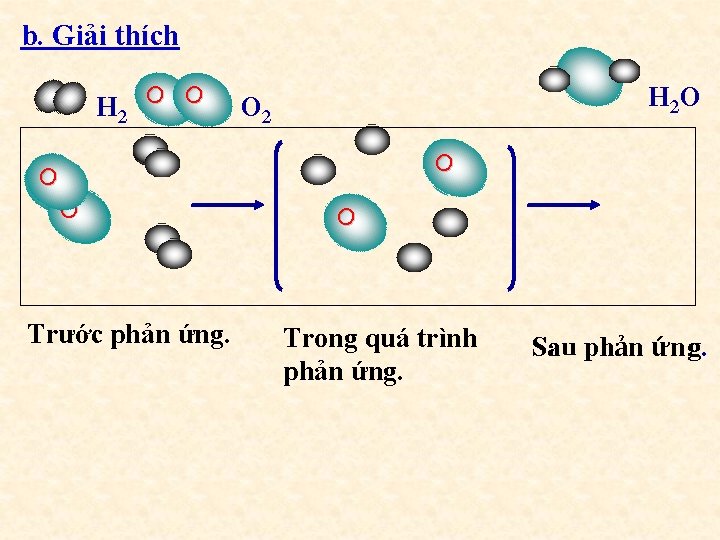
b. Giải thích H 2 O O H 2 O O 2 O O O Trước phản ứng. O Trong quá trình phản ứng. Sau phản ứng.

3, Áp dụng q Giả sử : A và B là hai chất phản ứng. C và D là hai chất sản phẩm. q Gọi m lần lượt là khối lượng của A, B, C, D. q Công thức về khối lượng: m. A + m. B = m. C + m. D

ØTrong thí nghiệm trên biết rằng sản phẩm sinh ra là Ba. SO 4 và Na. Cl Hãy viết công thức khối lượng của phản ứng trong thí nghiệm trên ? m. Ba. Cl 2 + m. Na 2 SO 4 = m. Ba. SO Ø Gọi 4 + m. Na. Cl a, b, c là khối lượng đã biết của 3 chất x là khối lượng của chất chưa biết ta có : a + b = c + x, hay a + x = b + c. _ Hãy tìm x ? x = ( b + c ) – a.

v Tóm lại : q Theo công thức về khối lượng: Trong một phản ứng có ( n ) chất, kể cả chất phản ứng và sản phẩm nếu biết ( n – 1 ) chất thì tính được khối lượng của chất còn lại.

Bài 1: Xem mô phỏng phản ứng hóa học của kim loại kẽm với axit clohidric: b. củalượng kẽm cho và axit clohidric đãkim phản a. Cho Viết biết côngkhối thứclượng về khối phản ứng giữa ứng là 13 gvàvàaxit 14, 6 g, khối lượng củarakẽm 27, 2 g. loại kẽm clohidric HCl tạo kẽmclorualàZn. Cl 2 và Tính khối lượng của khí hidro bay lên. khí hidro HCl Tröôùc phaûn öùng Zn Zn. Cl 2 Trong quaù trình phaûn öùng Sau phaûn öùng H 2

Bài 2: Khi nung nóng miếng đồng trong không khí ( đồng tác dụng với oxi có trong không khí ) sản phẩm thu được là đồng (II) oxit có màu đen. Khối lượng sản phẩm sau phản ứng so với khí lượng lá đồng trước phản ứng như thế nào: A. Không thay đổi B. Tăng lên C. Giảm đi HÃY GIẢI THÍCH PHƯƠNG ÁN CHỌN

Bài 3: Đá vôi ( thành phần chính là chất canxi cacbonat) xếp vào lò nung nóng thu được vôi sống (canxi oxit) và khí cacbon đioxit thoát ra. Khối lượng vối sống thu được sau phản ứng so với khối lượng đá vôi ban đầu: A. Không thay đổi B. Tăng lên C. Giảm đi HÃY GIẢI THÍCH PHƯƠNG ÁN CHỌN

Bài 4: Còn có thể điều chế khí oxi bằng cách đun nóng kali clorat KCl. O 3 ( là chất rắn màu trắng). Khi đun nóng 24, 5 g KCl. O 3, chất rắn còn lại trong ống nghiệm có khối lượng là 13, 45 g. a. Khối lượng khí oxi thu được là : A. 11 g B. 11, 1 g C. 11, 05 g D. 11, 5 g b. Tính khối lượng oxi thực tế thu được, biết hiệu suất của phản ứng phân hủy là 80%.

KẾT LUẬN: 1, ĐỊNH LUẬT:

HƯỚNG DẪN HỌC Ở NHÀ q Học bài theo nội dung đã ghi. q Làm bài tập sgk trang 54. q Xem lại kiến thức về lập công thức hoá học, hoá trị của một số nguyên tố.
- Slides: 17