Trng THCS B GV Thy Giang Bi 31

Trường THCS Bồ Đề GV: Đỗ Thúy Giang


Bài 31 - Tiết 39
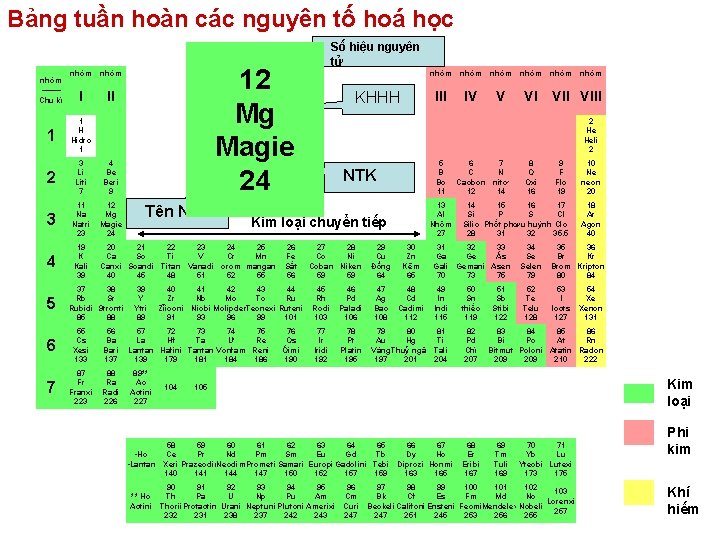
Bảng tuần hoàn các nguyên tố hoá học 19 14 9 12 K F Si Mg Silic Flo Kali Magie 19 28 39 24 nhóm Chu kì I II 1 1 H Hidro 1 2 3 Li Liti 7 4 Be Beri 9 3 11 Na Natri 23 12 Mg Magie 24 4 19 K Kali 39 20 21 22 23 24 25 Ca Sc Ti V Cr Mn Canxi Scandi Titan Vanadi crom mangan 40 45 48 51 52 55 nhóm 5 37 38 Rb Sr Rubidi Stronti 85 88 Số hiệu nguyên tử Tên NT 39 Y Ytri 89 40 41 42 43 44 Zr Nb Mo Tc Ru Zỉiconi Niobi Molipden. Tecnexi Ruteni 91 93 96 99 101 6 55 Cs Xesi 133 56 Ba Bari 137 57 72 73 74 75 La Hf Ta Ư Re Lantan Hafini Tantan Vonfam Reni 139 179 181 184 186 7 87 Fr Franxi 223 88 Ra Radi 226 89** Ac Actini 227 104 76 Os Óimi 190 nhóm III IV V VI KHHH nhóm VIII 2 He Heli 2 5 B Bo 11 NTK 13 Al Nhôm 27 Kim loại chuyển tiếp 26 Fe Sắt 56 nhóm 27 28 Co Ni Coban Niken 59 59 45 Rh Rodi 103 46 Pd Paladi 106 77 Ir Iridi 192 78 Pt Platin 195 29 Cu Đồng 64 30 Zn Kẽm 65 47 Ag Bạc 108 48 Cd Cadimi 112 79 80 Au Hg Vàng. Thuỷ ngân 197 201 6 7 C N Cacbon nitơ 12 14 9 F Flo 19 10 Ne neon 20 14 15 16 17 Si P S Cl Silic Phốt pho Lưu huỳnh Clo 28 31 32 35. 5 18 Ar Agon 40 31 32 33 Ga Ge Ás Gali Gemani Asen 70 73 75 49 In Indi 115 50 Sn thiếc 119 81 Ti Tali 204 82 Pd Chì 207 51 Sb Stibi 122 8 O Oxi 16 34 Se Selen 79 52 Te Telu 128 35 36 Br Kr Brom Kripton 80 84 53 I Ioots 127 83 84 85 86 Bi Po At Rn Bitmut Poloni Atatin Radon 209 210 222 Kim loại 105 58 59 60 61 62 63 64 65 Ce Pr Nd Pm Sm Eu Gd Tb • Họ • Lantan Xeri Prazeodim Neodim Prometi Samari Europi Gadolini Tebi 140 141 144 147 150 152 157 159 54 Xe Xenon 131 66 67 Dy Ho Diprozi Honmi 163 165 68 Er Eribi 167 69 Tm Tuli 169 70 71 Yb Lu Ytecbi Lutexi 173 175 97 90 91 92 93 94 95 96 98 99 100 101 102 103 Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No ** Họ Lorenxi Actini Thorii Protactini Urani Neptuni Plutoni Amerixi Curi Beckeli Califoni Ensteni Fecmi. Mendelevi. Nobeli 257 232 231 238 237 242 243 247 251 245 253 256 255 Phi kim Khí hiếm
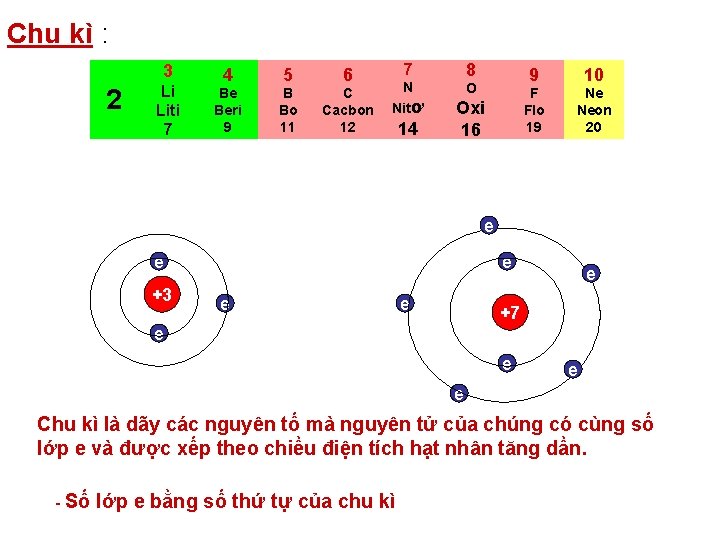
Chu kì : 3 2 Li Liti 7 4 5 6 Be Beri 9 B Bo 11 C Cacbon 12 7 8 N Nitơ O 14 Oxi 16 9 10 F Flo 19 Ne Neon 20 e e +3 e e +7 e e Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp e và được xếp theo chiều điện tích hạt nhân tăng dần. - Số lớp e bằng số thứ tự của chu kì
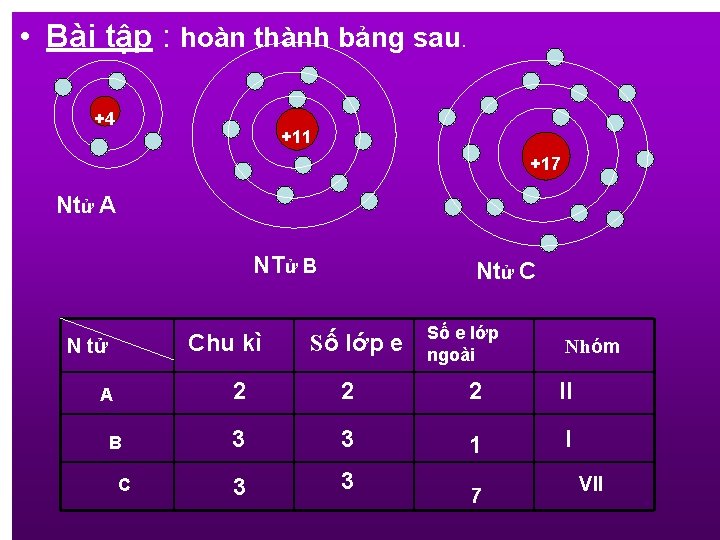
• Bài tập : hoàn thành bảng sau. +4 +11 +17 Ntử A NTử B Chu kì N tử A B C Ntử C Số lớp e Số e lớp ngoài Nhóm 2 2 2 II 3 3 1 I 3 3 7 VII
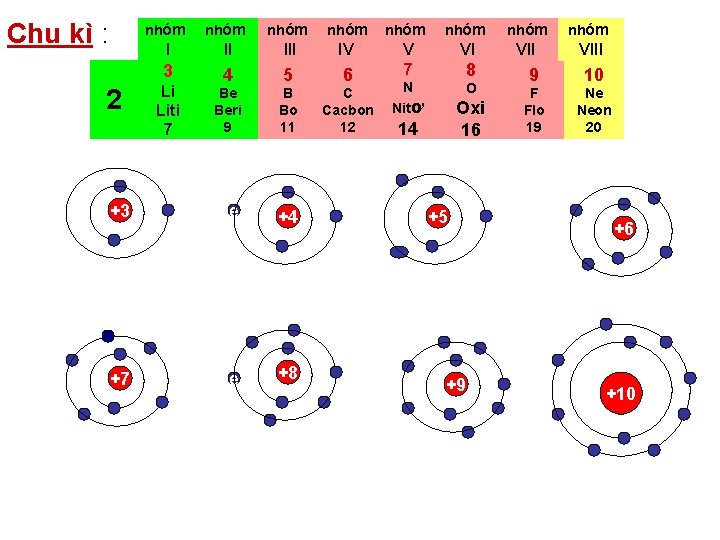
Chu kì : nhóm nhóm I II IV VI VIII 3 4 5 6 V 7 8 10 B Bo 11 C Cacbon 12 O 9 Be Beri 9 N Nitơ F Flo 19 Ne Neon 20 +3 e +4 +7 e +8 2 Li Liti 7 Oxi 16 14 +5 +9 +6 +10
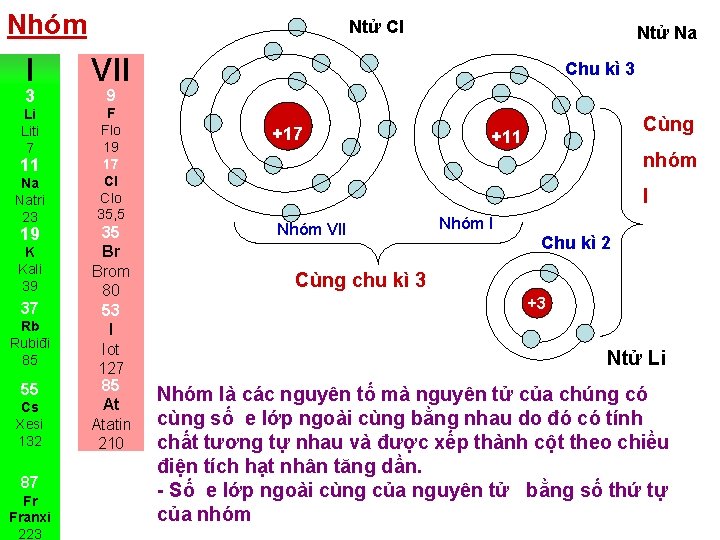
Nhóm Ntử Cl I VII Li Liti 7 F Flo 19 17 Cl Clo 35, 5 3 11 Na Natri 23 19 K Kali 39 37 Rb Rubiđi 85 55 Cs Xesi 132 87 Fr Franxi 223 Ntử Na Chu kì 3 9 35 Br Brom 80 53 I Iot 127 85 At Atatin 210 +17 Cùng +11 nhóm I Nhóm VII Nhóm I Chu kì 2 Cùng chu kì 3 +3 Ntử Li Nhóm là các nguyên tố mà nguyên tử của chúng có cùng số e lớp ngoài cùng bằng nhau do đó có tính chất tương tự nhau và được xếp thành cột theo chiều điện tích hạt nhân tăng dần. - Số e lớp ngoài cùng của nguyên tử bằng số thứ tự của nhóm

• Phiếu học tập. Bảng 1 Bảng 2 Cấu tạo nguyên tử Số điện Số e Số Số e Vị trí nguyên tố X - Y Số hiệu nguyên tử 8 STT Chu kì 2 STT nhóm 6 tích hạt nhân 8 lớp e lớp ngoài 8 2 6

Bảng 2 Cấu tạo nguyên tử Số điện Số e Số Số e Vị trí nguyên tố X - Y Số hiệu nguyên tử 8 STT Chu kì 2 STT nhóm VI tích hạt nhân 8 lớp e lớp ngoài 8 2 6

Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn Bảng tuần hoàn có hơn 100 nguyên tố và được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử MENDELEEV Mendeleev Đimitri Ivanovich (1834 – 1907) là nhà hóa học người Nga. Năm 1860 ông đề xuất ý tưởng xây dựng bảng tuần hoàn -Năm 1869 ông công bố bản “ bảng tuần hoàn các nguyên tố hóa học “ hệ thống này giữ một vai trò cực kì to lớn trong việc phát triển các môn Hóa học và Vật lý. -Nguyên tố ở ô thứ 101 là MENĐELÊVI để kỷ niệm nhà hóa học Menđeleep, người tìm ra bảng tuần hoàn các nguyên tố.

Bút tích của Mendeleev

• Bài tập : Sơ đồ cấu tạo nguyên tử của nguyên tố X : Hãy chỉ ra vị trí của X trong bảng tuần hoàn +12 Điện tích hạt nhân : + 12 STT : Ô số 12 3 lớp e chu kì 3 Số e lớp ngoài : 2 e Nhóm II


- BTVN : 1, 2 SGK ( 101). -Ôn lại dãy hoạt động hoá học của kim loại, mức độ hoạt động hoá học của các phi kim. -- Đọc trước bài : Sơ lược bảng HTTH ( phần III, IV)

- Slides: 16