TRNG I HC B RA VNG TU KHOA

TRƯỜNG ĐẠI HỌC BÀ RỊA – VŨNG TÀU KHOA HOÁ HỌC & CNTP HÓA HỌC DẦU MỎ 1

ĐIỂM THÀNH PHẦN CỦA MÔN HỌC - 10% Điểm chuyên cần (điểm danh + kiểm tra bài cũ, phát biểu). - 10% Kt 15’ (đề đóng) - 20% Kt 45’ báo trước một tuần (đề đóng) - 60% Thi cuối kỳ. 2

NỘI DUNG MÔN HỌC Phần I: NGUỒN GỐC, THÀNH PHẦN CỦA DẦU MỎ VÀ KHÍ o Nguồn gốc, phân loại dầu mỏ và khí o Thành phần hydrocacbon o Các thành phần phi hydrocacbon o Thành phần chưng cất phân đoạn Phần II: HÓA HỌC CÁC QUÁ TRÌNH CHẾ BIẾN DẦU o Tổng quan o Phản ứng hóa học và cơ chế của Cracking nhiệt o Phản ứng hóa học và cơ chế của Cracking xúc tác 3

TÀI LIỆU THAM KHẢO 1. 2. 3. 4. 5. 6. Hóa học dầu mỏ và khí – Đinh Thị Ngọ, Nguyễn Khánh Diệu Hồng, NXB Khoa Học và Kỹ Thuật, 2010. Hóa học dầu mỏ và khí – Trần Mạnh Trí Các sản phẩm dầu mỏ – Bùi Đình Kiểm, NXB Khoa Học và Kỹ Thuật, 2000. Nhiên liệu sạch và các quá trình xử lý trong hóa dầu – Đinh Thị Ngọ, Nguyễn Khánh Diệu Hồng, NXB Khoa Học và Kỹ Thuật, 2008. Chemistry of petrochemical processes – Sami Matar, Lewis F. Hatch, 2004. The chemistry and technology of petroleum and gas – Erikh V. N. , Rasina M. G. , Rudin N. G. 4

Phần I: NGUỒN GỐC, THÀNH PHẦN CỦA DẦU MỎ VÀ KHÍ 1. 2. 3. 4. 5. 6. Nguồn gốc Thành phần nguyên tố Thành phần hydrocacbon Thành phần phi hydrocacbon Thành phần chưng cất phân đoạn Phân loại dầu mỏ 5

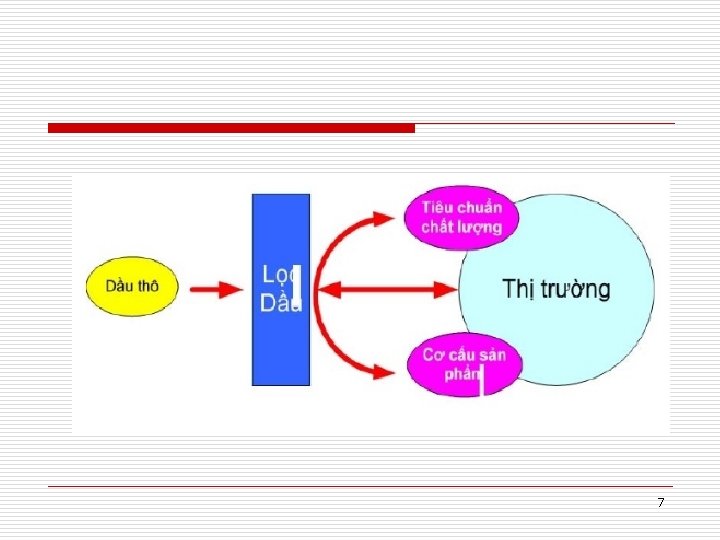
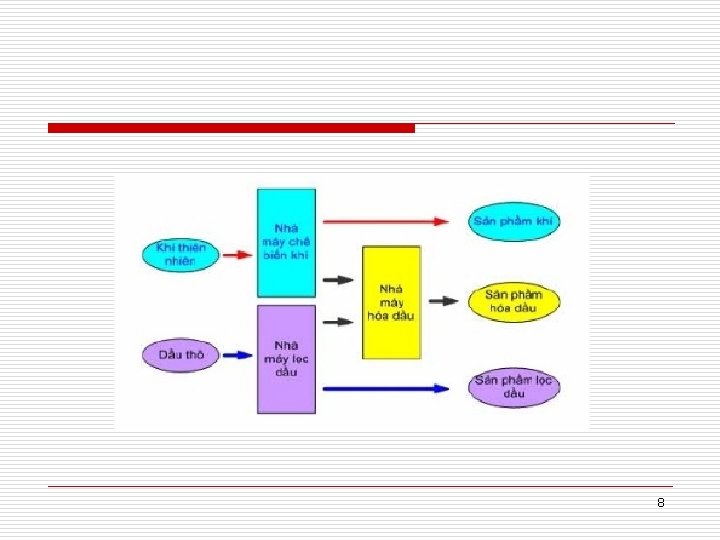
VAI TRÒ CỦA DẦU MỎ VÀ KHÍ o Năng lượng, nhiên liệu o Sản phẩm phi nhiên liệu o Nguyên liệu cho công nghiệp tổng hợp hóa dầu 6
7
8
9

Sơ lược nghành dầu khí Việt Nam o Những năm 60 -70: tìm thấy dầu mỏ. o Sau 1975: nghiên cứu, thăm dò, khai thác. o 19/6/1981 – Xí nghiệp liên doanh Vietsopetro thành lập. o 26/6/1986 – khai thác tấn dầu tiên. o 2001 – khai thác tấn dầu thứ 100 triệu. o 3/2009 – nhà máy lọc dầu Dung Quất cho ra dòng sản phẩm đầu tiên. o Nhà máy lọc dầu Nghi Sơn – Thanh Hóa, Long Sơn – BRVT. 10
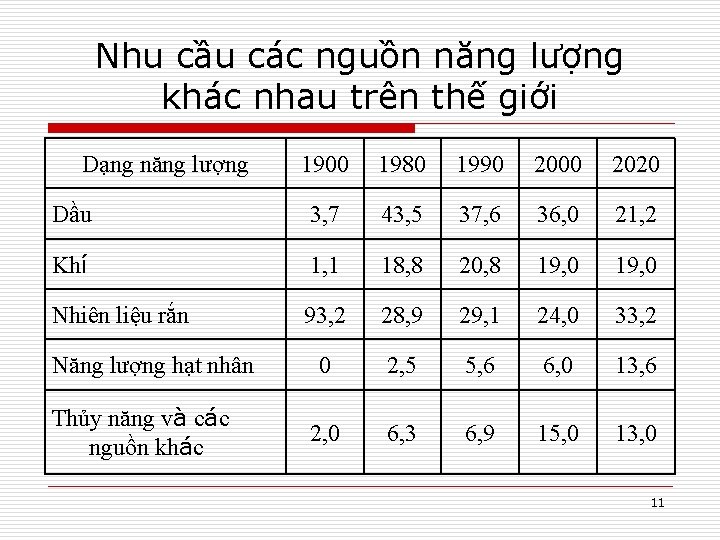
Nhu cầu các nguồn năng lượng khác nhau trên thế giới Dạng năng lượng 1900 1980 1990 2000 2020 Dầu 3, 7 43, 5 37, 6 36, 0 21, 2 Khí 1, 1 18, 8 20, 8 19, 0 Nhiên liệu rắn 93, 2 28, 9 29, 1 24, 0 33, 2 0 2, 5 5, 6 6, 0 13, 6 2, 0 6, 3 6, 9 15, 0 13, 0 Năng lượng hạt nhân Thủy năng và các nguồn khác 11
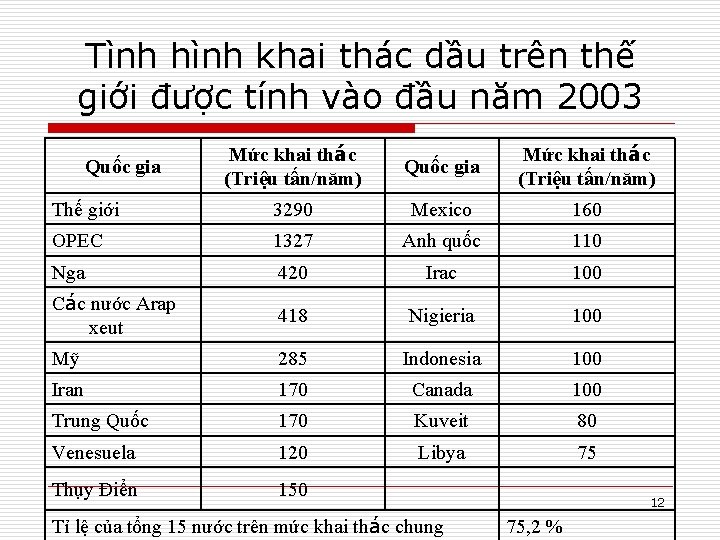
Tình hình khai thác dầu trên thế giới được tính vào đầu năm 2003 Mức khai thác (Triệu tấn/năm) Quốc gia Mức khai thác (Triệu tấn/năm) Thế giới 3290 Mexico 160 OPEC 1327 Anh quốc 110 Nga 420 Irac 100 Các nước Arap xeut 418 Nigieria 100 Mỹ 285 Indonesia 100 Iran 170 Canada 100 Trung Quốc 170 Kuveit 80 Venesuela 120 Libya 75 Thụy Điển 150 Quốc gia Tỉ lệ của tổng 15 nước trên mức khai thác chung 12 75, 2 %
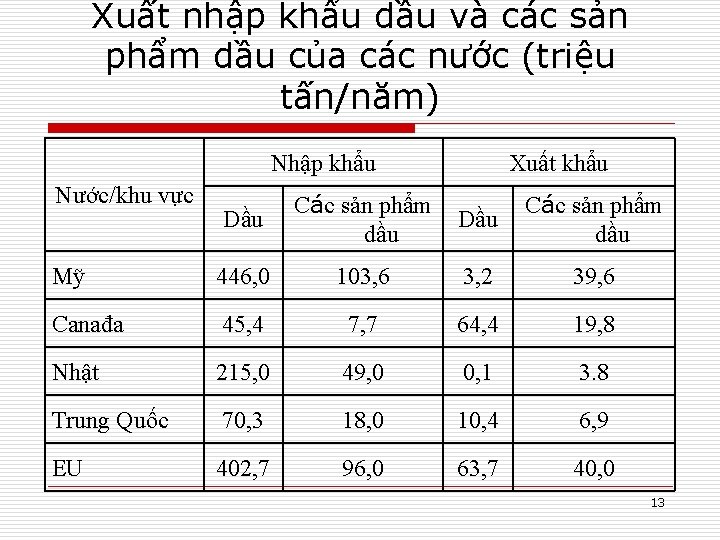
Xuất nhập khẩu dầu và các sản phẩm dầu của các nước (triệu tấn/năm) Nhập khẩu Nước/khu vực Xuất khẩu Dầu Các sản phẩm dầu Mỹ 446, 0 103, 6 3, 2 39, 6 Canađa 45, 4 7, 7 64, 4 19, 8 Nhật 215, 0 49, 0 0, 1 3. 8 Trung Quốc 70, 3 18, 0 10, 4 6, 9 EU 402, 7 96, 0 63, 7 40, 0 13
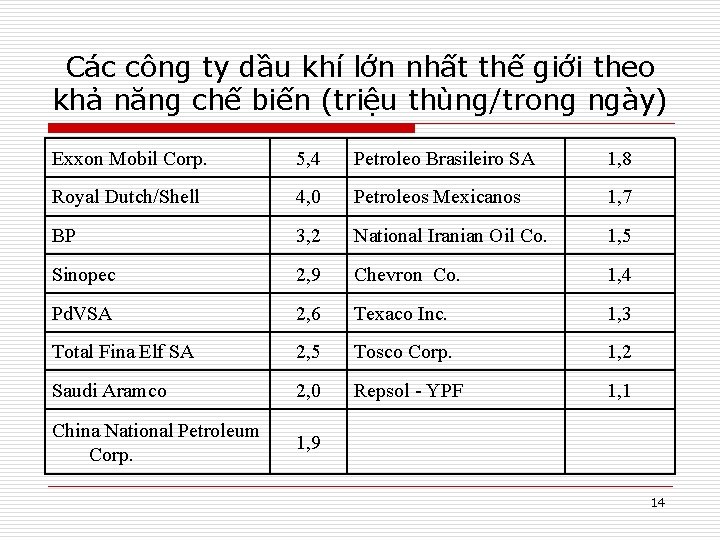
Các công ty dầu khí lớn nhất thế giới theo khả năng chế biến (triệu thùng/trong ngày) Exxon Mobil Corp. 5, 4 Petroleo Brasileiro SA 1, 8 Royal Dutch/Shell 4, 0 Petroleos Mexicanos 1, 7 BP 3, 2 National Iranian Oil Co. 1, 5 Sinopec 2, 9 Chevron Co. 1, 4 Pd. VSA 2, 6 Texaco Inc. 1, 3 Total Fina Elf SA 2, 5 Tosco Corp. 1, 2 Saudi Aramco 2, 0 Repsol - YPF 1, 1 China National Petroleum Corp. 1, 9 14

I. NGUỒN GỐC CỦA DẦU MỎ o. Thuyết vô cơ o. Thuyết hữu cơ 15

Thuyết vô cơ - Cacbua kim loại bị phân hủy bởi nước 3 Fem. Cn + 4 m. H 2 O → m. Fe 3 O 4 + C 3 n. H 8 m Ca. C 2 + 2 H 2 O → C 2 H 2 + Ca(OH)2 Al 4 C 3 + 12 H 2 O → 3 CH 4 + 4 Al(OH)3 Dưới tác dụng của T, P, xúc tác (khoáng sét) => hydrocacbon có trong dầu khí 16

Khuyết điểm o Ở độ sâu 40 -50 km dưới lòng đất, không có khe hở cho nước thấm vào trong. Vật chất trong lòng quả đất ở trạng thái dẻo, điều đó loại trừ các khe nứt, điều kiện bắt buộc của giả thuyết này. o Nếu có sự tồn tại của các khe nứt trong lòng quả đất thì nước cũng không thể thấm được xuống vì nhiệt độ quá cao. o Trong vỏ quả đất, hàm lượng cacbua kim loại là không đáng kể. o Các hydrocacbon thường gặp trong các lớp trầm tích, tại đó nhiệt độ ít khi vượt quá 150 -200 o. C (vì áp suất rất cao), nên không đủ nhiệt độ cần thiết cho phản ứng hóa học xảy ra. o Đã phân tích được trong dầu thô có chứa các clorofin có nguồn gốc từ động thực vật. 17

Thuyết hữu cơ Thành phần hóa học của dầu mỏ và khí đốt gồm hai nguyên tố đặc trưng đối với vật chất hữu cơ là cacbon và hydro. Ngoài ra trong thành phần của dầu mỏ còn có oxy, nitơ, lưu huỳnh và photpho là những nguyên tố cơ bản tạo nên vật chất sống cũng như các khoáng sản cháy. Hoạt tính quang học là một trong những dẫn chứng quan trọng nhất của lý thuyết nguồn gốc hữu cơ của dầu mỏ. Hoạt tính quang học trong dầu mỏ là do cholesterol - hợp chất hữu cơ có nguồn gốc thực vật. Các loại dầu tổng hợp không có hoạt tính quang học. 18

Thuyết hữu cơ Các phản ứng hình thành ankan R-COOH → RH +CO 2 R-OH + 2[H] → RH + H 2 O 19

CÁC PHẢN ỨNG TẠO ANKAN Đối với các ankan từ C 40 tới C 100 được hình thành như sau: 20
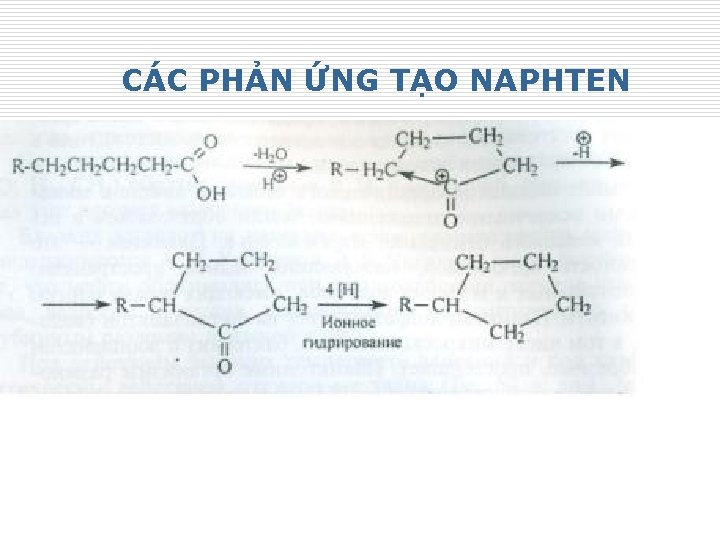
CÁC PHẢN ỨNG TẠO NAPHTEN 21
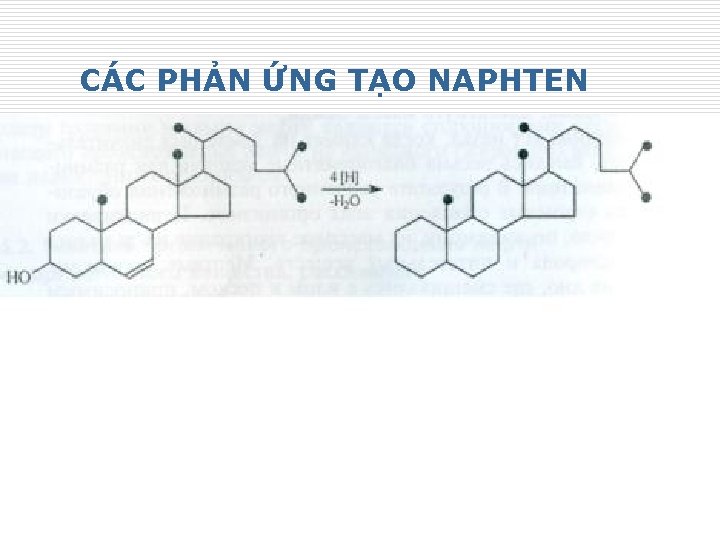
CÁC PHẢN ỨNG TẠO NAPHTEN 22
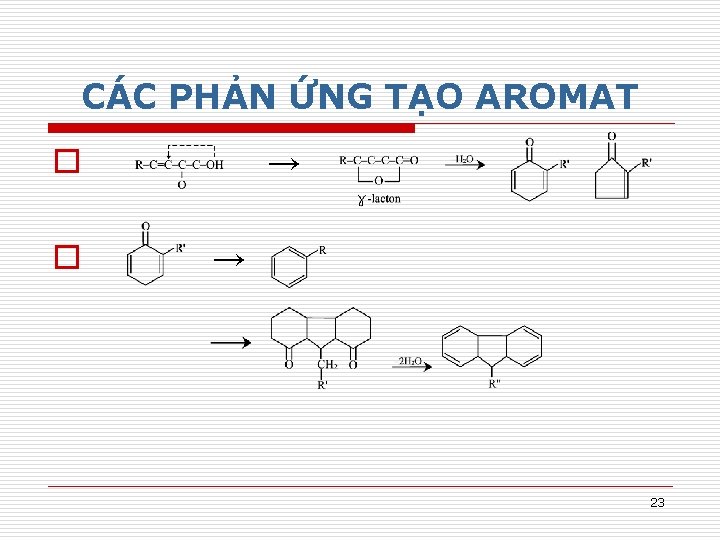
CÁC PHẢN ỨNG TẠO AROMAT o o → → 23
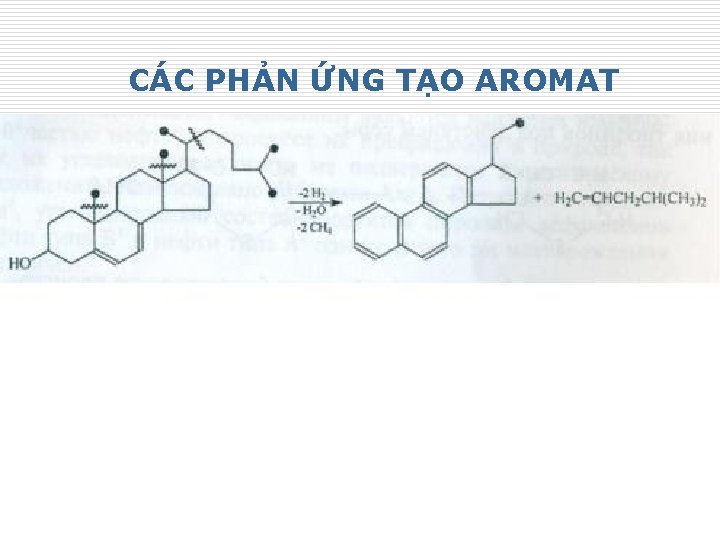
CÁC PHẢN ỨNG TẠO AROMAT 24
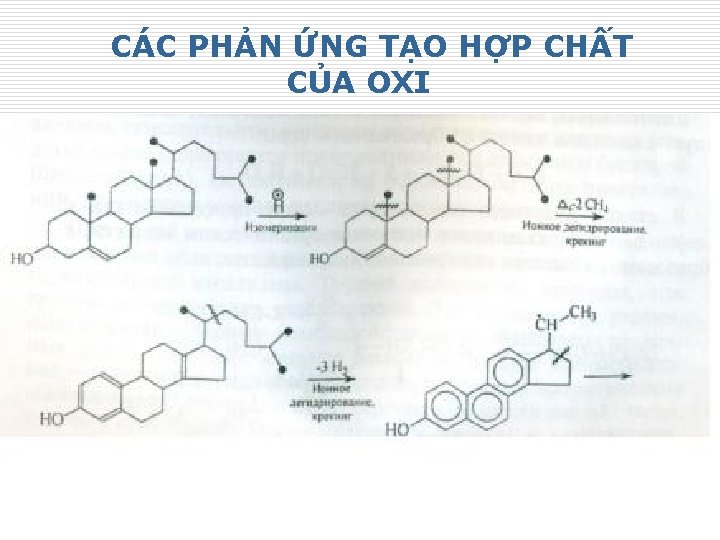
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA OXI 25
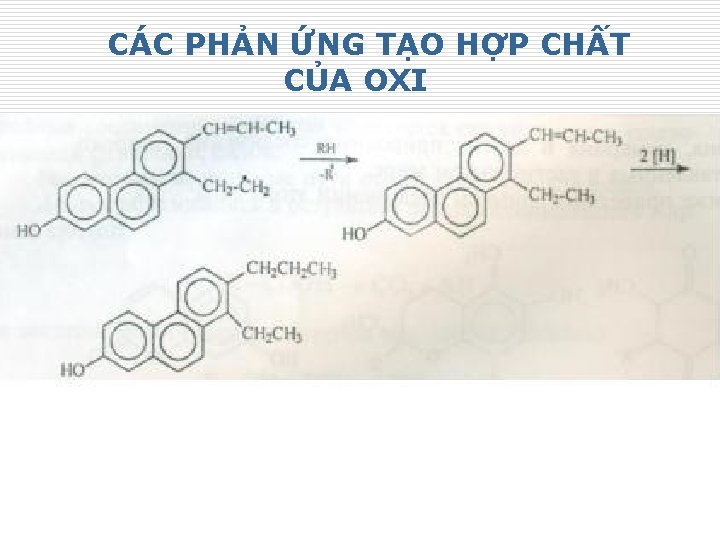
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA OXI 26
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA LƯU HUỲNH Na 2 SO 4 + 4 H 2 → Na 2 S + 4 H 2 O Na 2 S + 2 H 2 O → 2 Na. OH + H 2 S + Fe 2 O 3 → S + 2 Fe. O + H 2 O 2 RH + 2 S → R-S-R + H 2 S (T=150 -170 o. C) 2 R-SH + Fe 2 O 3 → R-S-S-R + H 2 O + Fe. O R-S-R → R’-CH=CH 2 + R’SH 27
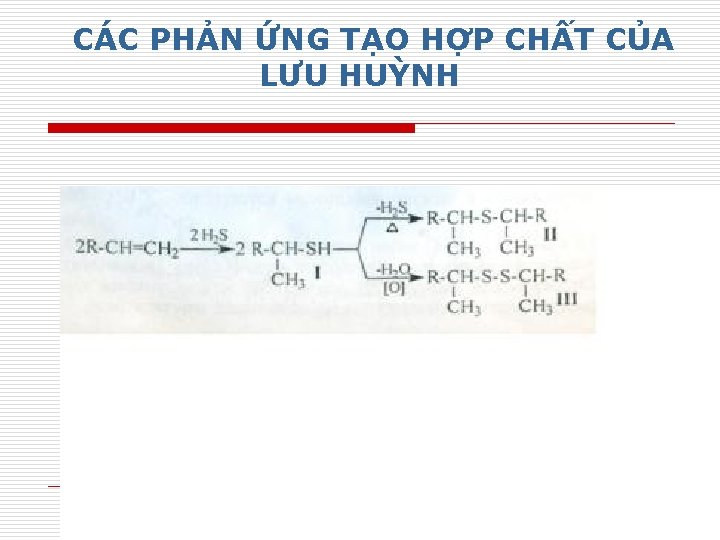
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA LƯU HUỲNH 28
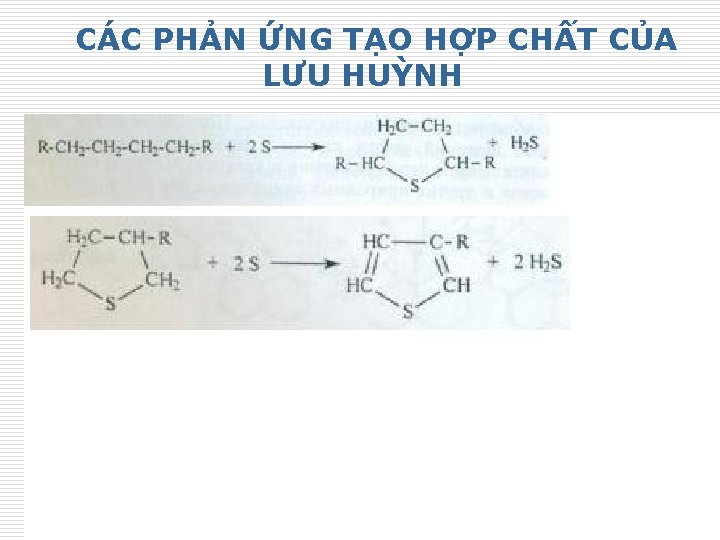
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA LƯU HUỲNH 29
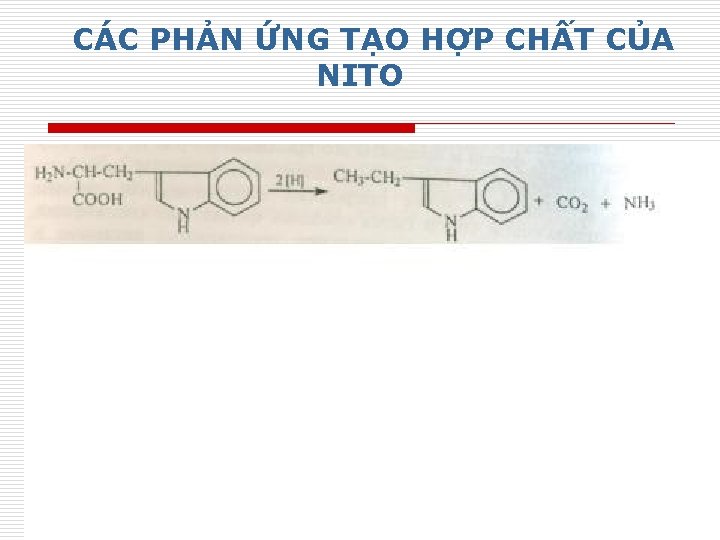
CÁC PHẢN ỨNG TẠO HỢP CHẤT CỦA NITO 30

THÀNH PHẦN CỦA DẦU MỎ I. THÀNH PHẦN NGUYÊN TỐ ¡ II. THÀNH PHẦN HIDROCACBON ¡ III. THÀNH PHẦN PHI HIDROCACBON ¡

I. THÀNH PHẦN NGUYÊN TỐ - Hàm lượng các nguyên tố (theo khối lượng) + C từ 83 đến 87% + H từ 11 đến 14% + Lưu huỳnh 0, 1 đến 6% + N dưới 1, 8 % + O dưới 3, 0% Ngoài ra trong dầu còn chứa gần 30 kim loại như: V, Ni, Fe, Zn, Cu, Mg, Al… Trong khí chứa các khí trơ như: Ar, Ne, N 2…

II. THÀNH PHẦN HIDROCACBON 1. Alkan (hydrocacbon parafinic) (20 -50%) - C 1 đến C 4 là khí - C 5 đến C 16 lỏng + C 5 đến C 10, 11 : xăng Ts < 180 o. C + C 11 đến C 16 : kerosen Ts = 180 o. C - 250 o. C - C 17 và lớn hơn rắn: nguyên liệu quý để tổng hợp hóa học: chất tẩy rửa tổng hợp, tơ sợi nhân tạo, phân bón, chất dẻo…
Parafin Khí C 1 – C 4 (khí đồng hành), trong đó butan chiếm tỷ lệ cao nhất. Ngoài ra còn có một lượng nhỏ pentan bay ra cùng chúng i-parafin: nằm trong phần nhẹ và trung bình. Cấu trúc đơn giản, mạch chính dài, nhánh phụ ít và ngắn, thường là metyl. Các i-parafin từ C 5 đến C 10 là cấu tử rất quý vì chúng làm tăng trị số octan Dầu VN có nhiệt độ đông đặc khá cao: dầu Bạch Hổ đông đặc ở 33 o. C, dầu Đại Hùng ở 27 o. C. Như vậy dầu Bạch Hổ là loại dầu điển hình có nhiều parafin rắn, ngay ở nhiệt độ thường chúng cũng không chảy lỏng tokt C 18 H 38 = 28, 1 o. C, C 19 H 40 = 32 o. C n-parafin chiếm đa số (2530% thể tích), thường chứa các HC từ C 1 -C 45. Với C>=18 thì nó tồn tại ở thể rắn. Đây là những cấu tử làm giảm giá thành của dầu thô do chúng làm tăng tođđ của dầu, dẫn đến làm giảm tính linh động, vì vậy người ta fải áp dụng các biện pháp khác nhau để tách bớt các parafin rắn ngay tại nơi khai thác như là gia nhiệt đường ống, cho thêm phụ gia.
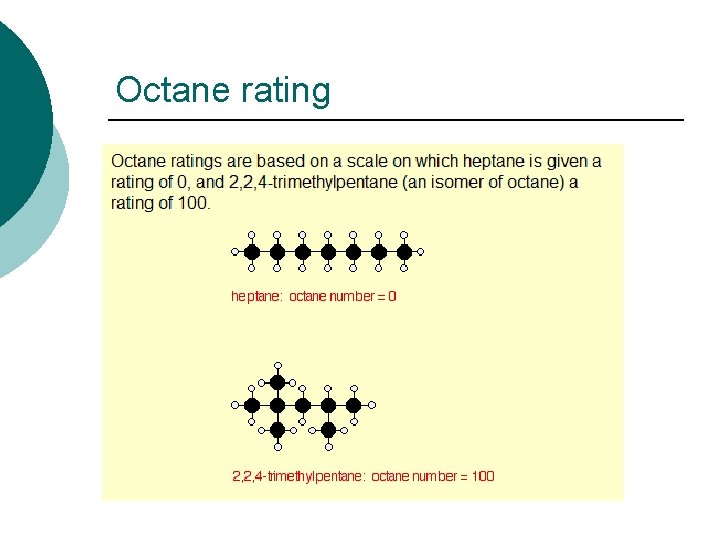
Octane rating

Phương pháp phân tích thành phần khí ¡ ¡ Thành phần: hydrocacbon, phi hydrocacbon (CO 2, N 2, H 2 S, H 2, He, Ar, Ne…) Phương pháp: hấp thụ, sắc kí khí

Phương pháp hấp thụ Cho hỗn hợp khí: alkan, alken, O 2, N 2, H 2, CO 2, H 2 S Xác định CO 2: CO 2 + 2 Na. OH → Na 2 CO 3 + H 2 O Xác định O 2: 2 C 6 H 3(ONa)3 + 1/2 O 2 → (Na. O)3 C 6 H 2 -C 6 H 2(ONa)3 + H 2 O Na 2 S 2 O 4 + 2 Na. OH + O 2 → Na 2 SO 4 + Na 2 SO 3 + H 2 O Xác định olefin: R-CH=CH 2 + Br 2 → R-CHBr-CH 2 Br Xác định CO, H 2 và tổng lượng alkan: phản ứng oxi hóa * Cho khí qua ống Cu. O ở T=280 o. C H 2(K) + Cu. O→ Cu + H 2 O(L) CO(K) + Cu. O → Cu + CO 2(K) CO 2 + 2 Na. OH → Na 2 CO 3 + H 2 O Cu 2 SO 4 + 2 CO → Cu 2 SO 4. 2 CO * Cho khí qua ống Cu. O ở T=850 -950 o. C CH 4 + Cu. O → CO 2(K) + H 2 O(L) + Cu

Phương pháp sắc kí khí Cho hỗn hợp khí: alkan, alken, O 2, N 2, H 2, CO

Phương pháp phân tích thành phần alkan Đối với các phân đoạn nặng phải tách sơ bộ các chất nhựa, aromat
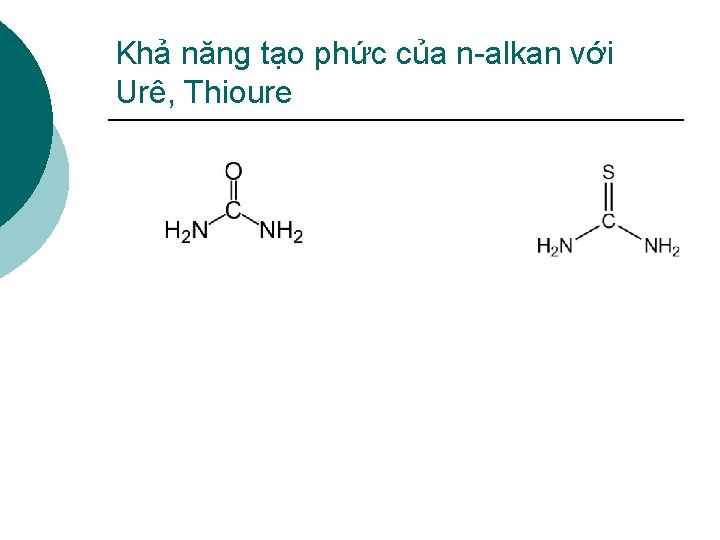
Khả năng tạo phức của n-alkan với Urê, Thioure

II. 3 Naphten (30 -50%) Trong dầu chứa naphten từ 1 đến 4 vòng. - Các phân đoạn nhẹ của dầu thì chứa chủ yếu đồng đẳng của vòng no 5 -6 cạnh. - Các phân đoạn có nhiệt độ sôi dưới 3000 C chứa tới 30% naphten đơn vòng (đối với dầu parafin) và 90% (dầu naphten). - Naphten đa vòng chủ yếu chứa trong phân đoạn có nhiệt độ sôi cao hơn 3000 C. - 41
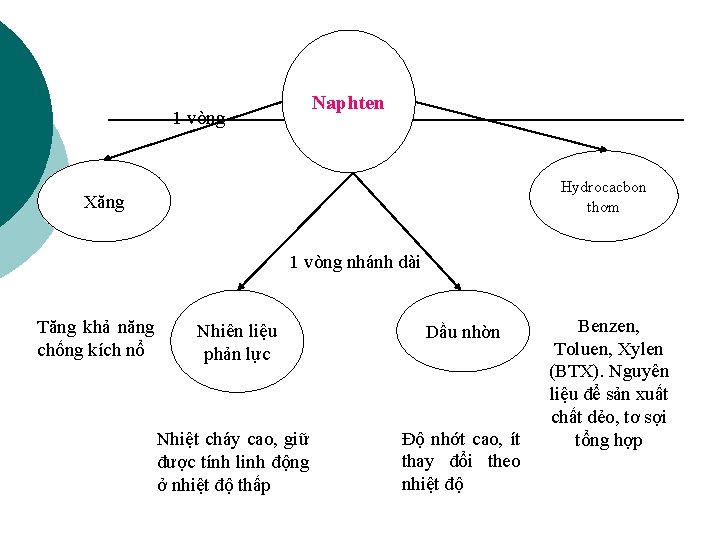
Naphten 1 vòng Hydrocacbon thơm Xăng 1 vòng nhánh dài Tăng khả năng chống kích nổ Nhiên liệu phản lực Dầu nhờn Nhiệt cháy cao, giữ được tính linh động ở nhiệt độ thấp Độ nhớt cao, ít thay đổi theo nhiệt độ Benzen, Toluen, Xylen (BTX). Nguyên liệu để sản xuất chất dẻo, tơ sợi tổng hợp
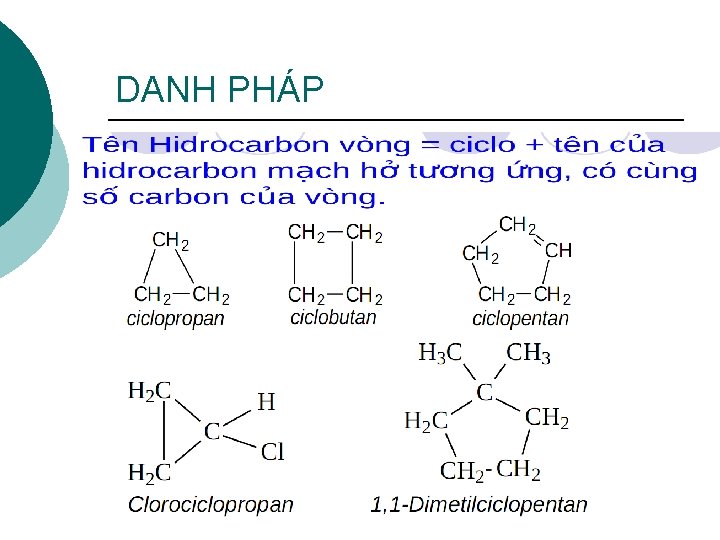
DANH PHÁP

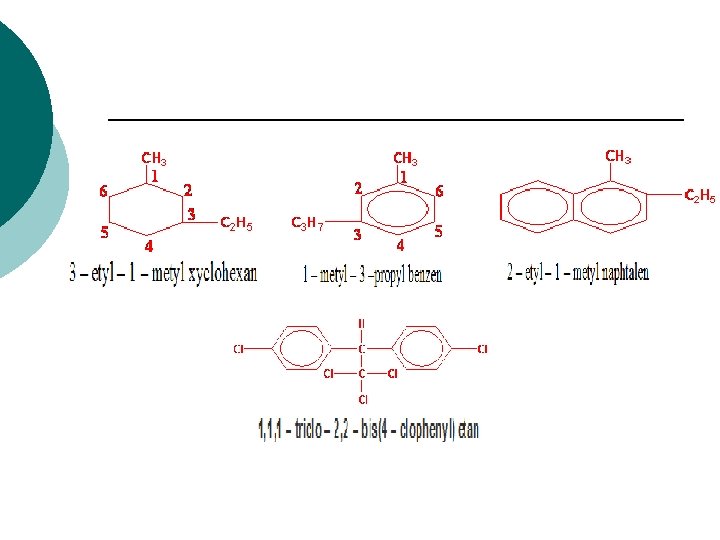
DANH PHÁP ¡ 1. 2. 3. Chú ý đối với Xicloankan mang nhóm thế: So sánh số nguyên tử cacbon trong vòng với số nguyên tử cacbon trên nhóm thế ankyl lớn nhất. Nếu lớn hơn hoặc bằng thì hợp chất là xicloankan mang nhóm thế ankyl, còn ngược lại là ankan mang nhóm thế. Đánh số nhóm thế sao cho locant là nhỏ nhất. Nếu có nhiều nhóm thế khác nhau có cùng cách đánh số thì ưu tiên theo thứ tự mẫu tự. Khi hợp chất có nhiều vòng rời rạc thì mạch chính là mạch thẳng.
![Spiro [2, 3] hexan Spiro [2, 3] hexan](http://slidetodoc.com/presentation_image/150cb18fce5ad65cf2442a8c5e1b4800/image-46.jpg)
Spiro [2, 3] hexan

TÍNH CHẤT VẬT LÍ ¡ ¡ ¡ Cicloankan có nhiệt độ sôi và tỉ trọng thường cao hơn ankan tương ứng. Không tan trong nước nhưng tan trong các dung môi phân cực yếu hoặc không phân cực. Metylciclopentan, metylciclohexan có nhiệt độ sôi, nhiệt độ nóng chảy thấp hơn ciclopentan, ciclohexan. Hydrocacbon Nhiệt độ sôi, o. C Nhiệt độ nóng chảy, o. C Pentan 36 -130 Ciclopentan 49 -94 Hexan 69 -95 Ciclohexan 81 6, 3 Metylciclohexan _ -126, 3 48

Trị số Octan của Naphten ¡ ¡ Naphten có trị số Octan cao hơn so với các Alkan mạch thẳng tương ứng. Naphten có mạch nhánh alkyl dài có trị số Xetan thấp hơn so với các n-alkan có cùng số C. Hydrocacbon Trị số Octan Pentan 62 Ciclopentan 87 Hexan 26 Ciclohexan 77 Metylciclohexan 72 Heptan 0 49

Khả năng chống kích nổ của Naphten ¡ ¡ Khi có nhiều nhánh phụ ngắn, thì khả năng chống kích nổ tốt hơn so với naphten có nhánh phụ dài, với số C trong nhánh phụ bằng tổng số C trong các nhánh phụ ngắn. Vị trí nhánh phụ dính vào đâu ở vòng naphten không ảnh hưởng mấy đến khả năng chống kích nổ của nó. Khi nhánh phụ của vòng naphten là mạch nhánh thì khả năng chống kích nổ sẽ tăng. Đối với các vòng không no thì khả năng chống kích nổ cao hơn đối với vòng naphten tương ứng.
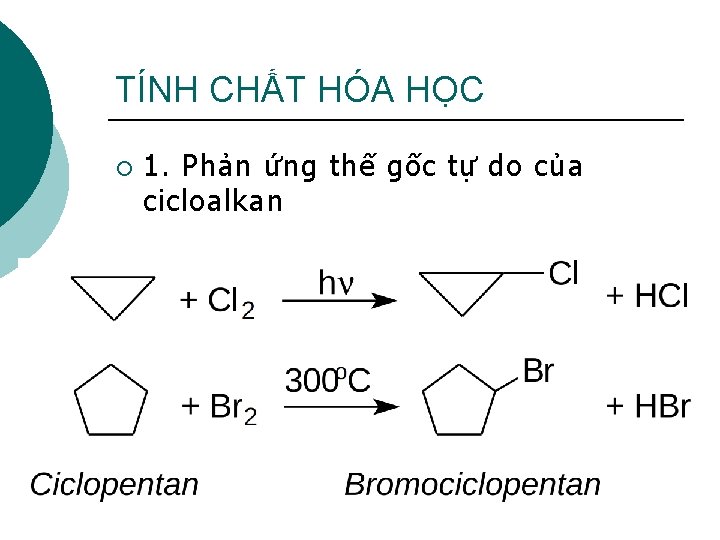
TÍNH CHẤT HÓA HỌC ¡ 1. Phản ứng thế gốc tự do của cicloalkan
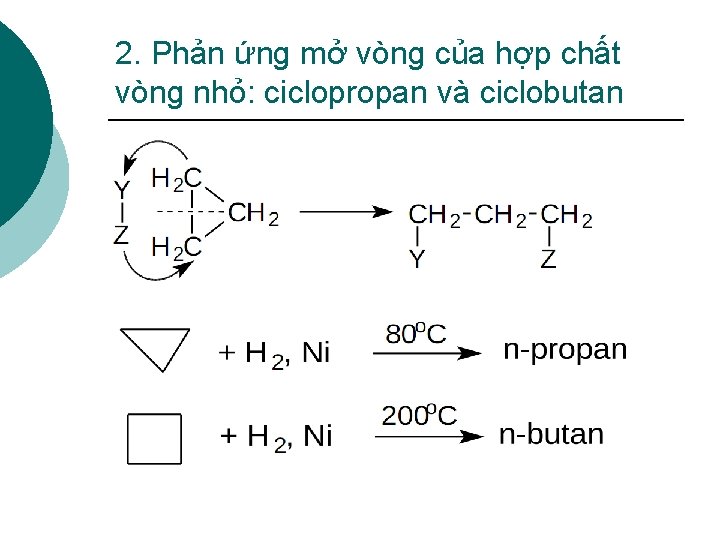
2. Phản ứng mở vòng của hợp chất vòng nhỏ: ciclopropan và ciclobutan

Sức căng Baeyer ¡ góc CCC trong xiclopropan bằng 60 o, ¡ góc CCC trong xiclobutan bằng 90 o, ¡ góc CCC của liên kết đơn là 109 o 28’ giống như trong alkan.
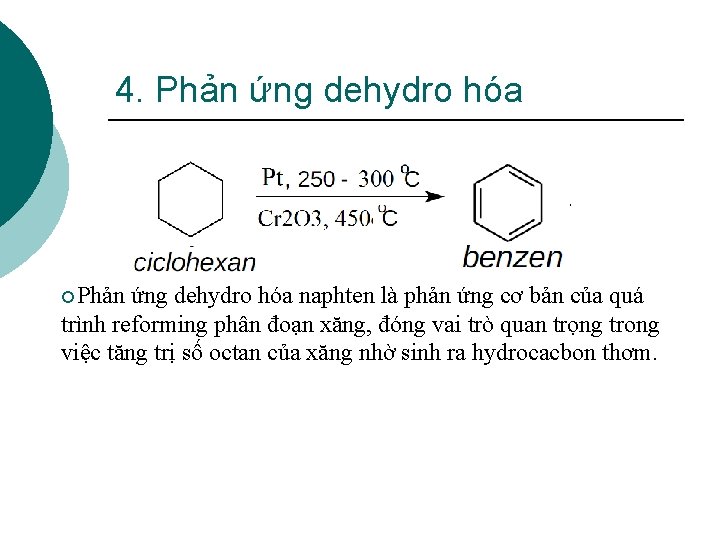
4. Phản ứng dehydro hóa ¡Phản ứng dehydro hóa naphten là phản ứng cơ bản của quá trình reforming phân đoạn xăng, đóng vai trò quan trọng trong việc tăng trị số octan của xăng nhờ sinh ra hydrocacbon thơm.

¡ ¡ Ở điều kiện nhiệt độ và xúc tác trên, các ciclopentan và đồng đẳng ciclopentan; 1, 1 -dimetylciclohexan, các naphten đa vòng nối cầu không xảy ra phản ứng dehydro hóa (về nhiệt động là không thể diễn ra, vì ở bất cứ nhiệt độ nào năng lượng tự do của hydrocacbon thơm tương ứng đều cao hơn naphten vòng 5). => Xác định lượng naphten vòng 6 cạnh trong các phân đoạn xăng và kerosen.

5. Phản ứng nối vòng Naphten Chuyển hóa vòng 5 thành vòng 6 cạnh, tạo các naphten đa vòng. ¡ Điều kiện phản ứng: nhiệt độ phòng, xúc tác Al. Br 3, thời gian ngắn để ngăn cản sự đồng phân hóa của các ciclohexan tạo thành. => Phản ứng xác định lượng naphten vòng 5 cạnh (tiếp theo dehyđro hóa tạo aromat) ¡

6. Phản ứng tạo phức với Thioure Độ bền phức tạo thành phụ thuộc vào cấu trúc phân tử hyđrocacbon và kích thước của nó. => tách các naphten có cấu trúc khác nhau hoặc có cùng khối lượng phân tử, thậm chí tách các naphten đơn vòng và đa vòng vì các hợp chất đa vòng tạo phức bền hơn với Thioure. ¡

7. Phản ứng cháy ¡ (CH 2)n + 3 n/2 O 2 → n. CO 2 + n. H 2 O + Nhiệt C 4 H 8 + 6 O 2 → 4 CO 2 + 4 H 2 O Lượng nhiệt này thay đổi tùy theo kích thước của vòng.
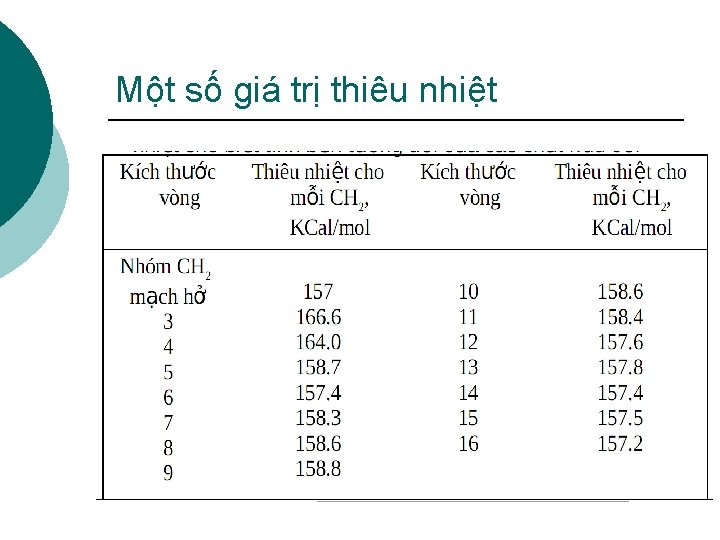
Một số giá trị thiêu nhiệt

8. Phản ứng cộng với dd Br 2 ¡ Ciclopropan giống như alken, làm phai màu dung dịch brom trong CCl 4. Nhưng Ciclopropan khác với alken và alkin là không tác dụng với dung dịch KMn. O 4 loãng, lạnh, trung hòa.

Phương pháp định lượng Naphten ¡ Phân đoạn xăng chứa 50% naphten. Xác định trong phân đoạn xăng trên chứa bao nhiêu phần trăm ciclopentan, ciclohexan?

Phương pháp loại Naphten ¡ Cho: hỗn hợp hydrocacbon gồm nalkan, izo-alkan, naphten.


II. 2 HIDROCACBON KHÔNG NO ¡ Trong dầu hầu như không tìm thấy olefin hoặc chỉ có một lượng rất nhỏ ở một số mỏ. Các olefin được tạo thành trong quá trình chế biến dầu – olefin (n-, izo-), xicloalken, aromat có liên kết bội ở mạch nhánh.

Tính chất hóa học đặc trưng Tác dụng với H 2: Xúc tác Pt, Pd, nhiệt độ phòng TN. Xúc tác Ni, T=180 o. C. R-CH=CH 2 + H 2 R-CH 2 -CH 3 Ở điều kiện này, các aromat không bị hydro hóa => phản ứng xác định hàm lượng alken trong các phân đoạn sản phẩm. ¡ 65

Tính chất hóa học đặc trưng ¡ Halogen hóa: R-CH=CH 2 + Br 2 R-CHBr-CH 2 Br Phản ứng dùng tách các hydrocacbon không no ra khỏi hỗn hợp các hydrocacbon còn lại. 66

Tính chất hóa học đặc trưng Tác dụng với H 2 SO 4(đđ) ¡ Tác dụng với Ozon (aromat không tác dụng) ¡

Tính chất hóa học đặc trưng ¡ Phản ứng với thủy ngân acetate:

Tính chất hóa học đặc trưng alkadien ¡ Phản ứng với maleic anhydride:

II. 4 HIDROCACBON THƠM ¡ Trong dầu chứa chủ yếu các hidrocacbon thơm từ 1 -4 vòng. (15 -20%) ¡ Phân đoạn có nhiệt độ sôi dưới 2000 C chủ yếu chứa các đồng đẳng của benzen. ¡ Phân đoạn có nhiệt độ sôi 200 đến 3000 C chứa các đồng đẳng của benzen và naphtalin. ¡ Phân đoạn có nhiệt độ sôi dưới 400 -5000 C chủ yếu chứa các đồng đẳng của naphtalin và antrasen.
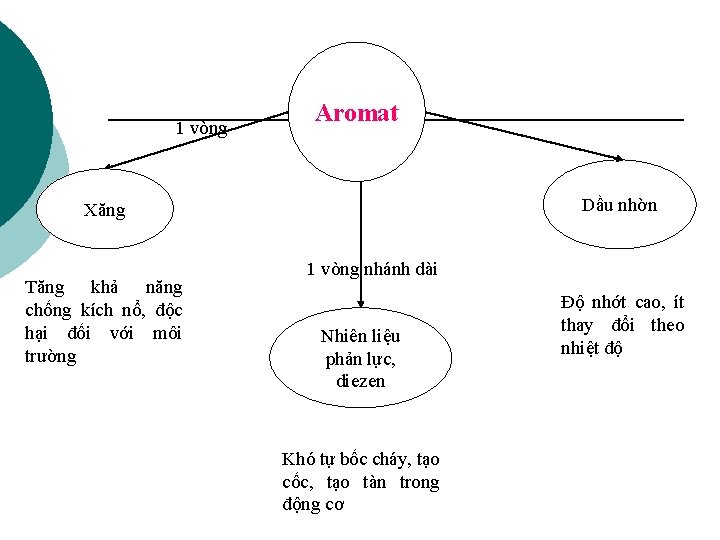
1 vòng Aromat Dầu nhờn Xăng Tăng khả năng chống kích nổ, độc hại đối với môi trường 1 vòng nhánh dài Nhiên liệu phản lực, diezen Khó tự bốc cháy, tạo cốc, tạo tàn trong động cơ Độ nhớt cao, ít thay đổi theo nhiệt độ

III. THÀNH PHẦN PHI HIDROCACBON 1. Các hợp chất chứa lưu huỳnh ¡ H 2 S ¡ RSH ¡ RSR ¡ RSSR ¡ Tiophen ¡ Tiophan
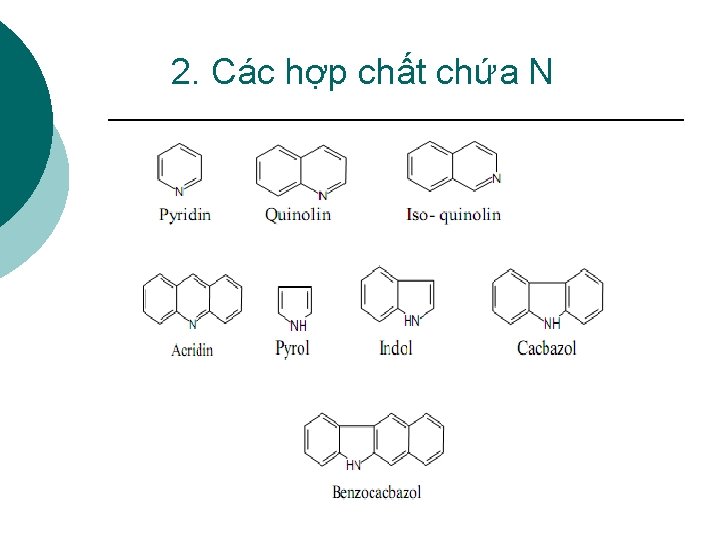
2. Các hợp chất chứa N

2. Các hợp chất chứa N ¡ Các hợp chất N được ứng dụng làm chất sát trùng, chất ức chế ăn mòn, phụ gia cho dầu bôi trơn và bitum, chất chống oxy hóa … Nhưng các hợp chất N lại làm giảm hoạt độ của xúc tác, tạo nhựa và tạo màu sẫm trong sp dầu.
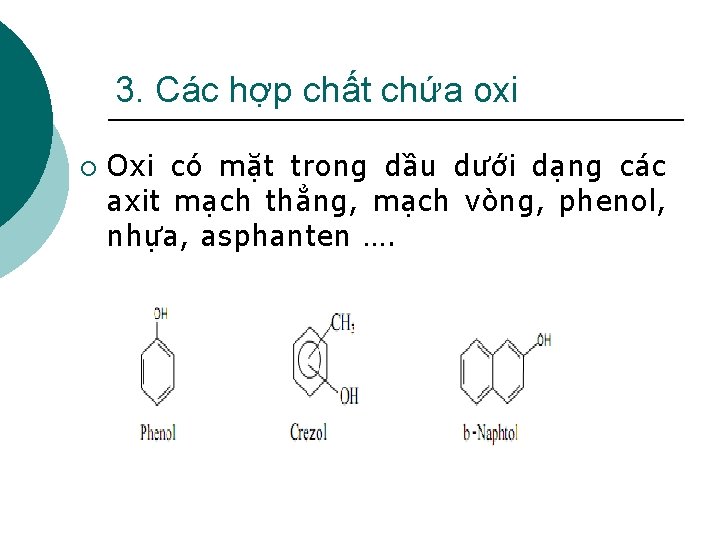
3. Các hợp chất chứa oxi ¡ Oxi có mặt trong dầu dưới dạng các axit mạch thẳng, mạch vòng, phenol, nhựa, asphanten ….

4. Các chất nhựa và asphanten ¡ Nhựa và asphanten là những chất chứa đồng thời các nguyên tố C, H, O, S, N; có phân tử lượng lớn hơn 500 đến 600 đ. v C trở lên. Nhìn bề ngoài chúng có màu xẫm, nặng hơn nước (tỉ trọng lớn hơn 1) và không tan trong nước.
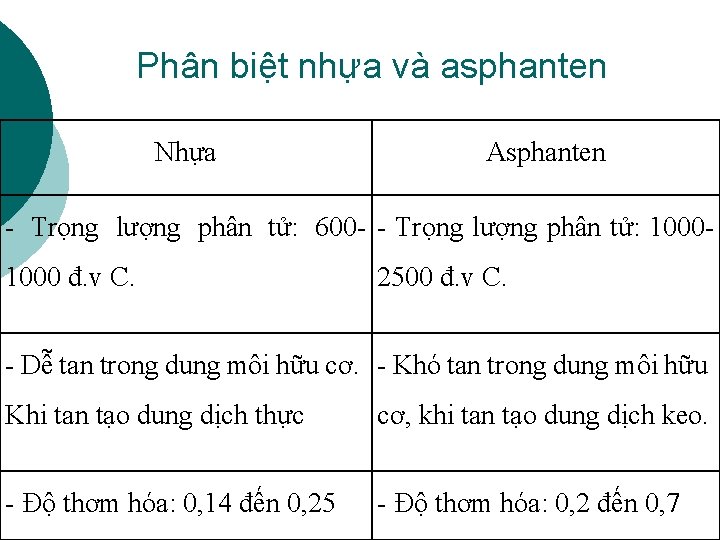
Phân biệt nhựa và asphanten Nhựa Asphanten - Trọng lượng phân tử: 600 - - Trọng lượng phân tử: 1000 đ. v C. 2500 đ. v C. - Dễ tan trong dung môi hữu cơ. - Khó tan trong dung môi hữu Khi tan tạo dung dịch thực cơ, khi tan tạo dung dịch keo. - Độ thơm hóa: 0, 14 đến 0, 25 - Độ thơm hóa: 0, 2 đến 0, 7

5. Các khoáng chất Trong dầu có thể chứa tới khoảng 4% nước và các muối khoáng hòa tan trong nước.

5. Các khoáng chất ¡ Trong nước khoan chứa một lượng lớn các muối khoáng. Các cation thường gặp là: Na+, Ca 2+, Mg 2+ và ít hơn có Fe 2+ và K+. Các anion thường gặp là: Cl-, HCO 3 - và ít hơn có SO 42 - và CO 32 -. Ngoài ra còn một số kim loại không phân ly ở dạng keo như Al 2 O 3, Fe 2 O 3, Si. O 2. Trong số này thì nhiều nhất là ion Na+ và Cl-, có khi lên đến 90%.

V. THÀNH PHẦN CHƯNG CẤT PH N ĐOẠN ¡ Một số phân đoạn chính thường được tách ra từ dầu: + Phân đoạn xăng: 28 – 180 o. C + Phân đoạn kerosen: 180 – 250 o. C + Phân đoạn diezen: 250 – 350 o. C + Mazut: > 350 o. C + Gasoil nặng: 350 – 550 o. C + Phần cặn gudron > 550 o. C

VI. PH N LOẠI DẦU MỎ ¡ Dầu thô muốn đưa vào các quá trình chế biến hoặc buôn bán trên thị trường, cần phải xác định xem chúng thuộc loại nào: dầu nặng hay nhẹ, dầu chứa nhiều hydrocacbon parafinic, naphtenic hay aromatic, dầu có chứa nhiều lưu huỳnh hay không? Từ đó mới xác định được giá trị trên thị trường và hiệu quả thu được các sản phẩm khi chế biến. 81

A. PH N LOẠI DẦU MỎ THEO BẢN CHẤT VẬT LÝ 1. Theo tỷ trọng Dựa vào tỷ trọng có thể phân loại dầu theo 3 cấp, 4 cấp hoặc 5 cấp. - Dầu nhẹ: d 15/4 < 0. 830, hoặc d 15/15 < 0. 828 - Dầu trung bình: 0. 830 – 0. 884 0. 828 – 0. 884 - Dầu nặng: > 0. 884 82

¡ 83

2. Theo chỉ số 0 API ¡ Chỉ ¡ số 0 API co thể thay thế cho tỷ trọng dầu trong phân loại dầu thô. 0 API = 141, 5/d (15/15) – 131, 5 84

3. Theo chỉ số tương quan ¡ CI = 48640/Ttr. b + 473, 7. d 15, 6 – 456, 8 ¡ Nếu CI từ: - 0 đến 15 là parafin - 15 đến 50 là naphten hoặc hỗn hợp parafin, naphten, aromat. - lớn hơn 50 là hydrocacbon thơm 85

B. PH N LOẠI THEO PHƯƠNG PHÁP HÓA HỌC 1. Theo phương pháp của viện dầu mỏ Hoa Kỳ ¡ Phương pháp này thực hiện bằng cách đo tỷ trọng của 2 phân đoạn dầu mỏ. ¡ Phân đoạn 1 với giới hạn nhiệt độ sôi 250 – 275 o. C, được tách ra bằng cách chưng cất dầu mỏ ở áp suất thường. ¡ Phân đoạn 2 với giới hạn nhiệt độ sôi 275 – 300 o. C ở áp suất chân không (40 mm. Hg) (tương đương 390 – 415 o. C ở áp suất thường). 86
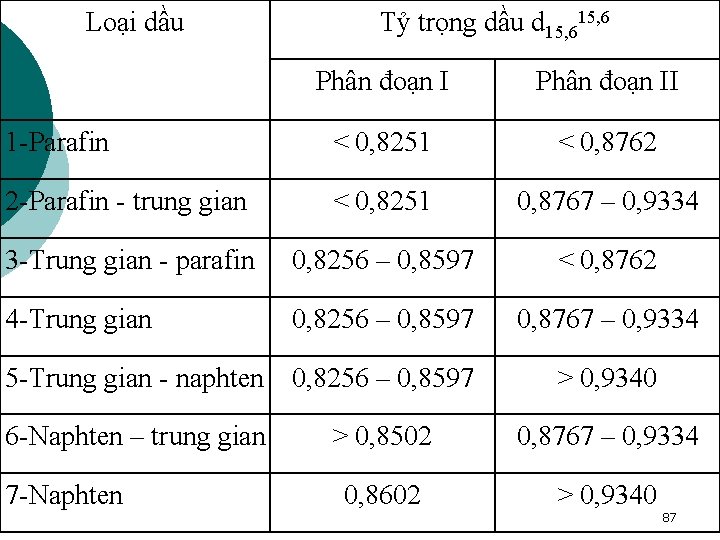
Loại dầu Tỷ trọng dầu d 15, 6 Phân đoạn II 1 -Parafin < 0, 8251 < 0, 8762 2 -Parafin - trung gian < 0, 8251 0, 8767 – 0, 9334 3 -Trung gian - parafin 0, 8256 – 0, 8597 < 0, 8762 4 -Trung gian 0, 8256 – 0, 8597 0, 8767 – 0, 9334 5 -Trung gian - naphten 0, 8256 – 0, 8597 6 -Naphten – trung gian 7 -Naphten > 0, 9340 > 0, 8502 0, 8767 – 0, 9334 0, 8602 > 0, 9340 87

2. Phân loại theo phương pháp Nelson, Watson và Murphy Theo phương pháp này Nelson và Walson đã đề ra một hằng số đặc trưng K: ¡ Trong đó, T - nhiệt độ sôi trung bình của dầu mỏ, tính bằng độ Reomuya (o. R) ¡ d – tỷ trọng dầu thô, xác định ở 15. 6 o. C (60 o. F) so với nước ở cùng nhiệt độ 88

2. Phân loại theo phương pháp Nelson, Watson và Murphy Giới hạn hệ số K đặc trưng để phân chia dầu mỏ như sau: ¡ Họ parafinic: K = 13 – 12. 15 ¡ Họ trung gian: K = 12. 10 – 11. 5 ¡ Họ naphtenic: K = 11. 45 – 10. 5 ¡ Họ aromatic: K = 10 89
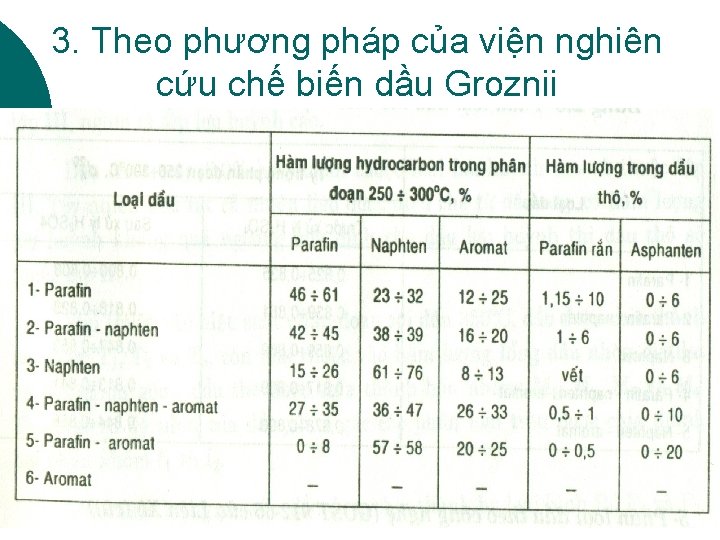
3. Theo phương pháp của viện nghiên cứu chế biến dầu Groznii 90

4. Theo phương pháp của viện dầu mỏ pháp 91
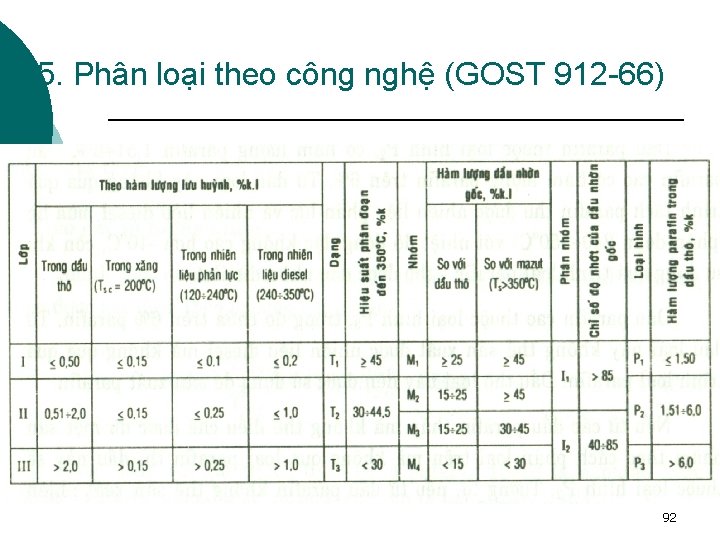
5. Phân loại theo công nghệ (GOST 912 -66) 92

¡ IIT 1 M 2 I 2 P 3 93

Các vòng kém bền như cicloanpropan, ciclobutan có thể tham gia cộng mở vòng tương tự hidrocacbon không no.

Thank you for your attention !!! Spasibo za vnhimanie !!!
- Slides: 95