Triagem da Doena Metablica ssea Prticas entre Neonatologistas

Triagem da Doença Metabólica Óssea Práticas entre Neonatologistas dos EUA Apresentador: Henrique Yuji Watanabe Silva R 3 UTIP- HMIB/SES/DF Unidade de Neonatologia do HMIB Email: wshenriqueyuji@gmail. com www. paulomargotto. com. br Brasília, 4 de janeiro de 2017

INTRODUÇÃO Baixo peso ao nascer e prematuridade sabidamente predispõem à doença metabólica óssea (DMO). Prevalência: 23% em nascidos <1500 g e 60% em <1000 g. (1) Mais prevalente naqueles em amamentação exclusiva (40%) e também reportado naqueles alimentados com fórmulas (16%). (2) A mineralização óssea ocorre predominantemente no 3° trimestre de gestação. Cerca de 80% da transferência de cálcio e fósforo para os ossos ocorre entre a 24ª semana de gestação e o período de termo. (3) Outros fatores de risco: pré-eclâmpsia, restrição de crescimento intrauterino, corioamnionite (associados com lesão placentária crônica, potencialmente associado com diminuição do transporte de fósforo intra-útero 4 ), uso de medicações (diuréticos, corticóides, metilxantinas, anfotericina b) e oferta inadequada de cálcio e fósforo.

INTRODUÇÃO Os movimentos do feto contra a parede uterina auxilia para o apropriado conteúdo mineral ósseo e o desenvolvimento muscular. (5) No entanto esta carga de movimentos não pode ser replicada no ambiente extrauterino e a ausência de estimulação pode resultar no aumento da reabsorção óssea e diminuição da massa óssea. A DMO tipicamente se desenvolve 6 -12 semanas após o nascimento, (1) mas geralmente vai ser assintomática por várias semanas antes de sua detecção. Fraturas podem ser vistas entre 10 -20% dos pacientes com baixo peso ao nascer. (3) Devido a falta de guidelines para o diagnóstico, tratamento e prevenção da DMO e a ampla variedade da prática quanto ao tema no Reino Unido(4), os autores apresentam os resultados de um questionário descrevendo a prática em uma Unidade de Cuidados Intensivos Neonatal nos Estados Unidos

AMOSTRA E MÉTODOS Pesquisa nacional (EUA) com aplicação de questionário a Neonatologistas via e-mail. Critério de inclusão: Neonatologistas membros da AAP (American Academy of Pediatrics -Academia Americana de Pediatria) Perinatal Section (Sessão Perinatal) que atendessem em Unidade de Cuidados Intensivos Neonatal (UTIN) nível IIIB e IIIC 7 (que rotineiramente cuidam de RN ≤ 28 semanas e peso de nascimento ≤ 1500 g).

QUESTIONÁRIO Pesquisa online composta de 29 questões fechadas, de múltipla escolha, com resposta aberta apenas no caso de escolha da opção “nenhuma das anteriores”. Perguntas: § 2 demográficas (CEP e número de leitos) § 12 screening (se era realizado, critérios para iniciar o screening, testes utilizados, tempo e frequência dos testes) § 15 diagnóstico e tratamento (prevenção de DMO, etiologia identificada da DMO, métodos e critérios diagnósticos, estratégias de tratamento, incluindo tempo de início e término da terapia). Manejo primário da equipe, follow-up e capacitação de staffs também foram avaliados.

RESULTADOS AMOSTRA 338 neonatologistas, representando 246 UTIN, responderam ao questionário. 86% (n= 292) responderam que realizavam algum tipo de screening para DMO e continuaram a pesquisa. Dos 292, 86% (253/292) completaram a pesquisa. O número de leitos referidos variou de 10 -135 (média de 44) por UTIN.

RESULTADOS SCREENING Foi baseado principalmente na idade gestacional (70, 8%) e peso ao nascimento (63, 8%). Os pontos de corte mais comuns para a idade gestacional (IG) e peso ao nascer (PN) foram <28 semanas (37, 5%) e <1000 g (35, 3%), respectivamente. Pontos de corte para IG variaram de 26 -36 semanas.

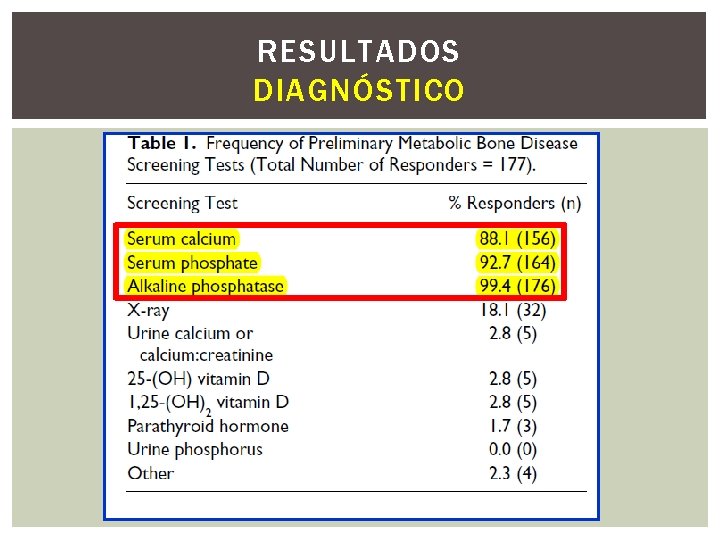
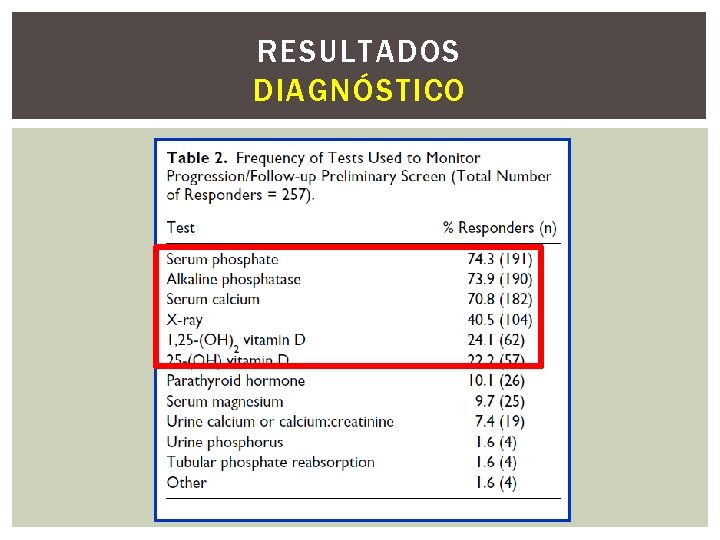
RESULTADOS SCREENING Outros critérios foram: achados radiográficos de osteopenia ou fratura (56, 1%), utilização de nutrição parenteral total (NPT) por tempo > 2 semanas (48, 3%), uso repetido de diurético (41, 13%), PIG, restrição de crescimento intrauterino (28, 4%), ou uso exclusivo de leite materno com ou sem fortificante (9, 6% ). O uso de um único teste para screening foi reportado apenas por 32, 7% dos participantes, com a grande maioria remanescente apontando o uso de 2 ou mais testes para o screening inicial. Na Tabela 1, os Teste usados para o screening, sendo os mais frequente a calcemia, a fosfatase alcalina e o fósforo sérico. Os testes avaliando a reabsorção tubular de fosfato foram usados como “testes adicionais” para monitorizar a progressão da doença ou para o seguimento do screen preliminar ( Tabela 2)
RESULTADOS DIAGNÓSTICO
RESULTADOS DIAGNÓSTICO

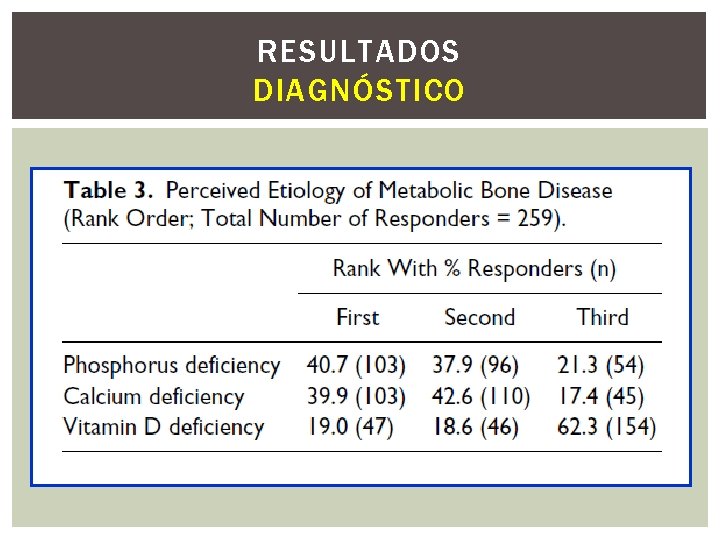
RESULTADOS Uso exclusivo de leite humano não foi o maior determinante para as práticas do screening. O tempo de início do screening para DMO variou pelo estado de alimentação 53, 2% indicariam o screening enquanto os recém nascidos estivessem em NTP, enquanto outros aguardariam até que ele estivessem com dieta plena (30, 2%) A opção outros foi escolhida por 33. 2% (sendo que alguns se baseariam na idade cronológica- screening iniciado empiricamente após 2 -4 semanas depois do nascimento) Screening seria continuado então semanalmente (45, 2%), quinzenalmente (32%), mensalmente (5, 4%), ou de forma individualizada (12, 7%). Em relação a etiologia, a deficiência de fósforo teve o maior impacto no desenvolvimento da doença, seguida pela deficiência de cálcio e vitamina D (Tabela 3). Fosfatase alcalina foi quase que universalmente utilizado como critério diagnóstico, mais comumente com valor de corte > 500 U /L (58, 6%). Valores de corte variando de >300 a > 1000 U/L.
RESULTADOS DIAGNÓSTICO

RESULTADOS TRATAMENTO A intervenção primária mais comumente relatada tanto para prevenir (93, 4%) como para tratar (83, 1%) a DMO foi a fortificação do leite humano. As suplementações de vitamina D, de cálcio, fósforo também foram amplamente utilizadas no tratamento da DMO (67%, 65%, e 65%, respectivamente). Os tratamentos alternativos incluíram fisioterapia (19%), calcitriol (29%), e bisfosfonatos (<1%). A decisão de parar a terapia foi baseada predominantemente em resultados de testes bioquímicos. Outros responderam parar o tratamento na alta (17, 4%) e outros apontaram parar a terapia no meio intrahospitalar (22, 5%).

RESULTADOS A Neonatologia foi relatada como o Departamento de manejo por 89, 8% O envolvimento nutricionista foi relatada por 84, 8% Medidas especiais sob a forma de precauções de manuseio (83, 0%), sinais de cabeceira (64, 8%), gráficos adesivos (7, 1%), e de sinalização eletrônica (3, 8%) também foram utilizados. 26, 4% relataram ter programas de treinamento de educação formal para o pessoal envolvido na assistência ao paciente em situação de risco manejo pós-alta: Pediatra geral (75, 8%), follow-up neonatal (34, 3%), endocrinologia (18, 8%) e gastroenterologia / nutrição (10, 2%)

DISCUSSÃO Os dados disponíveis são limitados para orientar as práticas de rastreio e tratamento da DMO. A experiência clínica, em vez de evidências sólidas, foi frequentemente citado recentemente pela AAP. Também houve uma mudança no panorama da prematuridade. O aumento da sobrevida de RN com idades gestacionais mais precoces, a introdução antecipada de nutrição enteral e o menor tempo de ventilação mecânica podem afetar o potencial de desenvolvimento da DMO. Dados publicados há 10 anos podem não refletir as necessidades dos RN pré-termos extremos e de baixo peso de hoje.

DISCUSSÃO O desenvolvimento da DMO provavelmente seja multifatorial, mas prematuridade é o fator de risco mais importante para o seu desenvolvimento. A demanda aumentada para o crescimento e estoques inadequados de minerais predispõem a doença, com a deficiência de fósforo como a peça fundamental para o desenvolvimento de DMO (hipodesenvolvimento da matriz óssea). Apesar da absorção de 60% de cálcio e de 80% de fósforo do leite humano pelo recém-nascido, a alimentação com leite humano não fortificado (180 a 200 m. L/d) só fornece um terço do nível de cálcio e fósforo oferecidos no meio intrauterino. (8) Cuidado deve ser tomado quando alimentar com Leite Humano de Banco não fortificado, pois o mesmo tem menor teor de fósforo do que o leite humano não estocado em Banco. (1)

DISCUSSÃO ENTENDO A FISIOPATOLOGIA DA DMO Independentemente da idade gestacional ao nascer, após o nascimento ocorre uma queda abrupta no suprimento mineral, apesar da demanda contínua. Os níveis mais baixos de cálcio nos RN a termo ocorre em 18 horas e nos recém-nascidos prematuros, 24 horas. (9) Em resposta à demanda contínua, os níveis de parathormônio (PTH) aumentam. O aumento do PTH promove perda renal de fósforo, estimula a reabsorção renal de cálcio diretamente e estimula a conversão renal de 25 - (OH) vitamina D inativa em 1, 25 - (OH)2 vitamina D, que promove a absorção intestinal de cálcio. Uma consequência do aumento da PTH é o alto nível de fósforo urinário nas primeiras 48 a 72 horas após o nascimento. (9) A fosfatúria, além de maiores exigências metabólicas para o fósforo, podem predispor a depleção do fósforo.

DISCUSSÃO ENTENDENDO A FISIOPATOLOGIA DA DMO Os níveis séricos de cálcio tipicamente permanecem normais no processo da doença, uma vez que o corpo mantém níveis séricos, invocando um estado hiperparatireoidismo compensatório que leva à reabsorção mineral óssea e perda de fosfato urinário. Mais frequentemente, fósforo sérico persistentemente baixo ou a sua queda refletem uma ingestão inadequada de fósforo, caso em que o PTH não está elevado e a perda de fósforo urinário não ocorre. (18) No entanto, em resposta a hipofosfatemia, 1, 25 - (OH)2 Vitamina D se torna cada vez mais abundante e pode até levar a hipercalcemia e hipercalciúria. (21) Com base nesta fisiologia, a utilidade de medir os níveis urinários de cálcio e fósforo como adjuvante na triagem torna-se aparente. Aumento dos níveis urinários de cálcio pode ser visto com diminuição da ingestão de fósforo. (19). O prematuros terão tipicamente um fósforo urinário baixo, um limiar com aumento da excreção, independentemente do baixo nível sérico. (23) Assim, o aumento da reabsorção tubular sugere diminuição da ingesta. (23)

DISCUSSÃO Tem sido dado recentemente ênfase maior a estratégias mais agressivas de alimentação que incluem NPT com suporte de proteína mais precoce e maior além de nutrição enteral com o objetivo de evitar o estado catabólico e promover o crescimento. O aumento de fornecimento de proteína aumenta a captação intracelular de fósforo. Prolongada exposição a medicamentos como furosemide, metilxantinas e corticosteróides promove aumento das perdas urinárias e mobilização do cálcio dos ossos. (1, 12) Koo et al, em 1980 descreveram os critérios radiográficos para o diagnóstico. No entanto a desmineralização pode ocorrer antes da evidência de raquirismo. (13) A densiometria óssea pode ter papel na facilitação do diagnóstico da DMO, porém não está disponível em larga escala.

DISCUSSÃO A medição da FAL sérica e do fosfato sérico como screening bioquímico para raquitismo tem sido recomendada. (6) Um aumento esperado da FAL ocorre após o nascimento com níveis de pico entre 5 e 6 semanas de idade. (14) Em alguns lactentes, porém, este pico pode não ocorrer por 2 a 3 meses após o nascimento. (14) Um nível crescente após o pico esperado pode refletir uma diminuição da oferta mineral.

DISCUSSÃO Existe fraca correlação entre níveis elevados de fosfatase alcalina (FAL) e o grau de mineralização. Além disso, níveis de FAL podem não ser confiáveis na vigência do uso de corticoides que podem suprimir os seus níveis. Embora níveis de FAL >800 -1000 IU/L sejam sugestivos de raquitismo, o raquitismo pode ser encontrado com níveis <600 IU/L Um nível de FAL >700 IU/L foi mais sensível (73%) e específico (74%) no diagnóstico em uma população de prematuros com idade gestacional média de 29 semanas no estudo de Hung et al. (16) No estudo de Pieltrain et al( 20) a FAL foi sugestiva ser um melhor marcador para risco de fratura do que DMO nos prétermos.

DISCUSSÃO Um desafio adicional é que o limiar para a "prevenção" do raquitismo pode não ser visto como o mesmo limiar que indica a necessidade de radiografias para excluir raquitismo. Assim, a identificação de uma FAL (abaixo do limiar típico de 800 a 1000 UI / L) e um fósforo sérico decrescente, particularmente no recém-nascido pré-termo amamentado ao seio com menos de 27 a 28 semanas de gestação pode necessitar de intervenção imediata com suplementação de fósforo. Esta abordagem usando a FAL e os níveis séricos de fósforo na prevenção do raquitismo e recomendações além da suplementação adequada de cálcio e fósforo não foi sistematicamente estudada.

DISCUSSÃO A justificação para a prevenção a curto prazo é óbvia: evitar fraturas, deficiente ganho de peso, dificuldade do desmame do suporte ventilatório. Catch-up da mineralização parece ocorrer em torno de 6 meses d idade corrigida, com base nos estudos nos anos 1990 (24), embora a prolongada nutrição parenteral total, doença hepática, malabsorção e o uso prolongado de corticosteróide podem alterar o curso nos pré-termos.

DISCUSSÃO No entanto, a consequência a longo prazo da diminuição da massa óssea permanece não esclarecida. Um uma coorte de pré-termos (idade gestacional<37 semanas; peso ao nascer <1850 g), recrutados entre 1982 e 1985, randomizados para o uso do leite materno versos fórmula e estudados no novamente na idade de adultos jovens, foram ientificados: menor estatura, maior índice de massa corporal, menor massa óssea na espinha lombar em relação aos dados de referência. (25) Neste estudo o impacto do raquitismo radiográfico ou bioquímico no pico da massa óssea não foi esclarecido e nem a extensão com que afetou os seus riscos de osteoporose mais tarde na vida.

CONCLUSÕES O presente estudo, através de um questionário, com as limitações inerentes a esse processo, mostra a falta de estudos que apontem a prevalência real da doença, assim como a falta de consenso sobre definição, screening, prevenção e tratamento de DMO Mais pesquisas são necessárias para o desenvolvimento e otimização de estratégias de prevenção, reconhecimento e manejo da doença

ABSTRACT

REFERENCES

REFERENCES

NOTA DO EDITOR DO SITE, DR. PAULO R. MARGOTTO CONSULTEM TAMBÉM! AQUI E AGORA! ESTUDANDO JUNTOS! Rio Araguaia (Caseara, Tocantins- 2/1/2017)

Serial serum alkaline phosphatase as an early biomarker for osteopenia of prematurity. Abdallah EA, Said RN, Mosallam DS, Moawad EM, Kamal NM, Fathallah MG. Medicine (Baltimore). 2016 Sep; 95(37): e 4837. . PMID: 2016 27631238 Dezesseis lactentes (13, 3%) que apresentaram evidência de osteopenia no Raio X e 104 bebês (86, 7%) que não foram osteopênicos tinham <1000 g de peso ao nascer. O peso ao nascer e a idade gestacional foram significantemente inversamente relacionados com os níveis de FAL séricas. Ambas as amostras mostraram significantemente maior nível médio de FAL em osteopênicos do que nos não-osteopênicos (P <0, 001 e P <0, 001, respectivamente). Não houve valor constante de FAL sérica relacionada à evidência radiológica de osteopenia. No entanto, o valor de corte da FAL sérica no qual a osteopenia é detectada é de 500 UI / L com 100% de sensibilidade e 80, 77% de especificidade. Altos níveis de FAL podem ser considerados um biomarcadores confiáveis para prever o estado da mineralização óssea e a necessidade de nos lactentes prematuros, particularmente aqueles <1000 g de peso ao nascer e <32 semanas de gestação
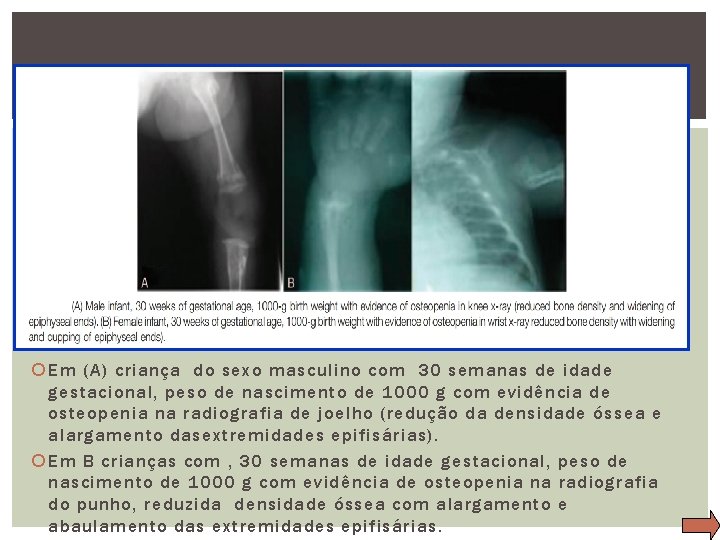
Em (A) criança do sexo masculino com 30 semanas de idade gestacional, peso de nascimento de 1000 g com evidência de osteopenia na radiografia de joelho (redução da densidade óssea e alargamento dasextremidades epifisárias). Em B crianças com , 30 semanas de idade gestacional, peso de nascimento de 1000 g com evidência de osteopenia na radiografia do punho, reduzida densidade óssea com alargamento e abaulamento das extremidades epifisárias.

A análise dos valores de FAL para o diagnóstico de osteopenia mostrou que não existe um valor constante no qual a evidência de osteopenia foi detectada. Contudo, o ponto de corte ótimo com um nível de FAL de 500 UI / L revelou sensibilidade a 100%, mas 80, 77% de especificidade, estando de acordo com autores que relataram que na ausência de doença hepática, níveis séricos de FAL> 4 vezes os níveis normais de adultos foram considerados como um marcador de doença óssea e níveis séricos de FAL> 600 IU / L têm uma sensibilidade diagnóstica de 100% e especificidade de 70%. Mitchel et al em uma revisão de 100 bebês de baixo peso ao nascer, relataram que os níveis de FAL> 600 IU / L foram comumente detectados. No entanto, nenhum valor único de FAL pode ser determinado como preditivo das alterações ósseas.

No entanto, os autores recomendam uma radiografia do pulso e / ou do joelho para avaliar raquitismo em prematuros quando múltiplas medidas de FAL são> 800 UI / L (2 valores medidos pelo menos uma semana de intervalo). Hung et al relataram que os níveis de FAL> 700 IU / L, com 3 semanas de idade, resultaram em uma sensibilidade e especificidade de 73% na predição de DMO em prematuros. No entanto, Backström et al relataram que uma combinação de FAL> 900 IU / L e concentrações séricas de fosfato inorgânico <5, 4 mg% produziu uma sensibilidade de 100% e uma especificidade de 70%. Eles também sugeriram este método para a triagem de baixa DMO em prematuros. As conclusões deste estudo: altos níveis de FAL podem ser considerados um biomarcador na predicção do status da mineralização óssea e a necessidade de avaliação radiológica nos pré-termos, principalmente aquele com peso ao nascer<1000 g ou idade gestacional <32 semanas. O valor para o ótimo ponto de corte da FAL sérica no qual a osteopenia é detectada é 500 UI/L com 100% de sensibilidade e 80, 77% de especificidade.

Bone Mineral Density According to Dual Energy X-ray Absorptiometry is Associated with Serial Serum Alkaline Phosphatase Level in Extremely Low Birth Weight Infants at Discharge. Lee J, Park HK, Kim JH, Choi YY, Lee HJ. Pediatr Neonatol. 2016 Sep 30. pii: S 1875 -9572(16)30180 -2. doi: 10. 1016/j. pedneo. 2016. 05. 005. [Epub ahead of print] PMID: 27780689 2016 Este estudo demonstrou que o fósforo baixo prolongado com 2 a 3 semanas pós-natais e FAL elevada com 4 a 5 semanas pós-natais foram correlacionados com a diminuição da densidade mineral óssea (submetidos à absortometria de Raio -X de dupla energia [DXA] por densitometria óssea) na alta em recém-nascidos de muito baixo peso. FAL tem sido sugerido como uma medida alternativa para rastreio precoce e suplementação mineral agressiva para a DMO
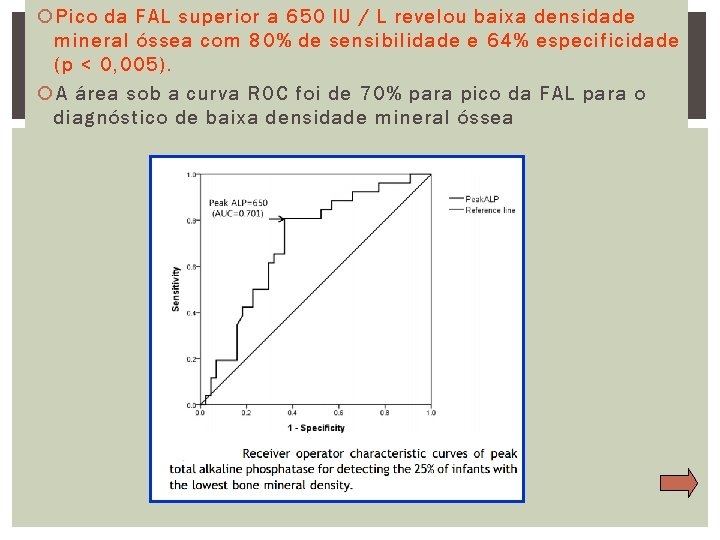
Pico da FAL superior a 650 IU / L revelou baixa densidade mineral óssea com 80% de sensibilidade e 64% especificidade (p < 0, 005). A área sob a curva ROC foi de 70% para pico da FAL para o diagnóstico de baixa densidade mineral óssea

O presente estudo indica que as medidas seriadas de FAL e fosfato podem predizer o risco de diminuição da densidade por DXA na alta de prematuros com peso ao nascer extremamente baixo. Os resultados deste estudo fornecem valores de referência para DMO volumétrica determinada pela DXA em prematuros clinicamente estáveis O valor da DXA volumétrica e correlação com o nível de FAL para predizer a presença de DMO ou restrição de crescimento na infância tardia devem se analisados em uma grande coorte

Doença metabólica óssea e densidade mineral óssea nos recém-nascidos muito pré-termos 2014 Josep Figueras-Aloy, Enriqueta Alvarez -Dominguez, Jose M. Perez-Fernandez, et al. Apresentação: Ana Angélica de S. Tavares, Manoela Fassino Barros, Alessandra C. Bertolino, Amanda V. de Melo Quadrado, Marina Fernandes de Oliveira, Paulo R. Margotto Os autores classificaram a Doença Metabólica Óssea da Prematuridade em 3 grupos: § Normal : FAL≤ 500 UI/L; § Leve : FAL >500 UI/L e P ≥ 4. 5 mg/d. L; § Severa : FAL>500 UI/L e P <4. 5 mg/d. L. ; Uma boa Densidade Mineral Óssea (DMO) foi associada a : § § Maior peso ao nascer; AIG; Curto período de nutrição parenteral; Ausência de ducto arterial patente, hemorragia intraventricular, colestase, sepse tardia; § Baixa necessidade de ventilação mecânica; § Alimentação exclusiva com leite materno fortificado; § Metabolismo de Ca e P normal (Ca e P altos e FAL baixa).

Nenhuma das variáveis avaliadas (Ca, P, FAL, PTH e vit D) pode ser considerada marcador da DOENÇA METABÓLICA ÓSSE A DA PREMATURIDADE (DMOP) de forma isolada; Níveis séricos de Ca e P podem estar normais apesar dos níveis de reserva reduzidos, devido ao efeito do PTH; FAL Marcador mais aceito: , NO ENTANTO O PONTO DE CORTE VARIA ENTRE 300→ 500 a 900 IU/L; No presente estudo: 500 IU/L DMO: corpo inteiro e da espinha; Mensuração da DMO na alta: reflete qualquer efeito das complicações neonatais e o tipo de nutrição e tratamento administrados (real situação clínica dessas crianças); DMO não está associada ao sexo e ↑ com a idade. 17/03/14

Medidas seriadas da fosfatase alcalina sérica para a predicção precoce da osteopenia da prematuridade (com discussão estatística) Autor(es): Yi-Li Hung et al. Apresentação: Marcela dos Santos Amorim 2011 Resultados deste estudo mostraram que a fosfatase alcalina sérica > 700 UI / L na idade de 3 semanas pós-natal, pode ser um dos primeiros preditores de osteopenia em prematuros A partir de 3 semanas de vida : período importante de mineralização óssea insulto osteopenia A relação observada entre fosfatase alcalina aumentada e alterações radiológicas apresentou provas para apoiar a utilidade de exame radiográfico

Alta oferta precoce de cálcio e fósforo na nutrição parenteral previne a curto prazo declínio da força óssea em recém-nascidos prematuros Autor(es): L. Pereira-da-Silva et al. Apresentação: Débora Cristiny 2011 Prestridge et al também testaram o efeito de dois regimes diferentes de Ca e P fornecidos pela NP em prematuros e encontrou um maior conteúdo de mineral ósseo naqueles que receberam precocemente maior aporte de minerais. Este efeito persistiu durante várias semanas além do intervalo de estudo, que os autores têm chamado efeito de memória devido a intervenção nutricional precoce. Prematuros perdem o período intra-uterino de maior depósito mineral, logo são mais sensíveis a uma ingestão precoce e mais elevada, levando a uma redução da desmineralização óssea precoce, possivelmente refletindo sobre a força dos ossos além do período de intervenção. A ingestão precoce de Ca 75 mg/kg/d e P 44 mg/kg/d contribuiu para prevenir a diminuição da força óssea em prematuros nas primeiras semanas de vida

Doença metabólica óssea da prematuridade: relato de 4 casos Mutlu GY et al. Apresentação: Marília Carolina Milhomem 2015 Os níveis séricos de P inferiores a 2 mmol / L (6, 1 mg / d. L) constituem um importante fator de risco para osteopenia e níveis abaixo de <1. 8 mmol / L (5, 4 mg / d. L) verificou-se estar relacionada com achados radiológicos positivos. A combinação de hipofosfatemia e elevada FA é um indicador altamente sensível na identificação de crianças em risco de DMO.

Doença metabólica óssea da prematuridade Autor(es): Miza Maria B. A. Vidigal, Paulo R. Margotto 2013 Capítulo do livro Assistência ao Recém-Nascido de Risco, ESCS, Brasília, 3ª Edição, 2013, pg. 193 -194 Fisioterapia motora (Estudo realizado em Israel no Hospital Kfar Saba, com media de peso de nascimento 1135 g e idade gestacional entre 28 - 30 semanas, mostrou que o exercício físico passivo atenuou a diminuição da perda óssea). Iniciar na primeira semana de vida movimentos de extensão e flexão passiva de membros superiores e inferiores durante 5 minutos /dia, 5 dias por semana até a alta. Effect of physical activity on bone mineralization in premature infants. Moyer-Mileur L, Luetkemeier M, Boomer L, Chan GM. J Pediatr. 1995 Oct; 127(4): 620 -5.

de Rx simples: impreciso e depende da gravidade e da duração da deficiência de minerais. As alterações radiológicas são Grau I - rarefação da metáfise e adelgaçamento da cortical Grau II - irregularidade matafisária com imagem em forma diferencial taça e alargamento da epífise/diagnóstico com sífilis Grau III-fraturas (estas ocorrem de forma geral entre 6 -12 semanas) *Padrão ouro: determinação da medida do conteúdo mineral ósseo por densitometria óssea com aparelho de absorção de fótons duplo (absorciometria por duplo Rx). *Ultrassom quantitativo (QUS) que mede a velocidade do som no osso e mede além da densidade óssea e outras propriedades do osso como espessura cortical, elasticidade e microarquitetura.

Bioquímica Ca sérico níveis normais (N=8 -11 mg/d. L)ou baixo Ca urinário elevado(>6 mg%, sinal precoce) P sérico baixo (N= 6, 6 -9, 4 mg/d. L) P urinário baixo (<1 mg%) Fosfatase Alcalina (FAL) elevada, usar como ponto de corte valores 5 vezes maior ao de referência para adultos normais(N= 45 -150 Ui). Tem sido evidenciado ser mais preditiva no diagnóstico precoce do que o fósforo e cálcio (indicadores mais tardios) 1, 25(OH) vit D normal ou alta; se baixa significa deficiência de vitamina D

Profilaxia A profilaxia é imperativa no bebe prematuro. -Recém nascidos com peso ao nascer abaixo de 1500 g fornecer 40 mg/kg de Ca (4 m. L/Kg de gluconato de Ca 10%) e 50 mg/kg de fósforo (0, 5 m. L/Kg de fosfato acido de potássio) e maiores concentrações de aminoácidos (4 g/Kg/dia). -Suplementação do leite humano a partir do décimo quinto dia de vida ou quando a ingesta oral atingir 100 m. L/kg/dia e manter até que o prematuro esteja com sucção completa ao seio -Quando dieta completa por sucção fazer suplementação de Ca e P ate 40 -45 semanas de idade gestacional pós-concepção e a seguir de acordo com o perfil bioquímico. -Fisioterapia motora (Estudo realizado em Israel no Hospital Kfar Saba, com media de peso de nascimento 1135 g e idade gestacional entre 28 - 30 semanas, mostrou que o exercício físico passivo atenuou a diminuição da perda óssea). Iniciar na primeira semana de vida movimentos de extensão e flexão passiva de membros superiores e inferiores durante 5 minutos /dia, 5 dias por semana ate a alta.

Tratamento -Hipofosfatemia - Oferecer 110 -125 mg/Kg/dia de P e 200250 mg/Kg dia Ca. Repetir dosagens em 15 dias se Ca, P e FA normais manter necessidades basais(Ca (120 -150 mg/kg/dia) e P ( 60 -75 mg/Kg/dia). Se ainda alterados dosar 1, 25(OH) Vit D, PTH. -Deficiência de vitamina D – dose total para repor 660000 UI. Aderogyl D 3 frasco ampola com 66000 UI - 2 vezes por semana durante 5 semanas. A nossa conduta consiste em iniciar seguimento de todo prematuro nascido com menos de 32 semanas de idade gestacional (em alimentação parenteral ou oral) com 2 semanas de vida dosando Ca e P sanguineos e urinários e a FAL. As dosagens serão repetidas a cada 21 dias até completar 40 semanas de idade gestacional pósconcepção e depois mensalmente ate 48 semanas ( 2 meses de idade corrigida).

Quantidade de Ca e P nas medicações, no leite humano, nas formulas lácteas e fortificantes do leite humano -Leite humano 24 mg de Ca e 14 mg de P em 100 m. L leite ( valores não variam no leite da mãe com bebe prematuro e termo) -Fosfato ácido de potássio 1 m. L=96 mg de P/ Fosfato tricálcico a 12, 9%: 1 ml=25 mg de P -Gluconato de Ca 10%%: 1 m. L=9, 6 mg de Ca elementar -Fosfato tricalcico 12, 9% suspensão: 1 m. L 50 mg de Ca e 25 mg de P -Pré-Nan: 100 mo preparado contém 70 mg de Ca e 46 mg de P Enfalac 95 mg de Ca e 53 mg de P para cada 100 m. L preparado -FM 85 51 mg de Ca e 34 mg de P cada 5 g do pó (dissolução 1 g em 20 m. L leite humano) -Enfamil e Similac 85 mg Ca e 45 mg P para cada 100 m. L de solução. Alguns serviços adicionam o Gluconato de Ca e o Fosfato acido de potássio no leite humano para reposição destes minerais. No HRAS usamos o fosfato tricálcico 12, 9% na impossibilidade de usar um fortificante do leite humano ou quando o prematuro já esta com adieta toda ao seio. Fazemos o calculo da taxa de aquisição intrauterina Ca 120 mg/kg/dia e P 60 mg/Kg/dia, descontamos o que vai no leite ingerido (capacidade gástrica 30 m. L/Kg) e o volume total é dividido em 4 tomadas ao dia. Exemplo: Bebe com 1330 g e recebendo dieta 20 m. Lx 8 Necessidade /dia Ca 156 mg. Na dieta recebe 38 mg. Os 118 mg que faltam de Ca será suplementado com 2, 3 m. L de fosfato tricálcico 12, 9% divido em 4 tomadas 0, 5 m. L /vez. Bebe com 2000 g e sucção ao seio exclusivo calcular a capacidade gástrica em torno de 30 m. L/Kg. Necessidade /dia Ca 240 mg. Na dieta recebe , em media, 115 mg Ca. Suplementar o restante de Ca com 2, 3 m. L de Fosfato tricálcico 12, 9% dividido em 4 tomadas.

ENFIM, RESUMINDO OS ESTUDOS. . . O estudo de Kelly A et al aqui Apresentado trata-se de ma avaliação da prática de 338 Neonatologistas dos Estados Unidos, representando 246 UTIN, através de um questionário, quanto à triagem da doença metabólica óssea (DMO). Os testes usados para o screening e progressão da doença mais frequentes foram a calcemia, a fosfatase alcalina (FAL: valor de corte >500 IU/L; os seus níveis podem não ser confiáveis na vigência do uso de corticoides que podem suprimir os seus níveis; melhor marcador do risco de fraturas) e o fósforo sérico (88. 1 a 94, 4. Os pontos de cortes mais comuns foram a idade gestacional <28 semanas e peso ao nascer<1000 g. A intervenção primária mais comum tanto para prevenir (93, 4%) como para tratar (83, 1%) foi a fortificação do leite humano (se não fortificado, só oferece um terço do nível de cálcio e fósforo oferecido no meio intrauterino). O leite humano do Banco tem ainda menores quantidades de cálcio e fósforo! No tratamento a suplementação de Vitamina D, cálcio e fósforo foram amplamente utilizados (65 a 67% e a fisioterapia em 19%. Informações de estudo recente Egípcio (Abdallah EA et al, 2 016), mostram que o valor de corte da FAL sérica (biomarcador confiável nos pré-termos <32 semanas e peso ao nascer <1000 g) no qual a osteopenia é detectada é de 500 UI / L com 100% de sensibilidade e 80, 77% de especificidade! Valores >800 IU/L por 2 semanas consecutivas está recomendada radiografias de pulso e/ou de joelhos. Estudo coreano (Lee J et al, 2016) mostrou que fósforo baixo prolongado com 2 -3 semanas pós-natais com elevação da FAL com 4 -5 semanas, correlacionaram-se com diminuição da densidade mineral óssea, avaliada através da densaitometria óssea (FAL>650 IU/L revelou baixa densidade mineral óssea com 80% de sensibilidade e 64% de especificade). Estudo israelense (Moyer-Mileur L et al, 1995) mostrou que iniciar na primeira semana de vida movimentos de extensão e flexão passiva de membros superiores e inferiores durante 5 minutos /dia, 5 dias por semana até a alta atenuou a diminuição da perda óssea. Paulo R. Margotto

OBRIGADO! Yuji Staffs e Residentes da Unidade de Neonatologia do HMIB/SES/DF

- Slides: 50