Tratamiento Farmacolgico de la Obesidad Actualizacin 2019 Dra

Tratamiento Farmacológico de la Obesidad Actualización 2019 Dra. Ada Cuevas Marin Departamento de Nutrición. Clínica Las Condes International Atherosclerosis Society Red Iberoamericana de Hipercolesterolemia Familiar World Obesity Federation

Conflictos de Interés Dra. Cuevas ha recibido honorarios por conferencia y/o participación en advisory boards de Abbott, Novo Nordisk, Saval, Teva.
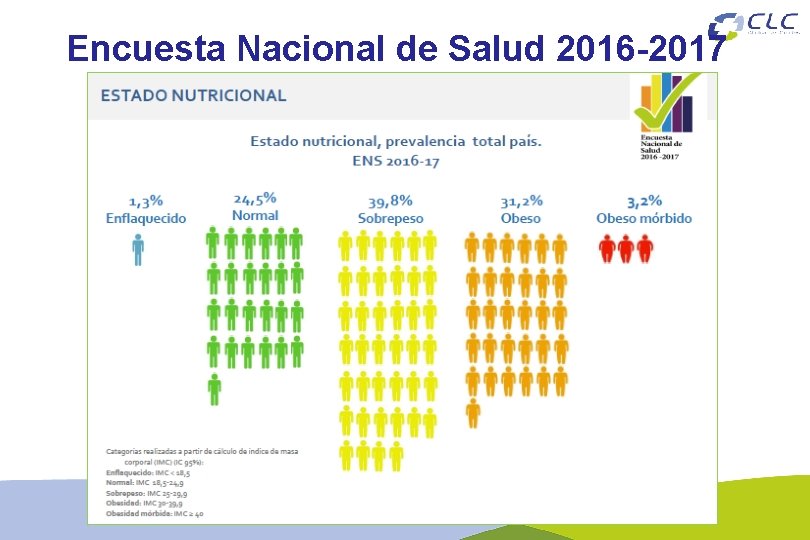
Encuesta Nacional de Salud 2016 -2017
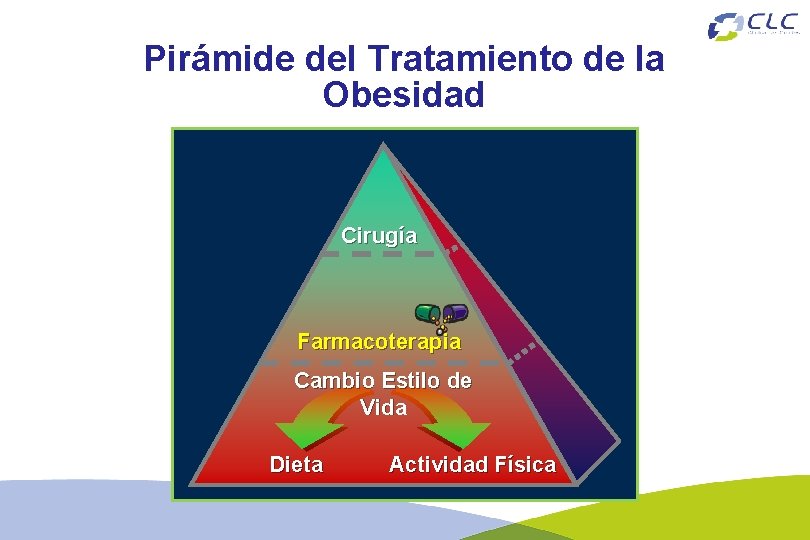
Pirámide del Tratamiento de la Obesidad Cirugía Farmacoterapia Cambio Estilo de Vida Dieta Actividad Física
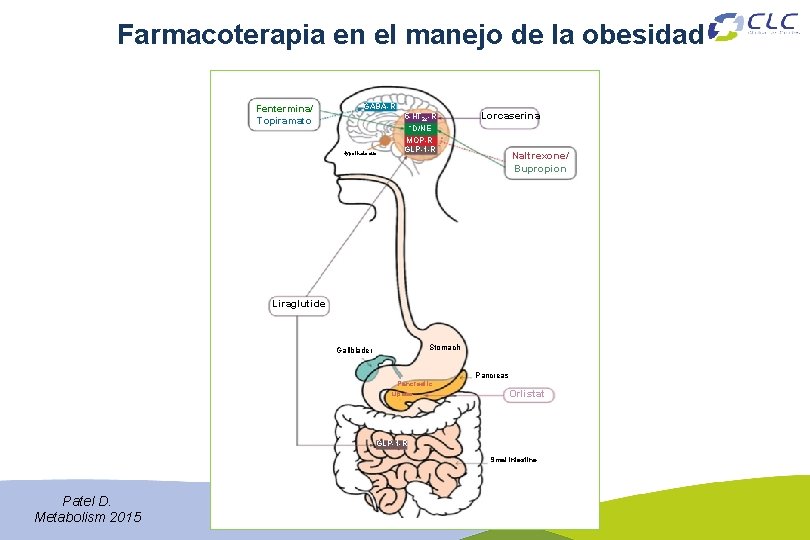
Farmacoterapia en el manejo de la obesidad Fentermina/ Topiramato GABA-R Hypothalamus 5 -HT 2 c-R ↑D/NE MOP-R GLP-1 -R Lorcaserina Naltrexone/ Bupropion Liraglutide Stomach Gallblader Pancreas Pancreatic Lipase Orlistat GLP-1 -R Smal intestine Patel D. Metabolism 2015

Fentermina Ø Disminuye el apetito al estimular la liberación de noradrenalina en el hipotálamo. Ø Aprobado por la FDA en 1959 para uso por 12 semanas, pero se ha utilizado a largo plazo (indicación Off-label) Ø 85% pacientes con fentermina logran una reducción de peso del 5% y un 50% una reducción del 10%. Ø Contraindicaciones: Estados de excitación, trastornos psiquiátricos, HTA no controlada, arritmia, enfermedad cardiovascular no controlada, hipertiroidismo, embarazo.
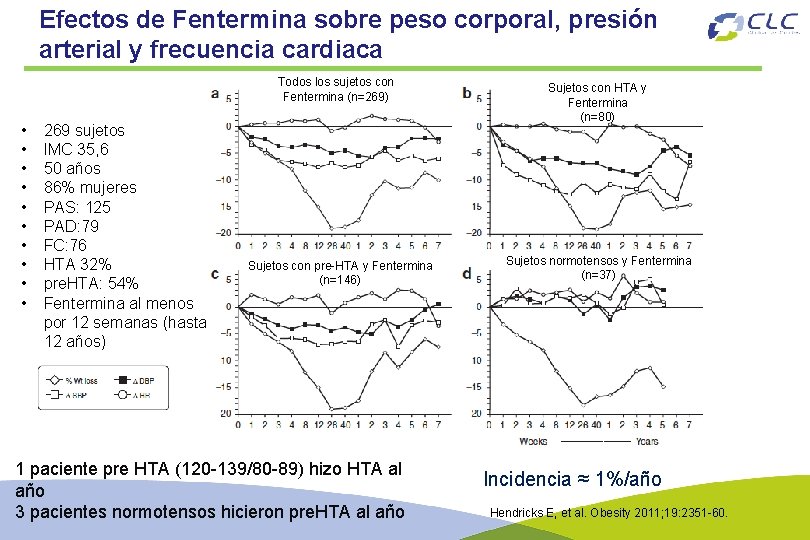
Efectos de Fentermina sobre peso corporal, presión arterial y frecuencia cardiaca Todos los sujetos con Fentermina (n=269) • • • 269 sujetos IMC 35, 6 50 años 86% mujeres PAS: 125 PAD: 79 FC: 76 HTA 32% pre. HTA: 54% Fentermina al menos por 12 semanas (hasta 12 años) Sujetos con pre-HTA y Fentermina (n=146) 1 paciente pre HTA (120 -139/80 -89) hizo HTA al año 3 pacientes normotensos hicieron pre. HTA al año Sujetos con HTA y Fentermina (n=80) Sujetos normotensos y Fentermina (n=37) Incidencia ≈ 1%/año Hendricks E, et al. Obesity 2011; 19: 2351 -60.
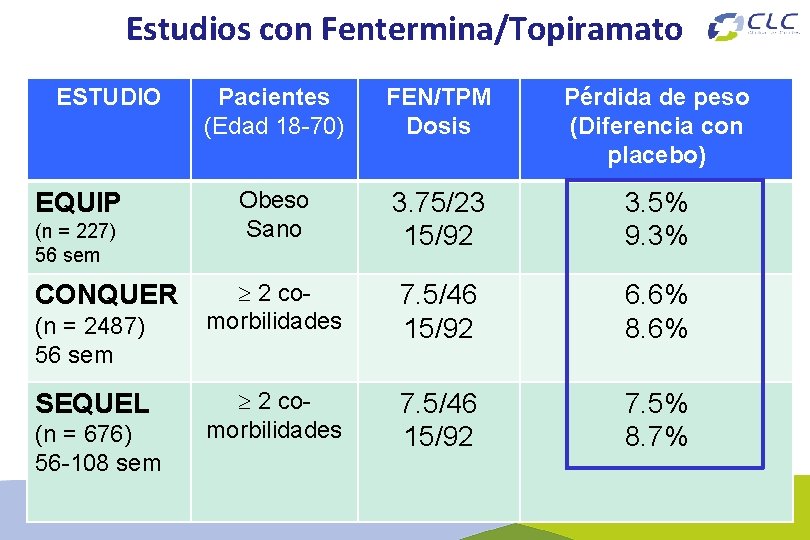
Estudios con Fentermina/Topiramato ESTUDIO EQUIP (n = 227) 56 sem CONQUER (n = 2487) 56 sem SEQUEL (n = 676) 56 -108 sem Pacientes (Edad 18 -70) FEN/TPM Dosis Pérdida de peso (Diferencia con placebo) Obeso Sano 3. 75/23 15/92 3. 5% 9. 3% 2 comorbilidades 7. 5/46 15/92 6. 6% 8. 6% 2 comorbilidades 7. 5/46 15/92 7. 5% 8. 7%
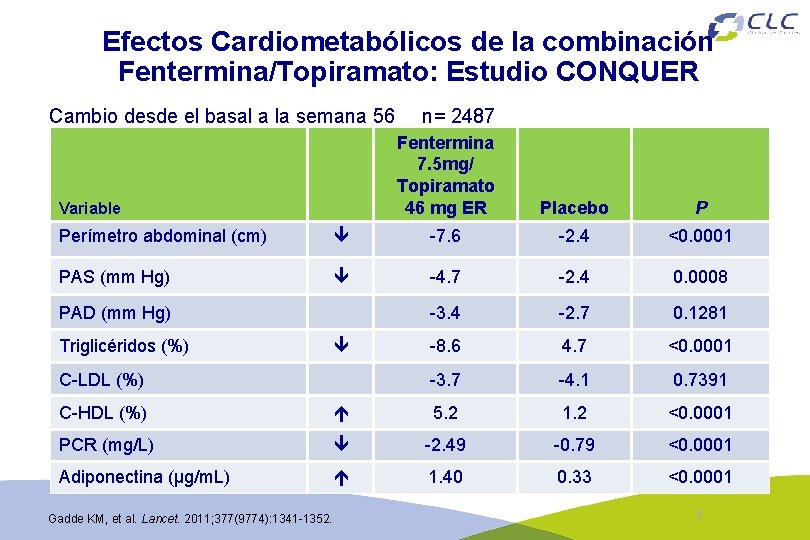
Efectos Cardiometabólicos de la combinación Fentermina/Topiramato: Estudio CONQUER Cambio desde el basal a la semana 56 Variable n= 2487 Fentermina 7. 5 mg/ Topiramato 46 mg ER Placebo P Perímetro abdominal (cm) -7. 6 -2. 4 <0. 0001 PAS (mm Hg) -4. 7 -2. 4 0. 0008 -3. 4 -2. 7 0. 1281 -8. 6 4. 7 <0. 0001 -3. 7 -4. 1 0. 7391 PAD (mm Hg) Triglicéridos (%) C-LDL (%) C-HDL (%) 5. 2 1. 2 <0. 0001 PCR (mg/L) -2. 49 -0. 79 <0. 0001 Adiponectina (µg/m. L) 1. 40 0. 33 <0. 0001 Gadde KM, et al. Lancet. 2011; 377(9774): 1341 -1352. 9
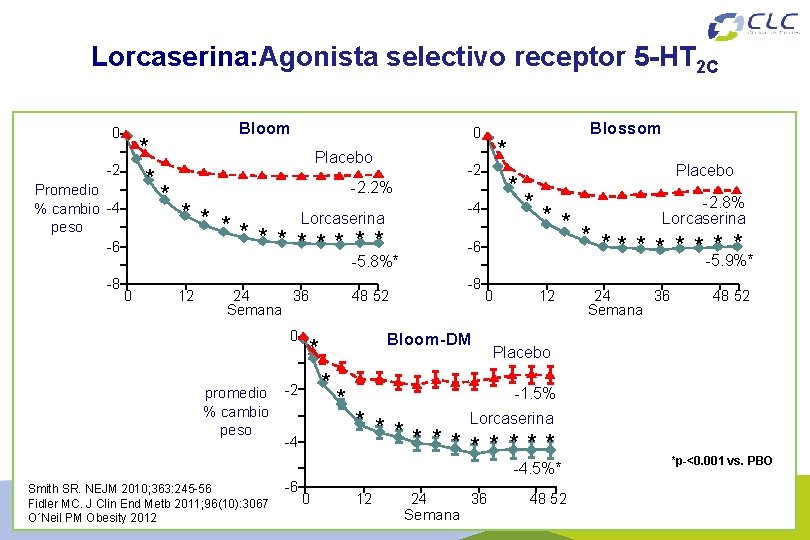
Lorcaserina: Agonista selectivo receptor 5 -HT 2 C 0 * * -2 Promedio % cambio -4 peso -6 -8 Bloom 0 Placebo * * -2. 2% -4 12 24 36 Semana 0 promedio % cambio peso * ** 0 12 SS Bloom-DM * -4 -8 48 52 * -2 Placebo -6 -5. 8%* 0 * -2 ** * Lorcaserina * ** Blossom * -6 0 * ** * * * -5. 9%* 24 36 Semana 48 52 Placebo -1. 5% Lorcaserina * ** *** -4. 5%* Smith SR. NEJM 2010; 363: 245 -56 Fidler MC. J Clin End Metb 2011; 96(10): 3067 O´Neil PM Obesity 2012 -2. 8% Lorcaserina 12 24 36 Semana 48 52 *p-<0. 001 vs. PBO
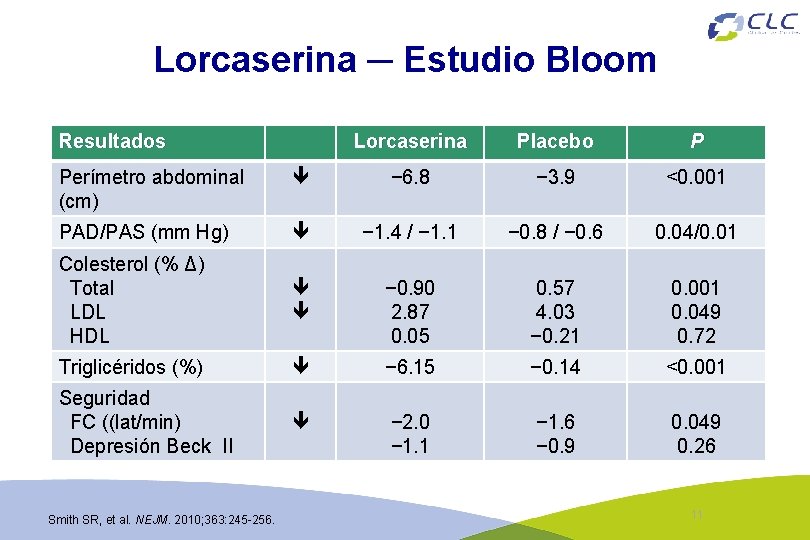
Lorcaserina ─ Estudio Bloom Resultados Lorcaserina Placebo P Perímetro abdominal (cm) − 6. 8 − 3. 9 <0. 001 PAD/PAS (mm Hg) − 1. 4 / − 1. 1 − 0. 8 / − 0. 6 0. 04/0. 01 Colesterol (% Δ) Total LDL HDL − 0. 90 2. 87 0. 05 0. 57 4. 03 − 0. 21 0. 001 0. 049 0. 72 Triglicéridos (%) − 6. 15 − 0. 14 <0. 001 Seguridad FC ((lat/min) Depresión Beck II − 2. 0 − 1. 1 − 1. 6 − 0. 9 0. 049 0. 26 Smith SR, et al. NEJM. 2010; 363: 245 -256. 11

Seguridad del uso de Lorcaserina a largo plazo en pacientes de alto riesgo cardiovascular Incidencia acumulada (%) Cociente de riesgo, 0. 99 (95% CI, 0. 85– 1. 14) P<0. 001 para la no inferioridad Placebo Lorcaserina Meses desde la aleatorización No. en riesgo Placebo 6000 5814 5614 4003 Lorcaserina 6000 5816 5623 4041 Bohula EA. NEJM 2018
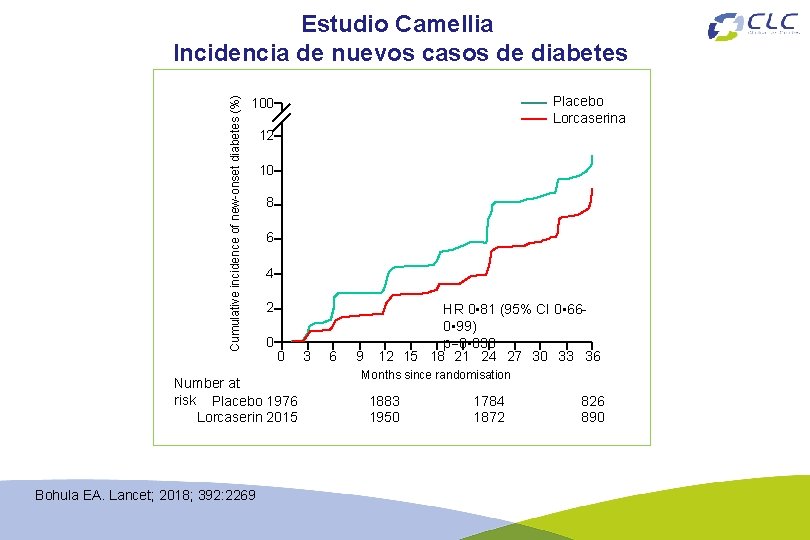
Cumulative incidence of new-onset diabetes (%) Estudio Camellia Incidencia de nuevos casos de diabetes Placebo Lorcaserina 100 12 10 8 6 4 2 0 0 Number at risk Placebo 1976 Lorcaserin 2015 Bohula EA. Lancet; 2018; 392: 2269 3 6 9 HR 0 • 81 (95% CI 0 • 660 • 99) p=0 • 038 12 15 18 21 24 27 30 33 36 Months since randomisation 1883 1950 1784 1872 826 890

Liraglutide: Análogo de GL 1 P Pancreas Secreción de Insulina 2, 3 (glucosa-dependiente) y la sensibilidad de las celulas beta Sintesis de Insulina al estimular la regeneracion y mas pancreatica 4 Secreción de Glucagon 3 (glucose-dependiente) Cerebro Afecta el peso corporal: 5‒ 7 Saciedad Ingesta energética Cardiovascular PA sistolica 8 Gastrointestinal vaciamiento gastrico Hígado Producción hepatica de Glucosa 4 1. Holst JJ et al. Trends Mol Med 2008; 14: 161– 168; 2. Flint A et al. Adv Ther 2011; 28: 213– 226; 3. Degn KB et al. Diabetes 2004; 53: 1187– 1194; 4. Baggio LL & Drucker DJ. Gastroenterology 2007; 132: 2131‒ 2157; 5. Horowitz M et al. Diabetes Res Clin Pract 2012; 97: 258‒ 266; 6. Vilsbøll T et al. BMJ 2012; 344: d 7771; 7. Niswender K et al. Diabetes Obes Metab 2013; 15: 42‒ 54; 8. Fonseca VA et al. Diabetes 2010; 59(suppl 1): A 79 (296 -OR)
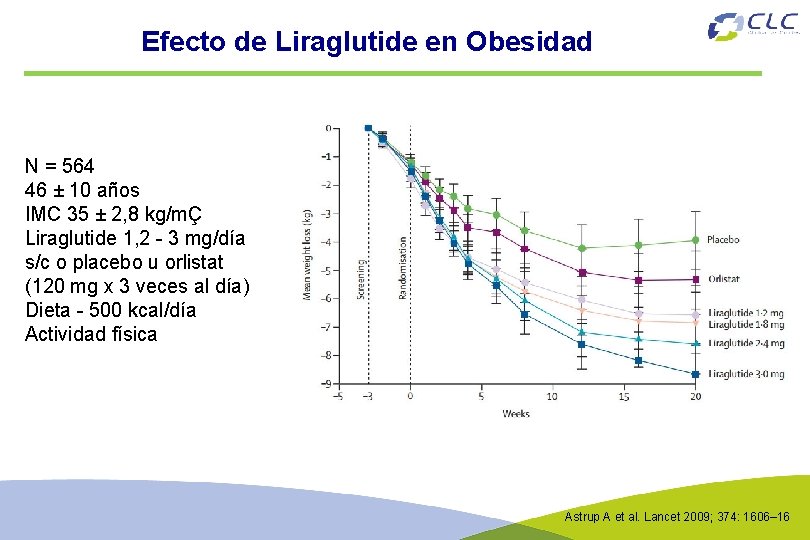
Efecto de Liraglutide en Obesidad N = 564 46 ± 10 años IMC 35 ± 2, 8 kg/mÇ Liraglutide 1, 2 - 3 mg/día s/c o placebo u orlistat (120 mg x 3 veces al día) Dieta - 500 kcal/día Actividad física Astrup A et al. Lancet 2009; 374: 1606– 16
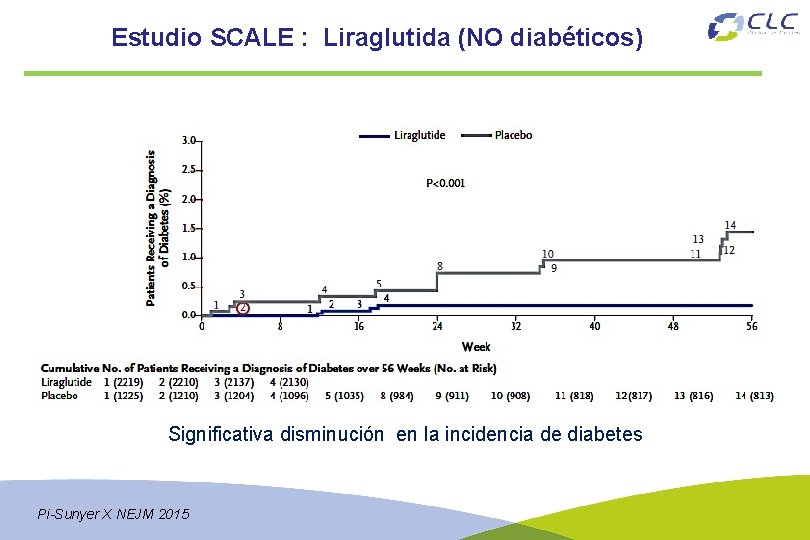
Estudio SCALE : Liraglutida (NO diabéticos) Significativa disminución en la incidencia de diabetes Pi-Sunyer X NEJM 2015
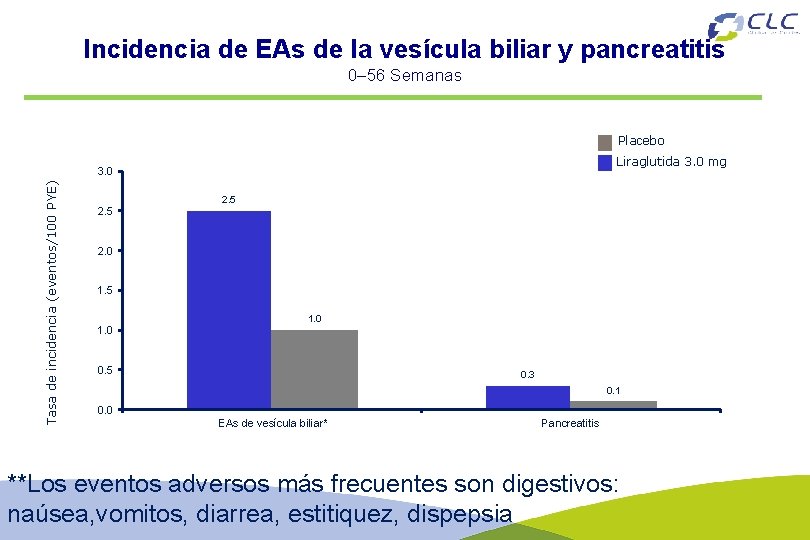
Incidencia de EAs de la vesícula biliar y pancreatitis 0– 56 Semanas Placebo Liraglutida 3. 0 mg Tasa de incidencia (eventos/100 PYE) 3. 0 2. 5 2. 0 1. 5 1. 0 0. 5 0. 3 0. 1 0. 0 EAs de vesícula biliar* Pancreatitis **Los eventos adversos más frecuentes son digestivos: naúsea, vomitos, diarrea, estitiquez, dispepsia
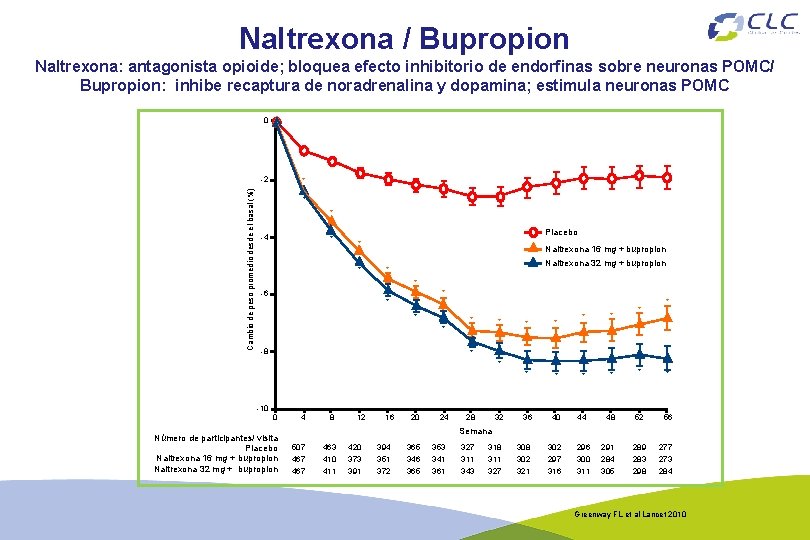
Naltrexona / Bupropion Naltrexona: antagonista opioide; bloquea efecto inhibitorio de endorfinas sobre neuronas POMC/ Bupropion: inhibe recaptura de noradrenalina y dopamina; estimula neuronas POMC 0 Cambio de peso promedio desde el basal (%) -2 * * * -4 * Placebo * * Naltrexona 16 mg + bupropion Naltrexona 32 mg + bupropion * * -6 * * -8 * * * * 32 36 40 44 48 52 56 * * -10 0 Número de participantes/ visita Placebo Naltrexona 16 mg + bupropion Naltrexona 32 mg + bupropion 4 8 12 16 20 24 28 Semana 507 463 420 394 365 353 327 318 302 296 291 289 277 467 410 411 373 391 351 372 346 365 341 361 311 343 311 327 302 321 297 316 300 311 284 305 283 298 273 284 Greenway FL et al Lancet 2010
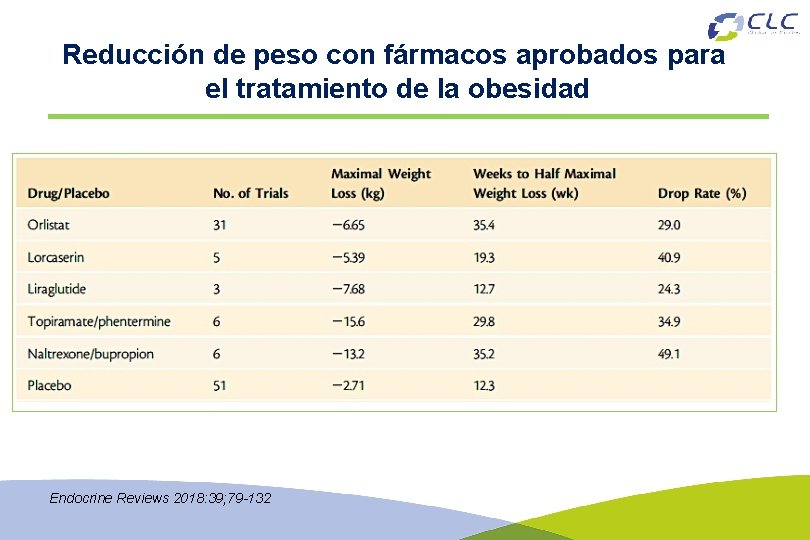
Reducción de peso con fármacos aprobados para el tratamiento de la obesidad Endocrine Reviews 2018: 39; 79 -132
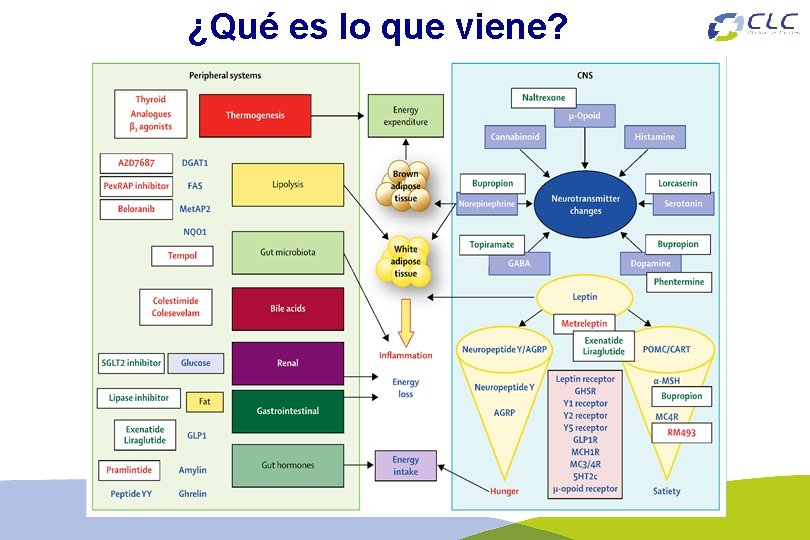
¿Qué es lo que viene?

Fármacos en estudio Ø Acción central Setmelanotide: agonista MCR 4 Tesofensina: Inhibe transportador de norepinefrina, dopamina y serotonina Ø Acción periférica Elpeglenatida; semaglutida: agonista GLP 1 Canaglifozina, Licoglifozina: i. SGLT 1 Sildenafil Agonistas duales y triples: de GLP 1, glucagón y/o péptido inhibidor gástrico Ø Combinaciones Canaglifozina/fentermina Dapaflifozina/exenatide Zonisamida/bupropión Tesofensina/metoprolol
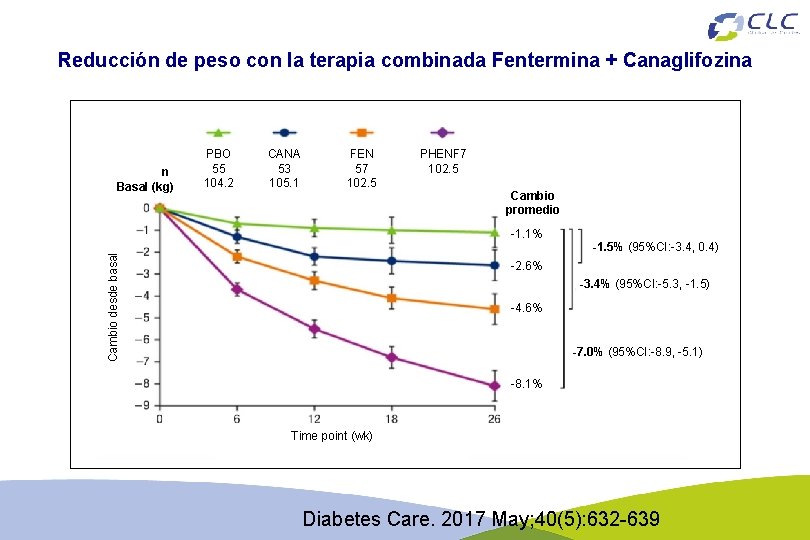
Reducción de peso con la terapia combinada Fentermina + Canaglifozina n Basal (kg) PBO 55 104. 2 CANA 53 105. 1 FEN 57 102. 5 PHENF 7 102. 5 Cambio promedio Cambio desde basal -1. 1% -1. 5% (95%CI: -3. 4, 0. 4) -2. 6% -3. 4% (95%CI: -5. 3, -1. 5) -4. 6% -7. 0% (95%CI: -8. 9, -5. 1) -8. 1% Time point (wk) Diabetes Care. 2017 May; 40(5): 632 -639

Reducción de peso con Semaglutida en pacientes diabéticos Formulación oral estudio fase II: Baja de peso 7 kg en 26 sem en DM 2 Nauck MA, et al. Diabetes Care 2016; 39(2): 231 -41.
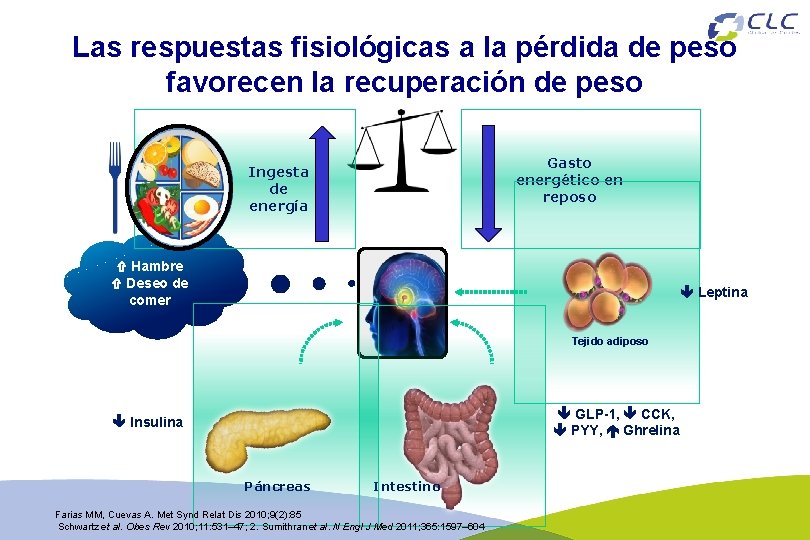
Las respuestas fisiológicas a la pérdida de peso favorecen la recuperación de peso Gasto energético en reposo Ingesta de energía Hambre Deseo de comer Leptina Tejido adiposo GLP-1, CCK, PYY, Ghrelina Insulina Páncreas Intestino Farias MM, Cuevas A. Met Synd Relat Dis 2010; 9(2): 85 Schwartz et al. Obes Rev 2010; 11: 531– 47; 2. Sumithran et al. N Engl J Med 2011; 365: 1597– 604
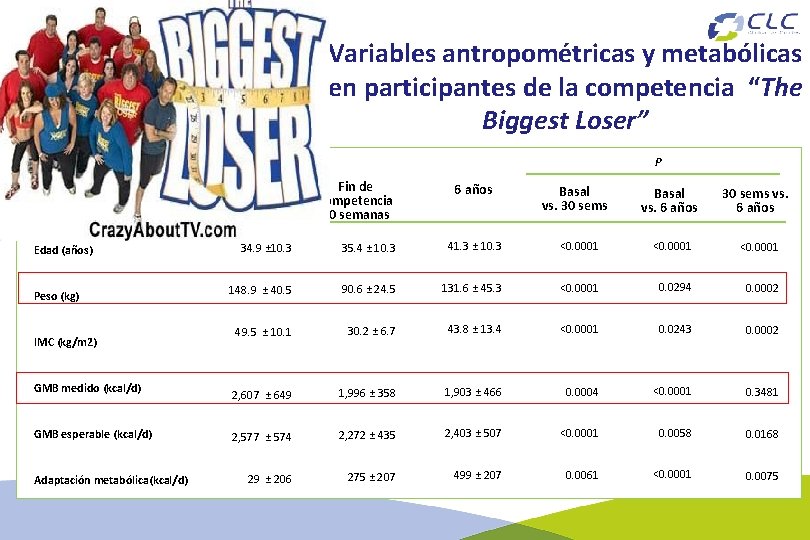
Variables antropométricas y metabólicas en participantes de la competencia “The Biggest Loser” P Basal Edad (años) Peso (kg) IMC (kg/m 2) GMB medido (kcal/d) GMB esperable (kcal/d) Adaptación metabólica(kcal/d) Fin de competencia 30 semanas 6 años Basal vs. 30 sems Basal vs. 6 años 30 sems vs. 6 años 34. 9 ± 10. 3 35. 4 ± 10. 3 41. 3 ± 10. 3 <0. 0001 148. 9 ± 40. 5 90. 6 ± 24. 5 131. 6 ± 45. 3 <0. 0001 0. 0294 0. 0002 49. 5 ± 10. 1 30. 2 ± 6. 7 43. 8 ± 13. 4 <0. 0001 0. 0243 0. 0002 2, 607 ± 649 1, 996 ± 358 1, 903 ± 466 0. 0004 <0. 0001 0. 3481 2, 577 ± 574 2, 272 ± 435 2, 403 ± 507 <0. 0001 0. 0058 0. 0168 29 ± 206 275 ± 207 499 ± 207 0. 0061 <0. 0001 0. 0075
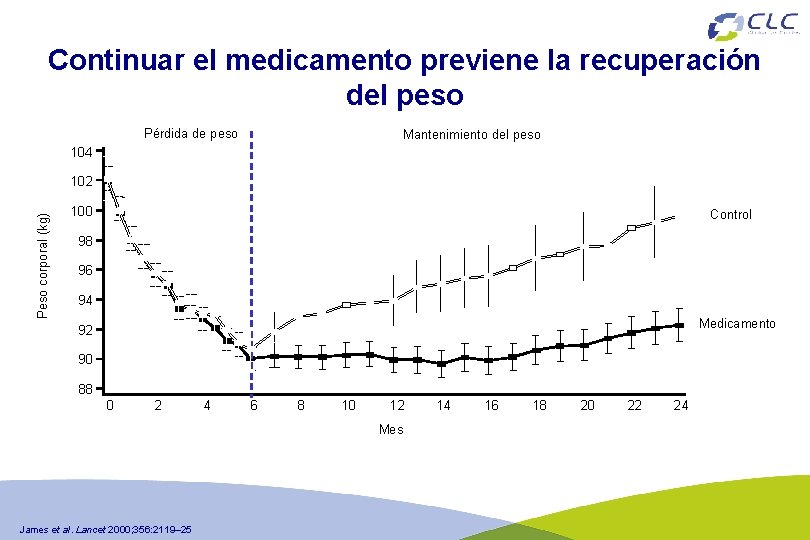
Continuar el medicamento previene la recuperación del peso Pérdida de peso Mantenimiento del peso 104 Peso corporal (kg) 102 100 Control 98 96 94 Medicamento 92 90 88 0 2 4 6 8 10 12 Mes James et al. Lancet 2000; 356: 2119– 25 14 16 18 20 22 24

Problemas en el manejo de la obesidad v Estigmatización del paciente. v Falta de entrenamiento de los profesionales de la salud en etiología, patogénesis, diagnóstico y tratamiento. v Promoción de dietas y suplementos milagrosos que aseguran una fácil y rápida baja de peso.

Gracias

Es necesario que conozcamos como el ser humano regula el peso corporal y aprendamos adecuadamente las diferentes opciones terapéuticas.
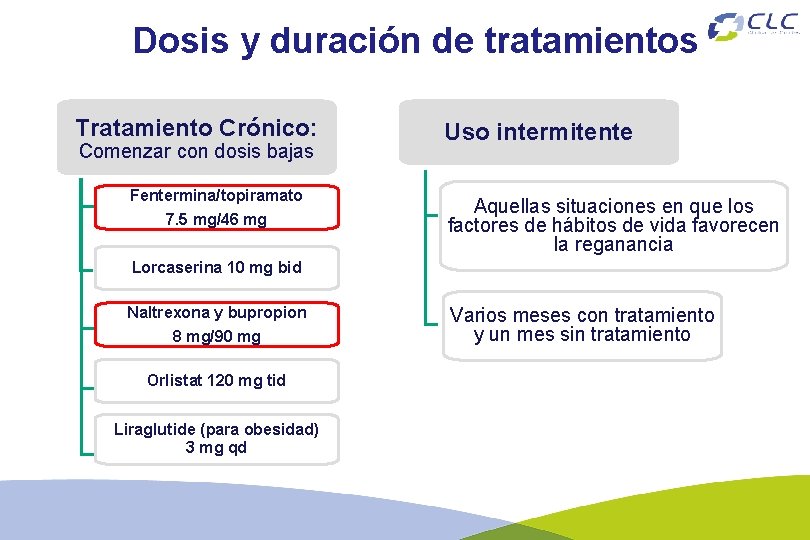
Dosis y duración de tratamientos Tratamiento Crónico: Comenzar con dosis bajas Fentermina/topiramato 7. 5 mg/46 mg Uso intermitente Aquellas situaciones en que los factores de hábitos de vida favorecen la reganancia Lorcaserina 10 mg bid Naltrexona y bupropion 8 mg/90 mg Orlistat 120 mg tid Liraglutide (para obesidad) 3 mg qd Varios meses con tratamiento y un mes sin tratamiento
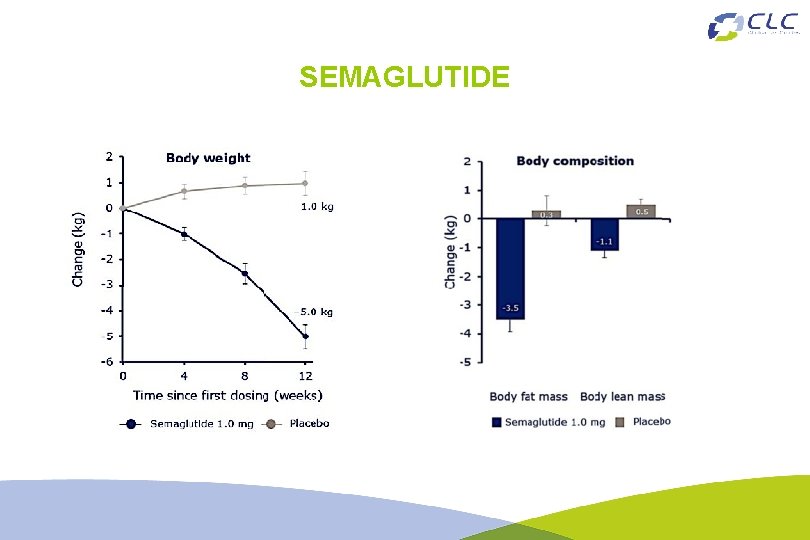
SEMAGLUTIDE

Criterios De Eficacia Según los Organismos Reguladores FDA: • perdida de peso sobre placebo ≥ 5%; y/o % de pacientes que pierden ≥ 5% debe ser ≥ 35% y duplicar al grupo placebo • ≥ 3000 sujetos en grupo fármaco y no menos de 1500 con placebo por 1 año • período para satisfacer aspectos de seguridad EMA: • Criterio primario: promedio de reducción de peso ≥ 10% al año y al menos 5% mayor que placebo • Criterio alternativo para ramas de tratamiento: % de respondedores Krentz AJ. Diabetes Obes Metab. 2016 Mar 3. doi: 10. 1111/dom. 12657.
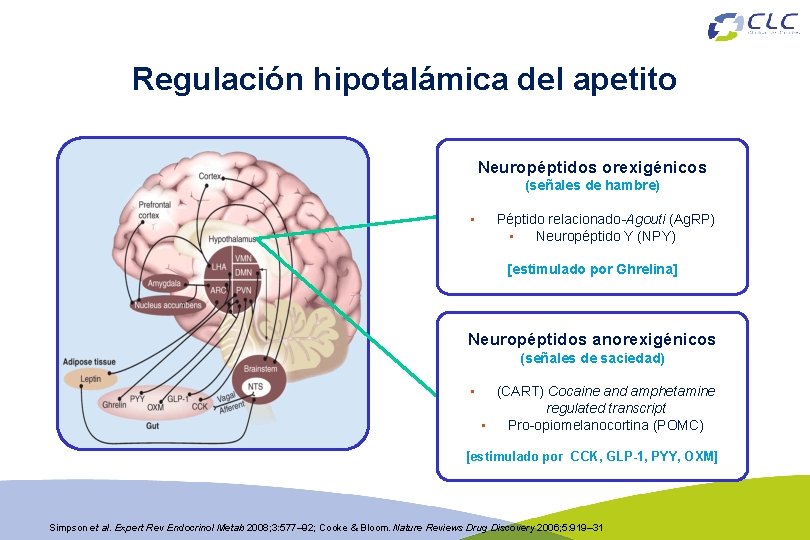
Regulación hipotalámica del apetito Neuropéptidos orexigénicos (señales de hambre) • Péptido relacionado-Agouti (Ag. RP) • Neuropéptido Y (NPY) [estimulado por Ghrelina] Neuropéptidos anorexigénicos (señales de saciedad) • (CART) Cocaine and amphetamine regulated transcript • Pro-opiomelanocortina (POMC) [estimulado por CCK, GLP-1, PYY, OXM] Simpson et al. Expert Rev Endocrinol Metab 2008; 3: 577– 92; Cooke & Bloom. Nature Reviews Drug Discovery 2006; 5: 919– 31

Efecto de la lorcaserina en peso y control glicémico en pacientes diabéticos Lorcaserina Acarbosa Sulfonilurea Lorcaserina Tiazolidinediona Acarbosa GLP-1 agonista Sulfonilurea Thiazolidinedione DPP-4 inhibitor GLP-1 agonist Glinide DPP-4 inhibitor Glinide SGLT-2 inhibidor -1. 5 -1. 3 ←Better than reference -1. 1 -0. 9 -0. 7 -0. 5 -0. 3 Neff LM. Clin Obesity 2017; 7: 337 -46 -0. 1 0. 3 0. 5 -6 ←Better than reference -4 -2 SGLT-2 inhibitor 0 2 4 6

Eventos adversos v/s eficacia Khera R. JAMA 2016

Características de pacientes que logran mantener baja de peso a largo plazo** Mantienen una dieta hipocalórica (1350 cal/día), baja en grasas • Alto nivel de actividad física (1 hora diaria) • Consumo regular de desayuno • Auto-monitoreo del peso • Mantienen un patrón de alimentación similar en días de semana y fines de semana • Bajos niveles de depresión • Autocontrol ** Registro americano de pacientes bajaron un promedio de 33 Kg de peso que fue mantenido por 5 años • Wing RR. Am J Clin Nutr 2005; 82: 222 S
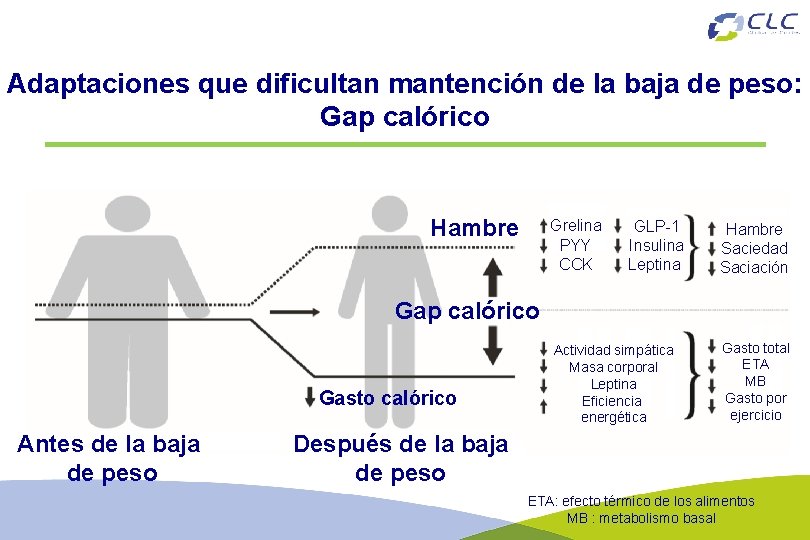
Adaptaciones que dificultan mantención de la baja de peso: Gap calórico Hambre Grelina PYY CCK GLP-1 Insulina Leptina Hambre Saciedad Saciación Gap calórico Gasto calórico Antes de la baja de peso Actividad simpática Masa corporal Leptina Eficiencia energética Gasto total ETA MB Gasto por ejercicio Después de la baja de peso ETA: efecto térmico de los alimentos MB : metabolismo basal
- Slides: 37




























































