Tratamiento de Hepatitis Crnica C con Pegasys en



















- Slides: 21

Tratamiento de Hepatitis Crónica C con Pegasys en pacientes con IRCT en HD Reporte Preliminar Dra. Rossana Román Vargas Unidad de Hígado - HNERM Es. Salud

Criterios de Inclusión • Pacientes con IRCT en hemodiálisis (pacientes deben estar en hemodiálisis por lo menos 2 meses antes de iniciar la primera dosis de la droga en estudio • Paciente masculino o femenino entre 18 y 50 años • Carga viral positiva, CUANTIFICABLE > 600 UI/ml • Biopsia hepática consistente con hepatitis crónica C, obtenida dentro del año previo a iniciar el tratamiento

Criterios de Inclusión • Enfermedad hepática compensada sin cirrosis • Pacientes con IRCT en hemodiálisis (pacientes deben estar en hemodiálisis por lo menos 2 meses antes de iniciar la primera dosis de la droga en estudio. • Los pacientes en terapia de mantenimiento con eritropoyetina, deben estar estables por los menos 3 meses antes del enrolamiento

Criterios de Inclusión • Prueba sérica de embarazo negativa, documentada en las 24 horas antes de la primera dosis de la droga en estudio (para las mujeres en edad potencial de gestación). • Todos los pacientes deben estar motivados a usar un método contraceptivo efectivo durante el tratamiento

Criterios de Exclusión • Pacientes con alguna de las siguientes características: -Terapia previa con interferón - Cirrosis Hepática - Signos y síntomas de carcinoma hepatocelular

Criterios de Exclusión • Terapia con cualquier tratamiento antiviral sistémico, anti neoplásico, inmunomodulador, dosis suprafisiológicas de esteroides y/o radiación. • Pruebas positivas en el screening para hepatitis A aguda o marcadores positivos para Hepatitis B o infección por HIV. • Historia u otra evidencia de condición médica asociada con enfermedad hepática crónica, diferente a hepatitis crónica C

Criterios de Exclusión • Historia de enfermedad psiquiátrica severa, especialmente depresión, caracterizado por un intento de suicidio, hospitalización por enfermedad psiquiátrica, o un periodo de incapacidad por una enfermedad psiquiátrica. • Historia de desorden convulsivo mayor, o uso de terapia anticonvulsivante.

Criterios de Exclusión • Historia de enfermedad autoinmune • Diabetes no compensada • Historia u otra evidencia de enfermedad pulmonar crónica asociada a limitación funcional. • Historia de enfermedad cardiaca severa (clase funcional III o IV), infarto de miocardio dentro de los 6 meses últimos, u otra enfermedad cardiovascular significativa.

Criterios de Exclusión • Disfunción tiroidea no controlada • Evidencia de retinopatía severa (ej. retinitis por CMV, degeneración macular), o desorden oftalmológico clínicamente relevante (ej, debido a DBM o HTA). • Insuficiencia renal aguda

Criterios de Exclusión • No compliance con la diálisis. • Historia de trasplante mayor de órgano, con un injerto funcionante existente. • Evidencia de consumo de drogas (incluyendo consumo excesivo de alcohol), dentro del año de ingreso al estudio. • Incapacidad de firmar consentimiento informado • Mujeres gestantes o en periodo de lactancia.

Criterios de Exclusión • Recuento de neutrófilos < 1500 cel/mm 3 • Hemoglobina menor de 10 g/d. L • Recuento de plaquetas < 90, 000 cél/mm 3

Tratamiento • El tratamiento durará 48 semanas • Después de iniciar el tratamiento , evaluaciones en las semanas 1, 2, 4, 6, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44, y, 48. • Un período de 24 semanas de seguimiento sin tratamiento, completa el estudio. • Los pacientes deben recibir la medicación durante una sesión de diálisis regular,

Seguimiento • Hemograma • Perfil Hepático: Transaminasas • Carga Viral: Inicio Tratamiento Semana 12 Semana 24 Semana 48 Semana 72

Características Epidemiológicas • Se han incluido 12 pacientes a partir de Diciembre del 2004 • Edad: 21 y 49 años (32. 7 años) • Sexo: - Masculino: 8 (66. 66%) - Femenino: 4 (33. 33%)


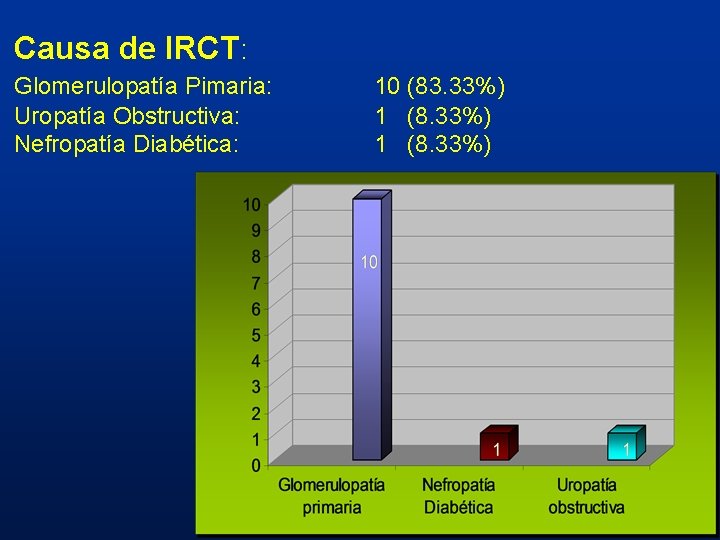
Causa de IRCT: Glomerulopatía Pimaria: Uropatía Obstructiva: Nefropatía Diabética: 10 (83. 33%) 1 (8. 33%)

Características Epidemiológicas • Tiempo de Permanencia en hemodiálisis: 1 a 13 años (7. 63 años) • Trasplante Renal Previo 1: (8. 33%) • Trasfusiones Sanguíneas (100%) • Tiempo de Infección por el HCV: 10 meses a 8 años (5. 3 años) • Carga Viral: 156, 000 UI a > 850, 000 UI 9 de ellos tuvieron menos de 850, 000 UI

Respuesta al Tratamiento • De los 12 pacientes: Finalizó Tratamiento: 1 paciente, carga viral negativa a semana 48 Respuesta a semana 12: 5 pacientes - 4: CV negativa a semana 12 - 1: CV sin variación al inicio de tratamiento (suspendió tratamiento) En los seis pacientes restantes aún no se puede evaluar la respuesta viral temprana

Eventos Adversos • Fiebre: 100% • Mialgia: 66. 66% • Depresión: Ninguno • Síntomas Gastrointestinales: Ninguno • Leucopenia, neutropenia y/o plaquetopenia: Ninguno • Anemia: 2 pacientes (suspendieron eritropoyetina)

Conclusiones • La viremia de la población en estudio aparentemente sería menor que la población con hepatitis crónica C, con función renal normal • El tratamiento con Interferón pegilado alfa 2 a, aparentemente, tiene un alto índice de respuesta viral temprana (5 de 6 pacientes: 83. 33%)

Conclusiones • La terapia con interferón pegilado alfa 2 a, a la dosis de 135 g es bien tolerada en la población con IRCT en hemodiálisis • Los eventos adversos son menores que en la población con hepatitis crónica sin compromiso de la función renal • La anemia es corregida con éxito por el uso concomitante de eritropoyetina