Tratamento da gua Conjunto de instalaes e equipamentos




























- Slides: 43

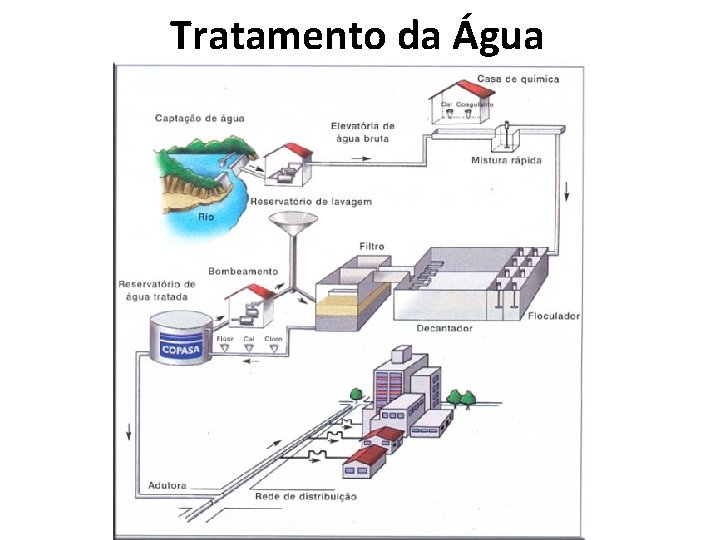
Tratamento da Água











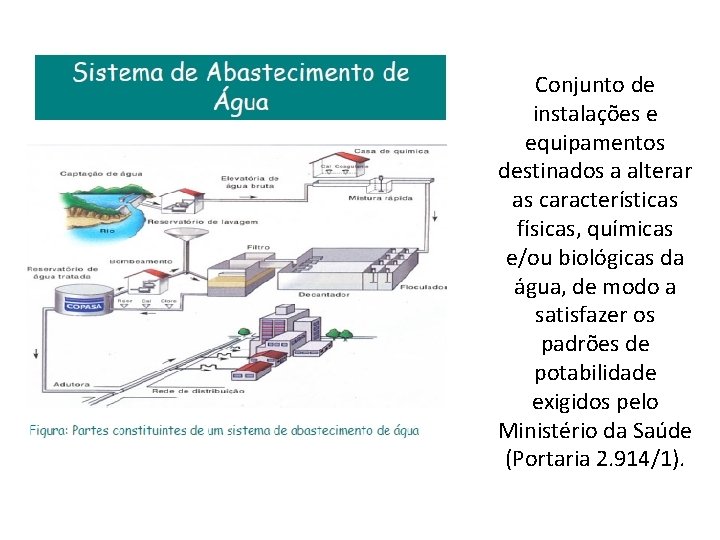
Conjunto de instalações e equipamentos destinados a alterar as características físicas, químicas e/ou biológicas da água, de modo a satisfazer os padrões de potabilidade exigidos pelo Ministério da Saúde (Portaria 2. 914/1).


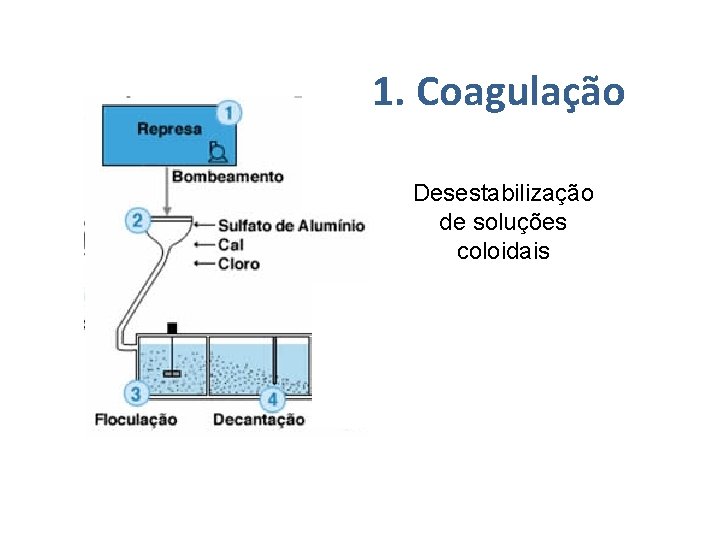
1. Coagulação Desestabilização de soluções coloidais

Mecanismo de Formação de Dispersões Coloidais • No p. H das águas naturais ocorrem partículas suspensas de silicatos ionizados, com cargas negativas. • Essas partículas sólidas, com pequenas dimensões (micelas), podem ter íons fixados à superfície. • Esses íons podem estar fixados por processos de adsorção ou ionização de grupos na superfície de sólidos.

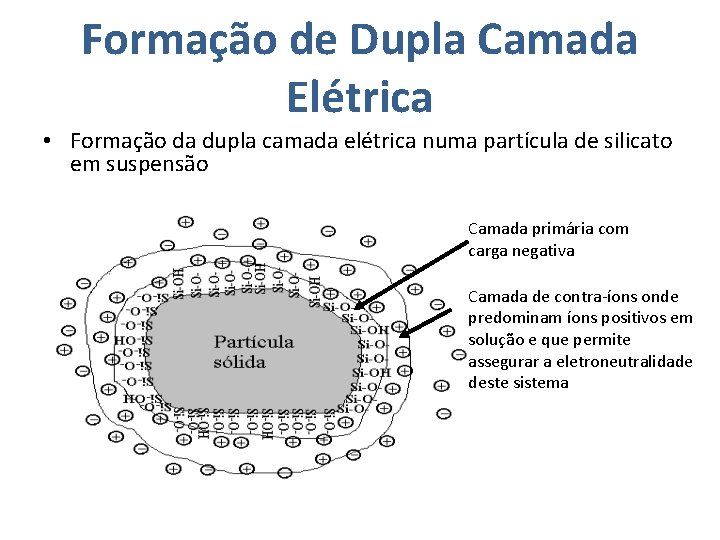
Formação de Dupla Camada Elétrica • Formação da dupla camada elétrica numa partícula de silicato em suspensão Camada primária com carga negativa Camada de contra-íons onde predominam íons positivos em solução e que permite assegurar a eletroneutralidade deste sistema

Estabilização de Suspensões Coloidais • Cargas elétricas iguais dificultam aproximação e união das partículas, que pode permanecer muito tempo sem precipitar.

1. Coagulação Resulta de: 4 fatores distintos.

Mecanismos de Desestabilização de Colóides 1. Compressão da camada difusa (dupla camada elétrica) diminuindo a espessura da camada de contra-íons. 2. Adsorção e neutralização da carga elétrica da camada primária. 3. Formação de pontes e adsorção entre partículas (polímeros). 4. Varredura num precipitado volumoso de Al(OH)3 ou de Fe(OH)3 - Fe III.

Coagulação Espécies com carga contrária à da superfície dos colóides causam sua desestabilização. • Coagulante gera cátions que neutralizam a carga negativa do colóide, antes da formação visível do floco. A agitação é importante nesta fase.

Coagulação Polieletrólitos - aniônicos, catiônicos, anfolíticos e não iônicos, de alto PM, com grupos carregados são capazes de atuar como coagulante (desestabilizam colóides).

Tipos de coagulantes 1. Alumínio Redução p. H natural da água (p. H 6 -8) Al+3 + H 2 O ↔ Al 13 O 4(OH)24+7 + 32 H⁺ p. H < 5, 7 A espécie química Al(OH)3↓ forma flocos e o CO 2 é o responsável pelo aumento da acidez da água.

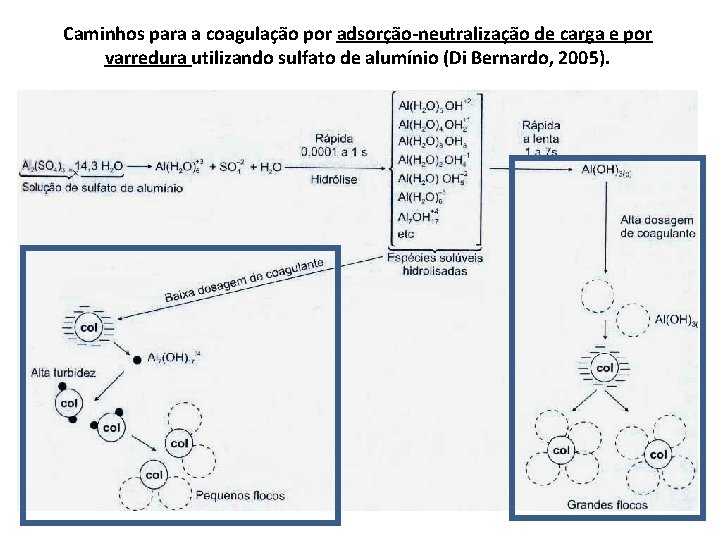
Caminhos para a coagulação por adsorção-neutralização de carga e por varredura utilizando sulfato de alumínio (Di Bernardo, 2005).

2. Sulfato férrico Fe. SO 4 → 2 Fe(OH)3↓ Usado primariamente, na coagulação de esgotos sanitários e industriais, e encontra aplicações limitados no tratamento de água. Disponível nas formas sólida e liquida, é altamente corrosivo.

3. Policloreto de Alumínio Inorgânico catiônico pre-polimerizados a base de policloreto de alumínio. • Carga = Aln(OH)m (3 n-m)+

Auxiliares de Coagulação Principais dificuldades com a coagulação: - flocos de baixa decantação - flocos frágeis - p. H • Melhoraram a coagulação promovendo o crescimento dos flocos e incrementando a velocidade de sedimentação destes. • Correção p. H Materiais mais utilizados são: polímeros, alcalinizantes, sílica ativada, agentes adsorventes de peso e oxidantes.

2. Floculação Transporte de Partículas Etapa que propicia condições para: - Contato e agregação de partículas desestabilizadas por coagulação química. - Flocos de tamanho e massa específica que favoreçam sua remoção por sedimentação, flotação ou filtração direta.

Coagulação X Floculação: • Coagulação e Floculação são muitas vezes usadas em química como equivalentes da formação de agregados de partículas coloidais. • Para conseguir a agregação de micelas, há que proceder de modo a diminuir ou mesmo suprimir as forças repulsivas. • Em tratamentos de águas, o termo Coagulação aplica -se a desestabilização das partículas coloidais para formação do pequenos agregados , os coágulos.

“Jar test”: copos com agitador, onde a amostra de água é ensaiada avaliando os efeitos que pode ter a adição de determinado agente químico e em diferentes condições.


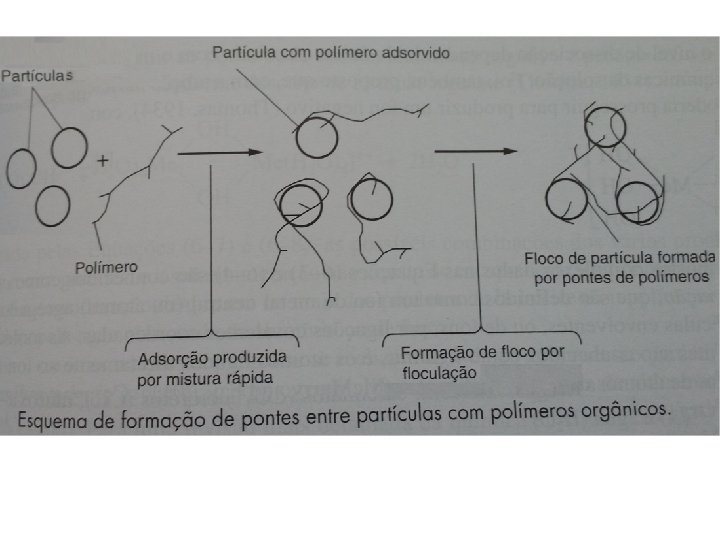
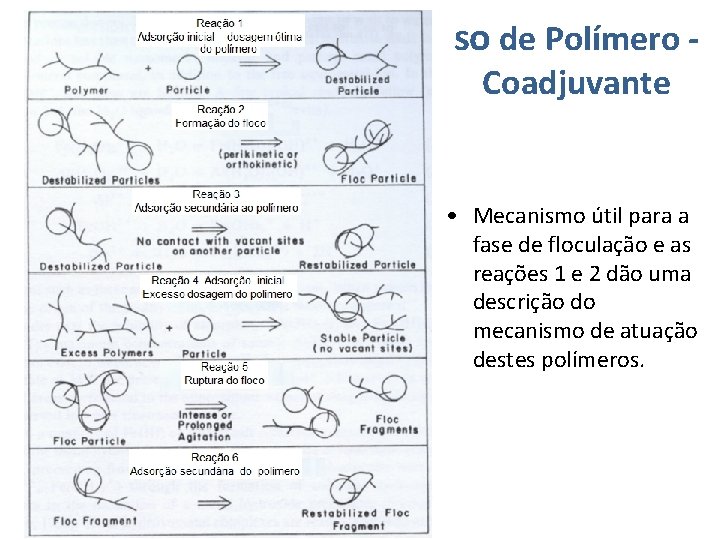
so de Polímero Coadjuvante • Mecanismo útil para a fase de floculação e as reações 1 e 2 dão uma descrição do mecanismo de atuação destes polímeros.

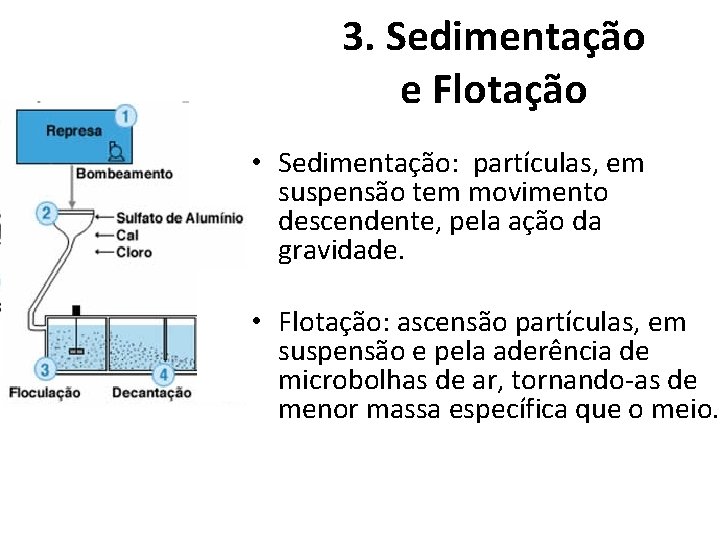
3. Sedimentação e Flotação • Sedimentação: partículas, em suspensão tem movimento descendente, pela ação da gravidade. • Flotação: ascensão partículas, em suspensão e pela aderência de microbolhas de ar, tornando-as de menor massa específica que o meio.

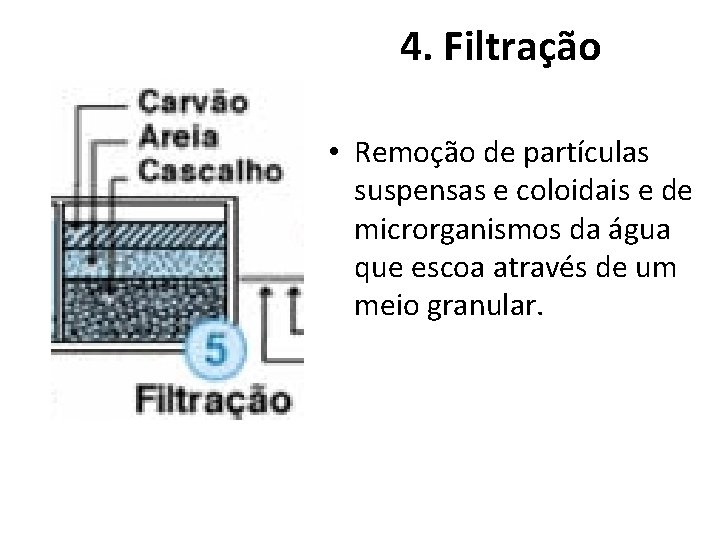
4. Filtração • Remoção de partículas suspensas e coloidais e de microrganismos da água que escoa através de um meio granular.

5. Adsorção em Carvão Ativado Na forma de pó, tem grande poder de adsorção. É bastante empregada no tratamento da água com gosto e odor provocador por material orgânico.

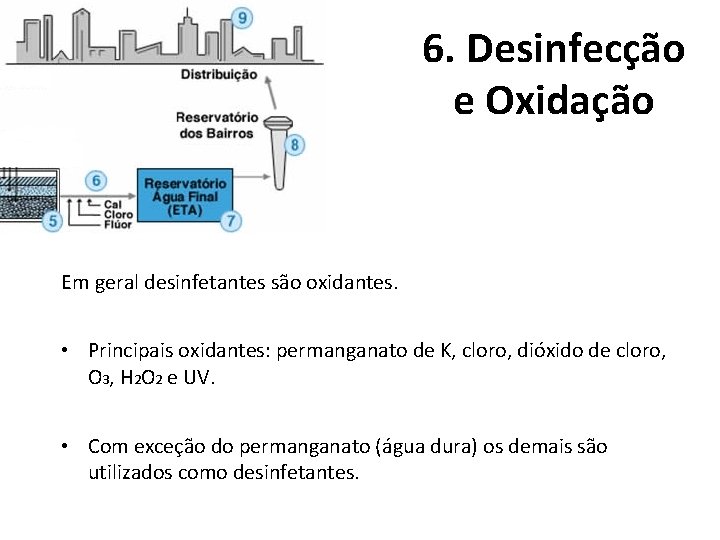
6. Desinfecção e Oxidação Em geral desinfetantes são oxidantes. • Principais oxidantes: permanganato de K, cloro, dióxido de cloro, O 3, H 2 O 2 e UV. • Com exceção do permanganato (água dura) os demais são utilizados como desinfetantes.



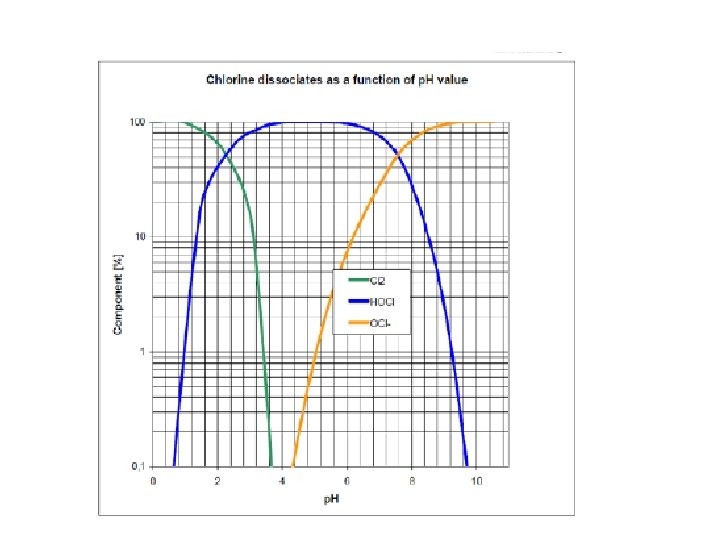
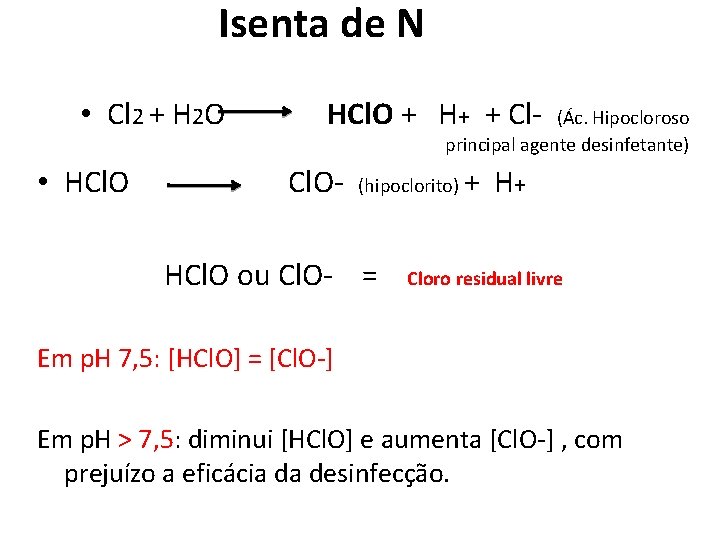
Isenta de N • Cl 2 + H 2 O • HCl. O + H+ + Cl- (Ác. Hipocloroso principal agente desinfetante) Cl. O- (hipoclorito) HCl. O ou Cl. O- = + H+ Cloro residual livre Em p. H 7, 5: [HCl. O] = [Cl. O-] Em p. H > 7, 5: diminui [HCl. O] e aumenta [Cl. O-] , com prejuízo a eficácia da desinfecção.

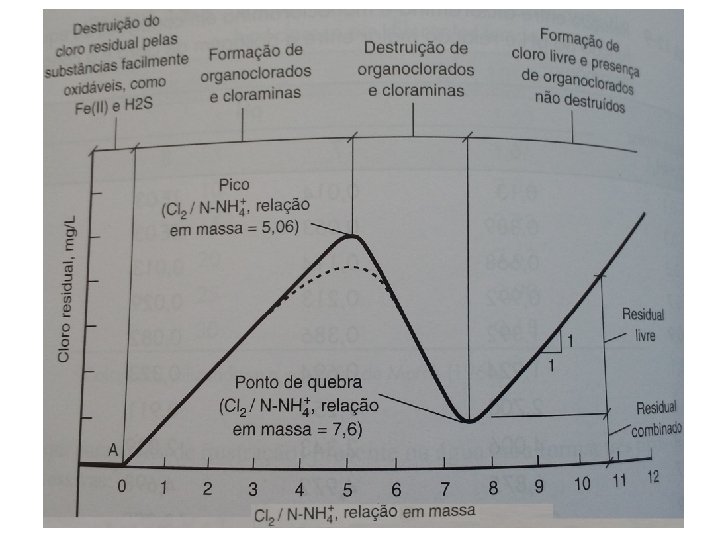
Na presença de amônia (N amoniacal consome o Cl na formação de cloraminas = cloro residual combinado) • HCl. O + NH 4⁺ → NH 2 Cl + H 2 O + H⁺ (monocloraminas) • HCl. O + NH 2 Cl → NHCl 2 + H 2 O (dicloraminas com > poder bactericida) • Cl. O + NHCl 2 → NCl 3 + H 2 O (tricloraminas não tem efeito) • Break point – quando toda a amônia disponível se combinou com o cloro para a formação de cloraminas. Teor residual mínimo de cloro livre.


Cloro ao reagir compostos orgânicos, de ocorrência natural na água de abastecimento, produz subprodutos da desinfecção. Os subprodutos mais TRIHALOMETANOS haloaceticos(AIH). comuns são e ácidos

