Trastornos del movimiento Dr Miguel A Barboza Elizondo

Trastornos del movimiento Dr. Miguel A. Barboza Elizondo Servicio de Neurología Hospital Rafael A. Calderón Guardia

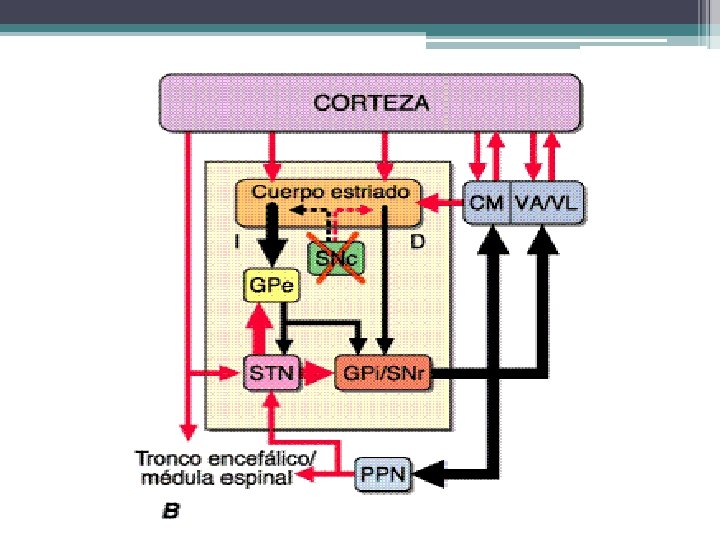
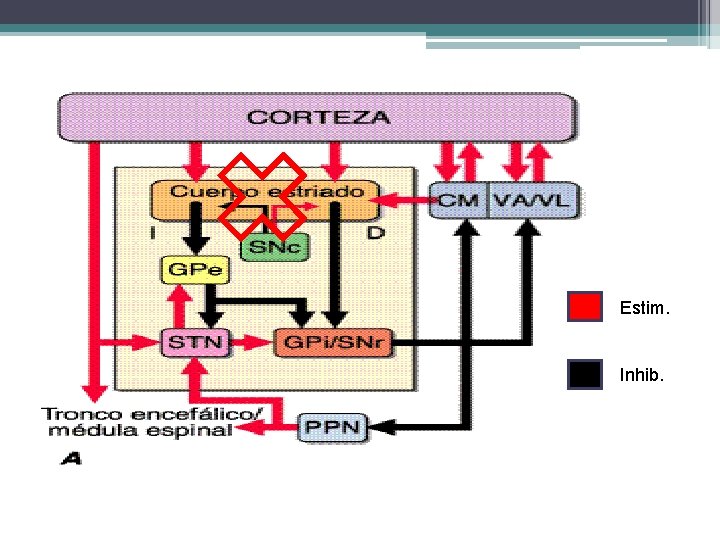
Ganglios de la base • Funciones: ▫ Regulación de los movimientos motores voluntarios a nivel superior. ▫ Regulación de los movimientos oculares y algunas funciones cognitivas (caudado) ▫ Modulación de la actividad motora superior. ▫ Integración de vías de relevo

Ganglios de la base (control extrapiramidal) • Caudado • Putamen ▫ Caudado + Putamen = Estriado • Globo pálido ▫ Caudado + Putamen + G. pálido = Cuerpo estriado • Núcleo subtalámico ▫ Globo pálido + N. subtalámico = Núcleo lenticular • Sustancia Nigra ▫ Pars compacta y pars reticular.
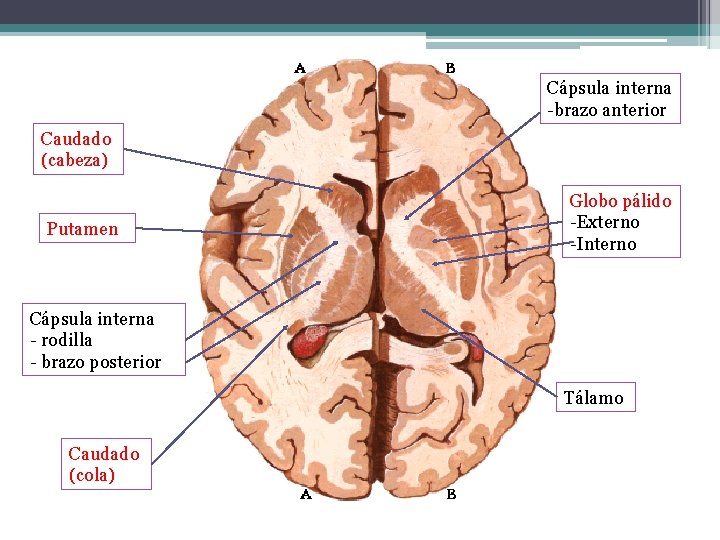
Cápsula interna -brazo anterior Caudado (cabeza) Putamen Globo pálido -Externo -Interno Cápsula interna - rodilla - brazo posterior Tálamo Caudado (cola)
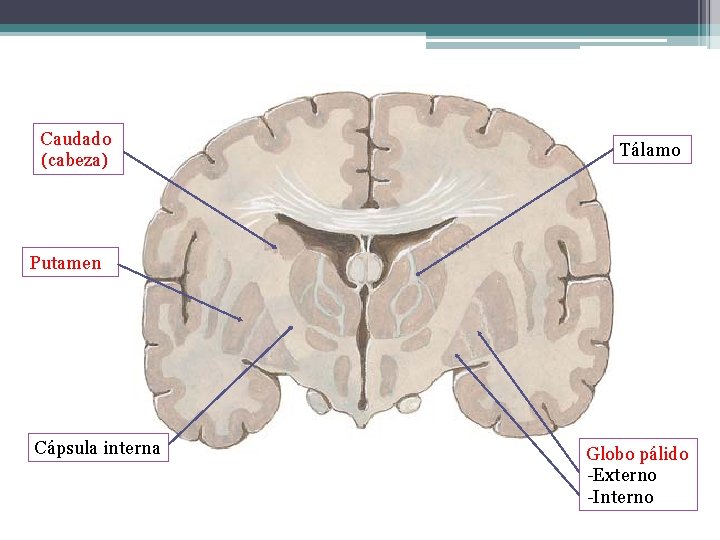
Caudado (cabeza) Tálamo Putamen Cápsula interna Globo pálido -Externo -Interno
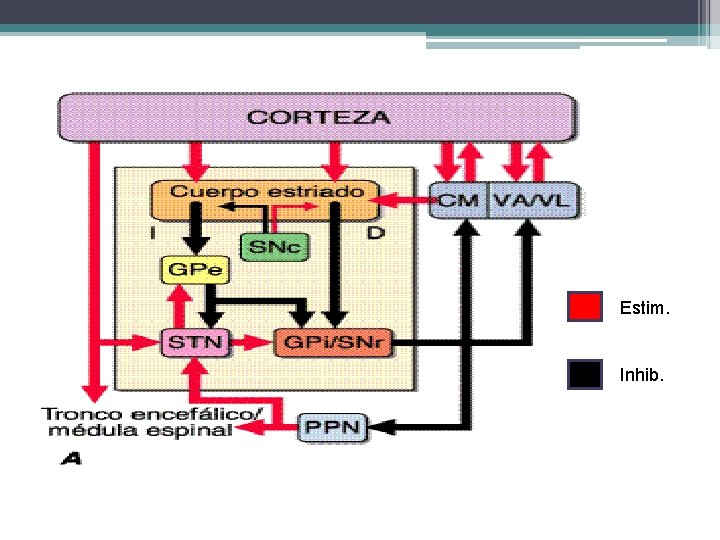
Estim. Inhib.

Clínica de la afectación de los ganglios basales • Corea ▫ Movimientos arrítmicos de tipo espasmódico, rápido y vigoroso que abarcan los dedos de las manos, las manos o toda una extremidad ▫ Gesticulación y ruidos respiratorios ▫ Entre uno y otro movimiento = flacidez ▫ Puede ser hemicorea ▫ Corea de Sydenham, corea gravídica, enfermedad de Huntington ▫ Lesión: núcleo caudado y putamen

Clínica de la afectación de los ganglios basales • Hemibalismo ▫ Movimientos que abarcan la porción proximal de una extremidad, con un carácter extraordinariamente violento y saltarín. ▫ Lesión: núcleo subtalámico de Luys contralateral, y afectación de las fibras que van al globo pálido ▫ Se puede acompañar de hemicorea

Clínica de la afectación de los ganglios basales • Atetosis ▫ Movimientos involuntarios, sinuosos y relativamente lentos que tienden a confluir entre sí. ▫ Flexo-supinación/extenso-pronación ▫ Entre uno y otro movimiento = rígido o espástico ▫ Puede ser generalizada (Huntington o fármacos) o limitada (cervical o craneal = discinesias oromandibular o tortícolis espasmódica) ▫ Lesión= cuerpo estriado contralateral


Clínica de la afectación de los ganglios basales • Distonía ▫ Actitud o postura contorsionada anormal, en uno u otro de los extremos de mov. atetoides ▫ Predilección por músculos del tronco y cintura escapular y pélvica. ▫ Pueden ser reversibles o fijas. ▫ Pueden ser como reacción aguda o crónica a medicamentos ▫ Lesión= cuerpo estriado contralateral

Enfermedad de Parkinson

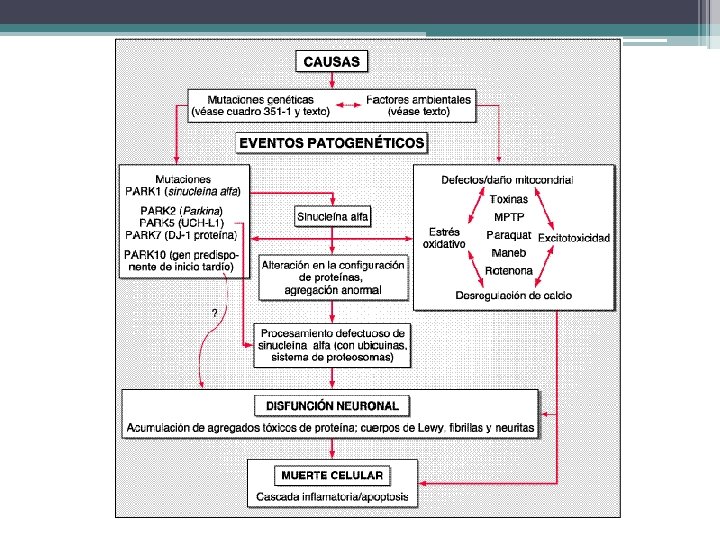
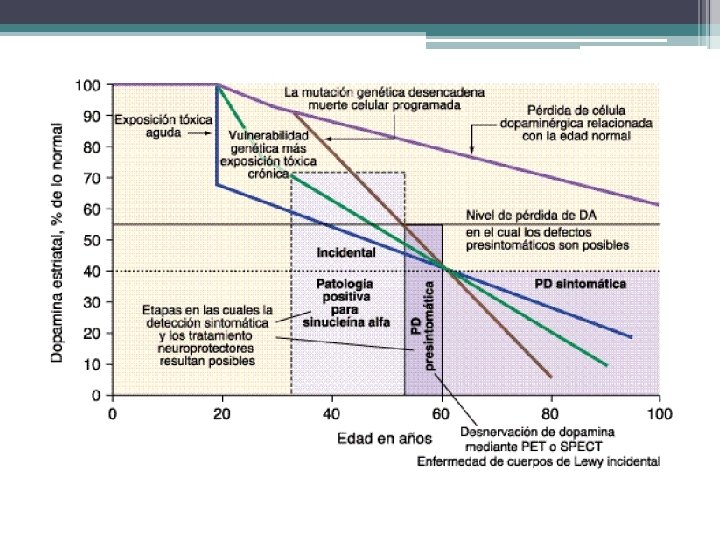
Definición del problema • Trastorno neurodegenerativo por acumulación neuronal de sinucleina alfa y grados variables de parkinsonismo • Casi todas las formas de parkinsonismo resultan en reducción en la transmisión dopaminérgica dentro de los GB • 75% esporádica

Epidemiología • • USA > 1000000 (1% de personas > 55 años) Edad máxima de inicio = 60 años Evolución entre 10 -25 años AD y AR aproximadamente 5% (edad de inicio más temprana y evolución más prolongada) • Factores de riesgo: AHF (+), masc. , TCE, exposición a pesticidas, resid. En medio rural • Factor protector: café, tabaco, AINES y E 2 (muj. )

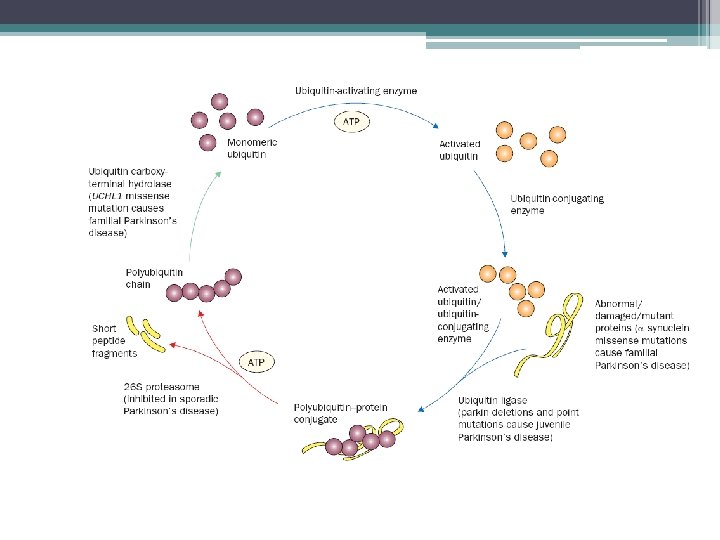
Genética y patogenia • Herencia importante en casos <50 años • Formas familiares: PARK 1, 5 (AD) y 2, 7 (AR) ▫ Síntesis de sinucleína alfa ▫ Síntesis de la parkina (ligasa de la ubicuina) ▫ Síntesis de la hidroxilasa carboxiterminal de la ubicuina L 1 • Muerte neuronal por ▫ ▫ Vulnerabilidad genética Estrés oxidativo Factores ambientales Disfunción proteasómica

Manifestaciones clínicas • Tres criterios cardinales: ▫ Tremor en reposo (85%) ▫ Rigidez ▫ Bradicinesia • Inicio unilateral y gradual • Manifestaciones motoras ▫ Bradicinesia ▫ Micrografía ▫ Hipofonía y sialorrea (bradicinesia bulbar)

Manifestaciones clínicas • Manifestaciones motoras ▫ Tremor en reposo: frecuencia de 4 -6 Hz, unilateral inicialmente, “cuenta monedas”. Diseminación proximal, ipsilateral y en un segmento del mismo lado antes de cruzar. ▫ Rigidez en rueda dentada ▫ Marcha festinante (postura encorvada + pérdida de reflejo postural) y vacilación de inicio. ▫ Alteración de automatismos de la marcha

Manifestaciones clínicas • Manifestaciones no motoras ▫ Depresión (50%) y ansiedad, anosmia. ▫ Alteraciones del sueño (piernas inquietas + desorden del ambiente REM). ▫ Inquietud interna (“acatisia” ? ? ) ▫ Disfx autonómica (hipotensión ortostática, sudación excesiva, estreñimiento, etc. ) ▫ Anormalidades cognitivas con tareas complejas, planificación a largo plazo y memoria.

Levo-Dopa (consideraciones) • Medicación de primera elección para el tx temprano sintomático en Parkinson ▫ Dosis deben mantenerse lo suficientemente bajas como para mejorar la fx y reducir complicaciones motoras. ▫ Las preparaciones de liberación prolongada no tienen mayor ventaja en las complicaciones motoras. ▫ L-Dopa genera mayor beneficio en la funcionalidad que los agonistas dopaminérgicos, pero se asocia a mayores complicaciones motoras. (NICE/AAN nivel A)

Levo-Dopa • • • L-3, 4 -dihidroxifenilalanina Efecto terapéutico al descarboxilarse Concentración máx. 0, 5 -2 h plasma Semivida de 1 -3 h Competencia con proteínas dietéticas Inhibición periférica de descarboxilasa de L-Dopa ▫ Carbidopa / Benserazida Brunton, L; Lazo, J; Parker, K. Goodman & Gillman: las bases farmacológicas de la terapéutica. 11 edición. Editorial Mc. Graw-Hill, Mexico, D. F. 2007
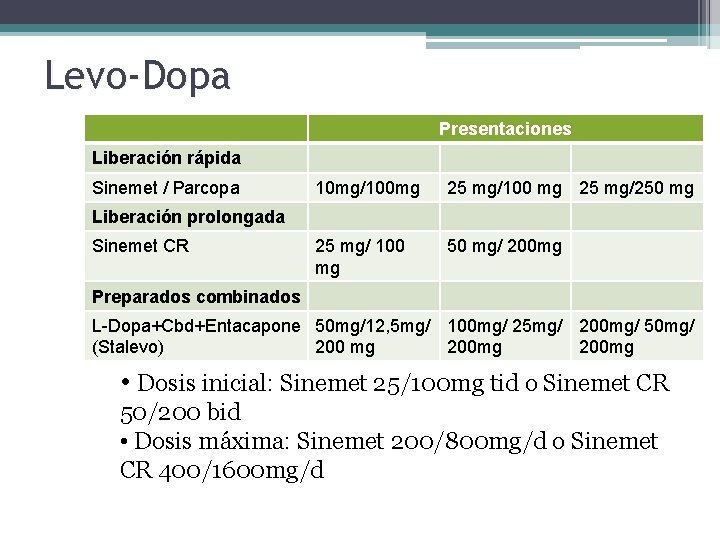
Levo-Dopa Presentaciones Liberación rápida Sinemet / Parcopa 10 mg/100 mg 25 mg/100 mg 25 mg/250 mg 25 mg/ 100 mg 50 mg/ 200 mg Liberación prolongada Sinemet CR Preparados combinados L-Dopa+Cbd+Entacapone 50 mg/12, 5 mg/ 100 mg/ 25 mg/ 200 mg/ 50 mg/ (Stalevo) 200 mg 200 mg • Dosis inicial: Sinemet 25/100 mg tid o Sinemet CR 50/200 bid • Dosis máxima: Sinemet 200/800 mg/d o Sinemet CR 400/1600 mg/d

Levo-Dopa (efectos adversos) • Náuseas y vómitos • SS/ abrupta puede llevar a síndrome neuroléptico maligno • Diskinesias • Fenómenos on – off • Akinesia paradójica • Hipotensión ortostática • Depresión • Delirios • Contraindicado en IMAO, glaucoma de ángulo cerrado o melanoma maligno

Agonistas dopaminérgicos • Pueden utilizarse como 1º línea de tx temprana (AAN/NICE nivel A) ▫ Menos efectivo para mejoría de síntomas motores • Disminuyen las complicaciones motoras pero asociado a más efectos adversos que L-Dopa en Parkinson temprano (Cochrane nivel 2) ▫ Revisión sistemática de 29 ensayos randomizados que evaluaron Ago. en 5247 pxs con Parkinson temprano ▫ Aumento de Ago en: Edema OR 3, 48 (95% CI 2, 53 -4, 79) Somnolencia OR 2, 18 (95% CI 1, 75 -2, 72) Náusea 34, 4% vs 23, 1% (OR 1, 86 CI 1, 56 -2, 23) Cochrane Database Syst Rev 2008 Apr 16; (2): CD 006564

Agonistas dopaminérgicos • Pramipexole (Mirapex) ▫ Agonista dopaminérgico no ergotamínico ▫ Puede reducir tiempo “off”, mejoría de sxs motores y discapacidad (nivel 2 evidencia) ▫ Dosis inicial: 0, 125 mg vo tid y aumentos progresivos cada semana hasta llegar a 1, 5 mg vo tid (semana 7) ▫ Ajuste con Función renal ▫ Efectos adversos: ataques de somnolencia, náusea, mareos, constipación, edema, hipotensión ortostática, rabdomiolisis, alucinaciones.

Agonistas dopaminérgicos • Ropirinole (Requip) ▫ Agonista dopaminérgico no ergotamínico ▫ Efectivo en reducir sxs como monotx o adyuvante (nivel 2 evidencia) ▫ Dosis inicial: 0, 25 mg vo tid y aumentos progresivos de 0, 25 mg en c/dosis cada semana hasta llegar a dosis total de 24 mg/d ▫ Efectos adversos: ataques de somnolencia, náusea, mareos, constipación, edema, hipotensión ortostática, pueden empeorar las diskinesias por LDopa, alucinaciones.

Agonistas dopaminérgicos • Bromocriptina ▫ Agonista dopaminérgico ergotamínico ▫ Efectivo en retardar complicaciones motoras en pxs con Parkinson temprano, pero no es más efectivo que L-Dopa (nivel 2 evidencia) ▫ Dosis inicial: 1, 25 mg bid con aumentos de 2, 5 mg/d cada 14 -28 d (dosis máxima 100 mg/d) ▫ Efectos adversos: ataques de somnolencia, náusea, constipación, hipotensión ortostática, convulsiones e ictus, derrame pleural o pericárdico, alteracioenes mentales o psicosis.

Inhibidores monoamino oxidasa B • Selegilina (Deprenyl) ▫ Tratamiento sintomático temprano (NICE A) ▫ Retrasa las complicaciones motoras comparado a LDopa ▫ “Ahorradores” de L-Dopa (nivel 1) sin aumentar mortalidad (nivel 2) ▫ Dosis inicial: 5 mg bid vo ▫ Efectos adversos: náusea, mareos, lipotimias, alucinaciones, sequedad de boca, diskinesias, sueños vividos

Inhibidores catecol-ometiltransferasa • Entacapone (Comptan) y Tolcapone (Tasmar) ▫ Reducen el tiempo “off” y el uso de L-Dopa (nivel 1) ▫ Mejoría de calidad de vida con menores fluctuaciones motoras (nivel 2) ▫ Entacapone: 200 mg con c/dosis de Sinemet (máximo 1, 6 g/d) ▫ Tolcapone: 100 mg tid (hasta 200 mg tid) ▫ Efectos adversos: hipotensión ortostática, diskinesias, diarrea, náuseas, mareos, dolosr abdominal, alucinaciones. Con Tolcapone aumento de enzimas hepáticas

Amantadina • Evidencia limitada, uso temprano pero no de primera elección (NICE nivel D) • Preferencia en el tx del tremor • Dosis inicial: 100 mg bid vo • Efectos adversos: nausea, insomnio, mareo, urgencia sexual y de apuestas, riesgo suicida, IC, crisis parkisoniana

Enfermedad de Huntington

Enfermedad de Huntington • Descrita por George Huntington, 1872

Epidemiología • Mundial 4 -5/100000 habitantes ▫ 30 -70/100000 hab. Europeos Norte • 3 ra a 4 ta década ▫ 3 -5% antes de los 15 años ▫ 30% sintomáticos después de los 50 años • Patrón de herencia autosómico dominante

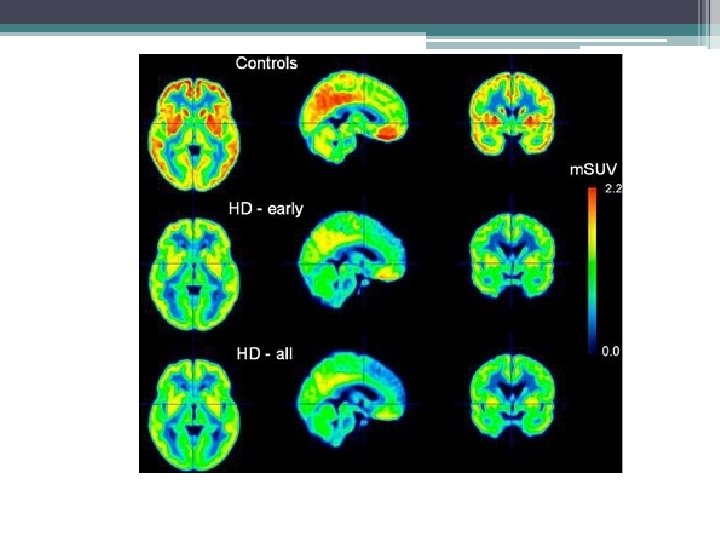
Patología y Patogénesis • Atrofia de la cabeza del núcleo caudado y putamen bilateral – Asociado a atrofia fronto-temporal – Ventriculomegalia • Estadio temprano: – Hipometabolismo en Caudado (PET) – Afectación de neuronas más pequeñas primero en el estriado – Gliosis por astrocitos – Pérdida neuronal cortical en capas 3, 5 y 6

Patología y Patogénesis • Marcada sensibilidad de los receptores estriatales dopaminérgicos ▫ Movimientos anormales • Alteraciones en el microambiente de Nt ▫ NE, GABA, Ach, Somatostatina y Glutamato
Estim. Inhib.

Patogénesis • Huntingtina – Codificada en cromosoma 4 – 11 a 34 (media 19) repeticiones de CAG • 35 -39 repeticiones síntomas / 42 = enfermedad – Mutación = expansión de la poliglutamina (CAG) – Acumulación y agregación en estriado y corteza • Toxicidad directa o en su forma protofibrilar – Acetilación de estonas ? ? – Disfunción mitocondrial ? ? – Sensibilidad a toxicidad mediada por Glutamato ? ? – Rol de la clatrina ? ?
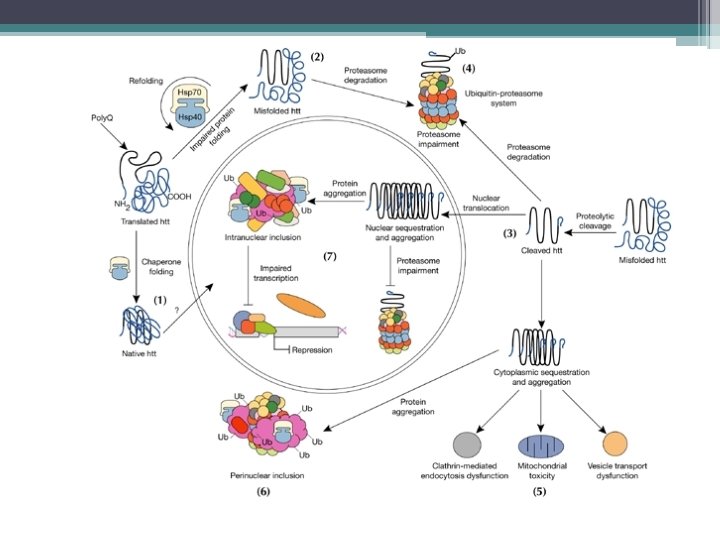
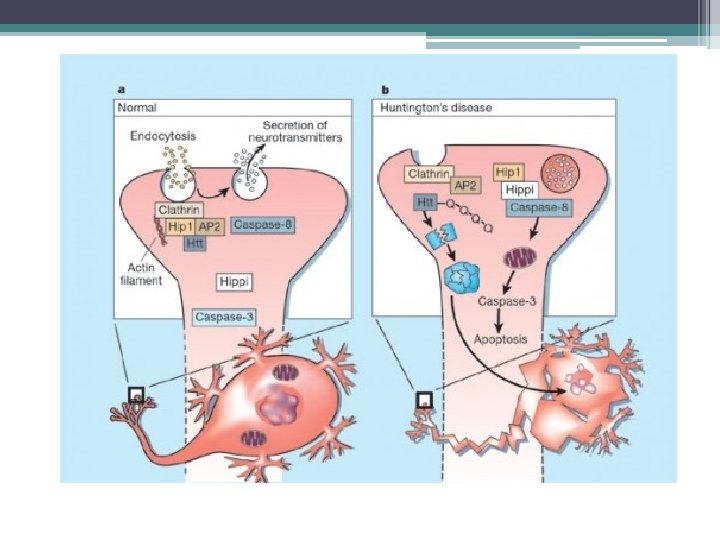
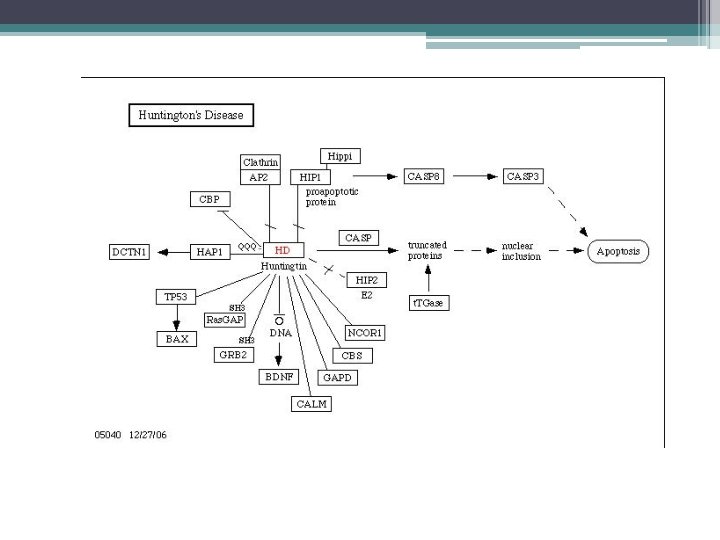

Cuadro clínico • Trastornos cognitivos – ½ inicialmente con alteraciones del estado de ánimo y del carácter • Irritables, impulsivos, excéntricos, hiperreligiosos, • Alcoholismo, pobre control de impulsos, hipersexual • Depresión – Deterioro cognitivo • Dispraxias, inatención, alteraciones del lenguaje • Memoria relativamente preservada – Alteraciones del sueño

Cuadro clínico • Trastorno del movimiento ▫ Inicialmente en manos y cara (“nerviosismo”) ▫ Dificultad para movimientos alternantes en dedos ▫ Progresión a corea (patrón estereotipado) Movimientos arrítmicos de tipo espasmódico, rápido y vigoroso que abarcan los dedos de las manos, las manos o toda una extremidad ▫ Etapa más avanzada = patrón atetoide o distónico ▫ 1/3 hiperreflexia

Cuadro clínico • Trastorno del movimiento ▫ Movimientos voluntarios más lentos de lo normal ▫ Lenguaje disártrico y explosivo (incoordinación lengua-diafragma) ▫ Movimientos oro-linguales ▫ Signo del ordeño ▫ Alteración en el inicio y lentitud de los movimientos sacádicos oculares, que se acompañan de movimiento cefálico.

Cuadro Clínico • 10 -15 años progresión a estado vegetativo, incapacidad de bipedestación o alimentación • Progresión a muerte casi invariable • Alta tasa de suicidio • Fenómeno de anticipación • La demencia es más severa en los de inicio temprano (30 -40 años)

Diagnóstico • Confirmación de la mutación en la Huntingtina (39 a 42 repeticiones) ▫ Consejo genético ? ? ? • Estudios funcionales: PET ▫ Hipometabolismo en caudado y putamen • RM: atrofia en caudado y putamen
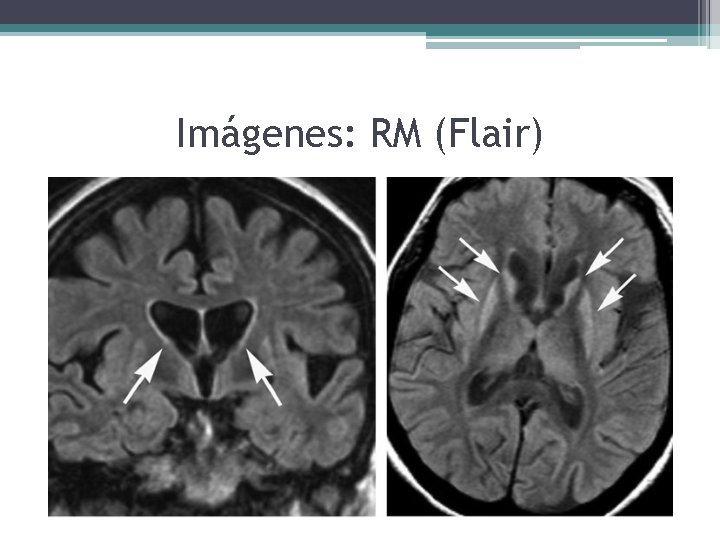
Imágenes: RM (Flair)

Tratamiento • Haloperidol – Supresión de la corea/atetosis – 2 a 10 mg /d VO • Tetrabenazina – 12, 5 mg/d con aumentos hasta tid • Antipsicóticos de nueva generación – Efectivos pero muchos efectos adversos • Antidepresivos y moduladores del estado de ánimo

Muchas gracias
- Slides: 55