Trasformazioni cicliche Trasformazione ciclica una trasformazione in cui















- Slides: 28

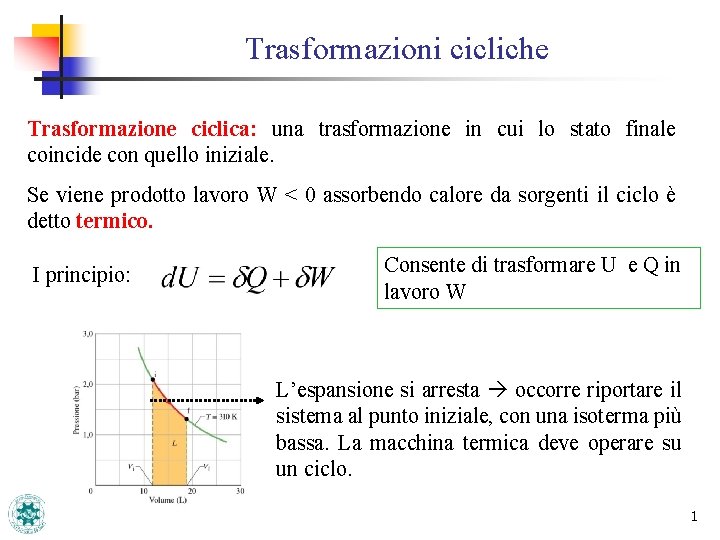
Trasformazioni cicliche Trasformazione ciclica: una trasformazione in cui lo stato finale coincide con quello iniziale. Se viene prodotto lavoro W < 0 assorbendo calore da sorgenti il ciclo è detto termico. I principio: Consente di trasformare U e Q in lavoro W L’espansione si arresta occorre riportare il sistema al punto iniziale, con una isoterma più bassa. La macchina termica deve operare su un ciclo. 1

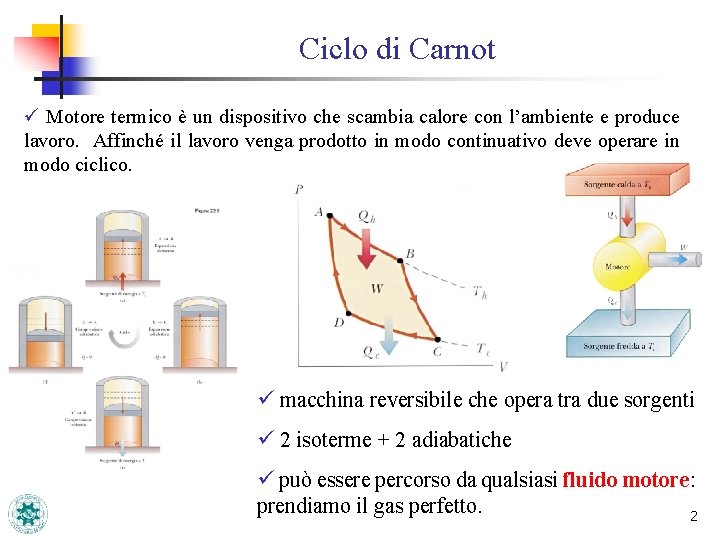
Ciclo di Carnot ü Motore termico è un dispositivo che scambia calore con l’ambiente e produce lavoro. Affinché il lavoro venga prodotto in modo continuativo deve operare in modo ciclico. ü macchina reversibile che opera tra due sorgenti ü 2 isoterme + 2 adiabatiche ü può essere percorso da qualsiasi fluido motore: prendiamo il gas perfetto. 2

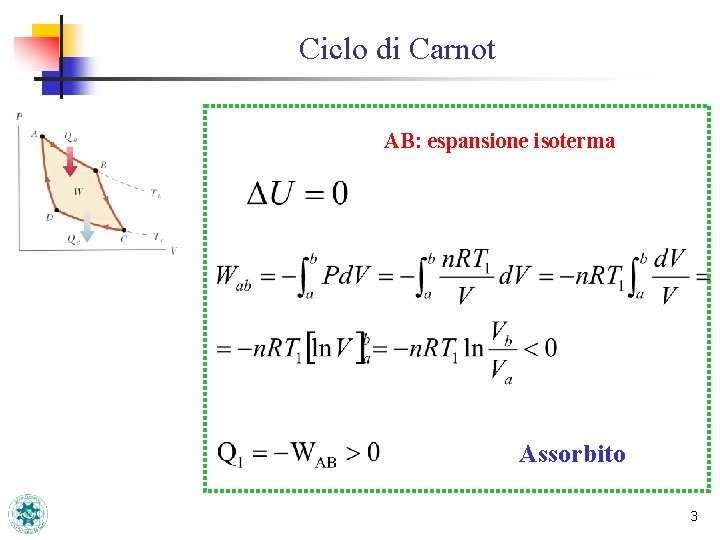
Ciclo di Carnot AB: espansione isoterma Assorbito 3

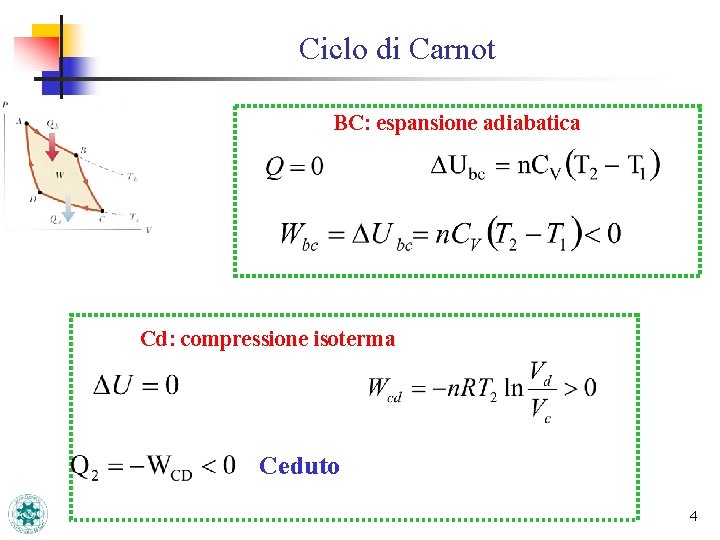
Ciclo di Carnot BC: espansione adiabatica Cd: compressione isoterma Ceduto 4

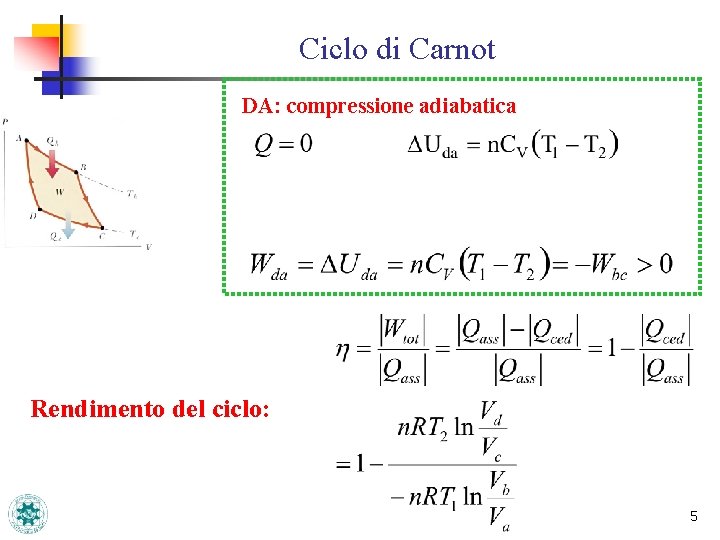
Ciclo di Carnot DA: compressione adiabatica Rendimento del ciclo: 5

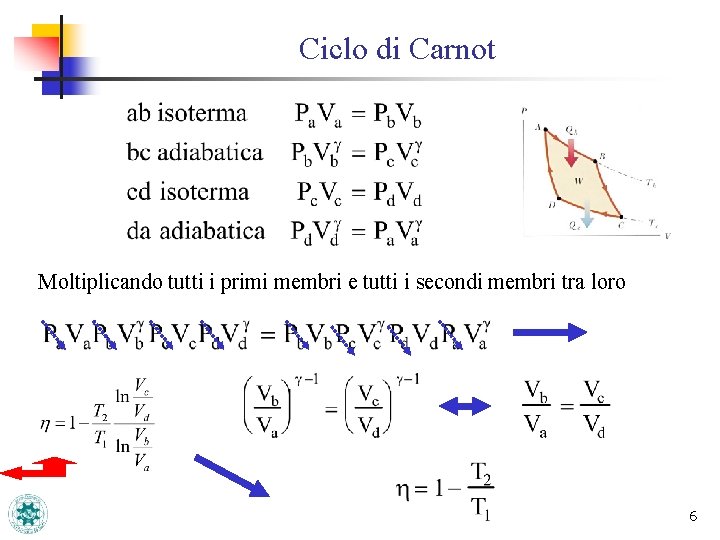
Ciclo di Carnot Moltiplicando tutti i primi membri e tutti i secondi membri tra loro 6

Applicazione: il Ciclo Otto Una macchina termica a combustione interna, il motore dell'automobile a benzina, può essere approssimata con il ciclo mostrato in figura. Si supponga che la miscela aria-benzina possa essere considerato un gas perfetto e che venga utilizzato un rapporto di compressione 4 a 1 (V 4 = 4 V 1). Si supponga inoltre che p 2=3 p 1. Determinate la pressione e la temperatura in ognuno dei quattro vertici del diagramma p-V in funzione di p 1 e T 1, e del rapporto g dei calori specifici del gas. Esprimere il rendimento del ciclo in funzione del rapporto di compressione. Confrontare con il rendimento di una macchina di Carnot che lavora tra le temperature estreme. 7

Applicazione: il Ciclo Otto 8

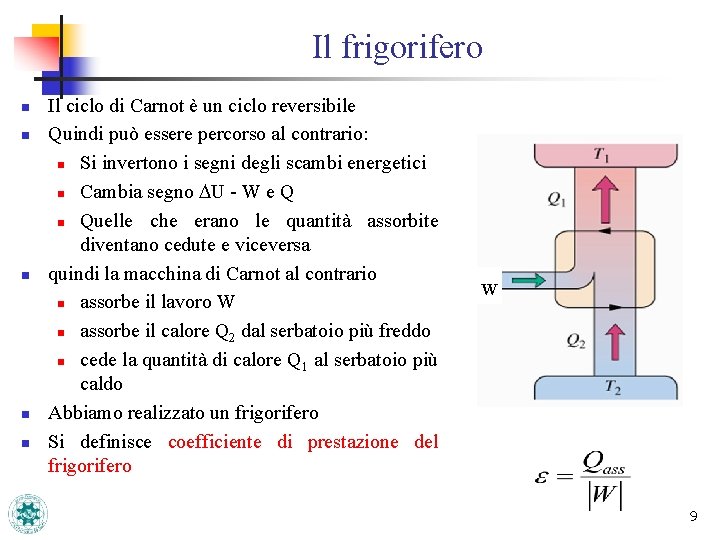
Il frigorifero n n n Il ciclo di Carnot è un ciclo reversibile Quindi può essere percorso al contrario: n Si invertono i segni degli scambi energetici n Cambia segno DU - W e Q n Quelle che erano le quantità assorbite diventano cedute e viceversa quindi la macchina di Carnot al contrario n assorbe il lavoro W n assorbe il calore Q 2 dal serbatoio più freddo n cede la quantità di calore Q 1 al serbatoio più caldo Abbiamo realizzato un frigorifero Si definisce coefficiente di prestazione del frigorifero w 9

Irreversibilità e II principio Øle trasformazioni in natura sono irreversibili!!! Procedono in un’unica direzione. Ø per es. due corpi a temperatura differente: il calore può passare da quello più caldo a quello più freddo ma non il viceversa. Ø Pendolo messo in oscillazione: parte dell’energia meccanica viene ceduta sotto forma di energia interna dell’aria. Non può accadere il viceversa. ØPerché? ? Il II principio della termodinamica 10

L’entropia Esiste una funzione di stato l’ entropia, S: tale che l’integrale del calore scambiato reversibilmente diviso per la T a cui avviene lo scambio, tra lo stato i e lo stato f, è dato dalla differenza dei valori della funzione S nello stato finale meno quello dello stato iniziale. n n La variazione di entropia non dipende dalla trasformazione, sia reversibile o irreversibile. Attenzione: il calcolo di DS deve essere fatto SOLO su una trasformazione REVESIBILE 11

L’entropia: funzione di stato Gas perfetto Vale per qualunque trasformazione tra i ed f 12

Applicazioni n n n Consideriamo due corpi a T 1 e T 2: il calore ceduto dal corpo 1 ed assorbito dal corpo 2, fino alla T di equilibrio. La trasformazione è irreversibile. Il calore trasferito da un corpo all’altro può essere calcolato come se la trasformazione fosse reversibile È a pressione costante T 1 Q 1 T 1>T 2 Q 2 13

Applicazioni 14

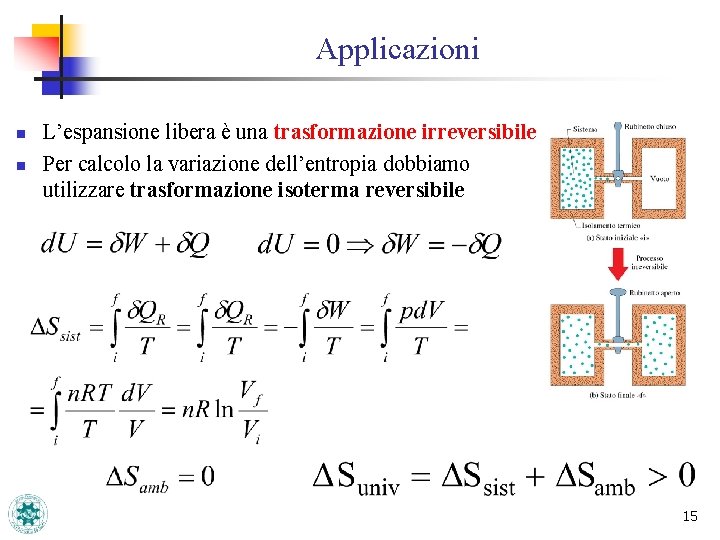
Applicazioni n n L’espansione libera è una trasformazione irreversibile Per calcolo la variazione dell’entropia dobbiamo utilizzare trasformazione isoterma reversibile 15

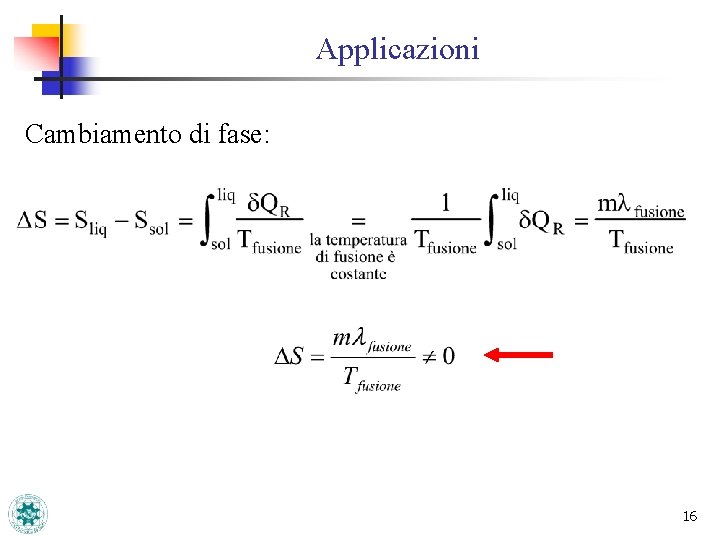
Applicazioni Cambiamento di fase: 16

Applicazioni c Per un trasformazione qualunque: poiché l’entropia è una funzione di stato, possiamo considerare una qualunque trasformazione reversibile. f i 17

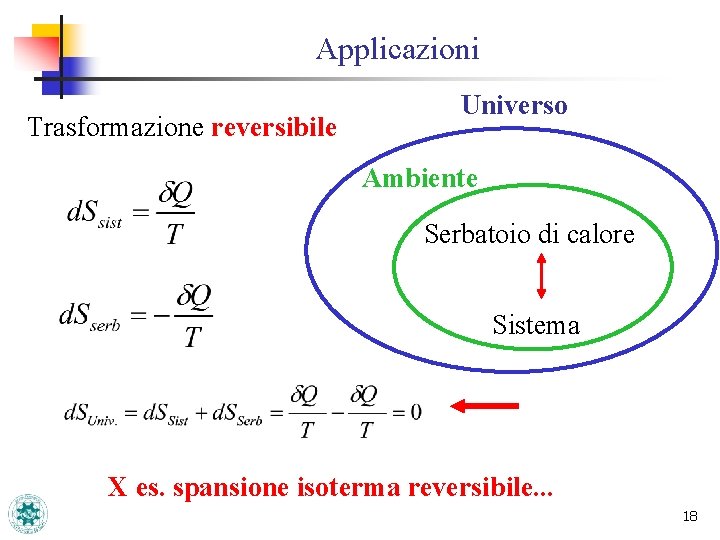
Applicazioni Trasformazione reversibile Universo Ambiente Serbatoio di calore Sistema X es. spansione isoterma reversibile. . . 18

II principio della Termodinamica: Enunciato I: se il sistema è isolato, l’entropia del sistema non può diminuire, aumenta se la trasformazione è irreversibile; resta costante se la trasformazione è reversibile. L’Universo è un sistema isolato Ciclo irreversibile Ciclo reversibile L’irreversibilità è sempre accompagnata da un aumento di entropia. !! Ogni processo naturale evolve sempre nella direzione verso cui aumenta l’entropia. 19

Le macchine termiche n Il I principio: Calore può essere trasformato in lavoro meccanico. n Un espansione isoterma trasforma tutto il Q in W n Le macchine termiche sono sistemi termodinamici che descrivono un ciclo. Una parte del ciclo assorbe calore da uno o più serbatoi, un’altra parte cede calore a uno o più serbatoi. n Esempi di macchine termiche: il motore dell’automobile, le locomotive a vapore. n Il rendimento della macchina: È possibile realizzare un processo il cui unico risultato sia quello di assorbire calore da un serbatoio e di convertirlo completamente in lavoro? ? Q ceduto = 0 Macchina mono-terma W(=Q 1) 20

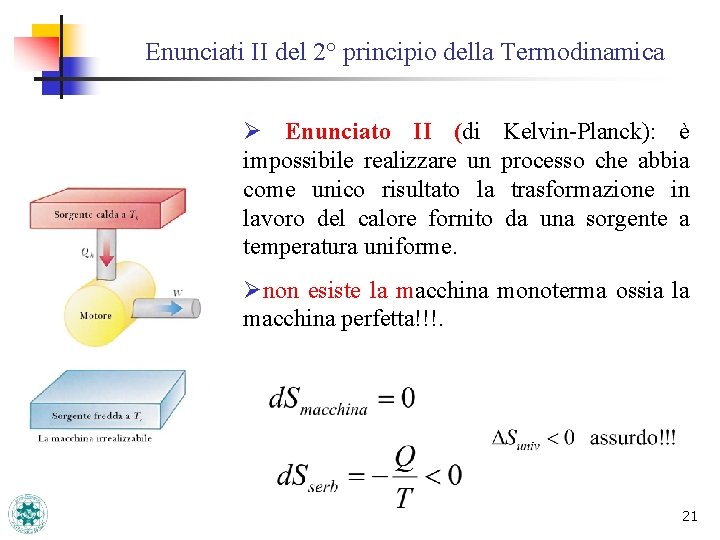
Enunciati II del 2° principio della Termodinamica Ø Enunciato II (di Kelvin-Planck): è impossibile realizzare un processo che abbia come unico risultato la trasformazione in lavoro del calore fornito da una sorgente a temperatura uniforme. Ønon esiste la macchina monoterma ossia la macchina perfetta!!!. 21

Enunciato III del II principio della Termodinamica Ø Enunciato III (di Clausius): è impossibile realizzare un processo che abbia come unico risultato il trasferimento di una quantità di calore da un corpo ad un altro a temperatura maggiore. SERVE W non esiste il frigorifero perfetto!! 22

Riassumiamo II principio Enunciato I: se il sistema è isolato, l’entropia del sistema non può diminuire, aumenta se la trasformazione è irreversibile; resta costante se la trasformazione è reversibile. Ø Enunciato II (di Kelvin-Planck): è impossibile realizzare un processo che abbia come unico risultato la trasformazione in lavoro del calore fornito da una sorgente a temperatura uniforme Ø Enunciato III (di Clausius): è impossibile realizzare un processo che abbia come unico risultato il trasferimento di una quantità di calore da un corpo ad un altro a temperatura maggiore. 23

Equivalenza degli enunciati II e III Ø Dimostriamo che la violazione di uno implichi la violazione dell’altro. Violato enunciato II Ø Supponiamo che esista una macchina termica 1 che trasformi tutto il calore il lavoro. Ø Prendiamo un’altra macchina di Carnot 2) che lavori come frigorifero. Ø Macchina complessiva: Cede Assorbe a l o Vi I I I il 24

Il teorema di Carnot n n Tutte le macchine che lavorano tra due termostati hanno un rendimento che è minore, o al massimo uguale, a quello di una macchina di Carnot che lavori tra gli stessi due termostati. tutte le macchine reversibili (tutte le macchine di Carnot) che lavorano tra gli stessi termostati hanno, tutte, lo stesso rendimento. 25

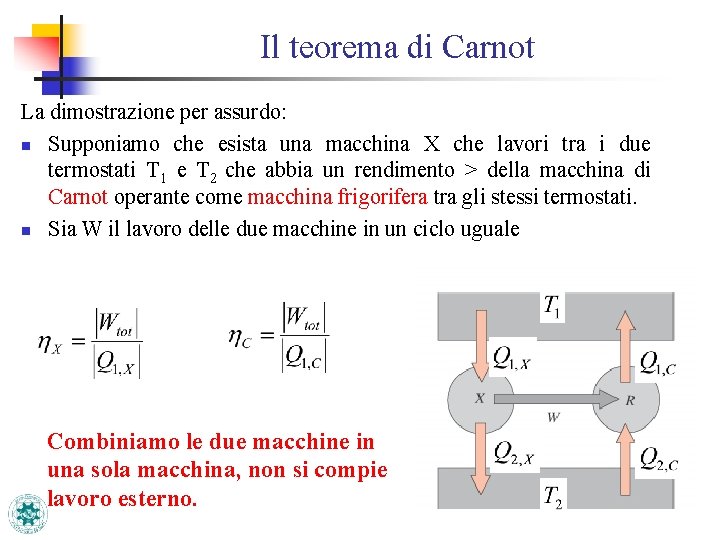
Il teorema di Carnot La dimostrazione per assurdo: n Supponiamo che esista una macchina X che lavori tra i due termostati T 1 e T 2 che abbia un rendimento > della macchina di Carnot operante come macchina frigorifera tra gli stessi termostati. n Sia W il lavoro delle due macchine in un ciclo uguale Combiniamo le due macchine in una sola macchina, non si compie lavoro esterno.

Il teorema di Carnot Assunto OSSIA

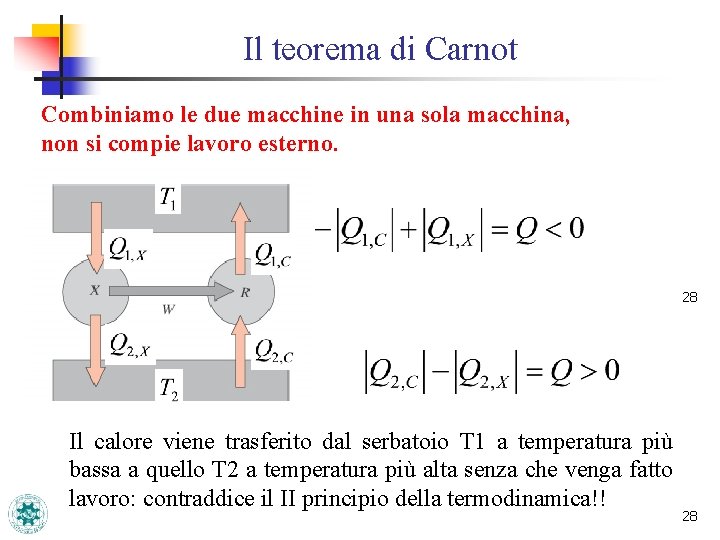
Il teorema di Carnot Combiniamo le due macchine in una sola macchina, non si compie lavoro esterno. 28 Il calore viene trasferito dal serbatoio T 1 a temperatura più bassa a quello T 2 a temperatura più alta senza che venga fatto lavoro: contraddice il II principio della termodinamica!! 28