Transporte de Calor Equilbrio Trmico Transporte de calor
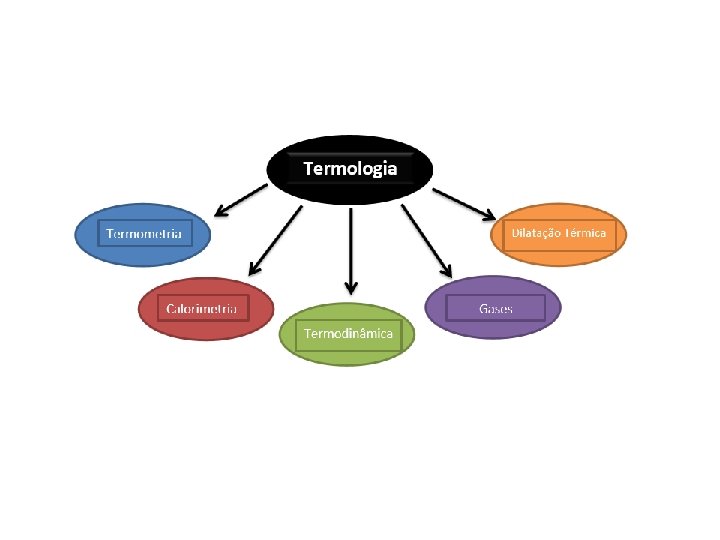
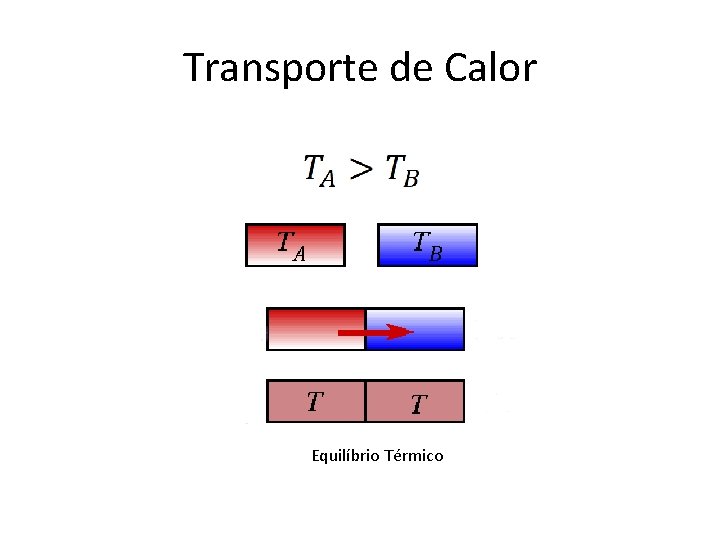
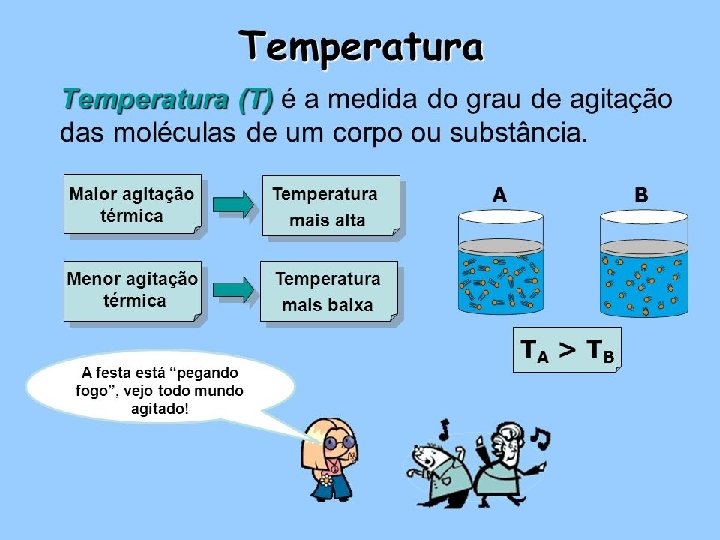
Transporte de Calor Equilíbrio Térmico
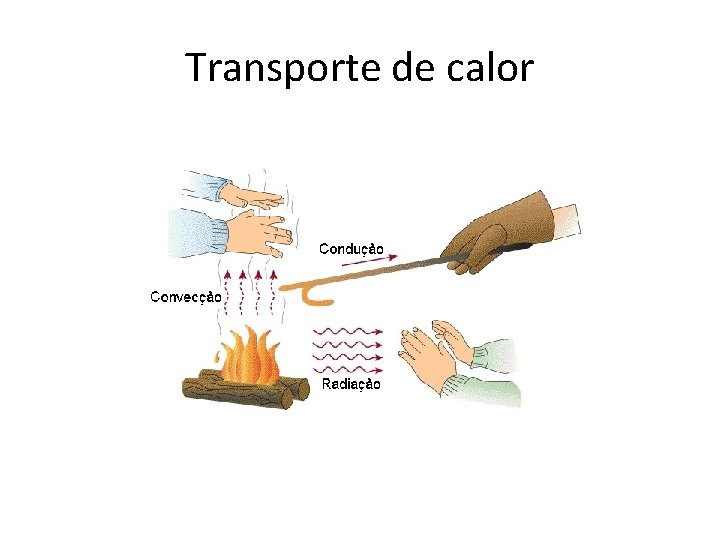
Transporte de calor
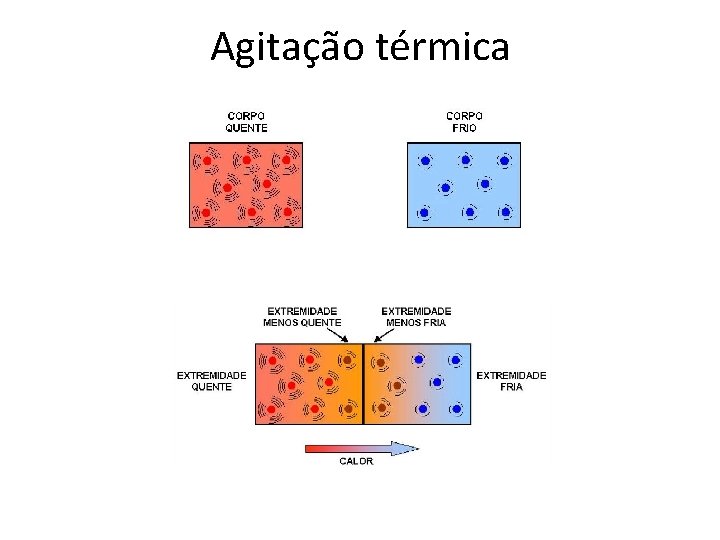
Agitação térmica

Conversão de escalas de temperatura

Lei de Boyle-Mariotte GÁS IDEAL As três variáveis de estado dos gases são: pressão, volume e temperatura. Numa transformação isotérmica, para uma dada massa de gás, o produto da pressão e do volume é uma constante. PV = constante

Trabalhos de Charles e Gay Lussac GÁS IDEAL PROCESSO ISOBÁRICO: Pressão constante PROCESSO ISOCÓRICO: Volume constante

Clapeyron concluiu que a constante da Lei Geral era proporcional ao número de moléculas do gás. Onde n é o número de mols de moléculas e R é uma constante válida para todos os gases. R é a Constante Universal dos Gases.

§Número de Avogadro: 6, 023 1023 §Mol: 1 mol contém 6, 023 1023 partículas (átomos, moléculas, elétrons etc. ) §Massa molar (M): a massa de 1 mol de moléculas, medida em gramas. §Número de mols (n):

TEORIA CINÉTICA DOS GASES • As moléculas de um gás estão em contínuo movimento e separadas por grandes espaços vazios. • O movimento das moléculas ocorre ao acaso e em todas as direções e sentidos.
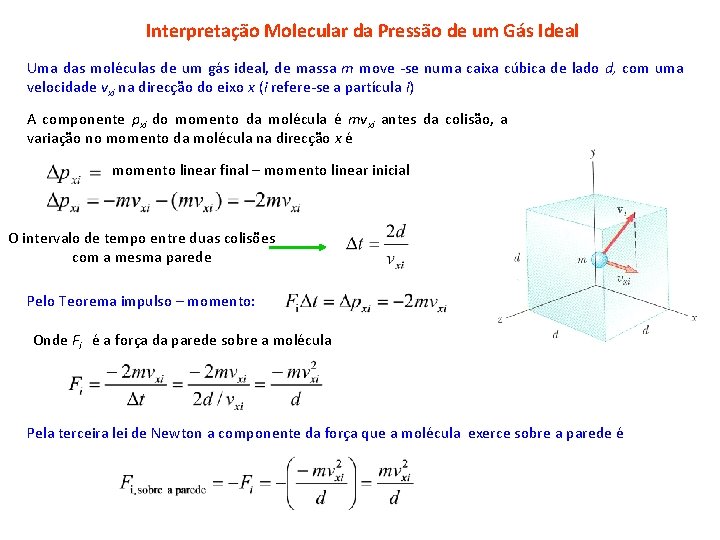
Interpretação Molecular da Pressão de um Gás Ideal Uma das moléculas de um gás ideal, de massa m move -se numa caixa cúbica de lado d, com uma velocidade vxi na direcção do eixo x (i refere-se a partícula i) A componente pxi do momento da molécula é mvxi antes da colisão, a variação no momento da molécula na direcção x é momento linear final – momento linear inicial O intervalo de tempo entre duas colisões com a mesma parede Pelo Teorema impulso – momento: Onde Fi é a força da parede sobre a molécula Pela terceira lei de Newton a componente da força que a molécula exerce sobre a parede é

Considerando as N moléculas do gás ideal no recipiente de volume V A força média total F exercida sobre a parede do recipiente pelo gás A força constante, F, sobre a parede devido às colisões moleculares tem o valor Pelo teorema de Pitágoras: e A força total sobre a parede é Obtemos a pressão exercida sobre a parede, dividindo F pela área da parede (A=d 2). Nota: V=Ad=d 3 A pressão é proporcional ao número de moléculas por unidade de volume e à energia cinética translacional média das moléculas

Interpretação Molecular da Temperatura de um Gás Ideal onde Número de Avogadro Constante de Boltzmann Substituindo obtemos A temperatura de um gás é uma medida direta da energia cinética translacional média das moléculas

Rescrevendo a equação anterior de outra forma é a energia translacional média por molécula como Teorema de equipartição de energia A energia de um sistema em equilíbrio térmico está igualmente dividida entre todos os graus de liberdade “Graus de liberdade” refere-se ao número de maneiras independentes pelas quais uma molécula pode ter energia. No caso do gás ideal cada molécula têm 3 graus de liberdade uma vez que se movimentam na direcção dos eixos x, y e z A energia cinética translacional total de N moléculas de gás é simplesmente N vezes a energia translacional média por molécula = Energia interna de um gás monoatómico


- Slides: 17